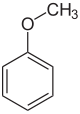
Anisol
| Anisol | |
|---|---|
| Numele IUPAC | |
| metoxibenzen | |
| Denumiri alternative | |
| fenilmetileter fenoximetan | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 7 H 8 O |
| Masa moleculară ( u ) | 108,14 |
| Aspect | lichid incolor |
| numar CAS | |
| Numărul EINECS | 202-876-1 |
| PubChem | 7519 |
| ZÂMBETE | COc1ccccc1 |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1,02 g / cm 3 |
| Solubilitate în apă | 1,04 g / l [1] |
| Coeficientul de partiție 1-octanol / apă | 2.11 |
| Temperatură de topire | −37 ° C (356 ° F; 236,15 K) |
| Temperatura de fierbere | 155 ° C (428,15 K) |
| Presiunea de vapori ( Pa ) la 25 ° C K. | 470 |
| Proprietăți toxicologice | |
| LD 50 (mg / kg) | 3700 mg / kg (șoarece, oral) |
| Informații de siguranță | |
| Punct de flacără | 52 ° C |
| Temperatură de autoaprindere | 475 ° C |
| Simboluri de pericol chimic | |
  | |
| Atenţie | |
| Fraze H | 226 - 315 - 319 |
| Sfaturi P | 305 + 351 + 338 [2] |
Anisolul este un compus aromatic care are o metoxid (CH3 O-) legată la inelul aromatic al benzenului .
Are mirosul și gustul tipic al anasonului și este conținut în el.
Acest compus este sintetizat în principal artificial și este un precursor al altor compuși sintetici.
Reactivitate
Anisolul poate suferi substituții electrofile aromatice mai repede decât benzenul , care la rândul său reacționează mai repede decât nitrobenzenul . Grupul metoxid este un grup orientator orto / para , ceea ce înseamnă că substituția va avea loc preferențial într-una din aceste trei poziții. Comportamentul mai nucleofil al anizolului comparativ cu benzenul arată influența grupului metoxid , ceea ce face inelul mai bogat în electroni .
Ca exemplu al comportamentului său nucleofil, anisolul reacționează cu anhidridă acetică producând 4-metoxiacetofenonă în funcție de reacție:
CH 3 OC 6 H 5 + (CH 3 CO) 2 O → CH 3 OC 6 H 4 C (O) CH 3 + CH 3 CO 2 H
Spre deosebire de multe acetofenone, oricât reflectă influența grupului metoxidic, metoxiacetofenona poate suferi o a doua acetilare. De exemplu, pentasulfura de fosfor transformă anisolul în reactivul Lawesson .
Legătura eterică este foarte stabilă, dar gruparea metil poate fi îndepărtată cu iodură de hidrogen :
CH 3 OC 6 H 5 + HI → HOC 6 H 5 + CH 3 I
Sinteză
Anisolul este preparat prin sinteza Williamson , prin reacția fenoxidului de sodiu cu brometan și agenți de metilare înrudiți [3] :
Utilizări
Anisolul este un precursor al parfumurilor , feromonilor insectelor și drogurilor . [4] De exemplu, anetolul sintetic este preparat din anisol.
Siguranță
Anisolul este relativ netoxic, cu un LD 50 de 3700 mg / kg la șoareci. [5] Principalul său pericol este inflamabilitatea. [5] [6]
Notă
- ^ http://www.hmdb.ca/metabolites/HMDB33895
- ^ Sigma Aldrich; rev. din 04.07.2013
- ^ http://www.orgsyn.org/demo.aspx?prep=cv1p0058 , la www.orgsyn.org . Adus pe 4 martie 2017 .
- ^ (EN) Helmut Fiege, Heinz-Werner Voges și Toshikazu Hamamoto, Ullmann's Encyclopedia of Industrial Chemistry , Wiley-VCH Verlag GmbH & Co. KGaA, 1 ianuarie 2000, DOI : 10.1002 / 14356007.a19_313 , ISBN 9783527306732 . Adus pe 4 martie 2017 .
- ^ a b Mallinckrodt Baker, Inc., Material Safe Data Sheet of anisole ( PDF ) (arhivat din original la 1 iulie 2010) .
- ^ ICSC 1014 - ANISOLE , pe www.inchem.org . Adus pe 4 martie 2017 .
Alte proiecte
-
 Wikționarul conține dicționarul lema « anisol »
Wikționarul conține dicționarul lema « anisol » -
 Wikimedia Commons conține imagini sau alte fișiere pe anisol
Wikimedia Commons conține imagini sau alte fișiere pe anisol
linkuri externe
- ( EN ) Anisole , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
| Controlul autorității | GND ( DE ) 4319568-4 |
|---|