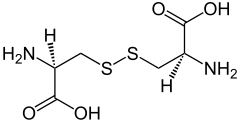
Cistină
| Cistină | |
|---|---|
| Numele IUPAC | |
| Acid (2 R , 7 R ) -3,3'-ditiobis (2-aminopropanoic) | |
| Denumiri alternative | |
| L - (-) - Cistină (2 S, 7 S) - (-) - Cistină Dicisteina | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 6 H 12 N 2 O 4 S 2 |
| Masa moleculară ( u ) | 240,29 |
| Aspect | Solid cristalin alb |
| numar CAS | |
| Numărul EINECS | 200-296-3 |
| PubChem | 67678 |
| DrugBank | DB00138 |
| ZÂMBETE | C(C(C(=O)O)N)SSCC(C(=O)O)N |
| Proprietăți fizico-chimice | |
| Solubilitate în apă | 112 mg / L |
| Temperatură de topire | 260-261 ° C (533,15-534,15 K) |
| Informații de siguranță | |
| Fraze H | --- |
| Sfaturi P | --- [1] |
Cistina este un aminoacid sulfurat caracterizat prin formula moleculară C 6 H 12 N 2 O 4 S 2 și obținut prin reacția oxidativă a două molecule de cisteină . Apare ca un solid incolor cu un punct de topire de 260-261 ° C. A fost descoperit în 1810 de William Hyde Wollaston, dar a fost recunoscut ca o componentă a proteinelor doar când a fost izolat de coarnele unei vaci în 1899 .
Cistina este prezentă în multe proteine și afectează în mod semnificativ structura lor terțiară . Cistina este, de asemenea, parțial responsabilă pentru formarea unei matrice de gluten în pâine , împreună cu stabilirea legăturilor de hidrogen și a interacțiunilor hidrofobe . Acest aminoacid este prezent în mod semnificativ în părul uman, în special este responsabil pentru forma ondulată a părului , ondulație datorată formării punților disulfură caracteristice (-SS-).
Importanța alimentelor
Cistina este utilizată de organism ca sursă de cisteină necesară pentru biosinteza glutationului , împreună cu glutamatul și glicina . În special, cistina este considerată a fi forma moleculară preferată pentru celulele sistemului imunitar , inclusiv macrofage și astrocite . Limfocitele și neuronii preferă în schimb să utilizeze cisteina direct pentru a efectua sinteza glutationului.
Surse nutritive
Suplimentele alimentare de N-acetilcisteină sunt o sursă de cistină, dar dozele sunt limitate de efectele secundare. Una dintre cele mai bogate surse de cistină este reprezentată de proteinele din zer nedenaturate . Cistina nu este digerată sau hidrolizată în mod semnificativ în stomac , ci este transportată de fluxul sanguin către diferitele districte celulare ale corpului. Aici legătura slabă disulfură este clivată producând cisteină, care este pusă la dispoziție pentru sinteza glutationului.
Notă
- ^ Sigma Aldrich; rev. din 26.01.2011
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe cistină
Wikimedia Commons conține imagini sau alte fișiere pe cistină