Liant de pod
În chimia compusului de coordonare , un ligand punte este un ligand care leagă doi sau mai mulți atomi, de obicei ioni metalici. [1] Ligandul poate fi monoatomic sau poliatomic. Practic toți compușii organici cu o anumită complexitate pot funcționa ca liganzi de legătură, astfel încât acest termen se referă în general la liganzi mici, cum ar fi pseudohalidele sau liganzii proiectați special pentru a lega două metale.
Când se scrie numele unui complex în care un liant leagă două metale, liantul bridging este precedat de litera grecească receptorii p ( „mu“) cu un subscript număr pentru a indica numărul de metale conectate. Numărul 2 nu este de obicei indicat, în loc de μ 2 este pur și simplu scris μ. [2] Simbolul μ nu trebuie confundat cu η („vârstă”) care se referă la hapticitate . Când este necesar să-l specificați, liantele care nu sunt punte se numesc lianți terminali (a se vedea figurile).
Lista de lianți anorganici de punte
Cu excepția amoniacului și a aminelor , practic toți lianții anorganici se pot lega. [3] [4] Chiar și anionii cei mai comuni pot acționa ca liganzi de legătură.
| liant de pod | Nume | exemplu |
|---|---|---|
| OH - | hidroxi | [Fe 2 (OH) 2 (H 2 O) 8 ] 4+ , vezi olation |
| O 2− | os | [Cr 2 O 7 ] 2− , vezi polioxometalați |
| SH - | hidrosulfură | Cp 2 Mo 2 (SH) 2 S 2 |
| NH 2 - | amido | HgNH 2 CI |
| N 3 - | azotură | [Ir 3 N (SO 4 ) 6 (H 2 O) 3 ] 4− |
| CO | carbonil | Fe 2 (CO) 9 |
| Cl - | clor | Nb 2 Cl 10 |
| H - | hidrură | B 2 H 6 |
| CN - | cian | Fe (III) 4 [Fe (II) (CN) 6] 3 nH 2 O |
Chiar și lianții organici simpli pot lega puternic două centre metalice. Câteva exemple obișnuite sunt derivații organici ai liganzilor anorganici enumerați mai sus (R = alchil sau arii): OR - , SR - , NR 2 - , NR 2− , PR 2 - , PR 2− .
Exemple
- Complexe și compuși care conțin liganzi punte
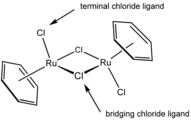
Dimerul dicloro (p-cimen) ruteniu conține doi liganzi terminali și doi liganzi de clorură de punte.
Acest complex binuclear de ruteniu, cunoscut sub numele de complex Creutz-Taube , conține o moleculă de pirazină ca ligand pod.
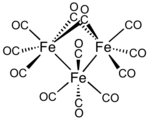
Tri-fierul dodecacarbonilic conține doi liganzi de CO pontați și zece terminali. Liantele de legătură și terminalele se schimbă rapid.
NbCl 5 conține doi liganzi de clorură în punte și opt terminali.
In reniu trioxid liganzii oxid sunt μ 2.
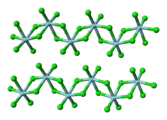
Tetraclorura de zirconiu conține atât liganzi terminali, cât și liganzi de clorură.
În acetat de rodiu (II) , cele patru grupe acetat acționează ca liganzi de punte.
Notă
Bibliografie
- ( EN ) NG Connelly, T. Damhus, RM Hartshorn și AT Hutton (eds), Nomenclatura chimiei anorganice - Recomandările IUPAC 2005 ( PDF ), Cambridge, Marea Britanie, Editura RCS, 2005, ISBN 0-85404-438-8 .
- AD McNaught și A. Wilkinson, ligand de legătură , pe IUPAC. Compendiu de terminologie chimică, ed. A II-a. („Cartea de aur”) , Blackwell Scientific Publications, 2006. Accesat la 20 ianuarie 2018 .
- (RO) P. Schwab, J. Wolf, N. Mahr, P. Steinert și alții, <4471 :: AID-CHEM4471> 3.0.CO 2-D bridging funcția unui ligand aparent nonbridging: biciclice rodiu complecși cu Rh (mu-SbR 3 ) Rh ca unitate moleculară , în Chem. Eur. J. , vol. 6, nr. 24, 2000, pp. 4471-4478, DOI : 10.1002 / 1521-3765 (20001215) 6:24 <4471 :: AID-CHEM4471> 3.0.CO; 2-D .
- ( EN ) H. Werner, The way into the bridge: a new bonding mode of tertiary phosphanes, arsanes, and stibanes , în Angew. Chem. Int. Ed. Engl. , vol. 43, nr. 8, 2004, pp. 938-954, DOI : 10.1002 / an.200300627 .