Reacția Mannich
Reacția Mannich este un organic chimic reacție care constă dintr - un amino alchilarea unui acid proton plasat lângă un carbonil grupare funcțională, în mod tipic între formaldehidă și un primar sau secundar amină sau amoniac . Produsul final este un compus β-amino-carbonil cunoscut și ca bază Mannich . Reacțiile dintre aldoimine și carbonilii cu alfa metilenele sunt, de asemenea, considerate reacții Mannich. Reacția poartă numele chimistului Carl Mannich . [1] [2]
Reacția Mannich este un exemplu de adăugare nucleofilă a unei amine la o grupare carbonil urmată de deshidratarea bazei Schiff. Baza Schiff , sau imină, este un electrofil care reacționează în a doua etapă a unei adiții electrofile cu un compus care conține un proton acid (care a fost sau a devenit un enol). Reacția Mannich este, de asemenea, considerată o reacție de condensare.
Aminele primare, secundare sau amoniacul sunt utilizate în reacția Mannich, în timp ce aminelor terțiare le lipsește un proton NH necesar pentru a forma intermediarul enaminei și, prin urmare, nu sunt utilizate. Compușii cu un proton acid în poziția alfa utilizabil pentru acest tip de reactivitate includ compuși carbonilici, nitrili , acetilenele , nitroaliphatic compuși, alfa - alchil- piridinele sau imine . De asemenea, este posibil să se utilizeze grupări fenil activate și heterocicluri bogate în electroni, cum ar fi furan , pirol și tiofen . Indolul este un substrat deosebit de activ; reacția produce derivați de gramamină.
Mecanism
Mecanismul începe cu formarea unui ion iminium din reacția dintre amină și formaldehidă într-un mediu acid:
Compusul cu gruparea funcțională carbonil (în acest caz o cetonă) se poate tautomeriza la forma enol, după care poate ataca ionul iminium.
Reacții asimetrice Mannich
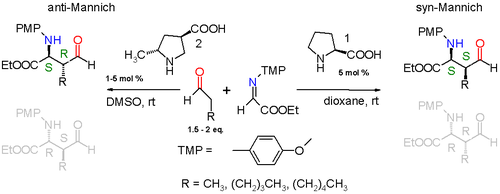
S-au făcut progrese semnificative în ceea ce privește aplicarea reacțiilor selective de enantium sau Mannich diasterice . Când este funcționalizat corect, puntea de etilenă nou formată posedă doi centri procirali, dând astfel naștere la două perechi distereoizomerice. Primul exemplu asimetric de Mannich este dat între o aldehidă și (S) -prolina ca catalizator chiral : [3]
Reacția care are loc este între o aldehidă simplă, cum ar fi propionaldehida și o imină derivată din etil glioxilat și p- metoxianilină (PMP = parametoxifenil) catalizată de (S) -prolină în dioxan la temperatura camerei. Reacția este diastereoselectivă cu o preferință pentru syn-Mannich 3: 1 când substituentul alchil de pe aldehidă este o grupare metil sau 19: 1 când gruparea alchil este gruparea pentil mult mai mare. Reacția este, de asemenea, enantioselectivă între cele două posibile adducte syn (S, S) sau (R, R), cu o preferință pentru aduct (S, S) cu un exces enantiomeric mai mare de 99%. Această stereoselectivitate este explicată în diagrama de mai jos.
Prolina intră într-un ciclu catalitic reacționând cu aldehida pentru a forma o enamină. Cei doi reactanți (imină și enamină) se aliniază pentru reacția Mannich cu atac din partea Si a enaminei de către imină. Datorită tensiunii sterice, este necesar ca reziduul alchil al enaminei și grupul imino să fie antiperiplanar într-o abordare care îl blochează astfel într-un mod de adăugare syn. Enantioselectivitatea este controlată în continuare de legăturile de hidrogen dintre gruparea acidului carboxilic a prolinei și iminei. Starea de tranziție pentru adăugare este un inel în formă de scaun cu nouă membri , cu legături parțiale simple și duble. Grupa prolină este convertită înapoi în aldehidă și se formează un singur izomer (S, S).
Modificând catalizatorul prolinei este posibil să se obțină aducti anti-Mannich. [4]
Aplicații
Reacția Mannich este utilizată în sinteza organică a compușilor naturali, cum ar fi peptide , nucleotide , antibiotice și alcaloizi (de exemplu, tropinonă ). Alte aplicații sunt în sectorul agrochimic, cum ar fi regulatorii de creștere a plantelor, [5] chimia vopselelor și polimerilor, catalizatorilor și este principalul mecanism de reticulare a formalinei ca fir.
Reacția lui Mannich este, de asemenea, utilizată în sinteza compușilor medicinali, cum ar fi rolitetraciclina (baza de tetraciclină a lui Mannich), fluoxetina (un antidepresiv ), tramadolul și tolmetina (medicamente antiinflamatoare) și azaciclofani. [6] [7]
Reacția Mannich este utilizată pentru a sintetiza alchilaminele, transformând hidrocarburile nepolare în săpunuri sau detergenți. Acesta este utilizat într-o varietate de aplicații de curățare, tratamente de combustibil auto și acoperiri epoxidice . [8]
Notă
- ^ (EN) C. Mannich și W. Krösche, Ueber ein aus Kondensationsprodukt Formaldehyd, Ammoniak und antipyrin , în Archiv der Pharmazie, vol. 250, n. 1, 1 ianuarie 1912, pp. 647–667, DOI : 10.1002 / ardp.19122500151 . Adus pe 24 octombrie 2016 .
- ^ FF Blicke, Organic Reactions , vol. 1, 1942, DOI : 10.1002 / 0471264180 , ISBN 9780471264187 . Adus pe 24 octombrie 2016 .
- ^ Armando Córdova, Shin-ichi Watanabe și Fujie Tanaka, O cale extrem de enantioselectivă către enantiomer al ambilor derivați alfa și beta-aminoacizi , în Journal of the American Chemical Society , vol. 124, nr. 9, 6 martie 2002, pp. 1866–1867. Adus pe 24 octombrie 2016 .
- ^ Susumu Mitsumori, Haile Zhang și Paul Ha-Yeon Cheong, Reacții directe asimetrice de tip anti-Mannich catalizate de un aminoacid proiectat , în Journal of the American Chemical Society , vol. 128, nr. 4, 1 februarie 2006, pp. 1040-1041, DOI : 10.1021 / ja056984f . Adus pe 24 octombrie 2016 .
- ^ Flávia AF da Rosa, Ricardo A. Rebelo și Maria G. Nascimento, Sinteza noilor acizi indolecarboxilici legați de hormonul vegetal acid indoleacetic IAA , în Journal of the Brazilian Chemical Society , vol. 14, n. 1, 1 ianuarie 2003, pp. 11–15, DOI :10.1590 / S0103-50532003000100003 . Adus pe 24 octombrie 2016 .
- ^ Rodolfo Quevedo și Bárbara Moreno-Murillo, Sinteza într-un singur pas a unei noi familii de heterociclofani , în Tetrahedron Letters , vol. 50, nr. 8, 25 februarie 2009, pp. 936–938, DOI : 10.1016 / j.tetlet.2008.12.023 . Adus pe 24 octombrie 2016 .
- ^ Augusto Rivera și Rodolfo Quevedo, Reacție de tip Mannich fără solvenți ca strategie pentru sintetizarea heterocalixarenelor noi , în Tetrahedron Letters , vol. 45, n. 45, 1 noiembrie 2004, pp. 8335–8338, DOI : 10.1016 / j.tetlet.2004.09.066 . Adus pe 24 octombrie 2016 .
- ^ [1] [2] [3] [4]
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre reacția lui Mannich
Wikimedia Commons conține imagini sau alte fișiere despre reacția lui Mannich
linkuri externe
- ( EN ) „Mecanism în mișcare: reacția Mannich” , pe youtube.com .
| Controlul autorității | LCCN (EN) sh94002476 · GND (DE) 4168833-8 |
|---|