Carbură de bor
| Carbură de bor | |
|---|---|
| Numele IUPAC | |
| Carbură de bor | |
| Denumiri alternative | |
| Tetraborură de carbon diamant negru | |
| Caracteristici generale | |
| Formula moleculară sau brută | B 4 C |
| Masa moleculară ( u ) | 55.255 g / mol |
| Aspect | pudra neagra |
| numar CAS | |
| Numărul EINECS | 235-111-5 |
| PubChem | 123279 |
| ZÂMBETE | B12B3C14B2B43 |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 2,52 g / cm 3 |
| Temperatură de topire | 2350 ° C (2623,15 K) |
| Temperatura de fierbere | > 3500 ° C (> 3773,15 K) |
| Informații de siguranță | |
| Temperatură de autoaprindere | Nu este inflamabil |
| Simboluri de pericol chimic | |
 | |
| Atenţie | |
| Fraze H | 302 - 332 - 361 |
| Sfaturi P | 261 - 280 - 304 + 341 - 308 + 313 - 312 [1] |
Carbura de bor (formula brută: B 4 C) este o moleculă care în condiții normale constituie agregate de material ceramic extrem de dur și, din acest motiv, este utilizată în armura unor tipuri de tancuri , în vesta antiglonț și în numeroase zone industriale. aplicații. Cu o duritate de 9,3 pe scara Mohs , este al cincilea material cel mai dur cunoscut, în spatele nitrurii de bor , diamantului , fulleritei ultra- dure și nanotuburilor de diamant agregate .
Istorie
Descoperit în secolul al XIX-lea ca produs secundar al reacțiilor care au loc între borurile metalice, materialul a fost studiat științific doar din anii 1930 . În prezent este produs industrial pentru reducerea carbo-termică a B 2 O 3 ( trioxid de dibor ) în cuptorul cu arc electric .
Stoichiometria reacției este următoarea:
- 2 B 2 O 3 + 7 C → B 4 C + 6 CO
Structura
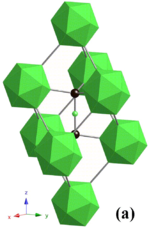
Carbura de bor are o structură complexă de icosaedru tipică borurilor metalice în care grupuri de 12 atomi de bor dispuse la vârfurile unui icosahedron formează o rețea romboedrică (grup de simetrie R 3 m N. 166, constante celulare a = 0,56 nm și c = 1,212 nm ) care înconjoară un lanț CBC situat în centrul celulei unitare unde fiecare dintre atomii de carbon este legat de trei icosaedre vecine.
Structura este stratificată: icosahedra lui B 12 și atomii de carbon formează rețele plane care sunt dispuse paralel cu planul c și stivuite de-a lungul axei c .
Rețeaua are două structuri de bază: un icosaedru B 12 și un octaedru B 6 . Datorită dimensiunilor mai mici, octaedrele lui B 6 nu se leagă de icosaedrele aceluiași plan, dar cu cele ale planurilor adiacente, aceasta scade forțele de legare din planul c [2] .
Datorită unităților structurale B 12 , formula chimică pentru carbură de bor „ideală” este adesea scrisă nu ca B 4 C, ci ca B 12 C 3 și deficiența de carbon descrisă în termeni de combinație a B 12 C 3 și B 12 C 2 [3] [4] .
Proprietate
Capacitatea sa de a absorbi neutronii fără a forma radio-nuclizi cu o perioadă lungă de înjumătățire radioactivă face ca materialul să fie deosebit de potrivit ca absorbant al radiației neutronice emise de reactoarele centralelor nucleare. Aplicațiile nucleare ale carburii de bor includ căptușeala reactorului, tijele de control și izolarea peletelor de combustibil nuclear.
Principalele caracteristici tehnice
| densitate | DIN EN 623-2 ρ [g / cm3] | > 2,48 |
| porozitate | DIN EN 623-2 P [%] | <0,5 (diametrul mediu al bobului [µm] <15) |
| Duritatea Vickers | DIN EN 843-4 HV 1 [GPa] | 31 |
| Duritatea Knoop | DIN EN 843-4 HK 0,1 [GPa] | 29 |
| Modulul lui Young | DIN EN 843-2 E [GPa] | 420 |
| Modulul Weibull | DIN EN 843–5 m | 15 |
| rezistență la încovoiere | DIN EN 843-1 σB [MPa] | 450 |
| rezistența la compresiune | σD [MPa] | > 2800 |
| coeficientul lui Poisson | v | 0,15 |
| rezistența la fractură | (SENB) Klc [MPa m ^ 0,5] | 5 |
| coeficient de dilatare termică | DIN EN 821-1 α [10-6 / K] | 4,5 (20 ° C - 500 ° C) - 7,2 (500 ° C -1000 ° C) |
| căldură specifică la 20 ° C | DIN EN 821-3 cp [J / gK] | 1 |
| conductivitate termică la 20 ° C | DIN EN 821-2 λ [W / mK] | 40 |
| rezistență electrică specifică la 20 ° C | DIN EN 50359 ρ (Ω / cm) | 1 |
| viteza sunetului | [Domnișoară] | 10920 |
Aplicații
- Armură în plăci anti-balistice personale și pentru vehicule, plăci de protecție suplimentare pentru a fi introduse în îmbrăcăminte, potrivite pentru oprirea gloanțelor de calibru mic.
- Duze care trag pulberi de siliciu sau aluminiu sub presiune (inclusiv nisip) pentru curățarea suprafețelor precum marmură sau statui metalice.
- Duze care pulverizează jeturi de apă de tăiat la presiune înaltă.
- Acoperiri rezistente la zgarieturi si uzura.
- Unelte de tăiat și fabricarea matrițelor .
- Abrazive, cum ar fi cele utilizate în roata diamantată sau rotativă .
- Absorbanți de neutroni în multe tipuri de reactoare nucleare .
Notă
- ^ Washington Mills; rev. din 01.09.2011
- ^ a b Zhang FX, Xu FF, Mori T, Liu QL, Sato A și Tanaka T, Structura cristalină a noilor solide bogate în boruri de pământuri rare: REB28.5C4 , în J. Alloys Compd. , vol. 329, 2001, p. 168, DOI : 10.1016 / S0925-8388 (01) 01581-X .
- ^ Musiri M. Balakrishnarajan, Pattath D. Pancharatna și Roald Hoffmann, Structura și legătura în carbura de bor: invincibilitatea imperfecțiunilor , în New J. Chem. , vol. 31, n. 4, 2007, p. 473, DOI : 10.1039 / b618493f .
- ^ Greenwood, NN; Earnshaw, A. (1997). Chimia elementelor (ed. A II-a). Butterworth-Heinemann. ISBN 0080379419 .
Bibliografie
- Sinteza și prelucrarea materialelor din carbură, azotură și borură ISBN 0-412-54060-6
- Fișe tehnice ESK CERAMICS
linkuri externe
- Site comercial care vinde TETRABOR în tuburi , pe pampado.com .
- Folosiți ca tije de control în reactorul de fisiune nucleară de la locul ENEL
- Abrazive - de pe site-ul Tecnimetal , pe tecnimetal-tm.com . Adus la 17 decembrie 2006 (arhivat din original la 10 noiembrie 2006) .
- ( EN ) Inventarul Național al Poluanților - Bor și compuși , pe npi.gov.au. Adus la 9 februarie 2006 (arhivat din original la 9 februarie 2006) .
- ( EN ) Introducerea bazei de date chimice NIST pentru carbura de bor , la webbook.nist.gov .
