Decorați
| Decorați | |
|---|---|
| Numele IUPAC | |
| decaborane (14) | |
| Caracteristici generale | |
| Formula moleculară sau brută | B 10 H 14 |
| Masa moleculară ( u ) | 122,22 |
| Aspect | cristale albe |
| numar CAS | |
| Numărul EINECS | 241-711-8 |
| PubChem | 6328162 |
| ZÂMBETE | [H]1[BH]234[BH]156[BH]278[BH]39([H]4)[BH]712[BH]853[BH]645[BH]311[BH]922[BH]14([H]5)[H]2 e [BH3]1[BH]23[BH]45[BH]26[BH]37[BH]18[BH]79[BH]64[BH]89[BH3]5 |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 0,94 |
| Temperatură de topire | 100 ° C (373 K) |
| Temperatura de fierbere | 486 (213 ° C) |
| Proprietăți toxicologice | |
| LD 50 (mg / kg) | 64 (oral, șobolan) |
| Informații de siguranță | |
| Punct de flacără | 353 (80 ° C) |
| TLV (ppm) | 0,05 |
| Simboluri de pericol chimic | |
| | |
| Expresii R. | 11, 24/25, 26 |
| Fraze S. | 9, 28, 36/37/39, 45 |
Decaboran este bor cu formula B 10 H 14. În condiții standard este un solid cristalin alb. Este una dintre principalele clustere hidrurile de bor , importante pentru structura si ca precursor al altor hidruri de bor.
Nomenclatură
În nomenclatura IUPAC a boranilor, B 10 H 14 se numește decaboran (14) , deoarece numărul atomilor de bor este indicat de prefix, iar numărul hidrogenilor este indicat între paranteze, cu cifre romane.
Proprietăți fizice
B 10 H 14 este un solid cristalin alb, diamagnetic, cu miros puternic caracteristic, tipic boranilor , uneori descris ca mucegai sau amar, similar cu ciocolata. Caracteristicile sale fizice seamănă cu cele ale compușilor organici precum naftalina și antracena , în sensul că poate fi sublimat sub vid la o temperatură moderată. Cea mai comună metodă de purificare este sublimarea . La fel ca compușii organici, este foarte inflamabil și arde cu o flacără verde, ca și alte hidruri de bor. În aerul umed este stabil, dar hidrolizează în apă clocotită, eliberând hidrogen și formând o soluție de acid boric . Este solubil în apă rece și în diferiți solvenți nepolari sau moderat polari.
Structura
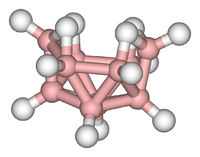
În B 10 H 14 cei zece atomi de bor sunt legați împreună și formează o structură care seamănă cu un octadecaedru incomplet (solid cu optsprezece fețe). Fiecare atom de bor are un hidrogen „radial”, iar cei patru atomi de bor de lângă deschiderea clusterului au și ceilalți patru hidrogeni legați împreună. În terminologia de chimie a clusterelor, această structură este numită „cuib”.
Sinteză
B 10 H 14 este , de obicei , sintetizat prin piroliza de bor clustere hidrură mai mici. De exemplu, decaboranul se obține prin încălzirea B 2 H 6 sau B 5 H 9 , cu eliminarea hidrogenului . [1]
Reactivitate
B 10 H 14 este un solid solid în aer, dar ușor inflamabil. Poate da naștere la diferite tipuri de reacții.
B 10 H 14 reacționează cu baze Lewis , cum ar fi CH3 CN și Me2S , pentru a da derivați cu formula B 10 H 12 • 2L.
- B 10 H 14 + 2 L → B 10 H 12 L 2 + H 2
Aceste specii, clasificate ca grupuri „arahno”, reacționează la rândul lor cu acetilena pentru a forma orto- carborani cu o structură „closo”:
- B 10 H 12 • 2L + C 2 H 2 → C 2 B 10 H 12 + 2L + H 2
B 10 H 14 este un acid Brønsted slab. Pierderea unui proton formează anionul [B 10 H 13 ] - , tot cu o structură „cuib”. În condiții mai drastice, un al doilea proton poate fi îndepărtat formând specia [B 10 H 12 ] 2– care poate acționa ca un ligand bidentat, ca de exemplu în [Zn (B 10 H 12 )] 2– . [1]
B 10 H 14 poate fi redus cu metale alcaline pentru a forma anionul [B 10 H 14 ] 2– , cu o structură „arahno” precum derivații B 10 H 12 • 2L.
Aplicații
B 10 H 14 este disponibil comercial în scopuri de cercetare. Nu a găsit aplicații industriale, deși a fost studiat în vederea utilizărilor multiple, de exemplu, ca posibil aditiv pentru combustibilii de rachetă.
Siguranță
La fel ca toate borani, de asemenea , B 10 H 14 este ușor inflamabil, și este foarte toxic prin inhalare, ingestie și contact cu pielea. Nu există date privind proprietățile cancerigene. [2]
Notă
- ^ a b NN Greenwood, A. Earnshaw, Chimia elementelor , ediția a II-a, Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4 .
- ^ Alfa Aesar, B 10 H 14 Fișa cu date de securitate ( PDF ), la alfa.com :. Accesat la 2 mai 2011 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre decaborane
Wikimedia Commons conține imagini sau alte fișiere despre decaborane