Organocataliza
Termenul de organocataliză înseamnă cataliza reacțiilor în care catalizatorul utilizat pentru a accelera reacția este o moleculă organică mică, lipsită de elemente anorganice, cum ar fi metalele. Termenul a fost inventat în 1935 de chimistul german Wolfgang Langenbeck . [1]
fundal
Prima utilizare a unei molecule organice ca catalizator este atribuită lui Justus von Liebig , care în 1859 a descoperit transformarea cianogenului în oxamidă catalizată de acetaldehidă . [2] Liebig a identificat acetaldehida ca catalizator al reacției și a recunoscut în efectele sale o analogie cu fermentii ( enzimele ).
Prima reacție a organocatalizei asimetrice a fost publicată de Breding și Fiske în 1912. În această reacție din benzaldehidă se formează o cianohidrină folosind alcaloizi drept catalizatori. Aceste studii au fost considerate foarte inovatoare, chiar dacă excesul enantiomeric realizat a fost mai mic de 10%. [3]
Zeci de ani mai târziu, s-a obținut stereoselectivitate semnificativă pentru prima dată într-o reacție de organocataliză. Aminoacidul ( S ) sau ( R ) - prolina dintr-un inel Robinson a fost folosit ca catalizator pentru a obține cetona Wieland-Miescher . Această reacție se numește acum reacția Hajos-Parrish-Eder-Sauer-Wiechert de la numele descoperitorilor și are o importanță considerabilă pentru sinteza totală a steroizilor . [4] [5] [6]
Cu modelul Houk, a fost propus pentru prima dată un mecanism coerent, analog modelului Zimmerman-Traxler , pentru reacția aldolică a enaminelor fără metal. [7] [8] Reacțiile încrucișate directe ale aldolului au fost dezvoltate independent de List, [9] Barbas, [10] Shibasaki [11] și Trost . [12] Prima reacție organocatalitică aldolică încrucișată selectivă a aldehidelor a fost dezvoltată în 2002 de MacMillan. [13]
Mecanism de reacție
În timpul ciclului catalitic, catalizatorul poate fi legat covalent de molecula substratului; în acest caz este necesară o concentrație relativ mare de catalizator organic. Chiar și prin legături necovalente, cum ar fi legături de hidrogen , pot apărea interacțiuni catalitice și, în acest caz, sunt necesare doar cantități mici de catalizator.
Mecanism covalent
Principiul majorității proceselor organocatalitice este că catalizatorul reacționează mai întâi cu un reactant pentru a forma (reversibil) o legătură covalentă. In prolina catalizată reacția aldolică , prolina dă inițial o reacție de condensare cu cetona utilizată. Cationul de imini rezultat se tautomerizează apoi în enamină , care în etapa următoare dă un atac nucleofil asupra aldehidei. Prin hidroliza ulterioară, produsul este eliberat și prolina este reformată.
În reacție, informațiile stereochimice sunt determinate de prolina chirală . Grupul carboxil al prolinei activează, de asemenea, aldehida prin formarea unei legături de hidrogen. Reacția se desfășoară printr-o stare de tranziție cu șase membri, în formă de scaun, similară cu modelul Zimmerman-Traxler pentru enolații de litiu. Substituentul aldehidei se află în planul pseudo-ecuatorial.
Cursul reacției printr-o stare de tranziție a scaunului a fost mai întâi postulat de Houk pe baza calculelor mecanice cuantice, [7] [8] și apoi demonstrat experimental de List folosind oxigen marcat. [14]
Mecanism non-covalent
În acest mecanism, catalizatorul nu formează legături covalente. Există interacțiuni direcționale slabe între substratul care trebuie activat și catalizatorul organic. Acesta este principiul prin care reacționează și multe enzime , care sunt, de asemenea, utilizate ca model pentru dezvoltarea catalizatorilor organici non-covalenți. În acest domeniu, se folosesc specii neutre care pot da legături de hidrogen, cum ar fi derivați de uree sau tiourea . [15] [16] Acei compuși care au inele fenilice cu structură rigidă și săraci în electroni, cu substituenți care atrag electronii și nu coordonează în pozițiile 3, 4 sau 5 s-au dovedit a fi catalizatori buni.
Avantajele derivaților de ditiourea (în special în comparație cu catalizatorii tradiționali care conțin acid acid Lewis) sunt:
- catalizatorul se leagă de substrat într-un mod non-covalent, produsul nu inhibă
- o cantitate mică de catalizator este suficientă (până la 0,001 mol%), valorile frecvenței de rotație sunt ridicate
- sinteza este simplă și convenabilă, cu modificări structurale
- catalizatorul poate fi legat de faza solidă, făcând posibilă recuperarea acestuia
- catalizatorul nu este sensibil la aer sau apă, nu este necesară o atmosferă de gaz inert, nu există probleme de manipulare
- cataliza este posibilă în condiții aproape neutre, substraturile labile pot fi utilizate în prezența acizilor
- catalizatorul nu conține metale și este netoxic, spre deosebire de mulți catalizatori cu acid Lewis care conțin metal
- catalizatorul este mai ecologic („ chimie verde ”)
Reacții
Unele tipuri de reacții care pot fi efectuate eficient prin organocataliză sunt:
- Reacția Aldol
- Knoevenagel condens
- Reacție asimetrică Diels-Alder
- Reacția asimetrică a lui Michael
- Reacția asimetrică a lui Mannich
- Shi epoxidare
- Reacție mai severă
- Reacția Baylis-Hillman
Catalizatori derivați din produse naturale
Derivații de aminoacizi ( S ) - prolină au fost și sunt utilizați în mod obișnuit. [17] [18] Derivații de ( S ) - fenilalanină sunt, de asemenea, des folosiți:
Alți catalizatori sunt derivați de alcaloizi conținuți în Cinchona :
De asemenea, sunt utilizați derivați ai acidului tartric , cum ar fi TADDOL :
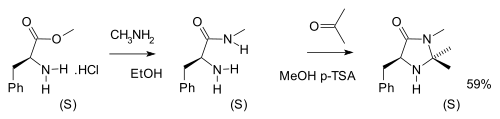
Catalizatorii MacMillan, utilizați în multe reacții de cataliză asimetrice, sunt obținuți din biomolecula fenilalaninei . Sinteza în doi pași lasă chiralitatea intactă: [19]
Notă
- ^ Langenbeck 1935
- ^ von Liebig 1860
- ^ Bredig și Fiske 1912
- ^ Eder și colab. 1971
- ^ Hajos și Parrish 1971
- ^ Hajos și Parrish 1974
- ^ a b Houk și Bahmanyar 2001
- ^ a b Bahmanyar și Houk 2001
- ^ List și colab. 2000
- ^ Kandasamy și colab. 2001
- ^ Yamada și colab. 1997
- ^ Trost și Ito 2000
- ^ Northrup și MacMillan 2002
- ^ Hoang și colab. 2003
- ^ Taylor și Jacobsen 2006
- ^ Connon 2006
- ^ Seebach și colab. 2007
- ^ Mukherjee și colab. 2007
- ^ Ahrendt și colab. 2000
Bibliografie
- KA Ahrendt, CJ Borths și DWC MacMillan, Noi strategii pentru cataliza organică: prima reacție Diels-Alder foarte organi-selectivă organocatalitică , în J. Am. Chem. Soc. , Vol. 122, nr. 17, 2000, pp. 4243–4244, DOI : 10.1021 / ja000092s . Adus pe 5 aprilie 2014 .
- S. Bahmanyar și KN Houk, Statele de tranziție ale reacțiilor aldolice catalizate de amină care implică intermediarii de enamină: studii teoretice ale mecanismului, reactivității și stereoselectivității , în J. Am. Chem. Soc. , Vol. 123, n. 45, 2001, pp. 11273-11283, DOI : 10.1021 / ja011403h . Adus pe 3 aprilie 2014 .
- G. Bredig și PS Fiske, Durch Katalysatoren Bewirkte Asymmetrische Synthese , în Biochem. Z. , vol. 46, nr. 7-23, 1912.
- SJ Connon, Organocataliza Mediată de (Thio) Derivați de uree , în Chem. Eur. J. , vol. 12, nr. 21, 2006, pp. 5418 –5427, DOI : 10.1002 / chem.200501076 . Adus pe 3 aprilie 2014 .
- U. Eder, G. Sauer și R. Wiechert, Neuartige asymmetrische Cyclisierung zu optisch aktiven Steroid-CD-Teilstücken , în Angew. Chem. , vol. 10, nr. 13, 1971, pp. 492–493, DOI : 10.1002 / ange . 19710831307 . Adus pe 3 aprilie 2014 .
- ZG Hajos și DR Parrish, Sinteza asimetrică a compușilor organici policiclici optic activi , în brevetul german DE 2102623 , 29 iulie 1971.
- ZG Hajos și DR Parrish, Sinteza asimetrică a intermediarilor biciclici ai chimiei produselor naturale , în J. Org. Chem. , vol. 39, nr. 12, 1974, pp. 1615-1621, DOI : 10.1021 / jo00925a003 . Adus pe 3 aprilie 2014 .
- L. Hoang, S. Bahmanyar, KN Houk și B. List, dovezi cinetice și stereochimice pentru implicarea unei singure molecule de prolină în statele de tranziție ale reacțiilor aldolice intra și intermoleculare catalizate de prolină , în J. Am. Chem. Soc. , Vol. 125, nr. 1, 2003, pp. 16-17, DOI : 10.1021 / ja028634o . Adus pe 3 aprilie 2014 .
- KN Houk, S. Bahmanyar, The Origin of Stereoselectivity in Proline-Catalyzed Intramolecular Aldol Reactions , in J. Am. Chem. Soc. , Vol. 123, n. 51, 2001, pp. 12911-12912, DOI : 10.1021 / ja011714s . Adus pe 3 aprilie 2014 .
- S. Kandasamy, W. Notz, T. Bui și CF Barbas, III., Reacții aldolice asimetrice directe catalizate de aminoacizi: o abordare bioorganică a reacțiilor catalitice asimetrice de formare a legăturii carbon-carbon , în J. Am. Chem. Soc. , Vol. 123, n. 22, 2001, pp. 5260–5267, DOI : 10.1021 / ja010037z . Adus pe 3 aprilie 2014 .
- ( DE ) W. Langenbeck, Die organischen Katalysatoren und ihre Beziehungen zu den Fermenten , Berlin, Springer, 1935.
- B. List, RA Lerner și CF Barbas, III, Reacții aldolice asimetrice directe catalizate prin prolină , în J. Am. Chem. Soc. , Vol. 122, nr. 10, 2000, pp. 2395-2396, DOI : 10.1021 / ja994280y . Adus pe 3 aprilie 2014 .
- S. Mukherjee, JW Yang, S. Hoffmann și B. List, Cataliză asimetrică a enaminei , în Chem. Rev. , vol. 107, nr. 12, 2007, pp. 5471–5569, DOI : 10.1021 / cr0684016 . Adus pe 5 aprilie 2014 .
- AB Northrup și DWC MacMillan, prima reacție directă și enantioselectivă a aldolelor încrucișate , în J. Am. Chem. Soc. , Vol. 124, nr. 24, 2002, pp. 6798-6799, DOI : 10.1021 / ja0262378 . Adus pe 3 aprilie 2014 .
- D. Seebach, AK Beck, DM Badine, M. Limbach, A. Eschenmoser, AM Treasurywala, R. Hobi, W. Prikoszovich, B. Linder, Oxazolidinonele sunt într-adevăr neproductive, specii parazite în cataliza prolinei? Gânduri și experimente care indică o perspectivă alternativă , în Helv. Chim. Acta , vol. 90, n. 3, 2007, pp. 425–471, DOI : 10.1002 / hlca.200790050 . Adus pe 5 aprilie 2014 .
- MS Taylor și EN Jacobsen, Cataliză asimetrică de către donatori chirali de legături de hidrogen , în Angew. Chem. Ed. Int. , Vol. 45, n. 10, 2006, pp. 1520–1543, DOI : 10.1002 / an.200503132 . Adus pe 3 aprilie 2014 .
- BM Trost și H. Ito, o reacție catalitică directă de aldol enantioselectivă printr-un design catalitic nou , în J. Am. Chem. Soc. , Vol. 122, nr. 48, 2000, pp. 12003–12004, DOI : 10.1021 / ja003033n . Adus pe 3 aprilie 2014 .
- J. von Liebig, Ueber die Bildung des Oxamids aus Cyan , în Justus Liebigs Ann. Chem. , vol. 113, nr. 2, 1860, pp. 246–247, DOI : 10.1002 / jlac.18601130213 . Adus pe 3 aprilie 2014 .
- YMA Yamada, N. Yoshikawa, H. Sasai și M. Shibasaki, Direkte katalytische asymmetrische Aldolreaktionen von Aldehyden mit nicht modifizierten Ketonen , în Angew. Chem. , vol. 109, nr. 17, 1997, pp. 1842–1944, DOI : 10.1002 / ange . 19971091716 . Adus pe 3 aprilie 2014 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre Organocataliză
Wikimedia Commons conține imagini sau alte fișiere despre Organocataliză