Spermatogeneza
La om și la alte mamifere, spermatogeneza este gametogeneza masculină, adică procesul de maturare a celulelor germinale masculine [1] care are loc în tubulii seminiferi ai testiculelor . Începe când individul a ajuns la pubertate [2] , datorită stimulării hormonilor FSH și testosteron [3] [4] .
Este analogul ovogenezei pentru femeie, dar diferă de aceasta în principal pentru momentul, deoarece producția de spermatozoizi începe în pubertate și durează întreaga viață a individului, în timp ce ovogeneza începe deja înainte de naștere și apoi se oprește. maturizarea individului pentru a se încheia la menopauză [2] . Spermatogeneza nu trebuie confundată cu spermiogeneza, care este a treia și ultima fază a spermatogenezei în sine, în care are loc diferențierea finală care duce la dezvoltarea spermatozoizilor maturi [5] . La sfârșitul spermatogenezei, doar 80% din spermatozoizi sunt normali, restul de 20% sunt spermatozoizi anormali funcțional sau morfologic [6] .
Caracteristicile generale ale spermatogenezei umane
Cu o durată de aproximativ 74 de zile [4] , spermatogeneza începe cu diviziunea celulară a celulelor nediferențiate care se află lângă lamina bazală a tubului seminifer (spermatogonia) care, cu o succesiune de mitoză și meioză, conduc la formarea de celule mature (spermatozoizi). ) care se desprind de partea cea mai luminală a peretelui tubular. Prin urmare, celulele germinale urmează un proces care le conduce din cele mai marginale regiuni ale peretelui către cele mai apicale regiuni până când sunt eliberate în lumenul tubului. Spermatozoizii, de fapt, se angajează în lumenul tubulilor seminiferi și apoi urmează calea indicată mai sus până la epididim, unde sunt capabili să aloce chiar mai mult de șapte zile dobândind motilitatea necesară pentru a putea ajunge la ovulul fertilizat. [7] .
Este important de reținut că spermatogeneza nu duce la crearea de spermatozoizi complet capabili să fertilizeze un ovul: acest lucru se datorează lipsei de motilitate. În călătoria prin epididim, apare decapacitarea: un fenomen biochimic care determină spermatozoizii să piardă complet motilitatea până când intră în contact cu tuburile uterine. Etapa finală de maturare are loc numai în interiorul uterului sau al trompelor uterine prin capacitație [8] . Această ultimă și fundamentală fază de maturare care durează aproximativ 7 ore permite spermatozoizilor să piardă învelișul glicoproteinelor și proteinelor seminale de pe suprafața acrosomului și, prin urmare, să participe la reacția acrosomului pentru fuziunea cu oul [8] .
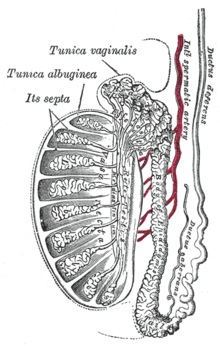
Schița anatomiei macroscopice normale a didimelor
Structura parenchimului testicular și a epiteliului germinativ
Spermatogeneza are loc în parenchimul testiculelor (sau didime) și mai precis în epiteliul germinativ al tubulilor seminiferi , conducte cu fundul orb cu diametrul de 150-200 µm care curg în tubulii seminiferi drepți (Russell și colab. 1990). Tubii drepți ajung apoi anastomozați în rete testicul de la care încep 15-20 de canale eferente și intră în epididim, care apoi continuă în canalul deferent .
Peretele acestor tubuli seminiferi este format din celule de susținere, numite celule Sertoli și diverse celule germinale reprezentate de elementele care alcătuiesc diferitele etape ale spermatogenezei [9] .
Vascularizația didimului și a barierei hemato-testiculare
Vasele de sânge care urmează stroma testiculară (ramuri ale arterei spermatice sau testiculare) ajung la interstițiul dintre tubii seminiferi, dar niciodată grosimea tubulilor (Hinton și Turner et.al 1993). Sângele arterial rezultat din circulație este separat de epiteliul germinativ prin intermediul barierei hemato-testiculare.
Anatomie microscopică normală a didimelor
Citotipuri implicate în spermatogeneză
Celulele care intră în joc în spermatogeneză se împart în două grupe mari: celulele germinale și celulele non-germinale . Primele sunt formate din spermatozoizi și precursorii lor; acestea din urmă din celule care nu sunt precursori și nu devin niciodată gameti, ci din celule cu funcții trofice și reglatoare.
Într-o secțiune transversală a tubului seminifer examinat de TEM este posibil să se identifice trei domenii principale în epiteliul germinativ . În sensul baso-apical (adică de la membrana bazală spre lumenul tubului seminifer) distingem trei compartimente separate prin două bariere:
- Compartiment interstițial (cu celule mioid și Leydig)
- Barieră formată din membrana bazală a epiteliului germinativ
- Compartiment bazal
2. Bariera așa-numita „barieră hemato-testiculară”
- Compartiment ad-luminal
1. Celulele germinale
Precursorii tulpinii, constând din spermatogonii , spermatocite și spermatide și spermatozoizi fac parte din celulele germinale [4] .
Spermatogonia
Spermatogonia este celulele cele mai nediferențiate și plasate spre lamina bazală a tubului seminifer. Au un diametru de 12 µm [1] și pot fi împărțite în trei tipuri:
- spermatogonia A [1] [9] : acestea constituie celule stem , adică celule în mitoză continuă care nu continuă în procesul de diferențiere și se subdivizează în continuare în:
- spermatogonia AD (de la întuneric , întunecat): sunt celule stem sau rezervă de spermatogonia datorită poziției lor extrem de departe de lumenul tubului seminifer și diviziunilor lor rare care pot duce la formarea altor AD sau la crearea spermatogoniei AP [ 10] [11] [12] ;
- Spermatogonia AP (de la pal , clar) [10] [12] : sunt spermatogonia care se reproduc ducând la formarea de spermatogonii mai diferențiate, până la spermatogonia B care sunt ultima etapă înainte de spermatocite;
- spermatogonia B : sunt spermatogonia succesivă, din punct de vedere al maturizării, până la cele de tip A și constituie celulele progenitoare ale spermatocitelor [1] [6] .
Din punct de vedere cromozomial, toate spermatogonia sunt celule diploide [13] .
Spermatocite
Spermatocitele sunt celulele care suferă meioză și, prin urmare, pornind de la un set cromozomial diploid, generează celule haploide. Există două tipuri de spermatocite:
- spermatocite primare sau de ordinul întâi : sunt cele care derivă direct din spermatogonia B și care suferă prima diviziune meiotică. În timpul acestei meioze, profaza durează aproximativ 22 [1] -24 [11] zile și este motivul pentru care acestea sunt celulele cele mai prezente în lamele histologice [1] . Sunt celule diploide [13] .
- spermatocite secundare sau de ordinul doi : sunt rezultatul primei diviziuni meiotice a spermatocitelor primare, au o viață foarte scurtă și sunt celule haploide [1] [13] .
Spermatide
Spermatidele sunt celulele care rezultă din a doua diviziune meiotică și derivă din spermatocitele secundare. Aspectul spermatidelor este rotunjit și nu foarte diferit de spermatocitele secundare: nucleul este mai mic, în timp ce aparatul Golgi are vezicula acrosomală . Spermatidele vor suferi spermiogeneză pentru a se transforma în spermatozoizi.
Spermatozoizii
Spermatozoizii sunt generați în timpul spermiogenezei de la spermatide ca spermatozoizi primitivi . Acestea constau din:
- un cap : ocupat în principal de nucleu (format din cromatină foarte condensată), de acrosomul care acoperă aproximativ 2/3 din nucleu și de care este separat de un spațiu subacrosomal subțire și de gropița de implantare pentru coadă. Acrosomul conține o serie de molecule de glicoproteină și enzime de protează esențiale pentru fertilizare. [14] [15]
- o coadă : lungime totală de 55-60 µm, este alcătuită din 4 segmente:
- gâtul care constituie porțiunea de legătură cu capul în gropița implantului și prezintă cei doi centrioli ai sistemului microtubular; [15] [16]
- partea intermediară (5 µm) de unde începe axonemul (format din 9 + 2 microtubuli) care va continua de-a lungul întregii cozi; este învelit de 9 fibrile externe și o teacă formată din mitocondrii înfășurate; [16] [17]
- partea principală (45-50 µm) formată din axonem și 9 fibrile exterioare înconjurate de o teacă fibroasă; [16] [18]
- partea terminală (4-6 µm) constituită din axonema înfășurată în membrana plasmatică. [16] [19]
Sunt celule haploide [13] .
Celule non-germinale
Celulele Sertoli, care devin parte a tubului seminifer și, între o celulă și cealaltă, conțin diferitele celule germinale [9] și celulele Leydig care joacă un rol extrem de marginal din punct de vedere material al spermatogenezei, dar fundamental din punct de vedere reglator, deoarece produc testosteron, care este principala moleculă care reglează activitatea celulelor Sertoli [4] .
Celulele Sertoli
Celulele Sertoli nu fac parte din celulele germinale, ci constituie celulele suport ale tubului seminifer. De fapt, se sprijină pe lamina bazală a tubului și dau direct în lumen. Diferitele etape ale spermatogenezei au loc între o celulă și următoarea și, prin urmare, într-o secțiune a tubului seminifer va fi posibil să se vadă celulele Sertoli cu diferitele spermatogonii, spermatocite, spermatide și spermatozoizi în procesul de diferențiere sau maturare intercalată . [9]
Rolul celulelor Sertoli este pur trofic și susține spermatogeneza, cu o funcție importantă de fagocitoză în etapele terminale ale maturării spermei [9] [20] . Celulele Sertoli nu mai sunt supuse diviziunii celulare după pubertate, menținând astfel o relație constantă cu celulele germinale adiacente [9] . În ciuda lipsei de reproducere, acestea sunt celule cu o rezistență foarte mare la adversitate (cum ar fi razele X, malnutriția sau infecțiile) în comparație cu omologii lor germinali mult mai delici și, prin urmare, susceptibili la insulte externe [20] .
Ele constituie bariera hemato-testiculară care împiedică sistemul imunitar să inducă eliminarea spermatocitelor. Acestea ca haploide ar fi recunoscute ca celule greșite cu ADN deteriorat și apoi eliminate.
Celulele Leydig
Celulele Leydig sunt celule prezente în stroma care înconjoară tubulii seminiferi [21] și, având în vedere distanța lor față de celulele germinale, nu sunt direct implicați, ca celulele Sertoli, în spermatogeneză. De fapt, rolul lor este fundamental pentru capacitatea lor de a produce testosteron sub stimularea hormonului LH , o gonadotropină hipofizară [22] .
Testosteronul produs se difuzează prin interstitiu către lamina bazală a tubului unde este absorbit de celulele Sertoli, care sunt sensibile la acest hormon, reglând astfel spermatogeneza [22] .
Etape
Spermatogeneza constă în esență în 3 faze principale: faza multiplicativă, meiotică și diferențiativă [11] .
În faza multiplicativă, precursorii diploizi se replică prin mitoză producând o parte a celulelor care vor continua să se înmulțească și o parte care se desfășoară în faza meiotică, unde există tranziția de la celule diploide la celule haploide care se vor diferenția în spermatozoizi în timpul fazei finale.
Faza multiplicativă (a mitozei)
În faza multiplicativă, principalul citotip implicat este spermatogoniul , care se află deasupra membranei bazale care separă epiteliul germinativ de țesuturile subiacente. În ultimele decenii, au fost propuse diferite modele de multiplicare și diferențiere („angajament”) a celulelor stem masculine umane. Conform lui Bani et.Al: spermatogonia AD se împarte continuu în spermatogonia AD sau AP. Acestea din urmă procedează prin diferențierea în spermatogonia B care evoluează în spermatocite de ordinul I, ultimele celule ale acestei faze.
Faza meiotică
În a doua fază, spermatocitele de ordinul întâi suferă meioză. În timpul fazei preleptotenice există o duplicare a ADN-ului care face ca aceste celule deja diploide să fie de fapt tetraploidă. În timpul primei diviziuni meiotice există o profază deosebit de lungă (aproximativ 22 [1] -24 [11] zile) formată din 5 etape [11] [23] :
- leptoten : cu cromozomi constituiți dintr-o grămadă de filamente subțiri [11] [23] ;
- zigoten : în timpul căruia are loc asocierea cromozomilor omologi și sexuali [11] [12] [23] ;
- pachytene : cu îngroșarea cromozomilor sexuali care formează așa-numita veziculă sexuală cu trecerea consecventă peste [12] [23] ;
- diploten : în care începe separarea cromozomilor omologi uniți în tetrade [12] [23] ;
- diakinezie : unde există detașarea definitivă a cromozomilor omologi [12] [23] .
După profaza I, prima diviziune meiotică se încheie, trecând prin fazele sale clasice: metafaza I (cu dispunerea cromozomilor omologi de-a lungul ecuatorului), anafaza I (cu migrarea cromozomilor către polii celulari) și telofaza I (reconstrucția nucleilor din cele două celule fiice). Această diviziune duce la formarea spermatocitelor secundare care, fiind rezultatul segregării cromozomilor omologi, sunt alcătuite dintr-un kit haploid format dintr-o copie dublă a ADN-ului (fiecare cromozom este format din două cromatide surori). [12]
Faza meiotică se încheie cu a doua diviziune meiotică care începe de la spermatocitele secundare pentru a forma spermatidele rotunde , celule haploide care nu vor mai suferi diviziuni celulare [12] .
Faza de diferențiere
A treia și ultima fază (numită și spermiogeneză ) este momentul în care spermatidele, în locul diviziunii lor celulare încetate, încep să se diferențieze și să se transforme în gameți prin trei faze: faza Golgi, faza acrosomului și faza de maturare [5]. ] . Această ultimă fază durează 12-24 de zile. În acest moment, spermatidele sunt celule care conțin un nucleu, mai multe mitocondrii, un aparat Golgi lângă nucleu, câteva centrioli, ribozomi liberi și un reticul endoplasmatic neted [5] . În general, acestea suferă fenomene de condensare nucleară, dezvoltarea flagelului, formarea acrosomului și pierderea citoplasmei [5] [14] .
Faza Golgi
În această primă fază în veziculele care constituie aparatul Golgi există o acumulare de granule proacrosomale care, la fuzionare, generează o singură granulă acrosomală mare în interiorul veziculelor acrosomale [14] . Toate acestea au loc în polul celular opus unde migrează centriolii și încep să dea formă axonemului din care va fi constituit flagelul [5] .
Faza acrosomică
Formarea acrosomului se completează cu mărirea veziculelor și a granulei acrosomale care acoperă acum aproximativ jumătatea superioară a nucleului, care se prelungește și se condensează [14] . Spirala mitocondriilor din jurul regiunii cozii numită partea intermediară [14], care este zona care în timpul mișcărilor flagelare va consuma cea mai mare energie și, prin urmare, va avea nevoie de cea mai mare mitocondrie [24] . În această a doua fază există, de asemenea, alinierea spermatozoizilor cu capul orientat către peretele tubulului și flagelul în alungire spre lumen [24] .
Faza de maturare
În această ultimă fază asistăm în esență la concluzia formării flagelului și a capului, dar mai presus de toate pierderea citoplasmei, care are loc odată cu detașarea veziculelor, corpurile reziduale , care sunt fagocitate de celulele Sertoli [14] [24] . În cele din urmă, există spermarea [25] constând în detașarea spermatozoizilor din celulele Sertoli (și, prin urmare, din tubul seminifer) și eliberarea lor în lumenul tubului [14] [26] .
Ciclul spermatogen
O caracteristică a mamiferelor masculine este producția continuă de spermă și, prin urmare, disponibilitatea relativ nelimitată a gametilor deja maturi în fiecare zi.
Ajustare
Hormoni
Principalele celule implicate în reglarea spermatogenezei sunt celulele Sertoli, celulele suport ale tubului seminifer care intră în contact cu toate tipurile diferite de celule germinale. Doi hormoni importanți acționează asupra celulelor Sertoli: hormonul foliculostimulant (FSH) produs de hipofiză și testosteronul produs de celulele Leydig (care la rândul lor produc acest hormon sub stimularea hormonului luteinizant hipofizar (LH) ) [3 ] [4] .
Mai mult, FSH nu numai că acționează direct asupra celulelor Sertoli pentru a le stimula, dar induce producția de proteine care leagă androgenii care se combină cu testosteronul și o transportă către tubulii seminiferi facilitând contactul cu celulele Sertoli în sine [3] .
Temperatura
Temperatura care trebuie să fie strict 35 ° C și nu 36/37 ° C ca restul organismului este, de asemenea, fundamentală pentru reglarea spermatogenezei [3] [27] . Plexul pampiniform , plexul venos care înconjoară arterele testiculare generând un schimb contracurent de temperatură, transpirația scrotală și contracția mușchilor cremasterici (cu consecința apropierii testiculelor de abdomen) sunt câteva dintre formele cu care temperatura este controlat și modificat.testicular [3] .
Patologii și disfuncții
În mod evident, orice disfuncție sau blocare a spermatogenezei duce la infertilitate sau dificultăți în concepție.
Temperatura
Una dintre principalele probleme care pot duce la disfuncționalitate este criptorhidia , adică condiția coborârii incomplete a testiculelor. Dacă testiculele, care în momentul dezvoltării prenatale (sau cel târziu în termen de trei luni de viață) [28] nu au coborât din cavitatea abdominală spre scrot, rămân într-o locație cu o temperatură mai mare decât cea care permite spermatogenezei au loc (37 ° C în loc de 35 ° C) cu o consecință sterilitate care poate fi rezolvată printr-o procedură chirurgicală care aduce testiculele înapoi la locul scrotal [3] [27] .
Alti factori
Alți factori care pot duce la disfuncționalități sau blocuri de spermatogeneză includ: radiații ionizante, medicamente [3] [27] , alcoolism, săruri de cadmiu [3] , stres mental și deficiențe de vitamine (A și E mai presus de toate) [27] .
Sindromul cililor imobile , care poate afecta și sistemul respirator, se caracterizează printr-o lipsă de proteine care să permită mișcarea flagelară cu imobilizarea consecventă a spermatozoizilor [24] .
Notă
- ^ a b c d e f g h Junqueira, Carneiro , p. 444 .
- ^ a b Keith Moore, TVN Persaud , p. 15 .
- ^ a b c d e f g h Junqueira, Carneiro , p. 453 .
- ^ a b c d și Anastasi și colab. , p. 377 .
- ^ a b c d e Junqueira, Carneiro , p. 447 .
- ^ a b Bani și colab. , p. 689 .
- ^ Anastasi și colab. , p. 386 .
- ^ a b Keith Moore, TVN Persaud , p. 29 .
- ^ a b c d e f Anastasi și colab. , p. 375 .
- ^ a b Bani și colab. , p. 687 .
- ^ a b c d e f g Anastasi și colab. , p. 378 .
- ^ a b c d e f g h Anastasi și colab. , p. 379 .
- ^ a b c d Keith Moore, TVN Persaud , p. 16 .
- ^ a b c d e f g Anastasi și colab. , p. 380 .
- ^ a b Bani și colab. , p. 691 .
- ^ a b c d Anastasi și colab. , p. 381 .
- ^ Bani și colab. , p. 692 .
- ^ Bani și colab. , p. 693 .
- ^ Bani și colab. , p. 694 .
- ^ a b Junqueira, Carneiro , p. 451 .
- ^ Anastasi și colab. , p. 372 .
- ^ a b Anastasi și colab. , p. 385 .
- ^ a b c d e f Bani și colab. , p. 690 .
- ^ a b c d Junqueira, Carneiro , p. 448 .
- ^ Spermiation , în Treccani.it - Treccani Vocabulary online , Institute of the Italian Encyclopedia.
- ^ Junqueira, Carneiro , p. 449 .
- ^ a b c d Anastasi și colab. , p. 383 .
- ^ Keith Moore, TVN Persaud , p. 281 .
Bibliografie
- Anastasi și colab., Tratat de anatomie umană, volumul II , Milano, Edi. Ermes, 2007, ISBN 978-88-7051-286-1
- Keith Moore, TVN Persaud, Dezvoltarea prenatală a omului , Napoli, EdiSES, 2009, ISBN 978-88-7959-348-9
- Bani și colab., Human histology , Naples, Idelson-Gnocchi, 2012, ISBN 978-88-7947-541-9
- Junqueira, Carneiro, Compendiu de histologie , Padova, Piccin, ediția a 5-a, 2006, ISBN 88-299-1817-2
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre spermatogeneză
Wikimedia Commons conține imagini sau alte fișiere despre spermatogeneză
linkuri externe
- ( EN ) Spermatogenesi , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
| Controlul autorității | Tezaur BNCF 47150 · LCCN (EN) sh85126541 · BNF (FR) cb122237643 (data) |
|---|