Mod de shikimato
Calea shikimate sau calea acidului shikimic este o cale metabolică găsită în bacterii, plante, ciuperci, alge și paraziți și definită de Bernard Davis în anii 1950 prin studiul tulpinilor mutante de Escherichia coli . [1] Este responsabil pentru biosinteza aminoacizilor aromatici ( fenilalanină , tirozină și triptofan ) din metabolismul carbohidraților . Animalele și oamenii sunt lipsiți de această cale, prin urmare, pentru aceste organisme, aceștia sunt aminoacizi esențiali (cu excepția tirozinei) care trebuie obținuți prin alimente . Această cale metabolică își ia numele de la intermediarul central, acidul shikimic , un compus izolat pentru prima dată de plante din genul illicium (în japoneză shikimi ) cu mulți ani înainte de descoperirea rolului său în metabolism.
Biosinteza corismatului
Fosfoenolpiruvatul și eritroza 4-fosfatul reacționează pentru a forma 3-deoxi-arabinoheptulsonat-7-fosfat (DAHP), într-o reacție catalizată de enzima DAHP sintază . DAHP este apoi transformat în 3-dehidrochinat (DHQ), într-o reacție catalizată de DHQ sintază . Reacția necesită NAD ca cofactor, care totuși, spre deosebire de ceea ce este prezentat în diagrama de mai jos, va fi ulterior regenerat.
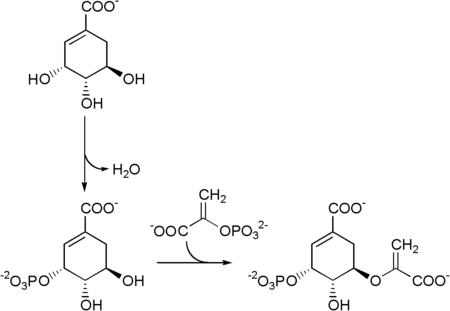
3-dehidrochinatul este deshidratat la 3-dehroshikimat de enzima dehidrocinază, ulterior dehidroshimatul este redus la acid shikimic de enzima shikimat dehidrogenază, care folosește NADPH ca cofactor.
Shikimato → shikimato-3-fosfat → 5-enolpiruvilshikimato-3-fosfat.
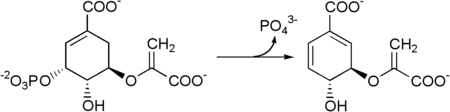
Corismatul sintază este enzima care catalizează reacția 5-enolpyruvilshikimate-3-fosfat → corismat .
Corismatul este intermediarul esențial pentru producerea de aminoacizi aromatici (fenilalanină, triptofan și tirozină) și alți compuși aromatici.
Cele șapte reacții ale căii shikimate care conduc la sinteza corismatului sunt rezumate în tabelul următor:
| Substraturi și coenzime | Produse | Enzimă | Tipul de reacție | |
|---|---|---|---|---|
| 1 | fosfoenolpiruvat + erythrosium 4-fosfat + H 2 O | 3-deoxi-arabinoheptulsonat-7-fosfat (DAHP) + fosfat | DAHP sintază | |
| 2 | 3-deoxi-arabinoheptulsonat-7-fosfat (DAHP) | 3-dehidrochinat | DHQ sintază | |
| 3 | 3-dehidrochinat | 3-dehidroshikimate | 3-dehidrochinat dehidratază | eliminarea unei molecule de apă |
| 4 | 3-dehidroshikimat + NADPH + H + | shikimato + NADP + | Shikimate dehidrogenaza | reducerea unei grupări carbonil în grupare hidroxil |
| 5 | shikimato + ATP | shikimate-3-fosfat + ADP | Shikimate kinaza | fosforilarea |
| 6 | fosfoenolpiruvat + shikimate-3-fosfat | 5-enolpiruvilshikimate-3-fosfat | 3-fosfosichimat 1-carboxinviniltransferază (EPSPS) | condensare |
| 7 | 5-enolpiruvilshikimate-3-fosfat + FMN | corismat | Corismate sintaza |
Biosinteza fenilalaninei și tirozinei
Plantele și microorganismele sintetizează în general fenilalanina și tirozina prin prefenat, care este biosintetizat printr-o transpunere Claisen a corismatului [2] [3] :
Reacția este catalizată de enzima corazată mutază .
Biosinteza tirozinei
Prefenatul suferă decarboxilare oxidativă dependentă de NAD cu retensie hidroxil , dând naștere p-hidroxifenilpiruvatului , supus ulterior unei reacții de transaminare în care glutamatul este donatorul grupului amino.
Biosinteza fenilalaninei
Prefenatul este decarboxilat cu pierderea hidroxilului pentru a forma fenilpiruvat. Aceasta suferă transaminare în fenilalanină, cu glutamat ca donator al grupării amino.
Mamiferele sintetizează tirozina din aminoacidul esențial fenilalanină ( phe ), care se introduce prin alimente. Conversia fenilalaninei în tirozină este catalizată de enzima fenilalanină hidroxilază , o oxigenază cu funcție mixtă care folosește un cofactor de pterină, tetrahidrobiopterina . Această enzimă catalizează reacția de conversie prin adăugarea unei grupări hidroxil pe atomul de carbon în poziția 6 a ciclului aromatic fenilalanină.
Biosinteza triptofanului
Plantele și microorganismele sintetizează în general triptofanul din acidul antranilic . Aceasta se condensează cu fosforibozil pirofosfat (PRPP), generând pirofosfat ca produs secundar. După deschiderea inelului fracției de riboză și după decarboxilarea reductivă, se generează indol -Gliceraldehidă-3-fosfat , care la rândul său se transformă în indol . În ultima etapă, enzima triptofan sintază catalizează formarea triptofanului din aminoacidul serină și indol.
Notă
- ^(EN) Bernard D. Davis, Biosinteza aromatică I. Rolul acidului shikimic , în Jurnalul de chimie biologică , vol. 191, 1951, pp. 315-326.
- ^(EN) Helmut Goerisch, Despre mecanismul reacției mutazice corismate, în Biochimie, Vol. 17, n. 18, 1978, p. 3700, DOI : 10.1021 / bi00611a004 .
- ^(EN) Peter Kast, B. Yadu Tewari, Olaf Wiest, Donald Hilvert, Kendall N. Houk și Robert N. Goldberg, Thermodynamics of the Conversion of Chorismate to Prephenate: Experimental Results and Theoretical predictions in J. Phys. Chem. B , vol. 101, nr. 50, 1997, pp. 10976-10982, DOI : 10.1021 / jp972501l .
Bibliografie
- ( EN ) Klaus M. Herrmann și Lisa M. Weaver, The Shikimate Pathway , în Revista anuală a fiziologiei plantelor și a biologiei moleculare a plantelor , vol. 50, nr. 1, 1999, pp. 473-503, DOI : 10.1146 / annurev.arplant.50.1.473 .
- (EN) KM Herrmann, The shikimate Pathway: Early Steps in the Biosynesis of Aromatic Compounds in The Plant Cell Online, vol. 7, nr. 7, 1995, pp. 907–919, DOI : 10.1105 / tpc.7.7.907 .
- ( EN ) Hiroshi Maeda și Natalia Dudareva, Calea Shikimate și Biosinteza aminoacizilor aromatici în plante , în Revista anuală a plantelor biologice , vol. 63, nr. 1, 3 mai 2012, pp. 73-105, DOI : 10.1146 / annurev-arplant-042811-105439 . Adus pe 10 februarie 2017 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe calea Shikimate
Wikimedia Commons conține imagini sau alte fișiere pe calea Shikimate