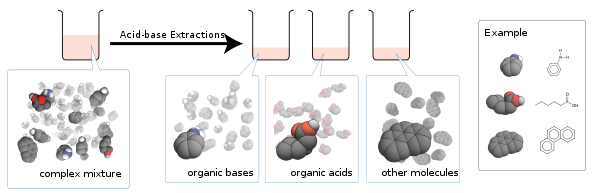
Extracția acido-bazică
Extracția acido-bazică este un proces progresiv, în care extracția lichid-lichid este utilizată pentru purificarea acizilor sau bazelor prezente în soluții, în funcție de proprietățile lor chimice . [1]
Acest proces se realizează în mod normal în urma sintezei chimice și pentru a izola compuși naturali și produse precum alcaloizi din extracte brute.
Teorie
Teoria fundamentală pe care se bazează această tehnică este că sărurile , care sunt ionice , tind să fie solubile în apă, în timp ce moleculele neutre tind să nu fie.
- Adăugarea unui acid la o soluție de bază organică și acid duce la protonarea bazei, în timp ce acidul nu se ionizează. Dacă acidul organic, cum ar fi acidul carboxilic, poate fi suficient de puternic, ionizarea acestuia poate fi suprimată prin adăugarea acidului.
- Adăugarea unei baze, pe de altă parte, implică deprotonarea acidului cu formarea consecventă a sării corespunzătoare acidului, în timp ce baza nu se ionizează. Din nou, ionizarea unei baze puternice este suprimată prin adăugarea bazei.
Procesul de extracție acid-bază poate fi, de asemenea, utilizat pentru a separa acizii (sau bazele) foarte slabi de acizii puternici (sau bazele), atâta timp cât diferența dintre constantele lor de disociere ( acide sau bazice ) este suficient de mare. Câteva exemple sunt:
- Acizi foarte slabi cu grupare fenolică OH cum ar fi fenol , 2-naftol (pK la aproximativ 10) din acizi mai puternici precum acidul benzoic sau acidul sorbic (pK la aproximativ 4-5)
- Bazele foarte slabe, cum ar fi cofeina sau 4-nitroanilina (pK b în jurul valorii de 13-14) din baze puternice, cum ar fi mescalina sau dimetiltryptamina (pK b în jurul a 3-4)
De obicei, pH - ul este reglat de valoarea aproximativă dintre cele două constante de disociere ale compușilor care urmează să fie separați. Acizi slabi, cum ar fi acidul citric , acidul fosforic sau acidul sulfuric diluat, sunt folosiți pentru valori ale pH-ului moderat acide, în timp ce acidul clorhidric și acidul sulfuric mai concentrat sunt utilizate pentru valori ale pH-ului puternic acide. Același lucru este valabil și pentru baze: bazele slabe, cum ar fi amoniacul sau bicarbonatul de sodiu, sunt utilizate pentru valori de pH moderat bazice, în timp ce bazele puternice, cum ar fi carbonatul de potasiu sau hidroxidul de sodiu, sunt utilizate în condiții puternic alcaline.
Tehnică
De obicei, compusul este dizolvat cu un solvent adecvat , cum ar fi diclormetan sau dietil eter și turnat într-o pâlnie separatoare . Se adaugă o soluție apoasă de acid sau bază și se ajustează pH-ul fazei apoase pentru a aduce compusul în forma dorită. După agitare pentru a permite separarea fazelor, se colectează faza care conține compusul de interes. Acest proces se repetă cu o valoare de pH opusă. Secvența nu este importantă și procesul poate fi repetat pentru a crește și a îmbunătăți separarea; cu toate acestea, este adesea convenabil ca compusul să fie dizolvat în faza organică după ultima etapă, astfel încât produsul dorit să fie obținut din evaporarea solventului.
Limitări
Procesul funcționează numai pentru acizi și baze cu o diferență mare de solubilitate între formele lor ionizate și neionizate. În consecință, acest proces nu poate funcționa în aceste cazuri:
- Zwitterion cu grupări funcționale acide sau bazice în aceeași moleculă (de exemplu, glicerină care tinde să fie solubilă la niveluri ridicate de pH)
- Amine sau acizi solubili în grăsimi care nu se dizolvă ușor în faza apoasă în forma lor ionizată ( trifenilamină sau acizi grași )
- Amine slabe, cum ar fi amoniacul , metilamina sau trietanolamina, care sunt semnificativ solubile în apă la niveluri ridicate de pH
- Acizi hidrofili precum acidul acetic , acidul citric sau majoritatea acizilor anorganici ( acid sulfuric , acid fosforic )
Alternative
Unele alternative pentru extracția acid-bazică pot fi:
- filtrarea compusului prin silicagel sau oxid de aluminiu care absorb sărurile
- cromatografia cu schimb de ioni
Notă
- ^ publicație: 13 iunie 1989 Laurence M. Harwood, Christopher J. Moody, Chimie organică experimentală: Principii și practică , ediție ilustrată, pp. 118–122, ISBN 0-632-02017-2 .
Elemente conexe
linkuri externe
- ( EN ) Extracția bazei acide , pe web.centre.edu . Adus la 28 aprilie 2012 (arhivat din original la 3 martie 2016) .