Aziridină
| Aziridină | |||
|---|---|---|---|
| Numele IUPAC | |||
| Aziridină | |||
| Denumiri alternative | |||
| Azaciclopropan, etilen imină, aminoetilenă, aziran, dimetilenimină, dimetilenimină, etilimină | |||
| Caracteristici generale | |||
| Formula moleculară sau brută | C 2 H 5 N | ||
| Masa moleculară ( u ) | 43.07 | ||
| Aspect | Lichid limpede, incolor, uleios [1] miros asemănător amoniacului [2] | ||
| numar CAS | Immagine_3D_aziridina | ||
| Numărul EINECS | 205-793-9 | ||
| PubChem | 9033 | ||
| ZÂMBETE | C1CN1 | ||
| Proprietăți fizico-chimice | |||
| Densitate (g / cm 3 , în cs ) | 0,8321 g / ml 20 ° C [3] | ||
| Temperatură de topire | −77,9 | ||
| Temperatura de fierbere | 56 | ||
| Informații de siguranță | |||
| Punct de flacără | -11 (12 ° F; 262 K) | ||
| Limite de explozie | 3,6-46% | ||
| Temperatură de autoaprindere | 322 (612 ° F; 595 K) | ||
| Simboluri de pericol chimic | |||
  | |||
| Atenţie | |||
| Fraze H | 351-315-335-334 | ||
| Sfaturi P | 201-280-262-260 | ||
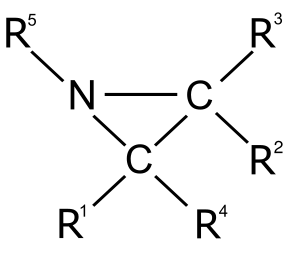
Aziridină este un compus organic care conține aziridină gruparea funcțională , un compus heterociclic cu o singură amină (-NH-) și două metilen punte grupe (CH 2 -). [4] [5]
Aziridinele sunt compuși derivați prin substituirea lui H cu radicali organici .
Sinteza aziridinelor
Există multe metode de sinteză a aziridinelor ( aziridinarea ).
Ciclizarea haloaminelor și amino alcoolilor
O grupare funcțională amină deplasează halogenul adiacent într-o reacție de substituție nucleofilă intramoleculară pentru a genera o aziridină. Alcoolii aminici au aceeași reactivitate, dar mai întâi trebuie să convertiți gruparea hidroxil într-o grupă plecătoare bună. Ciclizarea unei amine alcoolice se numește sinteza lui Wenker (1935), iar cea a unei haloamine metoda etileniminei lui Gabriel (1888).
Adăugarea nitrenelor
Reacțiile de adăugare a nitrenelor la alchene sunt o metodă stabilită pentru sinteza aziridinelor. Fotoliza sau termoliza azidelor este o modalitate bună de a genera nitrene. Nitrenii pot fi, de asemenea, preparați in situ din fenilodidă (III) diacetat și sulfonamide , de exemplu nitren etoxicarbonil nitren de la precursorul N- sulfoniloxi. [6]
Descompunerea triazolinei
Tratamentul termic sau fotoliza triazolinei elimină azotul , producând o aziridină. Triazolinele sunt generate de cicloadiția alchenelor cu o azidă .
Epoxizi
O metodă implică reacția în buclă deschisă a unui epoxid cu azidă de sodiu , urmată de reducerea azidei organice cu trifenilfosfină însoțită de expulzarea azotului gazos: [7]
Cealaltă metodă implică reacția în buclă deschisă a epoxizilor cu amine , urmată de închiderea inelului cu reacția Mitsunobu . [8]
Oximes
Sinteza etileniminei (aziridinei) Hoch-Campbell este reacția anumitor oxime cu reactivii lui Grignard : [9] [10] [11] [12]
Alchenele folosind compusul DPH
În 2014, a fost descrisă o nouă metodă de producere a aziridinelor prin reacția alchenelor mono-, di-, tri- sau tetra-substituite cu O- (2,4-dinitrofenil) hidroxilamină (DPH sau DPhHA) prin intermediul unui catalizator de rodiu omogen. Această metodă este simplă din punct de vedere operațional (adică un singur vas ) cu randament excelent.
Alchen + DPH Aziridină
De exemplu, Ph-Aziridina-Me poate fi sintetizată prin această metodă și apoi convertită printr- o reacție în buclă deschisă la (D) -amfetamină și (L) -amfetamină (cele două ingrediente active din medicamentul Adderall ). [13]
Reacții
Deschiderea inelului nucleofil
Aziridinele sunt substraturi reactive în reacțiile de deschidere a inelului cu mulți nucleofili datorită tensiunii lor inelare . Alcooliza și aminoliza sunt practic reacții inverse ale ciclizărilor. Nucleofilii de carbon, cum ar fi reactanții organo-litiu și organocupratele, sunt foarte eficienți.
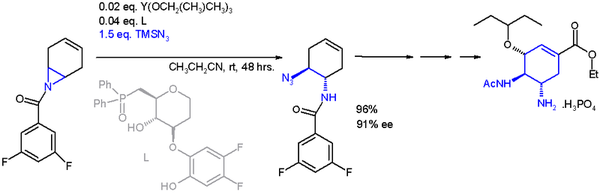
O aplicație a unei reacții în buclă deschisă în sinteza asimetrică este cea a trimetilsililazidei TMSN 3 cu un ligand asimetric [14] în următoarea imagine [15] în sinteza organică a oseltamivirului :
Formarea 1,3-dipolului
Anumite azirine N- substituite cu o grupă de preluare a electronilor pe ambii atomi de carbon formează ilizi de azometină într-o reacție electrociclică termică sau o reacție fotochimică în buclă deschisă . [16] [17] Acești ilizi pot fi prinși cu un dipolarofil adecvat într-o reacție de cicloadiție 1,3-dipolară . [18] :
Când substituentul N- este un grup de extragere a electronilor, cum ar fi grupul Ts , legătura carbon-azot este ruptă, formând o moleculă de zwitterion cu formula TsN - –CH 2 –CH + 2 –R [19]
Acest tip de reacție necesită un catalizator acid Lewis, cum ar fi trifluorura de bor . În acest fel, 2-fenil- N- tosilaziridina reacționează cu alchinele, nitrilii , cetonele și alchenele . Anumiți 1,4-dipoli sunt formați din azetidine .
Alte
Aziridine N-non - substituiți pot fi deschise cu olefine , în prezența unui Lewis puternic acid cum ar fi B (C 6 F 5) 3. [20]
Toxicologie
Toxicologia unui anumit compus aziridinic depinde de structura și activitatea acestuia, împărtășind în același timp caracteristicile generale ale aziridinelor. Ca electrofil , aziridinele sunt supuse atașării și deschiderii inelului de către nucleofili endogeni, cum ar fi baze azotate în perechi de baze ADN, rezultând potențial mutagen. [21] [22] [23]
Expunere
Inhalarea și contactul direct sunt principalele căi de expunere. Unele rapoarte menționează că purtarea mănușilor nu a împiedicat impregnarea aziridinei. Prin urmare, este important ca utilizatorii să monitorizeze cu atenție duratele de pătrundere a mănușilor și să evite contaminarea atunci când tratează leziunile provocate de glitch. Se așteaptă ca lucrătorii care manipulează azidirină să aibă și trebuie să poarte și să utilizeze un aparat de protecție cu filtru pe jumătate de față pentru praf, ceați și vapori. [24]
Există relativ puține date despre expunerea umană la aziridină. Acest lucru se datorează faptului că este considerat extrem de periculos. În mediile industriale, costumele de presiune de clasă A sunt preferate atunci când există potențial de expunere.
Cancerogenitate
IARC a examinat compușii aziridinici și i-a clasificat ca posibili agenți cancerigeni pentru oameni ( IARC Group 2B ). [25] În evaluarea generală, grupul de lucru IARC a subliniat că aziridina este un agent de alchilare cu acțiune directă și este mutagenă într-o gamă largă de sisteme de testare și formează aducti ADN care sunt promutagenici.
- Iritarea
Aziridinele sunt iritante pentru suprafețele mucoasei, inclusiv ochii, nasul, căile respiratorii și pielea.
- Sensibilizarea
Aziridina pătrunde rapid în piele la contact.
- Sensibilizant al pielii - provoacă dermatită alergică de contact și urticarie .
- Sensibilizator respirator - cauza astmului profesional.
Notă
- ^ Aziridină , în Reevaluarea unor substanțe chimice organice, hidrazină și peroxid de hidrogen , monografii IARC privind evaluarea riscurilor cancerigene pentru oameni, vol. 71, 1999.
- ^(RO) Ghid de buzunar pentru pericolele chimice , NIOSH .
- ^ (EN) Weast, RC (eds), Handbook of Chemistry and Physics, 59ed, West Palm Beach ( FL , SUA), CRC Press , 1978, ISBN 0-8493-0459-8 .
- ^(EN) TL Gilchrist, Chimie heterociclică, ISBN 0-582-01421-2 .
- ^(EN) Albert Padwaa; S. Shaun Murphreeb, Epoxides and aziridines - A mini review , Arkivoc (JC-1522R) pp 6-33.
- ^ ( EN ) M. Antonietta Loreto; Lucio Pellacani; Paolo A. Tardella; Elena Toniato, Reacții de adăugare a ionului etoxicarbonilnitren și etoxicarbonil nitreniu la eteri alilici , în Tetrahedron Letters , vol. 25, nr. 38, 1984, pp. 4271-4, DOI : 10.1016 / S0040-4039 (01) 81414-3 .
- ^ (EN) Ryan Hili; Andrei K. Yudin, Aminoaldehidele neprotejate disponibile în J. Am. Chem. Soc. , Voi. 128, nr. 46, 2006, pp. 14772–3, DOI : 10.1021 / ja065898s .
- ^ (EN) B. Pulipaka; Stephen C. Bergmeier, Synthesis of Hexahydro -1 H-benzo [c] chromen-1-amines via Intramolecular Ring-Opening Reof Aziridines by π-Nucleophiles , în Synthesis , vol. 2008, nr. 9, 2008, pp. 1420-30, DOI : 10.1055 / s-2008-1072561 .
- ^ Hoch, Compt. rend., 196, 1865 ( 1934 ); (a), ibid., aOS, 799 (1936); (e), ibidem, 204, 358 (1937).
- ^ (EN) Kenneth N. Campbell; James F. Mckenna, Acțiunea reactivilor Grignard asupra oximelor. . Acțiunea bromurii de fenilmagneziu asupra cetoximelor mixte , în J. Org. Chem. , vol. 4, nr. 2, 1939, pp. 198-205, DOI : 10.1021 / jo01214a012 .
- ^ (EN) Kenneth N. Campbell; Barbara Knapp Campbell; Elmer Paul Chaput, Reacția reactivilor Grignard cu oxime. ii. Acțiunea reactivilor aryl grignard cu cetoxime mixte , în J. Org. Chem. , vol. 8, nr. 1, 1943, pp. 99-102, DOI : 10.1021 / jo01189a015 .
- ^ (EN) Kenneth N. Campbell; Barbara K. Campbell; James F. Mckenna; Elmer Paul Chaput, Acțiunea reactivilor Grignard asupra oximelor. iii. Mecanismul acțiunii halogenurilor de arilmagneziu asupra ketoximelor mixte. O nouă sinteză a etileniminelor , în J. Org. Chem. , vol. 8, 1943, pp. 103-9, DOI : 10.1021 / jo01189a016 .
- ^ (EN) Jat Jawahar L.; Paudyal Mahesh P.; Gao Hongyin; Xu Qing-Long; Yousufuddin Muhammed; Devarajan Deepa; Ess Daniel H.; Kürti László; Falck John R., Sinteza directă stereospecifică a aziridinelor NH și N-Me neprotejate din Olefins , în Știință , vol. 343, nr. 6166, 2014, pp. 61-65, DOI : 10.1126 / science.1245727 , ISSN 0036-8075 , PMID 24385626 , PMC 4175444 .
- ^ (EN) Yuhei Fukuta; Tsuyoshi Mita; Nobuhisa Fukuda; Motomu Kanai; Masakatsu Shibasaki, De Novo Synthesis of Tamiflu via a Catalytic Asymmetric Ring-Opening of mezo-Aziridines with TMSN3 , în J. Am. Chem. Soc. , Voi. 128, nr. 19, 2006, pp. 6312-3, DOI : 10.1021 / ja061696k .
- ^ Catalizatorul se bazează pe itriu cu trei substituenți izopropiloxi și ca ligand o oxifosfină (Ph = fenil ), cu un exces enantiomeric (ee) de 91%.
- ^ (EN) Harold W. Heine; Richard Peavy, Aziridines XI. Reacția 1,2,3-trifenilaziridinei cu dietilacetilen dicarboxilat și anhidridă maleică , în Tetrahedron Letters , vol. 6, nr. 35, 1965, pp. 3123-6, DOI : 10.1016 / S0040-4039 (01) 89232-7 .
- ^ (EN) Albert Padwa; Lewis Hamilton, Reacțiile aziridinelor cu dicarboxilat de dimetilacetilenă , în Tetrahedron Letters , vol. 6, nr. 48, 1965, pp. 4363-7, DOI : 10.1016 / S0040-4039 (00) 71101-4 .
- ^ (EN) Philippe Dauban; Guillaume Malik, Un 1,3-dipol mascat dezvăluit din aziridine , în Angew. Chem. Ed. Int. , Vol. 48, nr. 48, 2009, pp. 9026-9, DOI : 10.1002 / anie.200904941 , PMID 19882612 .
- ^ (EN) Ioana Ungureanua; Cristian Bologab; Saïd Chayera; André Mann, Fenilaziridina ca 1,3-dipol. Aplicarea la sinteza pirolidinelor funcționalizate , în Tetrahedron Letters , vol. 40, nr. 29, 1999, pp. 5315-8, DOI : 10.1016 / S0040-4039 (99) 01002-3 .
- ^ (EN) Aravinda B. Pulipaka; Stephen C. Bergmeier, A Synthesis of 6-Azabicyclo [3.2.1] octanes. Rolul substituției N , în J. Org. Chem. , vol. 73, nr. 4, 2008, pp. 1462-7, DOI : 10.1021 / jo702444c .
- ^ (EN) Kanerva L, H Keskinen, Autio P, T Estlander, Tuppurainen M, R Jolanki, Sensibilizarerespiratorie și cutanată profesională Cauzatăde întăritorul polifuncțional aziridinic , în Clin. Exp. Alergie. , vol. 25, nr. 5, 1995, pp. 432-9, DOI : 10.1111 / j.1365-2222.1995.tb01074.x , PMID 7553246 .
- ^ (EN) Sartorelli P, P Pistolesi, Cioni F, R Naples, Sisinni AG, Bellussi L, Passali GC, Cherubini Di Simplicio E, L Flori, Boală alergică cutanată și respiratorie cauzată de aziridine polifuncționale, în Med. Lav. , vol. 94, nr. 3, 2003, pp. 285-95, PMID 12918320 .
- ^ (EN) Mapp CE, agenți, vechi și noi, care provoacă astm profesional în Occup. Mediu Med. , Vol. 58, nr. 5, 2001, pp. 354-60, DOI : 10.1136 / oem . 58.5.354 , PMID 11303086 , PMC 1740131 .
- ^(RO) Anexa E Cerințe de respirator OSHA pentru substanțe chimice selectate , NIOSH .
- ^ (EN) Some Aziridines, N-, S- and O-Mustards and Selenium (PDF), în monografiile IARC privind evaluarea riscurilor cancerigene pentru oameni, vol. 9, IARC , 1975, ISBN 92-832-1209-6 . Adus la 6 iunie 2019 (depus de „Adresa URL originală la 14 noiembrie 2009).
Elemente conexe
- Etilenimină binară , o formă dimerică de aziridină
- Azirina
- Diazirină
- Diaziridină
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe aziridină
Wikimedia Commons conține imagini sau alte fișiere pe aziridină