Dioxid de plutoniu
| Dioxid de plutoniu | |
|---|---|
| Caracteristici generale | |
| Formula moleculară sau brută | PuO 2 |
| Masa moleculară ( u ) | 276.06 |
| Aspect | solid cristalin galben maro |
| numar CAS | |
| Numărul EINECS | 235-037-3 |
| PubChem | 9795444 |
| ZÂMBETE | [Pu+4].[O-2].[O-2] |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 11.5 |
| Solubilitate în apă | insolubil |
| Temperatură de topire | 2400 ° C (2673,15 K) |
| Temperatura de fierbere | 2800 ° C (3073,15 K) |
| Informații de siguranță | |
Dioxidul de plutoniu este un compus chimic cu formula PuO 2 . Este un înalt -melting solid , care este unul dintre principalii compuși de plutoniu . Culoarea sa poate varia de la galben la verde măslin, în funcție de mărimea particulelor, de temperatură și de metoda de producție. [1]
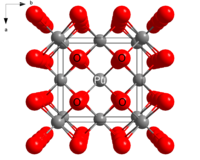
Structura
PuO 2 cristalizează în sistemul caracteristic de cristal al fluoritei , cu centrele Pu 4+ într-un sistem cubic centrat pe față și ioni de oxid care ocupă golurile tetraedrice. [2] Dioxidul de plutoniu este utilizat ca combustibil nuclear datorită faptului că golurile octaedrice permit găzduirea produselor de fisiune fără ruperea structurii materialului.
Sinteză
Plutoniul metalic se oxidează spontan la PuO 2 în prezența oxigenului . Dioxidul de plutoniu este produs în principal prin calcinarea oxalatului de plutoniu (IV), Pu (C 2 O 4 ) 2 · 6H 2 O, la 300 ° C. Oxalatul de plutoniu se obține în timpul procesării combustibilului nuclear.
Aplicații
Dioxidul de plutoniu este utilizat în MOX ca combustibil pentru reactoarele nucleare . Dioxidul de plutoniu-238 este utilizat ca sursă de energie pentru sondele spațiale, cum ar fi New Horizons . Izotopul se descompune emițând particule α care generează căldură în urma conversiei energiei cinetice în energie termică: puterea specifică a plutoniului-238 este de aproximativ 567 W / kg , care valorează aproximativ 390 W / kg sub formă de dioxid de plutoniu - izotopul de plutoniu-238 nu este niciodată pur, atingând în general o concentrație de 75 până la 80%, cu un conținut adesea de 15 până la 20% de plutoniu-239 și alte câteva actinide .
Această tehnologie are multe avantaje pentru explorarea spațiului, dar continuă să ridice temerile publice cu privire la riscurile de contaminare radioactivă în cazul unui accident în timpul lansării sau în cazul în care aeronava se prăbușește în atmosfera Pământului.
Siguranță
Dioxidul de plutoniu este extrem de toxic pentru oameni, în special prin inhalare. [3] La fel ca toți compușii plutoniului, este supus controlului inerentTratatului de neproliferare nucleară . Datorită descompunerii alfa a plutoniului, PuO 2 , la fel ca toți ceilalți compuși formați de acest element, este cald la atingere.
Notă
- ^ Prelucrarea acidului azotic , Laboratorul Los Alamos. Adus la 12 mai 2011 (arhivat din original la 27 mai 2010) .
- ^ Greenwood, Norman N.; Earnshaw, A. (1984), Chimia elementelor , Oxford: Pergamon, p. 1471, ISBN 0-08-022057-6
- ^ Profil toxicologic pentru plutoniu ( PDF ), la atsdr.cdc.gov , Departamentul SUA pentru Sănătate și Servicii Umane, 27 septembrie 2007. Accesat la 12 mai 2011 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre dioxidul de plutoniu
Wikimedia Commons conține imagini sau alte fișiere despre dioxidul de plutoniu