Chimia nucleară

Chimia nucleară este un domeniu al chimiei care se ocupă de reacțiile care schimbă natura nucleului . Prin reacție chimică înțelegem modificarea legăturilor care țin împreună atomii diferitelor molecule , care reacționează între ele. Fenomenul chimico-fizic studiat de chimia nucleară este radioactivitatea, iar cantitatea fizică corespunzătoare din sistemul internațional este activitatea (unitate de măsură becquerel , Bq; 1 Bq = 1 s -1 = 1 Hz = 1 dezintegrare nucleară pe secundă).
Cu toate acestea, în reacțiile nucleare se schimbă nu numai moleculele și legăturile care le formează, ci și atomii înșiși și nucleii lor. În timp ce fizica nucleară se ocupă mai ales de aspectele energetice și de particulele implicate într-o transformare nucleară, chimia nucleară se concentrează mai degrabă pe sinteza de noi elemente , pe studiul proprietăților nuclidilor radioactivi (caracterizați prin numărul atomic Z și numărul de masă A ), numite izotopi sau izomeri (izotopi egal care diferă doar pentru diferite stare excitată ) dacă acestea aparțin aceluiași element chimic (sau isobars , isotones și isodiverses în alte cazuri) și cu privire la toate aplicațiile posibile teoretice și practice ale fenomen de radioactivitate și la interacțiuni energetice particulare ale nucleului atomic (de exemplu RMN , spectroscopie Mössbauer și spectroscopie de anihilare a pozitronii (PAS)).
Radiochimia , în special, este principala ramură aplicată a chimiei nucleare: se ocupă, în sens larg, de reacțiile chimice care implică utilizarea substanțelor radioactive. Chimia radiofarmaceutică se ocupă de sinteza și caracterizarea compușilor radioactivi pentru utilizare în radiodiagnostic și radioterapie metabolică ( medicină nucleară ). Chimia radiațiilor studiază reacțiile chimice induse de radiațiile ionizante . Chimia atomilor exotici studiază proprietățile și aplicațiile cvasi-atomi, cum ar fi pozitroniul , muoniul , antiatomele . Chimia atomilor transfermici și ultra-grei studiază proprietățile chimice ale elementelor (artificiale) cu numere atomice de la 101 la 118.
Un atom este alcătuit dintr-un nucleu interior compus din protoni și neutroni și un anumit număr de electroni (egal cu cel al protonilor, dacă atomul este neutru). O reacție chimică nucleară determină o variație a numărului de nucleoni , adică de protoni și neutroni (care alcătuiesc nucleul), dintre speciile care iau parte la el. În plus, radiații ionizante , cum ar fi X- raze și raze gamma sunt emise.
În reacțiile nucleare, legea Lavoisier a conservării masei (tipică în locul reacțiilor chimice) nu se aplică, în timp ce legea conservării energiei și legea conservării sarcinii electrice sunt valabile.
Reacțiile nucleare particulare sunt dezintegrările radioactive , fisiunea nucleară , fuziunea nucleară și bombardamentul atomic . Energia solară este un exemplu clasic al energiei nucleare puternice dezvoltată de un astfel de fenomen. Unele reacții nucleare au făcut posibilă investigarea nucleului mai intim (de exemplu, au permis identificarea protonilor și neutronilor) sau crearea artificială a atomilor care nu sunt prezenți în natură. Cantități mici de substanțe radioactive sunt astăzi utilizate pe scară largă în electronică în diverse scopuri.
Reactoarele cu fisiune nucleară exploatează în prezent fisiunea nucleului pentru a produce electricitate și căldură, dar este, de asemenea, de dorit să îl utilizați pentru producerea de hidrogen sau hidricitate (hidricitate). În prezent se lucrează la ingineria industrială a reactoarelor de fuziune nucleară care ar permite în viitor să combine avantajele energiei nucleare cu un nivel foarte ridicat de siguranță operațională (emisia de radiații va fi redusă).
Istorie

După descoperirea de către Wilhelm Röntgen a razelor X , mulți oameni de știință au început să lucreze asupra radiațiilor ionizante . Unul dintre aceștia a fost Henri Becquerel , care a studiat relația dintre fosforescență și impresia plăcilor fotografice . Când Becquerel (care lucrează în Franța ) a descoperit că, fără sursă de energie externă prezentă, uraniul era capabil să genereze raze care ar putea impresiona o placă fotografică, s-a descoperit radioactivitatea. Marie Curie (la Paris ) și soțul ei Pierre Curie au izolat două elemente radioactive noi din minereuri de uraniu. Ei au folosit metode radiometrice pentru a identifica cantitatea de radiație prezentă după fiecare separare chimică; au separat uraniul mineral în fiecare dintre diferitele elemente chimice cunoscute atunci și au măsurat radioactivitatea fiecărei fracții obținute. Apoi au încercat să separe în continuare aceste fracții radioactive, pentru a izola o fracție mai mică cu o activitate specifică ridicată (radioactivitate pe unitate de masă). În acest fel, au izolat poloniul și radiul . În jurul anului 1901 s-a observat că dozele mari de radiații erau capabile să provoace rău oamenilor: Becquerel a dus o probă de radiu cu el în buzunar și datorită dozei mari de radiații localizate la care a fost expus a suferit o arsură la radiații [1 ] care a deschis terenul spre studiul efectelor biologice ale radiațiilor, ceea ce a permis la rândul său dezvoltarea tratamentelor medicale.
Ernest Rutherford , care lucrează în Canada și Anglia , a arătat că dezintegrarea radioactivă poate fi descrisă printr-o ecuație diferențială liniară simplă (o ecuație cinetică de ordinul întâi ), ceea ce implică faptul că o anumită substanță radioactivă are un timp de înjumătățire caracteristic (timpul necesar pentru masa se reduce cu jumătate din valoarea inițială). De asemenea, el a inventat termenii de raze alfa , beta și gamma , a transformat azotul în oxigen și, mai important, a dirijat ceea ce este cunoscut sub numele de experimentul Rutherford, care a arătat că modelul atomic al lui Thomson este greșit. În „modelul panettone”, propus de Thomson în 1904, atomul este compus din electroni înconjurați de un „nor” de sarcini pozitive care echilibrează sarcina negativă a electronilor. Potrivit lui Rutherford, experimentul său a presupus că sarcina pozitivă se afla într-un nucleu foarte mic care duce la modelul atomic Rutherford și ulterior la modelul Bohr , unde nucleul pozitiv este înconjurat de electroni negativi.
În 1934, fiica lui Marie Curie, Irène Joliot-Curie , și soțul ei au fost primii care au creat radioactivitate artificială: au bombardat borul cu particule alfa pentru a crea izotopul 13 7 N ; acest izotop se descompune prin emiterea de pozitroni . [2] În plus, au bombardat aluminiu și magneziu cu neutroni pentru a crea noi radioizotopi .
Reacții nucleare
În reacțiile nucleare , spre deosebire de reacțiile chimice care implică legăturile dintre atomi sau molecule , există o schimbare a naturii nucleului atomic . În astfel de reacții, mai degrabă decât conservarea masei totale, se păstrează conservarea numărului atomic (Z) și a numărului de masă (A). De exemplu, luați în considerare bombardarea azotului -14 cu particule α :
- 14 7 N + 4 2 α → 17 8 O + 1 1 H
se observă că în stânga există un total A egal cu 18 (14 + 4), precum și 18 (17 + 1) printre produsele de reacție. În mod similar, Z-ul total din stânga este 9 (7 + 2) la fel cum este egal cu 9 (8 + 1) pentru produse.
Spectrometria de masă a permis măsurarea cantitativă a defectului de masă , adică cantitatea de masă care a fost convertită în energie prin trecerea de la reactanți la produsele finale ale unei reacții nucleare. Energia corespunzătoare se obține prin aplicarea ecuației lui Einstein E = mc 2 : de exemplu, pentru consumul de 1 u de materie (1,66 · 10 −27 kg ) se calculează o energie egală cu 933 MeV .
Dezintegrarea radioactivă
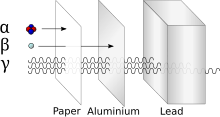
Nuclizii instabili sunt supuși decăderii radioactive . Există în principal trei tipuri de dezintegrare: decăderea α , β și γ .
Dezintegrarea α , caracteristică nucleelor grele care au un număr atomic mai mare de 83 și un număr de masă mai mare de 200, este cauzată de repulsia Coulomb între protoni . În acest tip de decădere se produce o particulă α (de fapt reprezintă un nucleu 4 2 He 2+ ):
- 238 92 U → 234 90 Th + 4 2 α
- 232 90 Th → 228 88 Ra + 4 2 α
Dezintegrarea β implică formarea a două tipuri diferite de particule indicate respectiv β - ( electroni cu energie ridicată) și β + ( pozitroni cu energie ridicată). Dezintegrarea β - apare în principal atunci când raportul dintre neutroni și protoni este foarte mare; un neutron se transformă într-un proton:
- 234 91 Pa → 234 92 U + 0 -1 β -
- 14 6 C → 14 7 N + 0 -1 β -
Dezintegrarea β + este în schimb caracteristică nuclizilor care au un raport foarte scăzut între neutroni și protoni; un proton este transformat în neutron:
- 30 15 P → 30 14 Da + 0 +1 β +
- 11 6 C → 11 5 B + 0 +1 β +
Dezintegrarea β este, de asemenea, însoțită de emisia altor particule, cum ar fi neutrinii .
Dezintegrarea γ produce radiații electromagnetice sub formă de raze γ , cu o lungime de undă de obicei mai mică de 10 −12 m . Un exemplu de procese care conduc la producerea razelor γ se referă la formarea unui nuclid de nichel -60 excitat :
- 60 27 Co → 60 28 Ni * + 0 -1 β - + γ
- 60 28 Ni * → 60 28 Ni + γ
Unii nuclizi, pentru a crește raportul dintre neutroni și protoni, pot duce la captarea unui electron orbitant cu transformarea unui proton în neutron:
- 65 31 Ga + 0 -1 și - → 65 30 Zn
Razele γ reprezintă radiația cu cea mai mare putere de penetrare și din acest motiv sunt cele mai periculoase datorită efectului ionizant pe care îl induc.
Radionuclizii pot genera un lanț de dezintegrare compus dintr-o serie de dezintegrări radioactive, pe o anumită scară de timp, care se încheie cu formarea unui nuclid stabil. De exemplu, seria radium începe de la 238 92 U și se termină cu formarea nucleului de plumb -208.
Cinetica decăderii este de primul ordin și, prin urmare, urmează ecuația unde n este numărul de nuclizi, λ este constanta degradare și t scurs timpul .
Fisiune nucleara

Fisiunea nucleară a fost descoperită de Otto Hahn și asistentul său Fritz Strassmann în 1938 la Berlin-Dahlem ( Institutul de Chimie Kaiser Wilhelm ).
Nucleii mari pot da fisiune spontană sau fisiune nucleară indusă de bombardamentul cu neutroni. In acest proces se formează o serie de nuclee mai mici, de exemplu prin bombardarea uraniu-235 ( fisionabil izotopul uraniului), este posibil să se obțină:
- 235 92 U + 1 0 n → 90 37 Rb + 144 55 Cs + 2 1 0 n
- 235 92 U + 1 0 n → 87 35 Br + 146 57 La + 3 1 0 n
- 235 92 U + 1 0 n → 72 30 Zn + 160 62 Sm + 4 1 0 n
După cum se poate observa din reacții, pornind de la un neutron inițial este produs un număr multiplu de neutroni: aceștia sunt capabili să alimenteze fisiunea unui număr tot mai mare de nuclei de uraniu-235 și, dacă aceștia din urmă sunt prezenți într-o cantitate corespunzătoare critic de masă , poate apărea o reacție în lanț .
Fisiunea controlată a uraniului este utilizată în scopuri civile în producția de energie electrică datorită centralelor nucleare .
Un alt izotop fisibil important este plutoniul -239, care poate fi utilizat în reactoare autofertilizante , dar pe de altă parte are o radioactivitate ridicată care îl face extrem de periculos.
Fuziune nucleară
Cu fuziunea nucleară, nucleele foarte ușoare se combină pentru a forma un nou izotop mai greu. Energia enormă produsă de Soare și alte stele în urma conversiei hidrogenului în heliu se bazează pe acest proces:
- 1 1 H + 1 1 H → 2 1 H + 0 +1 β +
- 2 1 H + 1 1 H → 3 2 He
- 3 2 H + 1 1 H → 4 2 He + 0 +1 β +
al cărui rezultat total este deci
- 4 1 1 H → 4 2 He + 2 0 +1 β +
O reacție de fuziune nucleară a fost reprodusă artificial cu detonarea bombei H , folosind fisiunea ca declanșator . Cercetările actuale vizează posibilitatea de a face practică utilizarea fuziunii în viitoarele centrale nucleare de fuziune , ceea ce ar prezenta printre avantaje formarea izotopilor stabili precum cei ai heliului-4 și posibilitatea utilizării materiilor prime mai disponibile în natură ( gândiți-vă la deuteriul prezent în toată hidrosfera ). Pe de altă parte, temperaturile ridicate necesare pentru a depăși repulsia electrostatică dintre nuclei ( energia barierei ) reprezintă principala problemă în reproducerea procesului de fuziune pe scară largă. O reacție care este studiată pentru aplicarea viitoare este următorul proces în două etape care utilizează deuteriu, tritiu (care poate fi sintetizat din același deuteriu) și litiu :
- 2 1 H + 3 1 H → 4 2 He + 1 0 n
- 2 1 H + 3 1 H → 4 2 He + 1 0 n
Implementarea fuziunii la rece ar depăși problemele asociate cu temperaturile ridicate necesare.
Nucleosinteza elementelor
Teoriile științifice moderne afirmă că la câteva ore după Big Bang, temperatura a scăzut suficient pentru a permite condensarea norilor de hidrogen și heliu odată cu formarea primelor stele . Influența gravitației ar fi creat în interiorul lor valori ale temperaturii și densității atât de mari încât să permită procesele de fuziune nucleară. În special, s-a observat că atunci când nucleele ușoare fuzionează pentru a forma elemente cu un număr atomic mai mic sau egal cu 26, un număr atomic corespunzător fierului și care identifică nivelul maxim de stabilitate energetică a unui nucleu, energia este eliberată: acest proces se numește combustie.elementele nucleare și formate constituie „cenușa de ardere” (arderea nucleară nu trebuie confundată cu arderea chimică ).
Ciclul heliului constă dintr-un ciclu de ardere nucleară care folosește 4 2 nuclee He ( particule α ). De exemplu, izotopul carbonului 12 16 C este obținut ca urmare a unor astfel de reacții
- 4 2 He + 4 2 He → 8 4 Be + γ
- 8 4 Fie + α → 12 6 C + γ
Elementele foarte ușoare precum litiu , beriliu și bor nu sunt produse finale stabile ale ciclului heliului. Mai degrabă, se crede că acestea sunt produse ca rezultat al proceselor umărului prin impactul cu particule de mare energie.
Pe de altă parte, nucleosinteza elementelor mai grele implică o varietate de procese în care intră în joc captarea și decăderea neutronilor. De exemplu, neutronii rezultați din reacțiile nucleare ale elementelor mai ușoare, ca în
- 23 10 Ne + α → 26 12 Mg + 1 0 n
pot genera o serie de reacții care, de exemplu, pot duce la formarea nucleului copil 99 43 Tc:
- 98 42 Mo + 1 0 n → 99 42 Mo + γ
- 99 42 Mo → 99 43 Tc + 0 -1 β + ν ( neutrino )
O supernova reprezintă o sursă naturală de flux intens de neutroni.
Prin exploatarea acceleratorilor puternici de particule și a reacțiilor de bombardare induse artificial (a se vedea bombardamentul atomic ), este posibilă realizarea nucleosintezei artificiale prin obținerea de noi izotopi care nu sunt prezenți în natură, izotopii având fiecare un nivel diferit de stabilitate și sintetizând noi elemente a căror existență este prima postulat din studii teoretice.
Sinteza elementelor transuranice
Elementele transuranice sunt definite ca o serie de elemente chimice ulterioare uraniului din tabelul periodic , adică care au un număr atomic mai mare de 92. Ele reprezintă o clasă importantă de elemente sintetice a căror chimie este un obiect de studiu care se încadrează în domeniul de aplicare de chimie nucleară. Primele două elemente transuranice, neptuniul (PA 93) și plutoniul (PA 94), au fost sintetizate în 1940, deschizând câmpul către teoriile și descoperirile ulterioare care au făcut posibilă sintetizarea elementelor prevăzute anterior doar la nivel teoretic.
Edwin McMillan și Philip Hauge Abelson au sintetizat neptuniul bombardând uraniul cu neutroni lenti:
- 238 92 U + 1 0 n → 239 92 U + γ
- 239 92 U (t 1/2 = 23,5 min) → 239 93 Np + β -
Următorul element, plutoniul, a fost sintetizat de Glenn T. Seaborg , Edwin M. McMillan , JW Kennedy și AC Wahl prin bombardarea uraniului cu un deuteron :
- 238 92 U + 2 1 H → 238 93 Np + 2 1 0 n
- 238 93 Np (t 1/2 = 2,12 zile) → 238 94 Pu + β -
Până în 1970 s-a crezut că elementele tabelului periodic care ar putea fi sintetizate în practică ar putea atinge o greutate atomică de aproximativ 108, datorită timpului de înjumătățire foarte scurt teoretizat pentru elementele mai grele. Cu toate acestea, teoriile ulterioare au prezis stabilitatea particulară a anumitor elemente cu un număr bine determinat de protoni și neutroni, așa-numitul număr magic . De exemplu, nucleul cu 114 protoni și 184 neutroni ( 238 Fl ) s-ar bucura de o stabilitate deosebită în ciuda dimensiunii sale. Aceste tipuri de elemente sunt denumite elemente super-grele .
Izotopi
Pentru o descriere generală a izotopilor, consultați tabelul cu izotopi .
Efecte izotopice
Efectele izotopului constau dintr-o serie de efecte observate atunci când un izotop este încorporat într-un compus chimic pentru a înlocui un atom al aceluiași element . Izotopii aceluiași element chimic posedă proprietăți chimice aproape identice, dar efectul izotopic este capabil să influențeze echilibrul chimic sau viteza de reacție în urma modificării proprietăților vibraționale și rotaționale ale moleculei.
Având în vedere reacția generică de schimb de izotopi
- AX + BX * AX * + BX
echilibrul va fi mai diferit în funcție de întinderea efectului izotopic, efect care poate fi neglijat atunci când numărul atomic este mai mic de 10. [3] De exemplu, prin înlocuirea unui izotop unchi-mare în apă cu unul de deuteriu prin reacția
- H 2 H (g) + H 2 O (l) H 2 (g) + 2 HOH (l)
există o deplasare marcată spre dreapta în raport cu cazul în care X = X *. Un efect izotop minor asupra echilibrului este observat prin schimbul de carbon-12 și carbon-14.
Efectul izotop care afectează viteza de reacție este cunoscut sub numele de efect izotop cinetic . Acest efect este exploatat în studiul mecanismelor de reacție prin analiza variației vitezei de reacție. Diferita energie vibrațională a legăturii care implică cei doi izotopi, de exemplu o legătură CH și o legătură C- 2 H, datorită diferitelor mase, are ca rezultat o energie de activare diferită asociată cu ruperea legăturii, ultima cerință necesară pentru formează un nou compus. În cazul exemplului citat, energia de activare pentru scindarea legăturii C- 2 H este mai mare decât cea pentru scindarea legăturii CH, astfel încât acesta din urmă este favorizat cinetic; divizarea legăturii dintre carbon și deuteriu este un proces mai lent.
Acestea doar enumerate sunt efecte izotopice chimice. Există, de asemenea, efecte izotopice fizice, cum ar fi viteza de revărsare diferită sau presiunea de vapori diferită.
Separarea chimică a izotopilor
Izotopii diferitelor elemente chimice, prezente în amestec , pot fi separate prin diferite metode chimice. De exemplu, este posibil să se efectueze o reacție chimică care tinde să formeze un compus mai volatil, pentru a putea ulterior să-l separe cu ușurință. Alte metode utilizează electroliza , extragerea solventului , schimbul de ioni și precipitarea .
Pe de altă parte, atunci când este necesar să separați doi izotopi ai aceluiași element, cum ar fi cei produși prin bombardarea cu neutroni și emisia γ (n, γ), nu este posibil să se utilizeze metode chimice bazate pe diferitele proprietăți chimice. Se folosește apoi efectul Szilard - Chalmers : [4] dacă reacția nucleară este însoțită de clivajul homolitic al legăturii chimice , cauzat de radiația γ emisă, radicalii izotopului produs pot fi separați de izotopul țintă. Luați în considerare, de exemplu, formarea izotopului de iod 128 53 I pornind de la bombardamentul de 127 53 I prezent sub formă de iodură de etil : se produc radicali iod-128 care se combină pentru a forma molecula de iod 128 53 I 2 , care poate fi separat de iodura de etil prin reducere cu sulfit de sodiu în soluție apoasă .
Ciclul combustibilului nuclear

Chimia nucleară este implicată activ în studiul și aplicarea tuturor operațiunilor implicate în producția de combustibil nuclear , de la exploatare până la prelucrarea și îmbogățirea minereului pentru a obține combustibilul final.
Îmbogățirea este faza ciclului combustibilului nuclear care vizează creșterea conținutului de izotop fisionabil , adică izotopul care poate fi exploatat în mod util pentru fisiunea nucleară . În cazul uraniului, este vorba de creșterea conținutului de uraniu-235 și de a proceda la separarea ulterioară de izotopul de uraniu-238, care constituie materia primă (a se vedea uraniul îmbogățit pentru informații suplimentare).
Un alt obiect de interes este, de asemenea, gestionarea combustibilului uzat și reprocesarea acestuia. PUREX ( recuperarea plutoniului și uraniului prin extracție) este metoda actuală de alegere care permite recuperarea, după obținerea nitraților respectivi prin tratarea cu soluție de acid azotic , a uraniului și plutoniului din combustibilul epuizat prin exploatarea unei extracții lichid-lichid cu un amestec de tributil fosfat - kerosen și separarea chimică ulterioară a celor două elemente.
Ramuri ale chimiei nucleare
Radiochimie
Radiochimia este ramura chimiei nucleare care exploatează radioactivitatea și folosește substanțe radioactive în reacțiile chimice . Un domeniu vast al acestei discipline se referă la metode radioanalytical, care folosesc de obicei activare cu neutroni , diluție a izotopilor și radiochimice titrari pentru determinări cantitative ale analiților . Datarea radiometrică, pe de altă parte, vă permite să datați un eșantion exploatând cinetica decăderii radioactive. Radiochimia se aplică și studiului echilibrului chimic și al cineticii chimice . Radioterapia și radiodiagnosticul utilizează substanțe radioactive.
Chimia radiațiilor
Chimia radiațiilor este ramura chimiei nucleare care studiază efectele chimice ale radiațiilor ionizante asupra materiei . Radiațiile ionizante pot interacționa pentru a forma specii foarte reactive, cum ar fi electronele solvatate , ionii și radicalii liberi . De exemplu prin iradiere în acest l ', astfel se formează apă , printr-o succesiune de reacții, specii precum H 2 O +, · OH și H · O ·. Înțelegerea acestui tip de fenomene chimice induse este utilă în căutarea de noi căi de sinteză și în studiul daunelor biologice datorate expunerii la radiații.
Notă
- ^ WCG Peh, Descoperirea radioactivității și radiului , Singapore Med J 1996; Vol 37: 627-630 [1]
- ^(EN) Biografie pe nobelprize.org
- ^ Loveland, Morrissey, Seaborg , p.106
- ^ Leo Szilard, TA Chalmers, Separarea chimică a elementului radioactiv de izotopul său bombardat în efectul Fermi , în natură , vol. 134, 1934, pp. 462-462, DOI : 10.1038 / 134462b0 .
Bibliografie
- V. Loveland, DJ Morrissey; GT Seaborg, Chimie nucleară modernă , John Wiley & Sons, 2006, ISBN 978-0-471-11532-8 .
Elemente conexe
linkuri externe
- ( EN ) Division of Nuclear and Radiochemistry of EuCheMS , la euchems.org . Adus la 6 decembrie 2006 (arhivat din original la 19 noiembrie 2006) .
- ( EN ) International Nuclear Chemistry Society (INCS) , pe incs.ege.edu.tr.
- ( EN )Journal of Radioanalytical and Nuclear Chemistry , la springerlink.metapress.com .
- ( RO ) IUPAC Gold Book, „chimie nucleară” , pe goldbook.iupac.org .
| Controlul autorității | Tezaur BNCF 18799 · LCCN (EN) sh85092951 · GND (DE) 4138530-5 · NDL (EN, JA) 00.576.324 |
|---|