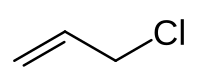
Clorură de alil
| Clorură de alil | |
|---|---|
| Numele IUPAC | |
| 3-cloropropen | |
| Denumiri alternative | |
| 1-clor-2-propenă | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 3 H 5 CI |
| Masa moleculară ( u ) | 76,53 |
| Aspect | lichid incolor |
| numar CAS | |
| Numărul EINECS | 203-457-6 |
| PubChem | 7850 |
| ZÂMBETE | C=CCCl |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 0,94 [1] |
| Solubilitate în apă | 3,6 g / L (20 ° C) [1] |
| Temperatură de topire | –136 ° C [1] |
| Temperatura de fierbere | 45 ° C [1] |
| Presiunea de vapori ( Pa ) la 293 K. | 398 mbar [1] |
| Proprietăți toxicologice | |
| LD 50 (mg / kg) | 460 (șobolan oral) [1] |
| Informații de siguranță | |
| Punct de flacără | –27 ° C [1] |
| Limite de explozie | 3,2-11,2% [1] |
| Temperatură de autoaprindere | 390 ° C [1] |
| Simboluri de pericol chimic | |
    | |
| Pericol | |
| Fraze H | 225 - 301 - 311 - 331 - 315 - 319 - 335 - 372 - 341 - 351 - 400 [1] |
| Sfaturi P | 210 - 233 - 273 - 280 - 302 + 350 - 305 + 351 + 338 - 309 + 311 [1] |
Clorura de alil este compusul organic clorurat având formula CH2 = CHCH2- CI. Este un lichid incolor cu miros neplăcut de muștar, nu foarte solubil în apă, dar solubil în solvenți organici obișnuiți. Se obține din propilenă și este utilizat în principal pentru sintetizarea epiclorhidrinei .
fundal
Clorura de alil a fost obținută pentru prima dată în 1857 de Auguste André Thomas Cahours și August Wilhelm von Hofmann prin reacția alcoolului alilic și a triclorurii de fosfor . [2]
Producție
Clorura de alil este preparată industrial prin reacția dintre propilenă și clor . La temperaturi mai scăzute, se formează în principal 1,2-dicloropropan , dar la 300-500 ° C principalul produs este clorura de alil:
Reacția se desfășoară cu un mecanism radical . În 1997, producția a fost de aproximativ 850.000 de tone. [2]
Reactivitate
Clorura de alil este un compus foarte reactiv, deoarece conține atât o legătură dublă , care poate da reacțiile obișnuite de adăugare și polimerizare , cât și un atom de clor care poate fi ușor înlocuit cu alte grupuri funcționale .
Aplicații
Majoritatea clorurii de alil este utilizată pentru a sintetiza epiclorhidrina . Alți derivați de importanță comercială includ alcool alilic , alilamină , izotiocianat de alil (ulei de muștar sintetic) și alil silan .
În laborator, clorura de alil este utilizată pentru proprietățile sale de alchilare , utile în sinteza medicamentelor și pesticidelor. Exemple sunt cianarea în cianură de alil (CH 2 = CHCH 2 CN), cuplarea [3] reductivă la dialil, adăugarea oxidativă la paladiu pentru a obține dimerul de clorură de alilpaladiu (C 3 H 5 ) 2 Pd 2 Cl 2 și dehidrohalogenarea în ciclopropen .
Informații privind toxicitatea / siguranța
Clorura de alil este un compus volatil și foarte inflamabil. Este toxic prin ingestie, inhalare și contact cu pielea. Provoacă iritarea ochilor, pielii și a căilor respiratorii. Este suspectat de cancerigen și mutagen. Este foarte periculos pentru organismele acvatice. [1]
Notă
Bibliografie
- GESTIS, clorură de alil , pe gestis-en.itrust.de . Adus pe 5 martie 2015 . Pagina clorurii de alil din baza de date GESTIS.
- ( EN ) L. Krähling, J. Krey și G. Jakobson, Allyl Compounds , în Ullmann's Encyclopedia of Industrial Chemistry , Wiley-VCH, 2000, DOI : 10.1002 / 14356007.a01_425 .
- ( EN ) JV Supniewski și PL Salzberg, cianură de alil , în Org. Sintetizator. , vol. 8, 1928, p. 4, DOI : 10.15227 / orgsyn.008.0004 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre clorură de alil
Wikimedia Commons conține imagini sau alte fișiere despre clorură de alil
| Controlul autorității | GND ( DE ) 4432944-1 |
|---|