Stări de oxidare a elementelor chimice
Salt la navigare Salt la căutare
Aceasta este o listă cu toate stările de oxidare ale elementelor chimice , excluzând valorile nesigure. Sunt evidențiate cele mai frecvente stări de oxidare. Acest tabel se bazează pe unul din Greenwood, [1] . Starea de oxidare 0, pe care o găsim pentru toate elementele, corespunde coloanei de simboluri chimice. Formatul tabelului, bazat pe o uniformă de la Mendeleev în 1889 , evidențiază „legile” tabelului periodic .
| −1 | H. | +1 | |||||||||||
| El | |||||||||||||
| −1 | Acolo | +1 | |||||||||||
| Bine | +2 | ||||||||||||
| B. | +1 | +2 | +3 | ||||||||||
| −4 | −3 | −2 | −1 | C. | +1 | +2 | +3 | +4 | |||||
| −3 | −2 | −1 | Nu. | +1 | +2 | +3 | +4 | +5 | |||||
| −2 | −1 | SAU | +1 | +2 | |||||||||
| −1 | F. | ||||||||||||
| Nici | |||||||||||||
| −1 | N / A | +1 | |||||||||||
| Mg | +2 | ||||||||||||
| Pentru | +1 | +3 | |||||||||||
| −4 | −3 | −2 | −1 | da | +1 | +2 | +3 | +4 | |||||
| −3 | −2 | −1 | P. | +1 | +2 | +3 | +4 | +5 | |||||
| −2 | −1 | S. | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| −1 | Cl | +1 | +2 | +3 | +4 | +5 | +6 | +7 | |||||
| Ar | |||||||||||||
| K. | +1 | ||||||||||||
| Aproximativ | +2 | ||||||||||||
| Sc | +1 | +2 | +3 | ||||||||||
| −1 | Tu | +2 | +3 | +4 | |||||||||
| −1 | V. | +1 | +2 | +3 | +4 | +5 | |||||||
| −2 | −1 | Cr | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| −3 | −2 | −1 | Mn | +1 | +2 | +3 | +4 | +5 | +6 | +7 | |||
| −2 | −1 | Fe | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| −1 | Co | +1 | +2 | +3 | +4 | +5 | |||||||
| −1 | Ni | +1 | +2 | +3 | +4 | ||||||||
| Cu | +1 | +2 | +3 | +4 | |||||||||
| Zn | +2 | ||||||||||||
| Ga | +1 | +2 | +3 | ||||||||||
| −4 | GE | +1 | +2 | +3 | +4 | ||||||||
| −3 | La fel de | +2 | +3 | +5 | |||||||||
| −2 | De sine | +2 | +4 | +6 | |||||||||
| −1 | Fr | +1 | +3 | +4 | +5 | +7 | |||||||
| Kr | +2 | ||||||||||||
| Rb | +1 | ||||||||||||
| Sr. | +2 | ||||||||||||
| Da | +2 | +3 | |||||||||||
| Zr | +1 | +2 | +3 | +4 | |||||||||
| −1 | Nb | +2 | +3 | +4 | +5 | ||||||||
| −2 | −1 | Mo | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| −3 | −1 | Tc | +1 | +2 | +3 | +4 | +5 | +6 | +7 | ||||
| −2 | Ru | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | ||||
| −1 | Rh | +1 | +2 | +3 | +4 | +5 | +6 | ||||||
| Pd | +2 | +4 | |||||||||||
| Ag | +1 | +2 | +3 | ||||||||||
| CD | +2 | ||||||||||||
| În | +1 | +2 | +3 | ||||||||||
| −4 | Sn | +2 | +4 | ||||||||||
| −3 | Sb | +3 | +5 | ||||||||||
| −2 | Tu | +2 | +4 | +5 | +6 | ||||||||
| −1 | THE | +1 | +3 | +5 | +7 | ||||||||
| Xe | +2 | +4 | +6 | +8 | |||||||||
| Cs | +1 | ||||||||||||
| Ba | +2 | ||||||||||||
| Acolo | +2 | +3 | |||||||||||
| Există | +2 | +3 | +4 | ||||||||||
| Relatii cu publicul | +2 | +3 | +4 | ||||||||||
| Nd | +2 | +3 | |||||||||||
| P.m | +3 | ||||||||||||
| Sm | +2 | +3 | |||||||||||
| Eu | +2 | +3 | |||||||||||
| Doamne | +1 | +2 | +3 | ||||||||||
| Tb | +1 | +3 | +4 | ||||||||||
| Dy | +2 | +3 | |||||||||||
| eu am | +3 | ||||||||||||
| Er | +3 | ||||||||||||
| Tm | +2 | +3 | |||||||||||
| Yb | +2 | +3 | |||||||||||
| lu | +3 | ||||||||||||
| Hf | +2 | +3 | +4 | ||||||||||
| −1 | Ta | +2 | +3 | +4 | +5 | ||||||||
| −2 | −1 | W | +1 | +2 | +3 | +4 | +5 | +6 | |||||
| −3 | −1 | rege | +1 | +2 | +3 | +4 | +5 | +6 | +7 | ||||
| −2 | Os | +1 | +2 | +3 | +4 | +5 | +6 | +7 | +8 | ||||
| −1 | Ir | +1 | +2 | +3 | +4 | +5 | +6 | ||||||
| Pt | +2 | +4 | +5 | +6 | |||||||||
| −1 | Au | +1 | +2 | +3 | |||||||||
| Hg | +1 | +2 | +4 | [2] | |||||||||
| Tl | +1 | +3 | |||||||||||
| −4 | Pb | +2 | +4 | ||||||||||
| −3 | Bi | +3 | +5 | ||||||||||
| −2 | Pic | +2 | +4 | +6 | |||||||||
| −1 | La | +1 | +3 | +5 | +7 | ||||||||
| Rn | |||||||||||||
| Pr | +1 | ||||||||||||
| Ra | +2 | ||||||||||||
| B.C | +3 | ||||||||||||
| Th | +2 | +3 | +4 | ||||||||||
| Pa | +3 | +4 | +5 | ||||||||||
| U | +3 | +4 | +5 | +6 | |||||||||
| Np | +3 | +4 | +5 | +6 | +7 | ||||||||
| Pu | +3 | +4 | +5 | +6 | +7 | ||||||||
| A.m | +2 | +3 | +4 | +5 | +6 | ||||||||
| Cm | +3 | +4 | |||||||||||
| Bk | +3 | +4 | |||||||||||
| Cf | +2 | +3 | +4 | ||||||||||
| Ex | +2 | +3 | |||||||||||
| Fm | +2 | +3 | |||||||||||
| Md | +2 | +3 | |||||||||||
| Nu | +2 | +3 | |||||||||||
| Lr | +3 | ||||||||||||
| Rf | +4 |
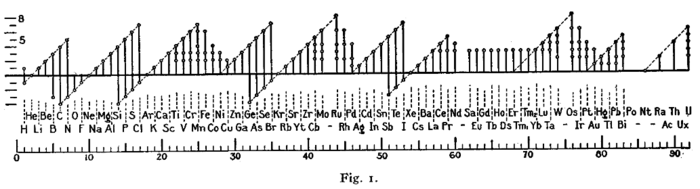
O figură cu un format similar (a se vedea imaginea) a fost folosită de Irving Langmuir în 1919 într-una din primele foi din Regula Octetului . [3] Periodicitatea stărilor de oxidare a fost unul dintre motivele evidente care l-au determinat pe Langmuir să adopte regula.
Notă
- ^ (EN) Neil Norman Greenwood și Alan Earnshaw, Chimia elementelor , ediția a II-a, Oxford , Butterworth-Heinemann, 1997, p. 28 , ISBN 0-7506-3365-4 .
- ^ Hg 4+ a fost observat la Tetrafluorură de mercur Xuefang Wang, Lester Andrews; Sebastian Riedel; și Martin Kaupp, Mercurul este un metal de tranziție: prima dovadă experimentală pentru HgF 4 . , în Angew. Chem. Ed. Int. , Vol. 46, nr. 44, 2007, pp. 8371–8375, DOI : 10.1002 / an.200703710 . .
- ^ (EN) Irving Langmuir , Aranjamentul electronilor în atomi și molecule, J. Am. Chem. Soc., 1919 41, pp. 868-934, DOI : 10.1021 / ja02227a002 .