CCR5
| Receptor CC pentru chemokine de tip 5 | |
|---|---|
| Structura CCR5 | |
| Gene | |
| HUGO | CCR5 CC-CKR-5; CCCKR5; CCR-5; CD195; CKR-5; CKR5; CMKBR5; IDDM22 |
| Locus | Chr. 3 p21.31 |
| Proteină | |
| UniProt | P51681 |
CCR5 , acronim pentru receptorul chemokinei CC tip 5 (receptor CC pentru chemokinele tip 5) și cunoscut și sub numele de CD195 , este o proteină prezentă pe membrana leucocitelor și implicată în sistemul imunitar ca receptor pentru chemokine , cu rolul de a atrage în anumite țesuturi și organe limfocitele T. Multe forme de HIV , virusul responsabil de SIDA , utilizează acest receptor în stadiile incipiente pentru a intra în celulele care urmează să fie infectate. Există indivizi care poartă o anumită mutație genetică , CCR5-Δ32, care îi protejează de infecția cu aceste forme virale.
La acești subiecți, gena CCR5 , localizată pe cromozomul 3 , este mutată prin ștergerea unei anumite porțiuni din materialul genetic; formele homozigote , adică subiecții care au ambele alele mutante, sunt rezistente la tulpinile virale tropicale HIV-1 R5 [1] .
Funcţie
CCR5 aparține familiei de receptori ß pentru chemokine și este o proteină membranară integrală [2] [3] . Este un receptor cuplat cu proteina G și leagă în mod specific familia chemokinelor CC [2] .
Liganzii naturali ai receptorului sunt RANTES , un factor chemotactic cunoscut și sub denumirea de CCL5 [4] [5] [6] și MIP ( proteină inflamatorie a macrofagelor ) 1 α și 1 β , cunoscută și sub denumirea de CCL3 și respectiv CCL4 . De asemenea, interacționează cu CCL3L1 [5] [7] .
Gena este exprimată mai ales în limfocite T , macrofage , celule dendritice și microglie și , deși rolul său exact în funcția imună normală nu a fost elucidat, se crede că joacă un rol în răspunsul inflamator la infecții.
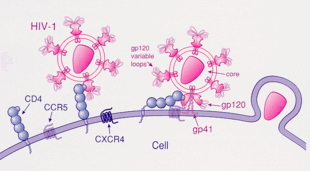
1) Proteina virală gp120 se leagă de CD4
2) Regiunea variabilă a gp120 leagă coreceptorul, de obicei CCR5 sau CXCR4
3) HIV intră în celulă
Rolul în infecția cu HIV
Coreceptorii pe care HIV îi utilizează pentru intrarea sa în celule sunt CCR5 și / sau CXCR4 ; deși numeroși receptori care chemokinele pot acționa ca coreceptori virali, CCR5 este cel mai important în istoria naturală a infecției. Liganzii săi fiziologici sunt RANTES , MIP-1 β și MIP-1 α , care sunt capabili să elimine infecția cu HIV-1 in vitro . La subiecții infectați cu HIV, tulpinile care utilizează CCR5 pentru intrarea celulelor sunt cele mai izolate în stadiile incipiente ale infecției [8] ; acest lucru sugerează că astfel de viruși au un avantaj selectiv în timpul transmiterii sau a fazei acute a bolii. Mai mult, cel puțin jumătate dintre pacienții infectați găzduiesc doar virusuri tropicale R5 pe parcursul întregului curs al infecției.
Un nou grup de medicamente, antagoniștii receptorilor CCR5 , a fost dezvoltat cu scopul de a interfera în interacțiunea dintre HIV și acest receptor; acestea includ PRO 140 , Vicriviroc , Aplaviroc și Maraviroc . Una dintre problemele limitative ale acestei abordări terapeutice este că, deși CCR5 este coreceptorul cel mai implicat în infecție, acesta nu este singurul. Cu toate acestea, atunci când se evaluează rezistența virală la AD101, un antagonist molecular al CCR5, virusurile rezistente nu au modificat co-receptorul țintă, dar continuă să utilizeze CCR5, chiar folosind domenii de legare alternative sau legând receptorul cu afinitate mai mare.
Varianta Δ32
CCR5-Δ32 , denumit și CCR5-D32 sau CCR5 delta 32 , este o variantă alelică a CCR5 [9] [10] .
CCR5-Δ32 este o mutație dăunătoare care are un impact specific asupra funcțiilor limfocitelor T [11] . Prezența a cel puțin o copie a acestei gene mutante ( heterozigoza ) a fost detectată la aproximativ 4-16% dintre indivizii de origine europeană, prezența ambelor copii ale genei mutante ( homozigoza ), la aproximativ 0,16-2, 5% din indivizi de origine europeană [12] . S-a speculat că această alelă ar fi putut favoriza selecția naturală în timpul morții negre din țările din nordul Europei, dar studii mai recente au exclus această posibilitate, relevând absența unui rol protector în acest context [13] . Se crede că această mutație ar fi putut oferi protecție împotriva variolei în timpul epidemiilor din Europa [13] , în special în marile orașe comerciale și în locuri izolate precum Islanda și Azore [14] și că această situație a favorizat o creștere a prevalenței a mutației [9] .
Se crede că în Grecia Antică , în zone precum Corint , dezvoltarea prostituției a dus la răspândirea unei infecții asemănătoare cu HIV, cu o imagine clinică asemănătoare gripei și imunosupresie ulterioară. În acel moment nu se știa nimic despre răspândirea acestei boli, dar se crede că ciuma din Atena și epidemiile ulterioare din Balcani ar fi putut fi favorizate de mutații genetice [15] . Cu toate acestea, mutația CCR5-Δ32 a fost detectată și în probele de sânge din epoca bronzului , la rate comparabile cu cele ale populației europene moderne [16] .
Această mutație are un efect negativ asupra funcției celulelor T, dar pare să joace un rol protector împotriva virusului Variola și HIV . Yersinia pestis , agentul cauzal al ciumei bubonice , sa dovedit în laborator că nu este asociat cu CCR5. Subiecții cu mutația Δ32 sunt sănătoși, sugerând că gena CCR5 este destul de superfluă; cu toate acestea CCR5 pare să joace un rol protector împotriva virusului West Nile și studiile clinice au arătat că subjects32 subiecții prezintă un risc disproporționat mai mare de a contracta această infecție [17] , demonstrând că nu toate funcțiile CCR5 pot fi compensate de alți receptori.
În ciuda variabilității genetice mari a CCR5 în regiunile sale de codificare, ștergerea de 32 pb duce la un receptor care nu funcționează, ceea ce împiedică intrarea în celulă a tulpinilor virale HIV R5-tropice; prezența acestei mutații în homozigozitate oferă o protecție puternică împotriva infecției cu HIV [18] . Această alelă a fost găsită la 5-14% dintre europeni, dar este rară în rândul africanilor și asiaticilor [19] ; prezența sa scade numărul de proteine CCR5 prezente în membrana celulară a limfocitului CD 4+ T, cu efecte asupra ratei de progresie a infecției cu HIV. Numeroase studii efectuate la persoanele infectate cu HIV au arătat că prezența unui exemplar al CCR5-Δ32 întârzie apariția SIDA timp de cel puțin doi ani. De asemenea, este posibil ca o persoană cu această mutație să nu se infecteze cu tulpini de HIV R5-tropice [20] .
Din punct de vedere terapeutic, s-a decis exploatarea acestei condiții pentru producerea anticorpilor monoclonali care blochează expresia genică a CCR5, pentru a fi utilizați la subiecții infectați cu HIV-1[21] . In vitro s- a demonstrat că celulele T, modificate pentru a nu avea CCR5 și amestecate cu celule T normale, sunt predispuse la preluarea în cultura celulară atunci când HIV atacă și ucide celulele normale[21] .
Această ipoteză a fost evaluată in vivo la un pacient cu SIDA, Timothy Ray Brown, care a dezvoltat în mod consensual leucemie mieloidă acută și care a fost tratat cu chimioterapie ; apoi a primit un transplant de celule stem hematopoietice de la un donator homozigot pentru CCR5-Δ32. După doi ani de tratament, pacientul a fost sănătos, cu un nivel nedorit de virioni în sânge, creier și epiteliu rectal [22] [23] . Înainte de transplant, pacientul avea, de asemenea, niveluri scăzute de XR4-tropic HIV, care nu utilizează CCR5 pentru intrarea celulară; cu toate acestea, după transplant, aceste tulpini virale au devenit, de asemenea, purtabile [23] . Acest eveniment poate fi explicat prin observația că celulele care exprimă varianta Δ32 sunt deficitare atât în CCR5, cât și în CXCR4 în membrana celulară, conferind rezistență la un număr mare de variante HIV [24] . În 2010, după trei ani de tratament, pacientul era încă rezistent la virus și a fost declarat vindecat [25] .
În 2009, a fost inițiat un studiu clinic pe pacienți HIV pozitivi pentru a evalua utilizarea unei terapii genetice care constă în transportul variantei CCR5-Δ32 printr-o nuclează de deget de zinc în celulele luate de la pacient; reinfuzarea acestor celule s-ar putea dovedi a fi o opțiune potențială în tratamentul HIV [26] [27] .
Notă
- ^ Samson M, Libert F, Doranz BJ, Rucker J, Liesnard C, Farber CM, Saragosti S, Lapoumeroulie C, Cognaux J, Forceille C, Muyldermans G, Verhofstede C, Burtonboy G, Georges M, Imai T, Rana S, Yi Y, Smyth RJ, Collman RG, Doms RW, Vassart G, Parmentier M, Rezistența la infecția cu HIV-1 la indivizi caucazieni care poartă alele mutante ale genei receptorului chemokinei CCR-5 , în Nature , vol. 382, nr. 6593, august 1996, pp. 722-5, DOI : 10.1038 / 382722a0 , PMID 8751444 .
- ^ a b Genetics Home Reference Arhivat 24 septembrie 2009 la Internet Archive .
- ^ Samson M, Labbe O, Mollereau C, Vassart G, Parmentier M, Clonarea moleculară și expresia funcțională a unei noi gene umane de receptor CC-chemokină , în Biochimie , vol. 35, nr. 11, martie 1996, pp. 3362-7, DOI : 10.1021 / bi952950g , PMID 8639485 .
- ^ Slimani H, Charnaux N, Mbemba E, Saffar L, Vassy R, Vita C, Gattegno L, Interacțiunea RANTES cu sindecan-1 și sindecan-4 exprimate de macrofage primare umane , în Biochim. Biofizi. Acta , vol. 1617, 1-2, octombrie 2003, pp. 80-8, DOI : 10.1016 / j.bbamem.2003.09.006 , PMID 14637022 .
- ^ a b Struyf S, Menten P, Lenaerts JP, Put W, D'Haese A, De Clercq E, Schols D, Proost P, Van Damme J, <2170 :: AID-IMMU2170> 3.0.CO; 2-D Divergent capacitățile de legare ale izoformelor naturale LD78beta ale proteinei inflamatorii macrofage-1alfa la receptorii 1, 3 și 5 ai chemokinelor CC afectează activitatea lor anti-HIV-1 și potențele chemotactice pentru neutrofile și eozinofile , în Eur. J. Immunol. , vol. 31, n. 7, iulie 2001, pp. 2170-8, DOI : 10.1002 / 1521-4141 (200107) 31: 7 <2170 :: AID-IMMU2170> 3.0.CO; 2-D , PMID 11449371 .
- ^ Proudfoot AE, Fritchley S, Borlat F, Shaw JP, Vilbois F, Zwahlen C, Trkola A, Marchant D, Clapham PR, Wells TN, Motivul BBXB al RANTES este principalul site pentru legarea heparinei și controlează selectivitatea receptorilor , în J Biol. Chem. , vol. 276, nr. 14, aprilie 2001, pp. 10620–6, DOI : 10.1074 / jbc.M010867200 , PMID 11116158 .
- ^ Miyakawa T, Obaru K, Maeda K, Harada S, Mitsuya H, Identificarea reziduurilor de aminoacizi critice pentru LD78beta, o variantă a proteinei inflamatorii macrofage umane-1alfa, care se leagă de CCR5 și inhibă replicarea virusului imunodeficienței umane R5 de tip 1 , în J. Biol. Chem. , vol. 277, nr. 7, februarie 2002, pp. 4649–55, DOI : 10.1074 / jbc.M109198200 , PMID 11734558 .
- ^ Anderson J, Akkina R, Knockdown complet al CCR5 de către ARNsi lentivirale exprimate vectorial și protecția macrofagelor transgenice împotriva infecției cu HIV-1 , în Terapia genică , vol. 14, n. 14, 2007, pp. 1287–1297, DOI : 10.1038 / sj.gt.3302958 , PMID 17597795 .
- ^ a b Galvani AP, Slatkin M, Evaluarea ciumei și a variolei ca presiuni selective istorice pentru alela CCR5-Delta 32 de rezistență la HIV , în Proc. Natl. Acad. Sci. SUA , vol. 100, nr. 25, decembrie 2003, pp. 15276–9, DOI : 10.1073 / pnas . 2435085100 , PMC 299980 , PMID 14645720 .
- ^ Stephens JC, Reich DE, Goldstein DB, Shin HD, Smith MW, Carrington M, Winkler C, Huttley GA, Allikmets R, Schriml L, Gerrard B, Malasky M, Ramos MD, Morlot S, Tzetis M, Oddoux C, di Giovine FS, Nasioulas G, Chandler D, Aseev M, Hanson M, Kalaydjieva L, Glavac D, Gasparini P, Kanavakis E, Claustres M, Kambouris M, Ostrer H, Duff G, Baranov V, Sibul H, Metspalu A, Goldman D , Martin N, Duffy D, Schmidtke J, Estivill X, O'Brien SJ, Dean M,Datând originea alelei rezistentei la SIDA CCR5-Delta32 prin coalescența haplotipurilor , în Am. J. Hum. Genet. , vol. 62, nr. 6, iunie 1998, pp. 1507–15, DOI : 10.1086 / 301867 , PMC 1377146 , PMID 9585595 .
- ^ Buseyne F, Janvier G, Teglas JP, Ivanoff S, Burgard M, Bui E, Mayaux MJ, Blanche S, Rouzioux C, Rivière Y, Impactul heterozigozității pentru receptorul chemokinei CCR5 32-bp-alelă eliminată asupra încărcăturii virusului plasmatic și Limfocite T CD4 la copiii infectați cu virusul imunodeficienței umane perinatal la vârsta de 8 ani , în J. Infect. Dis. , vol. 178, nr. 4, octombrie 1998, pp. 1019–23, DOI : 10.1086 / 515660 , PMID 9806029 .
- ^ John Novembre, Alison P Galvani și Montgomery Slatkin, The Geographic Spread of the CCR5 Δ32 HIV-Resistance Allele , în PLOS Biology , 18 octombrie 2005, DOI : 10.1371 .
- ^ a b Faure E, Royer-Carenzi M, Distribuția spațială europeană a alelei rezistente la HIV-1 CCR5-Delta32 este formată dintr-o defalcare a patocenozei datorată expansiunii istorice romane? , în Infect. Genet. Evol. , vol. 8, nr. 6, decembrie 2008, pp. 864–74, DOI : 10.1016 / j.meegid.2008.08.007 , PMID 18790087 .
- ^ Freitas T, Brehm A, Fernandes AT, Frecvența mutației CCR5-delta32 în populațiile insulei atlantice din Madeira, Azore, Cabo Verde și São Tomé e Príncipe , în Hum. Biol. , vol. 78, nr. 6, decembrie 2006, pp. 697–703, DOI : 10.1353 / hub.2007.0011 , PMID 17564248 .
- ^ Mirko D. Grmek, Boli în lumea greacă veche , martie 1991.
- ^ Hedrick PW, Verrelli BC, "Ground adevăr" pentru selecție pe CCR5-Delta32 , în Trends Genet. , vol. 22, n. 6, iunie 2006, pp. 293-6, DOI : 10.1016 / j.tig . 2006.04.007 , PMID 16678299 .
- ^ Glass WG, McDermott DH, Lim JK, Lekhong S, Yu SF, Frank WA, Pape J, Cheshier RC, Murphy PM,deficit de CCR5 crește riscul de infecție simptomatică cu virusul West Nile , în J. Exp. Med. , Vol. 203, nr. 1, ianuarie 2006, pp. 35–40, DOI : 10.1084 / jem . 20051970 , PMC 2118086 , PMID 16418398 .
- ^ Duncan SR, Scott S, Duncan CJ,Reevaluarea presiunilor selective istorice pentru mutația CCR5-Delta32 , în J. Med. Genet. , vol. 42, n. 3, martie 2005, pp. 205-8, DOI : 10.1136 / jmg.2004.025346 , PMC 1736018 , PMID 15744032 .
- ^ Sabeti PC, Walsh E, Schaffner SF, Varilly P, Fry B, Hutcheson HB, Cullen M, Mikkelsen TS, Roy J, Patterson N, Cooper R, Reich D, Altshuler D, O'Brien S, Lander ES,Cazul pentru selecție la CCR5-Delta32 , în PLoS Biol. , vol. 3, nr. 11, noiembrie 2005, pp. e378, DOI : 10.1371 / journal.pbio.0030378 , PMC 1275522 , PMID 16248677 .
- ^ Delta32 Genetic Testing ( PDF ), pe hârtie informativă pentru membrii AFAO , Federația Australiană a Organizațiilor SIDA, 1 iunie 2007. Accesat la 22 ianuarie 2011 (arhivat din original la 19 martie 2012) .
- ^ a b Steinberger P, Andris-Widhopf J, Bühler B, Torbett BE, Barbas CF, Ștergerea funcțională a receptorului CCR5 prin imunizare intracelulară produce celule care sunt refractare la infecția HIV-1 dependentă de CCR5 și fuziunea celulară , în Proc. Natl . Acad. Sci. SUA , vol. 97, nr. 2, ianuarie 2000, pp. 805-10, DOI : 10.1073 / pnas.97.2.805 , PMC 15412 , PMID 10639161 .
- ^ Schoofs M, A Doctor, a Mutation and a Potential Cure for AIDS , în The Wall Street Journal , 7 noiembrie 2008. Accesat la 15 decembrie 2010 .
- ^ a b Hütter G, Nowak D, Mossner M, Ganepola S, Müssig A, Allers K, Schneider T, Hofmann J, Kücherer C, Blau O, Blau IW, Hofmann WK, Thiel E, Controlul pe termen lung al HIV prin CCR5 Transplantul de celule stem Delta32 / Delta32 , în N. Engl. J. Med. , Vol. 360, n. 7, februarie 2009, pp. 692-8, DOI : 10.1056 / NEJMoa0802905 , PMID 19213682 .
- ^ Agrawal L, Lu X, Qingwen J, VanHorn-Ali Z, Nicolescu IV, McDermott DH, Murphy PM, Alkhatib G, Rol pentru proteina CCR5Delta32 în rezistența la virusul imunodeficienței umane R5, R5X4 și X4 tip 1 în celulele CD4 + primare , în J. Virol. , vol. 78, nr. 5, martie 2004, pp. 2277–87, DOI :10.1128 / JVI.78.5.2277-2287.2004 , PMC 369216 , PMID 14963124 .
- ^ Allers K, Hütter G, Hofmann J, Loddenkemper C, Rieger K, Thiel E, Schneider T, Evidence for the cure of HIV infection by CCR5Δ32 / Δ32 stem stem transplant , in Blood , vol. 117, nr. 10, decembrie 2010, pp. 2791-2799, DOI : 10.1182 / blood-2010-09-309591 , PMID 21148083 .
- ^ Celule T autologe modificate genetic la gena CCR5 de către Zinc Finger Nucleases SB-728 pentru HIV (Zinc-Finger) , la clinictrials.gov , US National Institutes of Health, 9 decembrie 2009. Accesat la 30 decembrie 2009 .
- ^ Nicholas Wade, Zinc Fingers ar putea fi cheia pentru reînvierea terapiei genice , în New York Times , 28 decembrie 2009. Accesat la 30 decembrie 2009 .
Perspective
- Wilkinson D, Cofactorii furnizează cheile de intrare. HIV-1 , în Curr. Biol. , vol. 6, nr. 9, 1997, pp. 1051–3, DOI : 10.1016 / S0960-9822 (02) 70661-1 , PMID 8805353 .
- Broder CC, Dimitrov DS, HIV și receptorii domeniului 7-transmembranar , în Pathobiology , vol. 64, n. 4, 1997, pp. 171-9, DOI : 10.1159 / 000164032 , PMID 9031325 .
- Choe H, Martin KA, Farzan M, Sodroski J, Gerard NP, Gerard C, Interacțiuni structurale între receptorii chemokinei, gp120 Env și CD4 , în Semin. Immunol. , vol. 10, nr. 3, 1998, pp. 249–57, DOI : 10.1006 / smim . 1998.0127 , PMID 9653051 .
- Sheppard HW, Celum C, Michael NL, O'Brien S, Dean M, Carrington M, Dondero D, Buchbinder SP, infecția cu HIV-1 la persoanele cu genotipul CCR5-Delta32 / Delta32: achiziționarea virusului inductor de sinciți la seroconversie , în J. Acquir. Imunodefic. Syndr. , vol. 29, nr. 3, 2002, pp. 307-13, PMID 11873082 .
- Freedman BD, Liu QH, Del Corno M, Collman RG, HIV-1 gp120 semnalizare mediată de receptorul chemokinei în macrofagele umane , în Immunol. Rez. , Vol. 27, 2-3, 2004, pp. 261–76, DOI : 10.1385 / IR: 27: 2-3: 261 , PMID 12857973 .
- Esté JA, Intrarea virusului ca țintă pentru intervenția anti-HIV , în Curr. Med. Chem. , vol. 10, nr. 17, 2004, pp. 1617–32, DOI : 10.2174 / 0929867033457098 , PMID 12871111 .
- Gallo SA, Finnegan CM, Viard M, Raviv Y, Dimitrov A, Rawat SS, Puri A, Durell S, Blumenthal R, Reacția de fuziune mediată de HIV Env , în Biochim. Biofizi. Acta , vol. 1614, nr. 1, 2003, pp. 36-50, DOI : 10.1016 / S0005-2736 (03) 00161-5 , PMID 12873764 .
- Zaitseva M, Peden K, Golding H, coreceptori HIV: rolul structurii, modificările posttranslaționale și internalizarea în fuziunea celulelor virale și ca ținte pentru inhibitorii de intrare , în Biochim. Biofizi. Acta , vol. 1614, nr. 1, 2003, pp. 51–61, DOI : 10.1016 / S0005-2736 (03) 00162-7 , PMID 12873765 .
- Lee C, Liu QH, Tomkowicz B, Yi Y, Freedman BD, Collman RG, Activarea macrofagelor prin căi de semnalizare provocate de gp120 mediate de CCR5 și CXCR4 , în J. Leukoc. Biol. , vol. 74, nr. 5, 2004, pp. 676–82, DOI : 10.1189 / jlb.0503206 , PMID 12960231 .
- Yi Y, Lee C, Liu QH, Freedman BD, Collman RG, utilizarea receptorilor de chemokine și semnalizarea macrofagelor prin virusul imunodeficienței umane de tip 1 gp120: Implicații pentru neuropatogeneză , în J. Neurovirol. , 10 Suppl 1, 2004, pp. 91-6, PMID 14982745 .
- Seibert C, Sakmar TP, antagoniști ai moleculelor mici ale CCR5 și CXCR4: o nouă clasă promițătoare de medicamente anti-HIV-1 , în Curr. Pharm. Des. , vol. 10, nr. 17, 2004, pp. 2041–62, DOI : 10.2174 / 1381612043384312 , PMID 15279544 .
- Cutler CW, Jotwani R, Expresia mucoasei orale a receptorilor, co-receptorilor și alfa-defensinelor HIV-1: tablou de rezistență sau susceptibilitate la infecția cu HIV? , în Adv. Adâncitură. Rez. , Vol. 19, nr. 1, 2006, pp. 49–51, DOI : 10.1177 / 154407370601900110 , PMID 16672549 .
- Ajuebor MN, Carey JA, Swain MG, CCR5 în bolile hepatice mediate de celule T: ce se întâmplă? , în J. Immunol. , vol. 177, nr. 4, 2006, pp. 2039–45, PMID 16887960 .
- Lipp M, Müller G, Formarea imunității adaptive: impactul CCR7 și CXCR5 asupra traficului de limfocite , în Verhandlungen der Deutschen Gesellschaft für Pathologie , vol. 87, 2006, pp. 90-101, PMID 16888899 .
- Balistreri CR, Caruso C, Grimaldi MP, Listì F, Vasto S, Orlando V, Campagna AM, Lio D, Candore G, receptor CCR5: implicații biologice și genetice în bolile legate de vârstă , în Ann. NY Acad. Știință , vol. 1100, 2007, pp. 162–72, DOI : 10.1196 / annals.1395.014 , PMID 17460174 .
- Madsen HO, Poulsen K, Dahl O, Clark BF, Hjorth JP, Retropseudogenes constituie partea majoră a familiei genei alfa a factorului de alungire 1 uman , în Nucleic Acids Res. , Vol. 18, nr. 6, 1990, pp. 1513–6, DOI : 10.1093 / nar / 18.6.1513 , PMC 330519 , PMID 2183196 .
- Uetsuki T, Naito A, Nagata S, Kaziro Y, Izolarea și caracterizarea genei cromozomiale umane pentru factorul de alungire a lanțului polipeptidic-1 alfa , în J. Biol. Chem. , vol. 264, nr. 10, 1989, pp. 5791-8, PMID 2564392 .
- Whiteheart SW, Shenbagamurthi P, Chen L, Cotter RJ, Hart GW, factorul de alungire murin 1 alfa (EF-1 alfa) este modificat posttranslațional prin noi porțiuni etanolamină-fosfoglicerol legate de amidă. Adăugarea de etanolamină-fosfoglicerol la reziduuri specifice de acid glutamic pe EF-1 alfa , în J. Biol. Chem. , vol. 264, nr. 24, 1989, pp. 14334–41, PMID 2569467 .
- Ann DK, Wu MM, Huang T, Carlson DM, Wu R, expresia genei reglată de retinol în celulele epiteliale traheobronșice umane. Exprimare sporită a factorului de alungire EF-1 alfa , în J. Biol. Chem. , vol. 263, n. 8, 1988, pp. 3546-9, PMID 3346208 .
- Brands JH, Maassen JA, van Hemert FJ, Amons R, Möller W,Structura primară a subunității alfa a factorului de alungire umană 1. Aspecte structurale ale siturilor de legare la guanină-nucleotide , în Eur. J. Biochem. , vol. 155, nr. 1, 1986, pp. 167–71, DOI : 10.1111 / j.1432-1033.1986.tb09472.x , PMID 3512269 .
