Variolă
| Variolă | |
|---|---|
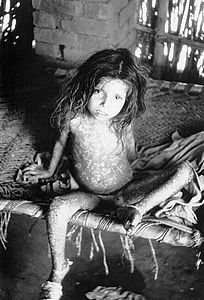
| Fetiță care prezintă erupția tipică datorată Variola maior | |
| Specialitate | boală infecțioasă |
| Etiologie | Virusul Variola |
| Clasificare și resurse externe (EN) | |
| ICD-9 -CM | 050050 |
| ICD-10 | B0303. |
| Plasă | D012899 |
| MedlinePlus | 001356 |
| eMedicină | 830328 și 237229 |
Variola a fost o boala infectioasa cauzata de doua variante ale Variola virusului , Variola și Variola minor maior [1] . Boala este, de asemenea, cunoscută prin termenii latini variola sau variola vera (din latină târzie variŏla , derivat din varius , care înseamnă vario, reperat [2] ), în timp ce termenul englezesc variolă a fost inventat în Regatul Unit în secolul al XV-lea pentru a distinge din sifilis , numit varicela mare [3] .
Virusul variolei este localizat în circulația mică a pielii , a cavității bucale și a faringelui . Pielea se manifestă printr-o „ erupție maculo - papulară și mai târziu cu vezicule ridicate umplute cu lichid. Variola maior provoacă manifestări clinice mai relevante și se caracterizează printr-o letalitate de 30-35% [4] [5] . Complicațiile pe termen lung includ cicatrici caracteristice, în special pe față, la 65-85% dintre cei care reușesc să supraviețuiască [6] ; în plus, orbirea , ca o consecință a ulcerelor corneene și a cicatricilor ulterioare, și a deformării membrelor , din cauza episoadelor de artrită și osteomielită, pot apărea, de asemenea, cu o prevalență mai mică estimată în 2-5% din cazuri. Variola minor cauzează o formă mai ușoară a bolii, cunoscută și sub numele de alastrim , care poate duce la deces în 1% din cazuri [4] .
Variola se crede că a apărut în populația umană în jurul mileniului al II-lea î.Hr. [3] și primele dovezi fizice pot fi urmărite până la erupția pustulară găsită pe mumea faraonului Ramses V [7] . Se estimează că boala a ucis în fiecare an aproximativ 400.000 de europeni în secolul al XVIII-lea [8] și a fost responsabilă pentru o treime din toate cazurile de orbire [4] [9] . Dintre toate persoanele infectate, aproximativ 20-60% dintre adulți și 80% dintre copii au murit [10] . Se consideră că variola a fost cauza a 300-500 de milioane de decese în secolul XX [11] [12] [13] . Numai în 1967 , potrivit datelor Organizației Mondiale a Sănătății , cincisprezece milioane de persoane au contractat boala și din aceste două milioane au murit [14] . După o campanie masivă de vaccinare desfășurată încă din secolul al XIX-lea și desfășurată cu un efort comun masiv între 1958 și 1977 , OMS a declarat boala eradicată în 1979 , după ce ultimul caz de variolă naturală cauzat de Variola minor a fost diagnosticat în Somalia pe 26 Octombrie 1977 [14] . A fost singura boală eradicată în istoria omenirii până în 2011 , când pesta bovina a suferit aceeași soartă [15] [16] [17] .
Etiologie
| Virusul Variola | |
|---|---|
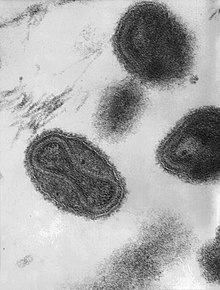
| Microscopie electronică de transmisie care arată câțiva virioni. Structura vizibilă din interior reprezintă nucleul , care conține ADN - ul viral (mărire: ~ 370.000 ×) | |
| Clasificare științifică | |
| Domeniu | Varidnaviria |
| Regatul | Bamfordvirae |
| Phylum | Nucleocytoviricota |
| Clasă | Pokkesviricetes |
| Ordin | Chitovirale |
| Familie | Poxviridae |
| Subfamilie | Chordopoxvirinae |
| Tip | Ortopoxvirus |
| Specii | Virusul Variola |
Variola este cauzata de virusul variolei infecție care face parte din Ortopoxvirus genul de Poxviridae familiei. Virusul este mare, în formă de cărămidă și măsoară aproximativ 302-350 nm până la 244-270 nm [18] cu un ADN unic liniar dublu-catenar și un genom de 186 kbp caracterizat printr-o buclă stem terminator la fiecare capăt [19] [20] . Există în două forme: Variola maior și Variola minor .
Cei patru ortopoxvirus care pot provoca infecții la om sunt, pe lângă virusul Variola, virusul vaccinia , virusul cowpox și cel al virusului maimuță . Virusul Variola infectează în mod natural numai oamenii, deși primatele și alte animale au fost infectate în laborator [21] .
Înțelegerea ciclului de viață al poxvirusurilor este complicată de faptul că există numeroase forme infecțioase cu mecanisme diferite de acces la celulă. Virusul se replică în citoplasma celulei, spre deosebire de alți viruși ADN care se reproduc în mod normal în nucleu . De asemenea, produce numeroase proteine specifice, dintre care cea mai importantă este o ARN polimerază dependentă de ADN . Atât virionii înveliți, cât și cei neînveliți sunt infecțioși; aceasta este sintetizată la nivelul aparatului Golgi al celulei și include mai multe polipeptide virale specifice, inclusiv o hemaglutinină [19] . Infecția cu unul dintre cei doi virusuri Variola conferă imunitate față de celălalt [5] .
Metoda de transmitere
Virusul este transmis prin aer, prin inhalarea picăturilor care conțin virioni, produse de mucoasa orală, nazală sau faringiană a unei persoane infectate. Se transmite de la o persoană la alta în principal prin contact direct, de obicei la mai puțin de doi metri, dar și prin obiecte contaminate. Rareori se transmite transportat de aer în locuri închise [22] . Virusul poate trece prin placentă , dar incidența variolei congenitale este relativ scăzută [5] .
Variola nu este deosebit de contagioasă în timpul fazei prodromale și transmiterea are loc de obicei după apariția manifestărilor cutanate, adesea însoțită de leziuni ale cavității bucale și ale faringelui. Virusul poate fi transmis pe durata bolii, în special în prima săptămână a erupției cutanate , când majoritatea leziunilor cutanate sunt intacte [21] . Faza infecțioasă se încheie la 7-10 zile după formarea crustelor, dar pacientul rămâne infecțios până când ultima crustă se desprinde [23] .
Boala este extrem de contagioasă, dar, în general, se răspândește mai încet și mai puțin pe scară largă decât alte boli virale, posibil pentru că transmiterea necesită un contact strâns și este posibilă numai după debutul erupției cutanate . Rata infecției este, de asemenea, redusă cu durata scurtă a etapei infecțioase. În zonele temperate, infecția apare mai ales în timpul iernii și primăverii , în timp ce în zonele tropicale diferența sezonieră este mai nuanțată, iar boala este prezentă pe tot parcursul anului [21] . Distribuția în funcție de vârstă depinde de statutul imunității dobândite : imunitatea datorată vaccinării a scăzut în timp și probabil a dispărut în majoritatea populației vaccinate [5] . Variola nu pare să fie transmisă de insecte sau alte animale [21] .
Clinica
Clasificare
Există două forme clinice de variolă. Variola maior este cea mai frecventă și mai severă formă, caracterizată printr-o erupție cutanată extinsă și febră mai mare. Variola minor este mai puțin frecventă și mai puțin severă, cu o letalitate mai mică de 1% [22] . S- au observat infecții asimptomatice , dar sunt destul de rare [21] . Mai mult, o formă numită variola sine eruptione poate fi văzută la persoanele vaccinate; această formă se caracterizează prin febră care apare după perioada normală de incubație a virusului și poate fi confirmată doar prin detectarea anticorpilor direcționați împotriva virusului prin tehnici serologice sau, rareori, prin izolarea virusului însuși [21] .
semne si simptome
Perioada de incubație dintre contactul cu virusul și debutul primelor manifestări clinice este de aproximativ 12 zile. Odată inhalat, virusul invadează mucoasa orofaringelui sau a sistemului respirator , migrează către ganglionii limfatici loco-regionali și începe să se înmulțească. În faza inițială de creștere, virusul pare să se deplaseze de la o celulă la alta, dar, după a 12-a zi, începe liza celulelor infectate și virusul reușește să pătrundă în sânge, într-o fază de viremie , și începe o nouă multiplicare la nivelul splinei , măduvei osoase și ganglionilor limfatici. Simptomele inițiale sunt similare cu alte boli virale, cum ar fi gripa și răceala : febră peste 38,5 ° C, dureri musculare , stare generală de rău, cefalee și decubit prostrat . Tractul gastrointestinal este adesea implicat și greața , vărsăturile și durerile de spate sunt frecvente. Etapa pre-eruptivă durează în mod normal 2-4 zile, în timp ce începând cu a 12-a-a 15-a zi apar primele leziuni enantematice în membrana mucoasă a gurii , limbii , palatului și faringelui și temperatura corpului se normalizează. Leziunile suferă mărirea și ruperea rapidă, cu eliberarea unei cantități mari de virioni în salivă [5] .

Virusul variolei atacă preferențial celulele pielii, provocând leziunile clasice asociate bolii. Erupția se dezvoltă la 24-48 de ore de la apariția leziunilor mucoasei, de obicei în principal în frunte, și apoi se localizează rapid pe întreaga față, zonele proximale ale membrelor, trunchiului și , în cele din urmă, pe mâini și picioare . Întregul proces nu durează mai mult de 24-36 de ore, după care nu apar noi leziuni [5] . În acest moment Variola maior se poate dezvolta în moduri diferite, dând naștere la patru tipuri diferite de variolă conform clasificării Rao [24] : obișnuită, modificată, malignă și hemoragică. Variola se caracterizează printr-o letalitate de 30%, totuși formele maligne și hemoragice sunt de obicei fatale [25] .
Formă obișnuită
90% din cazurile de variolă la persoanele nevaccinate sunt de tip obișnuit [21] . În acest caz, începând cu a 2-a zi a erupției cutanate, leziunile cutanate cresc în papule ; începând cu a 3-a-4-a zi se umplu cu un lichid opalescent, transformându-se în vezicule . În termen de 24-48 de ore, acest fluid devine opac și tulbure, dând leziunilor aspectul de pustule care, spre deosebire de pustulele reale, nu conțin puroi, ci reziduuri de țesut [5] ; după a 6-a-7-a zi toate leziunile au acest aspect, atingând dimensiunea maximă în aproximativ zece zile. Aceste pustule sunt ridicate, rotunde, strânse și greu la atingere. Acestea sunt situate adânc în derm , dând impresia de mici marmură. Lichidul se scurge lent din leziuni și, la două săptămâni după începerea erupției cutanate, se dezumflă și se usucă, formând cruste. În a treia săptămână, se formează cruste peste toate leziunile, care încep să se desprindă, lăsând cicatrici depigmentate [26] .
Forma obișnuită a variolei produce în general o erupție discretă cu pustule neconfluente [27] . Erupția este localizată în principal în față, este mai puțin densă în trunchi decât în extremități și mai densă în părțile anatomice distale decât în cele proximale. Palmele și tălpile picioarelor sunt implicate în majoritatea cazurilor. Uneori veziculele devin confluente, detașând straturile exterioare ale pielii de țesutul subiacent; în acest caz, rata de letalitate observată a fost de 62% [21] .
Forma modificată
Forma modificată apare în principal la persoanele vaccinate anterior și este numită pentru caracteristicile erupției cutanate și rapiditatea dezvoltării acesteia. În acest caz, pot apărea simptome prodromale, dar sunt în general mai puțin severe decât în forma obișnuită. În mod normal, nu există febră, iar leziunile sunt mai puține și se rezolvă rapid, sunt mai superficiale și mai uniforme ca în forma obișnuită [26] . Acest tip de variolă este rareori fatal și poate fi ușor confundat cu varicela [21] .
Forma malignă
În forma malignă, numită și formă plată, leziunile sunt localizate la nivelul pielii în același timp în care, în forma obișnuită, apar vezicule ridicate. Motivul pentru care anumite persoane dezvoltă această formă este necunoscut și reprezintă 5-10% din cazurile de variolă, apărând în principal la copii (72% din cazuri) [28] . Se presupune că apare în raport cu tulburările imunologice ale individului de tip deficitar [29] . Se caracterizează printr-un sindrom prodromal foarte proeminent care durează 3-4 zile, febră mare și de lungă durată și simptome clasice de septicemie . Erupția cutanată a limbii și a palatului este extinsă, iar leziunile cutanate se maturizează lent, rămânând adânc în piele și rămânând plate până în a șaptea până la a opta zi. Spre deosebire de forma obișnuită, veziculele conțin puțin lichid, sunt moi și catifelate la atingere și pot conține sânge . Această formă este aproape întotdeauna fatală [21] .
Forma hemoragică
Variola hemoragică este o formă severă caracterizată prin sângerări extinse ale pielii, membranelor mucoase și ale tractului gastro-intestinal. Se dezvoltă în aproximativ 2% din cazuri, în principal la adulți [21] . În această formă nu se dezvoltă vezicule și pielea rămâne netedă; sângerarea se dezvoltă în derma profundă, făcând pielea să pară neagră ca și când ar fi fost carbonizată [21] [30] . Forma se presupune că se datorează unor condiții particulare ale individului, cum ar fi imunosupresia , sau unei anumite tulpini de virus; cu toate acestea, datele conexe lipsesc [29] .
La început, în a 2-a-3-a zi, se prezintă cu hemoragie subconjunctivală . Variola hemoragică prezintă, de asemenea, eritem , petechii , hemoragii de splină, rinichi , peritoneu , mușchi și, mai rar, de epicard , ficat , testicule , ovare și vezică biliară . În forma timpurie, moartea apare rapid în jurul zilei a 5-a-a 7-a de boală, când sunt prezente doar un număr minim de leziuni ale pielii, în timp ce forma tardivă duce la moarte la pacient în 8-10 zile. Sângerarea are loc devreme și erupția cutanată rămâne plană, fără a ajunge în faza veziculară [21] .
Pacienții cu forma timpurie prezintă o reducere rapidă a factorilor de coagulare , trombocite , globuline și protrombină și o creștere a antitrombinei circulante. Forma târzie arată o deficiență mai mică a factorilor de coagulare, trombocitopenie marcată și o creștere a antitrombinei [5] . Această formă, în mod normal fatală [21] , reprezintă 3 până la 25% din cazurile fatale de variolă în raport cu virulența tulpinii virale [25] .
Diagnostic
În definiția sa clinică, variola este considerată o boală caracterizată printr-un debut acut al febrei peste 38,3 ° C, urmată de o erupție cu vezicule sau pustule profunde și solide în același stadiu de dezvoltare, în absența altor cauze aparente [21] . Confirmarea este dată de diagnosticul de laborator .
La microscop , pot fi observate incluziunile clasice citoplasmatice ale poxvirusurilor, dintre care cele mai importante sunt numite corpuri Guarnieri , care reprezintă locuri de replicare virală . Aceste incluziuni pot fi ușor identificate în biopsiile cutanate colorate cu hematoxilină și eozină sub formă de vezicule roz și sunt prezente în toate infecțiile cu poxvirus; cu toate acestea, absența lor nu poate exclude diagnosticul de boală [31] . Diagnosticul infecției cu ortopoxvirus poate fi obținut rapid și prin microscopia electronică a fluidului conținut în pustule sau cruste, dar virionii sunt identici între toți ortopoxvirusurile [5] .
Diagnosticul definitiv se face prin supunerea virusului la creșterea în membrana corioalantoidă , o parte a embrionului puiului și prin examinarea leziunilor la condiții de temperatură definite [32] . Diferitele genotipuri ale virusului pot fi distinse prin reacția în lanț a polimerazei (PCR) și analiza polimorfismului de lungime a fragmentului de restricție (RFLP). Testele serologice și testele ELISA , care măsoară imunoglobulinele specifice îndreptate împotriva antigenelor virusului Variola , pot fi utile în diagnostic [33] .
Varicela a fost ușor confundată cu variola înainte de eradicare și, prin urmare, a intrat în diagnosticul diferențial . Cele două boli se pot distinge prin diferite metode. Spre deosebire de variolă, varicela nu apare în mod normal pe palmele mâinilor și tălpilor picioarelor; în plus, pustulele cu variceloză au o dimensiune variabilă în funcție de momentul în care sunt create, în timp ce pustulele de variolă au aproximativ aceeași dimensiune. În plus față de clinică, sunt disponibile numeroase teste de laborator pentru a determina dacă este vorba de varicelă în evaluarea cazurilor suspectate de variolă [21] .
Tratament și prevenire
Prima procedură utilizată în prevenirea variolei a fost variolarea . Practicat în India în primul mileniu î.Hr. , acesta a constat în inocularea, prin insuflarea nazală, a crustelor pulverizate de variolă sau a materialului obținut din zgârierea leziunilor cutanate ale pacienților ușor bolnavi [34] [35] .
Cu toate acestea, faptul că variolizarea își are originea în India a fost contestat de faptul că doar unele dintre textele medicale antice scrise în sanscrită descriu procesul [36] . Această tehnică de prevenire a fost utilizată în China deja în ultimii ani ai secolului al X-lea și a fost răspândită și practicată pe scară largă în secolul al XVI-lea , în timpul dinastiei Ming [37] . Dacă are succes, variolarea generează imunitate la variolă, totuși, pe măsură ce persoana se infectează cu virusul, se poate infecta grav și poate transmite boala altora. Variolizarea are o rată de letalitate de 0,5-2%, semnificativ mai mică decât 20-30% din boală [21] .
În timpul șederii sale în Imperiul Otoman , Lady Mary Wortley Montagu a observat procesul de variolare, descriind în detaliu tehnica și promovând cu entuziasm introducerea acesteia în Regatul Unit la întoarcerea ei în 1718 [38] . În 1721 Cotton Mather și colegii săi au provocat controverse amare prin inocularea a sute de oameni în Boston . În 1796 , Edward Jenner a descoperit că imunitatea la variolă poate fi obținută și prin inocularea pacientului cu material obținut din leziuni ale variolei , o boală a animalelor cauzată de un virus din aceeași familie ca și cel al variolei. Jenner a numit materialul folosit „ vaccin ”, din „vacă”, un cuvânt latin pentru vacă . Procedura a fost mult mai sigură decât variolarea și nu a prezentat niciun risc de transmitere a bolii, astfel încât sa răspândit rapid în întreaga lume. În secolul al XIX-lea , virusul variolei bovine a fost înlocuit cu virusul Vaccinia , întotdeauna din aceeași familie ca virusul Variola, dar genetic diferit. Nu se cunoaște originea și de ce a început să fie utilizată în vaccinare [21] .
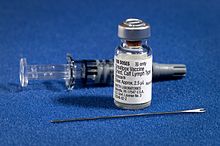
Formularea actuală a vaccinului împotriva variolei este dată de un preparat viu și infecțios pentru virusul Vaccinia . Se administrează cu un ac bifurcat, care este mai întâi scufundat în soluția de vaccin și apoi utilizat pentru a străpunge pielea, de obicei a brațului, de un număr diferit de ori în câteva secunde. Dacă vaccinarea este eficientă, la locul injectării se dezvoltă o umflare roșie, cu mâncărime în decurs de 3-4 zile. În prima săptămână, acesta devine un blister mare care se umple cu puroi și începe să se usuce. A doua săptămână începe să se formeze o crustă, care cade în timpul celei de-a treia, lăsând o mică cicatrice [39] .
Anticorpii produși după vaccinare sunt de protecție împotriva tuturor ortopoxvirusurilor și sunt încă detectabili la zece ani de la prima vaccinare și la șapte zile după revaccinare. Conform datelor statistice, acestea conferă protecție eficientă la 95% dintre subiecții vaccinați [40] . Acoperirea este ridicată în primii 3-5 ani și scade în următorii, în timp ce în cazul revaccinării acoperirea este și mai durabilă. În Europa , în anii 1950 și 1960 , mortalitatea la subiecții vaccinați mai puțin de zece ani în momentul expunerii la virus a fost de 1,3%, în timp ce era de 7% la subiecții vaccinați de peste 10 ani și de 11% la cei vaccinați de peste douazeci de ani. În schimb, letalitatea la cei nevaccinați a fost de 52% [41] . Vaccinarea în primele trei zile de expunere la virus previne sau reduce semnificativ severitatea bolii în marea majoritate a populației; vaccinarea efectuată între a 4-a și a 7-a zi de expunere poate garanta o protecție parțială și poate modifica severitatea bolii [40] .
Există efecte secundare și riscuri asociate cu vaccinarea împotriva variolei. În trecut, aproximativ 0,1% din vaccinurile pentru prima dată au prezentat efecte grave, dar care nu pun viața în pericol, inclusiv reacții alergice la locul injectării cu eritem multiform și dispersarea virusului Vaccinia în alte părți ale corpului. Efectele care pun viața în pericol au apărut la 14-500 de persoane pe milion vaccinate și se estimează că 1-2 persoane pe milion au murit, în principal ca o consecință a encefalitei post-vaccinare sau a necrozei progresive a locului de vaccinare [40] .
Odată ce variola a fost eradicată, cazurile de boli secundare vaccinării au depășit cele de contagiune naturală și vaccinarea copiilor a fost oprită în 1972 în Statele Unite și la începutul anilor 1970 în majoritatea țărilor europene [14] [42] . Din 1986 , vaccinarea împotriva variolei a încetat în toate țările [14] și este recomandată numai celor care, lucrând în laboratoare biologice, sunt expuse riscului de expunere profesională [21] .
În afară de vaccinare, tratamentul împotriva variolei este numai de susținere și se bazează pe hidratare, monitorizarea infecției și, eventual, ventilație artificială . Formele hemoragice și maligne sunt tratate cu terapii de șoc septic și, în cazul pustulelor confluente, tratamentul este similar cu cel stabilit pentru pacienții cu arsuri extinse [43] .
Nu sunt aprobate medicamente pentru tratamentul variolei, deoarece medicamentele antivirale au fost dezvoltate numai după eradicarea bolii. Studiile sugerează că cidofovirul administrat intravenos poate fi eficient în terapie, deși este caracterizat de toxicitate renală [44] .
Prognoză
Rata de letalitate pentru forma obișnuită a variolei este de aproximativ 30%, dar variază în funcție de leziunile cutanate: dacă este confluentă, letalitatea este de 50-75%, în timp ce dacă sunt semi-confluente scade la 25-50%, pentru a trece mai puțin mai mult de 10% în cazul unei erupții corecte. Letalitatea la copiii cu vârsta sub un an este în schimb de 40% - 50%. Formele maligne și hemoragice au cea mai mare rată de letalitate, respectiv 90% și respectiv 100%. Variola minor se caracterizează în schimb printr-o letalitate mai mică de 1% [26] . Nu există dovezi că boala poate deveni cronică sau reapare [26] .
În cazurile fatale de variolă, moartea apare de obicei între a 10-a și a 16-a zi de boală. Nu se cunoaște cauza morții cauzate de variolă, dar se știe că boala implică multe organe; formarea complexelor imune circulante, viremia masivă și răspunsul imun necontrolat pot contribui la aceasta [21] . În forma hemoragică timpurie, moartea are loc la aproximativ șase zile de la apariția febrei, în general din cauza insuficienței cardiace asociate cu edemul pulmonar , în timp ce în forma hemoragică târzie cauza se datorează trombocitopeniei severe, viremiei și răspunsului imun slab [28] . În forma malignă, moartea se datorează deshidratării , cu pierderea proteinelor și electroliților și a sepsisului , așa cum apare în general în arsurile severe [43] .
Variola poate deveni complicată în sistemul respirator , cu manifestări variind de la bronșită simplă la pneumonie fatală. Complicațiile respiratorii apar de obicei în a 8-a zi de boală și pot rezulta și din infecții virale sau bacteriene oportuniste . Infecțiile bacteriene secundare ale pielii sunt relativ rare, dar atunci când apar, febra tinde să rămână crescută pe toată durata bolii [21] .
Alte complicații includ encefalita , care apare la unul din 500 de pacienți și este mai frecventă la adulți, boli oculare în 2% din cazuri și cicatrici permanente, situate în principal pe față. Pustulele se pot forma pe pleoapă , conjunctivă și cornee , complicându-se cu conjunctivită , cheratită , ulcer cornean , irită , iridociclită și atrofie optică . Orbirea apare la aproximativ 35-40% dintre pacienții cu cheratită și ulcer cornean. Variola hemoragică poate provoca, de asemenea, hemoragia conjunctivei și a retinei . La 2-5% dintre copiii bolnavi, virusul se poate deplasa la articulații și la oase , provocând osteomielită . Leziunile osoase sunt simetrice și implică în principal cotul , tibia și fibula , provocând o separare a epifizei și o reacție periostală . Leziunile articulare restricționează mișcarea, iar artrita poate duce la deformări ale membrelor, anchiloză și degete îndesate [5] .
Istorie

Momentul apariției variolei nu este definit, dar se presupune că ar fi putut evolua dintr-un virus al rozătoarelor [45] [46] . L'ampia variabilità del periodo è dovuta ai differenti dati utilizzati per calibrare la frequenza molecolare. Un clade è quello del ceppo di Variola maior che si diffuse partendo dall' Asia tra 400 e 1 600 anni fa ed è responsabile della forma più grave di vaiolo. Un altro clade include entrambi i ceppi di Variola minor descritti nel continente americano e isolati in Africa occidentale , che si suppone si siano separati dal ceppo ancestrale tra i 1 400 ei 6 300 anni fa; questo clade si pensa possa essersi distinto in due subclade almeno 800 anni fa.
Una seconda stima è basata sull'ipotesi che il Variola virus si sia separato dal virus del vaiolo del gerbillo circa 3 000-4 000 anni fa [47] . Questa stima è coerente con le prove storiche e archeologiche che identificano il vaiolo come una malattia umana con un'origine relativamente recente. Tuttavia, supponendo che il tasso di mutazione genetica sia simile a quella dei virus della famiglia degli Herpesviridae , si stima che la separazione tra Variola virus e il virus del vaiolo del gerbillo sia avvenuta circa 50 000 anni fa. Questa stima è coerente con le altre stime pubblicate e suggerisce che le prove archeologiche e storiche siano decisamente incomplete. Sono quindi necessarie migliori stime dei tassi di mutazione di questi virus per poter uniformare i dati [47] .
Il vaiolo sembra essere emerso come malattia endemica in India circa 2 500-3 000 anni fa [48] , mentre il suo trasferimento dall'Africa orientale al Sud America è avvenuto nel XIX secolo .
La prima evidenza clinica attendibile di vaiolo è stata trovata nella mummia del faraone egiziano Ramses V , morto oltre 3 000 anni fa [7] , mentre archivi storici asiatici descrivono una malattia simile al vaiolo in India [49] e in Cina nei secoli successivi [50] . Si è ipotizzato che i commercianti egiziani abbiano importato la malattia in India nel I millennio aC , dove è rimasta endemica per oltre 2 000 anni; il vaiolo sembra poi essere stato introdotto in Cina nel I secolo aC dai territori a sud-ovest e da qui in Giappone nel VI secolo [28] . In Giappone si stima che l' epidemia del 735-737 abbia ucciso un terzo della popolazione dell'arcipelago [8] [51] . Almeno sette divinità sono state specificatamente associate al vaiolo, tra i quali Sopona della religione del popolo Yoruba e Shitala Devi dell' induismo [52] .
L'arrivo del vaiolo in Europa e nel Sud-est asiatico è invece meno chiaro. La malattia non è descritta nell' Antico e nel Nuovo Testamento della Bibbia e nemmeno nella letteratura greca e romana e gli studiosi concordano che molto difficilmente una tale malattia possa essere sfuggita a una descrizione da parte di Ippocrate se si fosse manifestata nell'area mediterranea [53] .
Mentre la peste antonina , che dilagò attraverso l' Impero romano tra il 165 e il 180 , si pensa possa essere stata causata da un'epidemia di vaiolo [54] [55] , altri storici ipotizzano che siano state le truppe arabe a portare per prime la malattia dall'Africa all'Europa sud-orientale nel VII - VIII secolo [28] . Nel IX secolo il medico persiano Abu Bakr Mohammad Ibn Zakariyya al-Razi compì una delle osservazioni più importanti sul vaiolo e fu il primo a distinguerlo dal morbillo e dalla varicella nella sua opera Kitab fi al-jadari wa-al-hasbah , in italiano Il libro del vaiolo e del morbillo [56] .
Durante il Medioevo il vaiolo si presentò con epidemie periodiche, ma non divenne endemico finché la popolazione non crebbe, aiutato anche dai grandi movimenti di persone che caratterizzarono il periodo delle crociate . A partire dal XVI secolo il vaiolo era presente in quasi tutta Europa, infettando soprattutto i bambini e causando la morte di oltre il 30% degli individui infetti [28] . Le successive esplorazioni e colonizzazioni europee favorirono la diffusione della malattia in tutto il mondo conosciuto e il vaiolo divenne una delle più importanti cause di morbilità e mortalità [28] .

Non esistono descrizioni attendibili di casi di vaiolo nel continente americano prima dellacolonizzazione europea del XV secolo [46] . Nel 1507 fu introdotto sull'isola di Hispaniola e nel 1520 sulla terraferma, quando i coloni spagnoli si spostarono in Messico. Il vaiolo decimò la popolazione nativa amerinda e rese più rapida e facile la conquista degli imperi azteco e inca [28] . Nel 1633 , alla fondazione delle colonie nella costa orientale del Nord America seguì una devastante epidemia presso le popolazioni native americane [57] e, successivamente, per i coloni nati nel Nuovo Mondo [58] . Le stime parlano di un tasso di letalità della malattia presso i nativi americani dell'80-90% [59] . In Australia il vaiolo fu introdotto prima nel 1789 e di nuovo nel 1829 [28] , diventando la prima causa di morte per gli aborigeni australiani tra il 1780 e il 1870 [60] .
A partire dalla metà del XVIII secolo il vaiolo era la maggior malattia endemica in tutto il mondo, con l'eccezione dell'Australia e di altre piccole isole; in Europa rappresentava la prima causa di morte, con 400 000 decessi l'anno [9] .
Il vaiolo rappresentava il 10% delle cause di mortalità infantile in Svezia [8] e il tasso si stima fosse ancora più elevato in Russia [50] . L'uso della variolizzazione in alcuni Paesi, come in Cina, nel Regno Unito e nelle sue colonie nordamericane, ridusse l'impatto della malattia nei confronti delle classi agiate durante l'ultimo periodo del XVIII secolo, ma una vera riduzione dell' incidenza si ebbe solo quando la vaccinazione divenne prassi comune alla fine del XIX secolo. I vaccini e la pratica della rivaccinazione portarono a una riduzione dei casi solamente in Europa e in Nord America, mentre il vaiolo rimaneva incontrollato nel resto del mondo. Negli ultimi anni del XIX secolo fu identificata, negli Stati Uniti e in Sudafrica , la variola minor , che nella prima metà del XX secolo si espanse in molte parti del continente africano. Questa malattia, che causa una forma molto più lieve di vaiolo ed è caratterizzata da una minore letalità, garantisce l'immunità alla variola maior . Pertanto, nel giro di pochi anni, divenne la forma principale di vaiolo, soprattutto negli Stati Uniti, in Canada , in Sud America e nel Regno Unito, riducendo ulteriormente i tassi di mortalità [28] .
Eradicazione

Sin dalla dimostrazione di Jenner dell'efficacia della vaccinazione nel 1796 , furono fatti numerosi tentativi per eliminare il vaiolo su scala regionale. Nel 1803 il Regno di Spagna organizzò una missione per trasportare il vaccino nelle colonie dell' Impero spagnolo in America e nelle Filippine e vi creò un massiccio programma di vaccinazione [61] , e lo stesso fu fatto dal governo inglese in India [62] . Tuttavia, le campagne di vaccinazione britanniche in India e in Birmania furono ostacolate dalla testarda preferenza indigena per la variolizzazione e la diffidenza nei confronti della vaccinazione, nonostante le dure leggi, il miglioramento dell'efficacia della conservazione locale del vaccino e l'educazione sanitaria [63] . A partire da 1832 il Governo federale degli Stati Uniti d'America introdusse un programma di vaccinazione per i nativi americani [64] . Nel 1842 il Regno Unito bandì la pratica della variolizzazione, introducendo la vaccinazione obbligatoria nel 1853 [65] . Lo stesso avvenne negli Stati Uniti tra il 1843 e il 1855 , a partire dallo Stato del Massachusetts ; nonostante l'avversione di alcuni per questa misura [50] , nel 1897 il vaiolo era quasi scomparso dal Paese [66] . In molti Paesi dell'Europa settentrionale la malattia era stata debellata agli inizi del XIX secolo e, nel 1914 , l'incidenza nei Paesi industrializzati si era ridotta a valori relativamente bassi. La vaccinazione venne mantenuta fino ai tardi anni settanta per evitare la possibile reintroduzione del vaiolo da Paesi ancora endemici. L'Australia e la Nuova Zelanda furono invece un caso a parte, in quanto non introdussero mai un programma di vaccinazione preferendo la quarantena rigorosa, in quanto le grandi distanze e la bassa densità abitativa rendevano difficile il contagio [67] .
Il primo grande sforzo per eradicare il vaiolo dall'emisfero occidentale fu la campagna lanciata nel 1950 dalla Pan American Health Organization [68] ed ebbe successo nell'eliminare la malattia in tutti i Paesi americani, con l'eccezione dell' Argentina , del Brasile , della Colombia e dell' Ecuador [67] . Nel 1958 il ministro della sanità dell' Unione Sovietica , Viktor Zhdanov , fece un appello all' Assemblea mondiale della sanità dell' Organizzazione mondiale della sanità per intraprendere un'iniziativa mondiale finalizzata all'eradicazione globale della malattia, proposta che fu accettata, con la risoluzione WHA 11.54 , nel 1959 , anno in cui ancora due milioni di persone ogni anno morivano per il vaiolo [69] .
Nel complesso, tuttavia, i progressi verso l'eliminazione furono deludenti, soprattutto in Africa e nel subcontinente indiano . Nel 1967 l'OMS intensificò gli sforzi, contribuendo con 2,4 milioni di dollari annui e introducendo il metodo della sorveglianza sanitaria, una metodica epidemiologica che permette il monitoraggio della diffusione della malattia al fine di stabilire i modelli di progressione [70] .
Si stima che i casi di vaiolo annui fossero, nei primi anni cinquanta , oltre 50 milioni [14] . Per sradicare il vaiolo, si doveva impedire a ogni focolaio di diffondersi, attraverso l'isolamento dei malati e la vaccinazione di tutti coloro che vivevano nelle vicinanze. La chiave strategica è stata il monitoraggio di tutti casi di una comunità e il contenimento. Il problema iniziale che l'OMS si trovò di fronte era l'inadeguata segnalazione dei casi di vaiolo, in quanto molti casi non venivano denunciati alle autorità sanitarie, pertanto fu creata una rete di consulenti che aiutassero i Paesi nella creazione di strutture di sorveglianza e di contenimento. Il fatto che gli esseri umani fossero l'unico serbatoio del virus e che non esistessero portatori sani , giocò un ruolo fondamentale nell'eradicazione del vaiolo. All'inizio le dosi di vaccino furono fornite principalmente da Unione Sovietica e Stati Uniti, ma, nel 1973 , oltre l'80% della produzione avveniva nei Paesi in via di sviluppo [67] .
L'ultimo focolaio di vaiolo in Europa avvenne in Jugoslavia nel 1972 , a causa di un pellegrino del Kosovo ritornato dal Medio Oriente , dove aveva contratto il virus, e causò l'infezione di 175 persone, delle quali 35 morirono. Le autorità decisero di instaurare la legge marziale , forzando la quarantena, intraprendendo una massiccia campagna di rivaccinazione e richiedendo l'aiuto dell'OMS. In due mesi l'epidemia terminò [71] . Precedentemente a questa ci fu un focolaio a Stoccolma , tra il maggio e il luglio del 1963 , causato da un marinaio svedese di ritorno dall' Estremo Oriente . Anche in questo caso l'epidemia fu tenuta sotto controllo da misure di quarantena e vaccinazione della popolazione locale [72] .
Alla fine del 1975 il vaiolo resisteva solo nel Corno d'Africa , in Etiopia e Somalia . Le condizioni erano difficili per via della guerra civile, della carestia , dei profughi e della carenza di strade e altre vie di comunicazione. Un programma di sorveglianza intensiva, di contenimento e di vaccinazione fu avviato in questi Paesi nella prima metà del 1977 [73] . L'ultimo caso di contagio naturale con il virus, nella variante variola minor , fu diagnosticato in Somalia il 26 ottobre 1977 [21] . L'ultimo caso di variola maior contratta naturalmente risale all'ottobre del 1975 , in una bambina bengalese di due anni [30] .
L'eradicazione mondiale del vaiolo fu certificata da una commissione di eminenti scienziati, dopo intense attività di verifica nei vari Paesi, il 9 dicembre 1979 e successivamente approvata con una risoluzione dell' Assemblea mondiale della sanità dell'OMS l'8 maggio 1980 [14] [74] . Le prime due frasi della risoluzione riportano:
| ( EN ) «Having considered the development and results of the global program on smallpox eradication initiated by WHO in 1958 and intensified since 1967 … Declares solemnly that the world and its peoples have won freedom from smallpox, which was a most devastating disease sweeping in epidemic form through many countries since earliest time, leaving death, blindness and disfigurement in its wake and which only a decade ago was rampant in Africa, Asia and South America [75] .» | ( IT ) «Dopo aver considerato lo sviluppo ei risultati del programma globale di eradicazione del vaiolo avviato dall'OMS nel 1958 e intensificato a partire dal 1967 [...] dichiara solennemente che il mondo ei suoi popoli hanno ottenuto la libertà dal vaiolo, una delle malattie più devastanti a manifestarsi con epidemie in molti paesi sin dai tempi più remoti, lasciando morte, cecità e deturpazione nella sua scia e che solo un decennio fa era dilagante in Africa, Asia e Sud America.» |
| ( World Health Organization, Risoluzione WHA 33.3 ) | |
Dopo l'eradicazione
Gli ultimi due casi di vaiolo al mondo si sono verificati a Birmingham , nel Regno Unito, nel 1978 , quando due dipendenti della Facoltà di Medicina dell' Università di Birmingham contrassero il virus e uno dei due morì, l'11 settembre 1978 [75] . Dopo questo fatto Henry Bedson, responsabile scientifico dell'Università per la ricerca contro il vaiolo, si suicidò [3] . Alla luce di questo incidente, tutte le riserve conosciute di vaiolo furono distrutte o trasferite in uno dei due laboratori di riferimento dell'OMS dotati di un livello di sicurezza adeguato : il CDC di Atlanta e il Centro di ricerca statale di virologia e biotecnologia VECTOR di Kol'covo , in Russia [76] .
È del 1986 la prima raccomandazione dell'OMS riguardo alla distruzione del virus, con data fissata il 30 dicembre 1993 e poi posposta al 30 giugno 1999 [77] . A causa della resistenza da parte degli Stati Uniti e Russia, nel 2002 l' Assemblea mondiale della sanità dell'OMS ha deciso di consentire il mantenimento temporaneo degli stock di virus a scopo di ricerca [78] . La distruzione delle scorte esistenti potrebbe ridurre il rischio che comporta la ricerca in corso sul vaiolo e le scorte non sono necessarie per rispondere a un'eventuale epidemia di vaiolo [79] , tuttavia alcuni scienziati sostengono che le scorte possano essere utili nello sviluppo di nuovi vaccini, farmaci antivirali e test diagnostici [80] . Una pubblicazione del 2010 di una squadra di esperti di salute pubblica, nominati dall'OMS, ha concluso che non vi sia alcuna essenziale questione di sanità pubblica che giustifichi Stati Uniti e Russia a mantenere riserve di virus [81] e questa opinione è generalmente condivisa dalla comunità scientifica , in particolare tra gli ex responsabili del programma dell'OMS per l'eradicazione del vaiolo [82] .
Il vaiolo come arma biologica
Gli inglesi considerarono di utilizzare il vaiolo come arma biologica nell'assedio di Fort Pill durante la guerra franco-indiana (1754-1763) contro i francesi ei loro alleati nativi americani [83] [84] [85] [86] , mentre è stato ipotizzato che lo stesso agente patogeno sia stato utilizzato come arma durante la guerra di indipendenza americana (1775-1783) [87] [88] .
Durante la seconda guerra mondiale gli scienziati del Regno Unito, degli Stati Uniti e del Giappone sono stati coinvolti nella ricerca per produrre un'arma biologica dal vaiolo [89] . Tuttavia non furono mai attuati piani per una produzione in larga scala, poiché si ritenne che, in presenza di un vaccino efficace, l'arma non avrebbe avuto l'efficacia sperata [90] .
Nel 1947 l'Unione Sovietica costruì una fabbrica per la creazione di armi biologiche basate sul vaiolo nella città di Zagorsk , 75 km a nord di Mosca [91] e si suppone si sia verificata un'epidemia causata da alcuni test negli anni settanta [92] . In seguito a pressioni internazionali, il governo sovietico autorizzò nel 1991 un'ispezione da parte di un team anglo-americano di quattro dei più importanti impianti bellici. Gli ispettori ricevettero risposte evasive e smentite da parte dagli scienziati sovietici e alla fine furono allontanati dalla struttura [93] . Nel 1992 , Ken Alibek, un disertore russo, sostenne che il programma sovietico di armi biologiche a Zagorsk abbia prodotto una scorta di venti tonnellate di virus da usare eventualmente come arma e testate refrigerate per il loro trasporto [94] . Nel 1997 , il governo russo annunciò che tutti i suoi campioni di vaiolo rimanenti sarebbero stati trasferiti al Centro di ricerca statale di virologia e biotecnologia VECTOR di Kol'covo [93] . Dopo il crollo dell'Unione Sovietica e la disoccupazione di molti degli scienziati responsabili del programma bellico, i funzionari del governo degli Stati Uniti hanno espresso la preoccupazione di come il vaiolo e la competenza per ottenerne un'arma possa permettere ad altri governi oa gruppi terroristici di utilizzare il virus come mezzo di guerra biologica [95] . Accuse specifiche mosse contro l' Iraq a tale proposito, tuttavia, si sono rivelate false [96] . Alcuni hanno espresso la preoccupazione che la sintesi genetica artificiale possa essere utilizzata per ricreare il virus a partire da genomi già esistenti per utilizzarlo come arma biologica, dal momento che è teoricamente fattibile l'inserimento del DNA del virus del vaiolo all'interno di strutture virali simili, come altri Orthopoxvirus [97] .
Dopo gli attacchi terroristici dell'11 settembre 2001 , il governo degli Stati Uniti si allertò contro il rischio di un attacco bioterroristico . Fu prodotto un gran numero di dosi di vaccino per essere in grado di immunizzare la popolazione americana nel caso di una nuova epidemia di vaiolo e, nel dicembre 2002 , un programma speciale del governo ha offerto la possibilità, a qualunque cittadino lo desiderasse, di vaccinarsi contro il virus del vaiolo. Tra il dicembre 2002 e il marzo 2003 sono stati vaccinati oltre 25 000 civili e oltre 325 000 militari americani [98] .
L' Italia possiede cinque milioni di dosi di vaccino che, in caso di necessità, possono essere diluite con la possibilità di vaccinare 25 milioni di persone [98] .
Note
- ^ ( EN ) Ryan KJ, Ray CG (editors), Sherris Medical Microbiology , 4th, McGraw Hill, 2004, pp. 525–8, ISBN 0-8385-8529-9 .
- ^ vaiolo , in Treccani.it – Vocabolario Treccani on line , Istituto dell'Enciclopedia Italiana.
- ^ a b c ( EN ) Barquet N, Domingo P, Smallpox: the triumph over the most terrible of the ministers of death , in Ann. Intern. Med. , vol. 127, 8 Pt 1, 15 ottobre 1997, pp. 635–42, PMID 9341063 .
- ^ a b c ( EN ) Behbehani AM, The smallpox story: life and death of an old disease , in Microbiol Rev , vol. 47, n. 4, 1º dicembre 1983, pp. 455–509, PMC 281588 , PMID 6319980 .
- ^ a b c d e f g h i j ( EN ) Smallpox , su afip.org , Armed Forces Institute of Pathology: Department of Infectious and Parasitic Diseases, 9 ottobre 2007. URL consultato il 7 luglio 2012 (archiviato dall' url originale il 9 ottobre 2007) .
- ^ ( EN ) Jezek Z, Hardjotanojo W, Rangaraj AG, Facial scarring after varicella. A comparison between variola major and variola minor , in Am. J. Epidemiol. , vol. 114, n. 6, 1981, pp. 798–803, PMID 7315828 .
- ^ a b ( EN ) Donald Hopkins, Ramses V:Earliest known victim? ( PDF ), su whqlibdoc.who.int , WHO. URL consultato il 6 luglio 2012 .
- ^ a b c ( EN ) JN Hays, Epidemics and pandemics: their impacts on human history , ABC-CLIO, 2005, p. 151, ISBN 1-85109-658-2 .
- ^ a b ( EN ) Donald A. Henderson and Bernard Moss, Vaccines , Filadelfia, Saunders, 1999.
- ^ ( EN ) Riedel S, Edward Jenner and the history of smallpox and vaccination , in Proc (Bayl Univ Med Cent) , vol. 18, n. 1, 2005, pp. 21–5, PMC 1200696 , PMID 16200144 .
- ^ ( EN ) Koplow, David A., Smallpox: the fight to eradicate a global scourge , Berkeley, University of California Press, 2003, ISBN 0-520-24220-3 .
- ^ ( EN ) UC Davis Magazine, Summer 2006: Epidemics on the Horizon , su ucdavismagazine.ucdavis.edu . URL consultato il 7 luglio 2012 (archiviato dall' url originale il 30 maggio 2012) .
- ^ ( EN ) How Poxviruses Such As Smallpox Evade The Immune System , su sciencedaily.com , ScienceDaily, 1º febbraio 2008. URL consultato il 7 luglio 2012 .
- ^ a b c d e f ( EN ) Smallpox , su WHO Factsheet . URL consultato il 6 luglio 2012 (archiviato dall' url originale il 23 ottobre 2012) .
- ^ ( EN ) De Kevin M. Cock, (Book Review) The Eradication of Smallpox: Edward Jenner and The First and Only Eradication of a Human Infectious Disease , in Nature Medicine , vol. 7, n. 1, 2001, pp. 15–6, DOI : 10.1038/83283 .
- ^ ( EN ) Tognotti E., The eradication of smallpox, a success story for modern medicine and public health: What lessons for the future? ( PDF ), in J Infect Dev Ctries , vol. 4, n. 5, giugno 2010, pp. 264–266, PMID 20539058 . URL consultato il 7 luglio 2012 (archiviato dall' url originale il 2 aprile 2015) .
- ^ ( EN ) The world is free of rinderpest , su mg.co.za , The Mail and Guardian, 25 maggio 2011. URL consultato il 7 luglio 2012 .
- ^ ( EN ) Dubochet J, Adrian M, Richter K, Garces J, Wittek R, Structure of intracellular mature vaccinia virus observed by cryoelectron microscopy , in J. Virol. , vol. 68, n. 3, 1994, pp. 1935–41, PMC 236655 , PMID 8107253 .
- ^ a b ( EN ) Moss B, Poxviridae: the viruses and their replication , in Fields BN, Knipe DM, Howley PM, et al. (eds) (a cura di), Fields Virology , Vol 2, 5ª ed., Filadelfia, Lippincott-Raven, 2006, pp. 2905–46, ISBN 0-7817-6060-7 .
- ^ ( EN ) Damon I, Poxviruses , in Fields BN, Knipe DM, Howley PM, et al. (eds) (a cura di), Fields Virology , vol. 2, 5ª ed., Filadelfia, Lippincott-Raven, 2006, pp. 2947–76, ISBN 0-7817-6060-7 .
- ^ a b c d e f g h i j k l m n o p q r s t u v ( EN ) Atkinson W, Hamborsky J, McIntyre L, Wolfe S (eds.), Smallpox ( PDF ), in Epidemiology and Prevention of Vaccine-Preventable Diseases (The Pink Book) , 9ª ed., Washington DC, Public Health Foundation, 2005, pp. 281–306 (archiviato dall' url originale il 9 aprile 2010) .
- ^ a b ( EN ) CDC Smallpox , su Smallpox Overview . URL consultato il 7 luglio 2012 (archiviato dall' url originale il 2 aprile 2013) .
- ^ ( EN ) Henderson DA, Parker G, Perl T, Inglesby TV, Bartlett JC et al. , Smallpox as a biological weapon: medical and public health management. Working Group on Civilian Biodefense , in JAMA , vol. 281, n. 22, 1999, pp. 2127–37, DOI : 10.1001/jama.281.22.2127 , PMID 10367824 .
- ^ ( EN ) Ayyagari Ramachandra Rao, Smallpox , Bombay, Kothari Book Depot, 1972.
- ^ a b ( EN ) Hogan CJ, Harchelroad F, CBRNE – Smallpox , su eMedicine . URL consultato il 7 luglio 2012 .
- ^ a b c d ( EN ) Smallpox Disease and Its Clinical Management ( PDF ), su dal corso di formazione denominato "Smallpox: Disease, Prevention, and Intervention" . URL consultato il 7 luglio 2012 (archiviato dall' url originale il 10 maggio 2016) .
- ^ Si tratta di pustole confluenti quando la loro dimensione e numerosità è tale che queste si toccano tra loro, convergendo e apparendo come un liquido che cola.
- ^ a b c d e f g h i ( EN ) Fenner, Frank, Smallpox and Its Eradication (History of International Public Health, No. 6) ( PDF ), Geneva, World Health Organization, 1988, ISBN 92-4-156110-6 .
- ^ a b Vassil St. Georgiev, National Institute of Allergy and Infectious Diseases, NIH: Impact on Global Health , 2º, Springer, 2009, p. 229, ISBN 978-1-60327-296-4 .
- ^ a b ( EN ) Richard Preston, A reporter at large: Demon in the Freezer , su cryptome.org , The New Yorker, 12 luglio 1999. URL consultato il 7 luglio 2012 .
- ^ ( EN ) Riedel S, Smallpox and biological warfare: a disease revisited , in Proc (Bayl Univ Med Cent) , vol. 18, n. 1, gennaio 2005, pp. 13–20, PMC 1200695 , PMID 16200143 .
- ^ ( EN ) Smallpox: Current, comprehensive information on pathogenesis, microbiology, epidemiology, diagnosis, treatment, and prophylaxis , su cidrap.umn.edu , Center for Infectious Disease Research & Policy. URL consultato il 7 luglio 2012 .
- ^ ( EN ) LeDuc JW, Jahrling PB, Strengthening national preparedness for smallpox: an update , in Emerging Infect. Dis. , vol. 7, n. 1, 2001, pp. 155–7, DOI : 10.3201/eid0701.010125 , PMC 2631676 , PMID 11266310 .
- ^ ( EN ) Bourzac K, Smallpox: Historical Review of a Potential Bioterrorist Tool , in Journal of Young Investigators , vol. 6, n. 3, 2002. URL consultato l'8 luglio 2012 (archiviato dall' url originale il 1º novembre 2012) .
- ^ ( EN ) Pankhurst R., The history and traditional treatment of smallpox in Ethiopia. ( PDF ), in Med Hist. , vol. 9, n. 4, ottobre 1965, pp. 343-55, PMID 5323754 . URL consultato il 6 novembre 2010 .
- ^ ( EN ) Dominik Wujastyk, "Medicine in India" in Oriental Medicine: An Illustrated Guide to the Asian Arts of Healing , Londra, Serindia Publications, 1995, p. 29, ISBN 0-906026-36-9 .
- ^ ( EN ) Robert Temple, The Genius of China: 3,000 Years of Science, Discovery, and Invention , New York, Simon and Schuster, Inc., 1986, pp. 135–7, ISBN 0-671-62028-2 .
- ^ ( EN ) Modern History Sourcebook: Lady Mary Wortley Montagu (1689–1762): Smallpox Vaccination in Turkey , su fordham.edu . URL consultato il 7 luglio 2012 .
- ^ ( EN ) Frequently Asked Questions About Smallpox Vaccine , su bt.cdc.gov , Centers for Disease Control and Prevention, Ultima revisione del 7 febbraio 2007. URL consultato l'8 luglio 2012 (archiviato dall' url originale il 16 novembre 2015) .
- ^ a b c ( EN ) Vaccine Overview ( PDF ), su Smallpox Fact Sheet . URL consultato l'8 luglio 2012 (archiviato dall' url originale il 2 gennaio 2008) .
- ^ ( EN ) Mack TM, Smallpox in Europe, 1950–1971 , in J. Infect. Dis. , vol. 125, n. 2, 1972, pp. 161–9, DOI : 10.1093/infdis/125.2.161 , PMID 5007552 .
- ^ ( EN ) Pütz MM, Alberini I, Midgley CM, Manini I, Montomoli E, Geoffrey L. Smith, Prevalence of antibodies to Vaccinia virus after smallpox vaccination in Italy , in J. Gen. Virol. , vol. 86, n. 11, 2005, pp. 2955–60, DOI : 10.1099/vir.0.81265-0 , PMID 16227216 . URL consultato l'8 luglio 2012 (archiviato dall' url originale il 12 febbraio 2009) .
- ^ a b ( EN ) Fenner, Frank, Development of the Global Smallpox Eradication Programme ( PDF ), in Smallpox and Its Eradication (History of International Public Health, No. 6) , Geneva, World Health Organization, 1988, pp. 31,125, ISBN 92-4-156110-6 (archiviato dall' url originale il 15 gennaio 2011) .
- ^ ( EN ) Bray M, Roy CJ, Antiviral prophylaxis of smallpox , in J. Antimicrob. Chemother. , vol. 54, n. 1, 2004, pp. 1–5, DOI : 10.1093/jac/dkh286 , PMID 15163655 .
- ^ ( EN ) Esposito JJ, Sammons SA, Frace AM, et al. , Genome sequence diversity and clues to the evolution of variola (smallpox) virus , in Science , vol. 313, n. 5788, agosto 2006, pp. 807–12, DOI : 10.1126/science.1125134 , PMID 16873609 .
- ^ a b ( EN ) Li Y, Carroll DS, Gardner SN, Walsh MC, Vitalis EA, Damon IK, On the origin of smallpox: correlating variola phylogenics with historical smallpox records , in Proc Natl Acad Sci USA , vol. 104, n. 40, 2007, pp. 15787-15792.
- ^ a b ( EN ) Spaeth GL, Reversibility of optic disc cupping. A phenomenon that may change the management of glaucoma , in Arch. Ophthalmol. , vol. 107, n. 11, novembre 1989, pp. 1583–4, PMID 2818276 .
- ^ ( EN ) Shchelkunov SN, Emergence and reemergence of smallpox: the need for development of a new generation smallpox vaccine , in Vaccine , 29 Suppl 4, dicembre 2011, pp. D49–53, DOI : 10.1016/j.vaccine.2011.05.037 , PMID 22185833 .
- ^ ( EN ) Herbert M. Shelton, Vaccine and Serum Evils , Health Research Books, 1996, p. 5, ISBN 1-85810-029-1 .
- ^ a b c ( EN ) Hopkins DR,The Greatest Killer: Smallpox in history , University of Chicago Press, 2002, ISBN 0-226-35168-8 . originariamente pubblicato come Princes and Peasants: Smallpox in History (1983), ISBN 0-226-35177-7
- ^ ( EN ) Horst R. Thieme, Mathematics in population biology , Princeton University Press, 2003, ISBN 0-691-09291-5 .
- ^ ( EN ) Donald Henderson, Richard Preston, Smallpox- the Death of a Disease: The Inside Story of Eradicating a Worldwide Killer , 1ª ed., Prometheus Books, 23 giugno 2009, p. 334, ISBN 1-59102-722-5 .
- ^ ( EN ) Cyril William Dixon, Smallpox , Londra, Churchill, 1962, ISBN 0-7000-1124-2 .
- ^ Conclusione di H. Haeser, in Lehrbuch der Geschichte der Medicin und der epidemischen Krankenheiten III:24–33 (1882), seguita da Zinsser 1996.
- ^ ( EN ) Past pandemics that ravaged Europe , su news.bbc.co.uk , BBC News, 7 novembre 2005. URL consultato l'8 luglio 2012 .
- ^ ( EN ) Harminder S. Dua, Ahmad Muneer Otri, Arun D. Singh, Abu Bakr Razi , in British Journal of Ophthalmology , vol. 92, BMJ Group, 2008, p. 1324.
- ^ ( EN ) Frederick E. Hoxie, Encyclopedia of North American Indians , 1996, p. 164, ISBN 0-395-66921-9 .
- ^ ( EN ) David A. Koplow, Smallpox The Fight to Eradicate a Global Scourge , su ucpress.edu , University of California Press, 2003. URL consultato l'8 luglio 2012 .
- ^ ( EN ) Arthur C. Aufderheide, Conrado Rodríguez-Martín, Odin Langsjoen, The Cambridge encyclopedia of human paleopathology , Cambridge University Press, 1998, p. 205, ISBN 0-521-55203-6 .
- ^ ( EN ) Ian Glynn, Jenifer Glynn, The life and death of smallpox , Cambridge University Press, 2004, p. 145, ISBN 0-521-84542-4 .
- ^ ( EN ) Rafael E. Tarrago, The Balmis-Salvany Smallpox Expedition: The First Public Health Vaccination Campaign in South America , su paho.org , 2001. URL consultato l'8 luglio 2012 .
- ^ ( EN ) Smallpox History: Other histories of smallpox in South Asia , su smallpoxhistory.ucl.ac.uk , 18 luglio 2006. URL consultato l'8 luglio 2012 (archiviato dall' url originale il 16 aprile 2012) .
- ^ ( EN ) Atsuko Naono, State of Vaccination: The Fight Against Smallpox in Colonial Burma , su indianmedicine.eldoc.ub.rug.nl , Orient BlackSwan, 2009. URL consultato l'8 luglio 2012 (archiviato dall' url originale il 24 luglio 2011) .
- ^ ( EN ) Indian Health Program - Capitolo 3 , su ihs.gov , Indian Health Service. URL consultato l'8 luglio 2012 .
- ^ ( EN ) Nadja Durbach, Bodily Matters: The Anti-Vaccination Movement in England, 1853–1907 , Duke University Press, ISBN 0-8223-3423-2 .
- ^ ( EN ) CV Chapin, Variation in type of infectious disease as shown by the history of smallpox in the United States 1895–1912 , in Infect Dis , vol. 13, n. 2, 1913, pp. 171–196, DOI : 10.1093/infdis/13.2.171 .
- ^ a b c ( EN ) Walter A. Orenstein, Stanley A. Plotkin, Vaccines , Philadelphia, WB Saunders Co, 1999, ISBN 0-7216-7443-7 .
- ^ ( EN ) Rodrigues BA, Smallpox eradication in the Americas , in Bull Pan Am Health Organ , vol. 9, n. 1, 1975, pp. 53–68, PMID 167890 .
- ^ ( EN ) Frank Fenner, Development of the Global Smallpox Eradication Programme ( PDF ), in Smallpox and Its Eradication (History of International Public Health, No. 6) , Geneva, World Health Organization, 1988, pp. 366–418, ISBN 92-4-156110-6 (archiviato dall' url originale il 15 gennaio 2011) .
- ^ ( EN ) Holland WW, Karel Raska: The development of modern epidemiology. The role of the IEA ( PDF ), in Cent. Eur. J. Public Health , vol. 18, n. 1, marzo 2010, pp. 57–60, PMID 20586233 .
- ^ ( EN ) BBC History - Smallpox: Eradicating the Scourge , su bbc.co.uk . URL consultato l'8 luglio 2012 .
- ^ ( EN ) Centers for Disease Control and Prevention (CDC), International Notes: Quarantine Measures Smallpox—Stockholm, Sweden, 1963 , in MMWR , vol. 45, n. 25, 1996, pp. 538–45, PMID 9132571 .
- ^ ( EN ) William Grimes, Frank Fenner Dies at 95 , su NYTimes.com , 8 luglio 2012. URL consultato il 27 novembre 2010 .
- ^ ( EN ) Frank Fenner, Nature, Nurture and Chance: The Lives of Frank and Charles Fenner , Canberra, Australian National University Press, 2006, ISBN 1-920942-62-9 .
- ^ a b ( EN ) Pennington H, Smallpox and bioterrorism , in Bull. World Health Organ. , vol. 81, n. 10, 2003, pp. 762–7, DOI :10.1590/S0042-96862003001000014 , PMC 2572332 , PMID 14758439 .
- ^ ( EN ) World Health Organization, WHO establishing smallpox vaccine reserve , su who.int , 25 maggio 2005. URL consultato l'8 luglio 2012 .
- ^ ( EN ) Lawrence Altman, Final Stock of the Smallpox Virus Now Nearer to Extinction in Labs , su nytimes.com , New York Times, 25 gennaio 1996. URL consultato l'8 luglio 2012 .
- ^ ( EN ) Debora MacKenzie, Stay of execution , su newscientist.com , New Scientist, 26 gennaio 2002. URL consultato l'8 luglio 2012 .
- ^ ( EN ) Edward Hammond, Should the US and Russia destroy their stocks of smallpox virus? , in BMJ , vol. 334, n. 7597, 2007, p. 774, DOI : 10.1136/bmj.39155.695255.94 , PMC 1851992 , PMID 17431261 .
- ^ ( EN ) John O. Agwunobi,Should the US and Russia destroy their stocks of smallpox virus? , in BMJ , vol. 334, n. 7597, 2007, p. 775, DOI : 10.1136/bmj.39156.490799.BE , PMC 1851995 , PMID 17431262 .
- ^ ( EN ) Advisory Group of Independent Experts to review the smallpox research program (AGIES), Comments on the Scientific Review of Variola Virus Research, 1999‐2010 , su who.int . URL consultato l'8 luglio 2012 .
- ^ ( EN ) Michael J. Lane, Gregory A. Poland, Why not destroy the remaining smallpox virus stocks? ( PDF ), in Vaccine , vol. 29, n. 16, Elsevier, 2011, pp. 2823–2824, DOI : 10.1016/j.vaccine.2011.02.081 , PMID 21376120 .
- ^ ( EN ) Howard Henry Peckham, Pontiac and the Indian Uprising , Wayne State University Press, 1947, p. 226, ISBN 0-8143-2469-X .
- ^ Fred Anderson, Crucible of War: The Seven Years' War and the Fate of Empire in British North America, 1754-1766 , Vintage Books, id= ISBN 0-375-70636-4 , p. 542.
- ^ ( EN ) ( EN ) John Grenier, The First Way of War , Cambridge University Press, 2005, p. 144, ISBN 978-0-521-84566-3 .
- ^ ( EN ) William Nester, Haughty Conquerors: Amherst and the Great Indian Uprising of 1763 , Greenwood Publishing Group, 2000, pp. 114–15, ISBN 0-275-96770-0 .
- ^ ( EN ) BBC History: Silent Weapon: Smallpox and Biological Warfare , su bbc.co.uk . URL consultato l'8 luglio 2012 .
- ^ ( EN ) Elizabeth A. Fenn, Biological Warfare in Eighteenth-Century North America: Beyond Jeffery Amherst , in The Journal of American History , vol. 86, n. 4, marzo 2000, pp. 1552–1580 (archiviato dall' url originale il 3 aprile 2015) .
- ^ ( EN ) USAMRIID's Medical Management of Biological Casualties Handbook ( PDF ), su usamriid.army.mil . URL consultato l'8 luglio 2012 (archiviato dall' url originale il 9 febbraio 2015) .
- ^ ( EN ) BBC History: Silent Weapon: Smallpox and Biological Warfare , su bbc.co.uk . URL consultato l'8 luglio 2012 .
- ^ ( EN ) Kenneth Alibek, Handelman S,Biohazard: The Chilling True Story of the Largest Covert Biological Weapons Program in the World Told from Inside by the Man Who Ran It , New York, Delta, 1999, ISBN 0-385-33496-6 .
- ^ ( EN ) Shoham D, Wolfson Z, The Russian biological weapons program: vanished or disappeared? , in Crit. Rev. Microbiol. , vol. 30, n. 4, 2004, pp. 241–61, DOI : 10.1080/10408410490468812 , PMID 15646399 .
- ^ a b ( EN ) Richard Preston, The Demon in the Freezer , Fawcett, pp. 105–115, ISBN 0-345-46663-2 .
- ^ ( EN ) Ken Alibek, Steven Handelman,Biohazard: The Chilling True Story of the Largest Covert Biological Weapons Program in the World - Told from Inside by the Man Who Ran It , Random House, 1999, ISBN 0-385-33496-6 .
- ^ ( EN ) History and Epidemiology of Global Smallpox Eradication ( PDF ), su bt.cdc.gov . URL consultato l'8 luglio 2012 (archiviato dall' url originale il 15 luglio 2007) .
- ^ ( EN ) Oliver Burkeman, No evidence of smallpox , su guardian.co.uk , 19 settembre 2003. URL consultato l'8 luglio 2012 .
- ^ ( EN ) The Genetic Engineering of Smallpox. WHO's Retreat from the Eradication of Smallpox Virus and Why it Should be Stopped ( PDF ), su biosafety-info.net , 2002. URL consultato l'8 luglio 2012 (archiviato dall' url originale il 3 marzo 2016) .
- ^ a b Vaiolo - Portale dell'epidemiologia per la sanità pubblica a cura del Centro Nazionale di Epidemiologia, Sorveglianza e Promozione della Salute , su epicentro.iss.it . URL consultato l'8 luglio 2012 .
Approfondimenti
- ( EN ) Bhattacharya, Sanjoy, Expunging variola: the control and eradication of smallpox in India, 1947–1977 , Hyderabad, Orient Longman, 2006, ISBN 81-250-3018-2 .
- ( EN ) Fenner, Frank, Smallpox and Its Eradication (History of International Public Health, No. 6) ( PDF ), Geneva, World Health Organization, 1988, ISBN 92-4-156110-6 .
- ( EN ) Koplow, David A.,Smallpox: the fight to eradicate a global scourge , Berkeley, University of California Press, 2003, ISBN 0-520-24220-3 .
- ( EN ) Mack T, A different view of smallpox and vaccination , in N. Engl. J. Med. , vol. 348, n. 5, 2003, pp. 460–3, DOI : 10.1056/NEJMsb022994 , PMID 12496354 .
- ( EN ) McNeill, William Hardy, Plagues and peoples , Oxford, Basil Blackwell, 1977, ISBN 0-385-12122-9 .
- ( EN ) Naono, Atsuko, State of Vaccination: The Fight Against Smallpox in Colonial Burma , Hyderabad, Orient Blackswan, 2009, p. 238, ISBN 978-81-250-3546-6 .
- ( EN ) Preston, Richard, The Demon in the Freezer: A True Story , New York, Random House, 2002, ISBN 0-375-50856-2 . (Estratto presente qui )
- ( EN ) Tucker, Jonathan B., Scourge: The Once and Future Threat of Smallpox , New York, Grove Press, 2001, ISBN 0-8021-3939-6 .
Bibliografia
- TR Harrison, Principi di medicina interna , 16ª ed., Milano, McGraw-Hill, 2005, ISBN 88-386-2999-4 .
- RL Robbins, RS Cotran, V.Eusebi, AK Abbas, V. Kumar, JA Perkins, N. Fausto, La basi patologiche delle malattie , Milano, Elsevier Italia, 2006, ISBN 88-85675-53-0 .
- Murray, Rosenthal, Microbiologia , Napoli, EdiSES, 2007, ISBN 88-7959-262-9 .
Voci correlate
Altri progetti
-
 Wikiquote contiene citazioni sul vaiolo
Wikiquote contiene citazioni sul vaiolo -
 Wikizionario contiene il lemma di dizionario « vaiolo »
Wikizionario contiene il lemma di dizionario « vaiolo » -
 Wikimedia Commons contiene immagini o altri file sul vaiolo
Wikimedia Commons contiene immagini o altri file sul vaiolo -
 Wikispecies contiene informazioni sul vaiolo
Wikispecies contiene informazioni sul vaiolo
Collegamenti esterni
- ( EN ) Vaiolo , su Enciclopedia Britannica , Encyclopædia Britannica, Inc.
- ( EN , FR ) Vaiolo , su Enciclopedia canadese .
- La storia del vaiolo , su pediatria.it .
- Immagini di vaiolo e sinossi diagnostica , su logicalimages.com .
- Genoma del Variola Virus , su poxvirus.org . URL consultato il 7 luglio 2012 (archiviato dall' url originale il 12 settembre 2015) .
- Poxviridae sul Virus Pathogen Database and Analysis Resource (ViPR) , su viprbrc.org .
| Controllo di autorità | Thesaurus BNCF 43162 · LCCN ( EN ) sh85123612 · GND ( DE ) 4135714-0 · BNF ( FR ) cb11962556k (data) · NDL ( EN , JA ) 00573369 |
|---|