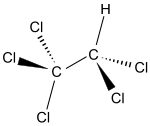
Pentacloretan
| pentacloretan | |||
|---|---|---|---|
| Numele IUPAC | |||
| 1,1,1,2,2-pentacloretan [1] [2] [3] | |||
| Denumiri alternative | |||
| Pentalino, pentaclorură de etan | |||
| Caracteristici generale | |||
| Formula moleculară sau brută | C 2 HCI 5 | ||
| Masa moleculară ( u ) | 202.09 [4] | ||
| Aspect | lichid incolor, miros dulce, similar cu cloroformul | ||
| numar CAS | Immagine_3D | ||
| Numărul EINECS | 200-925-1 | ||
| PubChem | 6419 | ||
| ZÂMBETE | C(C(Cl)(Cl)Cl)(Cl)Cl | ||
| Proprietăți fizico-chimice | |||
| Densitate (g / cm 3 , în cs ) | 1,68 | ||
| Solubilitate în apă | 0,05% (20 ° C) | ||
| Temperatură de topire | -29 ° C | ||
| Temperatura de fierbere | 162 ° C | ||
| Presiunea de vapori ( Pa ) la 295 K. | 3 mmHg (20 ° C) | ||
| Informații de siguranță | |||
| Simboluri de pericol chimic | |||
  | |||
| Fraze H | 351 - 372 - 411 [5] | ||
| Sfaturi P | 201 - 202 - 260 - 264 - 270 - 273 - 281 - 308 + 313 - 314 -391 - 405 - 501 [5] | ||
Pentacloretanul este un compus chimic inflamabil, dar toxic format din clor , hidrogen și carbon . Aparține clasei de compuși organici numiți halogenuri de alchil . Unul dintre cele 9 cloroetani, adică derivați ai etanului în care cinci din cei șase hidrogeni sunt înlocuiți cu clor.
Este insolubil în apă și mai dens. Este toxic prin inhalare și ingestie și poate irita pielea și ochii. Este utilizat în principal ca solvent pentru ulei și grăsimi, în curățarea metalelor și în separarea cărbunelui de impurități.
Sinteză
Deoarece tetracloretilena este produsă mai economic prin procesul de clorinoliză (o reacție chimică similară cu hidroliza în care clorul joacă rolul apei), producția industrială de pentacloretan este de mică importanță și, în prezent, practic nu este produsă, chiar și pentru efectele sale toxice. Dacă este necesar, sinteza poate fi realizată cu diferite procese:
- Oxiclorarea etilenei , obținând, pe lângă pentacloretan, hidrocarburi clorurate.
- Clorinarea unui cloretan, CHC 2 CHC 2 , sub radiație ultravioletă sau tricloretilenă la 70 ° C în prezență de clorură ferică , sulf sau de radiații ultraviolete.
- De asemenea, poate fi produs cu randamente bune prin clorurarea tricloretilenei, obținută într-un proces în două faze care implică clorinarea acetilenei pentru a obține tetracloretan, și îndepărtarea clorurii de hidrogen prin acțiunea unei baze .
Impact asupra mediului
Datorită impactului său asupra mediului , pentacloretanul nu este nici comercializat, nici importat în multe țări, inclusiv în Statele Unite. Cu toate acestea, acest compus poate fi eliberat în mediu ca produs al arderii din PVC. Când este eliberat în sol umed, acesta este moderat până la foarte mobil și poate suferi hidroliză chimică lentă. Pentacloretanul se poate volatiliza încet pe suprafețele uscate ale solului. Când este eliberată în apă, volatilitatea este un mecanism important, dacă nu dominant, de îndepărtare (timpul de înjumătățire de 5 ore într-un râu).
Acest compus are, de asemenea, potențialul de a se oxida în prezența luminii pentru a forma fosgenă și clorură de tricloracetil . Hidroliza chimică nu pare a fi importantă din punct de vedere ecologic. Dacă este eliberat în atmosferă, este de așteptat să fie aproape complet în faza de vapori. Poate apărea o ușoară absorbție a pentacloretanului în solidele suspendate sau sedimentate. Datorită persistenței sale în atmosferă, pot apărea procese de transport pe distanțe lungi.
Cloroetani
Raportăm cei 6 cloroetani și cei 3 izomeri structurali ai acestora
- Cloroetan
- 1,1-dicloroetan
- 1,2-dicloroetan (izomer)
- 1,1,1-tricloroetan
- 1,1,2-tricloroetan (izomer)
- 1,1,1,2-tetracloretan
- 1,1,2,2-tetracloretan (izomer)
- Pentacloretan
- Hexacloretan
Notă
- ^ (EN) R. Panico, WH Powell și JC Richer (eds), A Guide to IUPAC Nomenclature of Organic Compounds , Hoboken (New Jersey, SUA), IUPAC / Blackwell Science , 1993 ISBN 0-632-03488-2 .
- ^ (EN) PubChem Compound, Pentachloroethane - Compound Summary , pe pubchem.ncbi.nlm.nih.gov, Centrul Național pentru Informații despre Biotehnologie, 27 martie 2005. Adus pe 7 mai 2021.
- ^ (EN) Entități chimice de interes biologic, CHEBI: 76287 - pentacloretan , pe ebi.ac.uk, EBI (Marea Britanie), 14-01-2009. Adus 05-05-2021 .
- ^ (EN) Comisia IUPAC pentru abundențe izotopice și greutăți atomice. , Greutățile atomice ale elementelor 2017 , la Universitatea Queen Mary din Londra .
- ^ a b ( EN ) Foaia de siguranță și pericole a compusului pe Pubchem
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe pentacloretan
Wikimedia Commons conține imagini sau alte fișiere pe pentacloretan