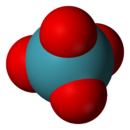
Tetroxid de xenon
| Tetroxid de xenon | |||
|---|---|---|---|
| Numele IUPAC | |||
| tetroxid de xenon | |||
| Caracteristici generale | |||
| Formula moleculară sau brută | XeO 4 | ||
| Masa moleculară ( u ) | 195,29 | ||
| Aspect | gaz incolor solid galben sub –36 ° C | ||
| numar CAS | |||
| ZÂMBETE | O=[Xe](=O)(=O)=O | ||
| Proprietăți fizico-chimice | |||
| Temperatură de topire | -35,9 ° C (237,3 K) | ||
| Proprietăți termochimice | |||
| Δ f H 0 (kJ mol −1 ) | 643 | ||
| Informații de siguranță | |||
| Simboluri de pericol chimic | |||
| | |||
Tetroxidul de xenon este compusul chimic cu formula XeO 4 , unde xenonul are un număr de oxidare +8 (cel mai mare posibil din tabelul periodic ). În condiții normale, este un gaz incolor foarte instabil. La temperaturi sub –35,9 ° C este mai stabil ca un solid cristalin galben, dar la temperaturi mai ridicate tinde să explodeze, descompunându-se în xenon și oxigen . [1] [2] XeO 4 este un compus de interes academic, fără uz practic.
Structura moleculară și configurația electronică
Molecula XeO 4 are 32 de electroni în stratul cel mai exterior și are o structură tetraedrică, în conformitate cu teoria VSEPR . Distanța Xe-O este 174 pm .
Sinteză
Pentru sinteza a 4 Xeo au nevoie de perxenati (ossoanioni Xe VIII), care sunt accesibile de la xenati (ossoanioni Xe VI) prin două metode. Prima este dismutarea xenatului în perxenat și xenon:
- 2XeO 4 2– → XeO 6 4– + Xe + O 2
Al doilea este oxidarea xenatului cu ozon în soluție de bază:
- XeO 4 2– + O 3 + 2OH - → XeO 6 4– + O 2 + H 2 O
Din aceste soluții, perxenatul de bariu ușor solubil Ba 2 XeO 6 poate fi precipitat, care este apoi tratat cu acid sulfuric concentrat . Instabil acidului perxenic se formează , care este deshidratat pentru a ajunge la XEO 4. Aceste reacții sunt realizate la -5 ° C și XEO 4 dezvoltă ca un gaz.
- Ba 2 XeO 6 + 2H 2 SO 4 → 2Ba 2 SO 4 + H 4 XeO 6
- H 4 XeO 6 → 2H 2 O + XeO 4
Reactivitate
Tetroxidul de xenon este un gaz cu o entalpie standard de formare puternic pozitivă (643 kJ / mol), [3] și tinde să se descompună exploziv pentru a forma xenon gaz și oxigen:
- XeO 4 → Xe + 2O 2
La temperaturi sub –39,5 ° C, este solid și considerabil mai stabil, dar trebuie tratat în continuare cu mare prudență, deoarece chiar și la temperaturi atât de scăzute au existat cazuri de explozie.
Prin reacția XeO 4 cu hexafluorură de xenon este posibilă prepararea altor compuși de xenon în starea de oxidare +8, cum ar fi XeO 3 F 2 și XeO 2 F 4 : [4]
- XeO 4 + XeF 6 → XeO 3 F 2 + XeOF 4
- XeO 3 F 2 + XeF 6 → XeO 2 F 4 + XeOF 4
Notă
- ^ John L. Huston, Martin H. Studier și Eric N. Sloth, Xenon Tetroxide: Mass Spectrum , în Știință , vol. 143, nr. 3611, 1964, pp. 1161-1162, DOI :10.1126 / science.143.3611.1161-a .
- ^ H. Selig, HH Claassen, CL Chernick, JG Malm, JL Huston, tetroxid de xenon: preparare și unele proprietăți , în Știință , vol. 143, nr. 3612, 1964, pp. 1322-1323. Adus pe 2 aprilie 2011 .
- ^ SR Gunn, Căldura de formare a tetroxidului de xenon , în J. Am. Chem. Soc., Voi. 87, nr. 10, 1965, pp. 2290–2291, DOI : 10.1021 / ja01088a038 .
- ^ CE Housecroft, AG Sharpe, Chimie anorganică , ediția a 3-a, Harlow (Anglia), Pearson Education Limited, 2008, ISBN 978-0-13-175553-6 .
Bibliografie
- NN Greenwood, A. Earnshaw, Chimia elementelor , ediția a II-a, Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4 .
- JG Malm, H. Selig, J. Jortner și SA Rice, Chimia xenonului , în Chem. Rev. , vol. 65, nr. 2, 1965, pp. 199-236, DOI : 10.1021 / cr60234a003 .