Camfor
| Camfor | |||
|---|---|---|---|
| Denumiri alternative | |||
| D - (+) - camfor, 1,7,7-trimetil-bicicletă [2.2.1] heptan-2-on | |||
| Caracteristici generale | |||
| Formula moleculară sau brută | C 10 H 16 O | ||
| Masa moleculară ( u ) | 152,24 g / mol | ||
| Aspect | solid incolor până la alb | ||
| numar CAS | |||
| Numărul EINECS | 200-945-0 | ||
| PubChem | 2537 | ||
| DrugBank | DB14156 | ||
| ZÂMBETE | CC1(C2CCC1(C(=O)C2)C)C | ||
| Proprietăți fizico-chimice | |||
| Densitate (g / cm 3 , în cs ) | 0,99 (20 ° C) | ||
| Solubilitate în apă | (20 ° C) insolubil | ||
| Temperatură de topire | 175 ° C (~ 448 K) | ||
| Temperatura de fierbere | 210 ° C (~ 483 K) | ||
| Informații de siguranță | |||
| Punct de flacără | 66 ° C (339 K) | ||
| Limite de explozie | 0,6 - 4,5% Vol | ||
| Temperatură de autoaprindere | 460 ° C (733 K) | ||
| Simboluri de pericol chimic | |||
   | |||
| Pericol | |||
| Fraze H | 228 - 315 - 319 - 335 | ||
| Sfaturi P | 210 - 302 + 352 - 304 + 340 - 305 + 351 + 338 [1] | ||
Camforul (sau D - (+) - camforul ), cu formula chimică C 10 H 16 O, este o cetonă ciclică, produsă prin oxidarea unui terpen , pinen C 10 H 16 .
Camforul este o substanță ceară, albă sau limpede, cu un miros puternic aromatic. Se găsește în mai multe plante, dar este extras în principal din lemnul Cinnamomum camphora ( Laurus camphora ), un arbore mare veșnic verde [2] , precum și al Dryobalanopsului aromatic (camforul Borneo), un gigant al pădurilor Borneo.
Substanța poate fi găsită și în alte plante înrudite din familia laurului, în special în Ocotea usambarensis (camfor african). Poate fi produs și sintetic din ulei de terebentină . Este folosit pentru parfumul său, ca ingredient în gătit (în special în India), ca fluid de îmbălsămare, în ceremoniile religioase și în scopuri medicinale. Una dintre principalele surse de camfor din Asia este Ocimum kilimandscharicum (Ocimum kilimandscharicum Baker ex Gurke, în engleză Camphor busuioc). Camforul se găsește și în busuioc , coriandru , maghiran , rozmarin și salvie [ fără sursă ] .
Istorie
Cuvântul camfor derivă din latina medievală camfora , din arabul kafur , din sanscrită karpoor . [3] Barus era portul de pe coasta de vest a insulei Sumatra, unde negustorii străini veneau să cumpere camfor, așa că în malaeză a devenit Kapur Barus. Camforul era cunoscut în Arabia deja în perioada pre-islamică, așa cum se menționează în Coranul LXXVI: 5, folosit ca aromă pentru băuturi. În secolul al IX-lea, filosoful și chimistul arab al-Kindi (cunoscut în Europa sub numele de Alkindus), a furnizat prima rețetă pentru producerea camforului în Kitāb kīmīyāʾ al-ʿitr (Cartea de chimie a parfumurilor). [4] Începând din secolul al XIII-lea , acesta a fost folosit în rețete în întreaga lume musulmană , de la feluri de mâncare principale, cum ar fi taridul tradițional, până la tocănițe și deserturi. [5]
Încă din secolul al XIX-lea se știa că, cu acidul azotic , camforul ar putea fi oxidat în acid camforic . Haller și Blanc au publicat o semisinteză a camforului din acidul camforic, care, deși și-a demonstrat structura, nu a dovedit-o. Prima sinteză totală completă pentru acid camforic a fost publicată de Gustaf Komppa în 1903 . El a început de la oxalat de dietil și acid 3,3-dimetilpentanoic, care a reacționat prin condensarea Claisen dând acidul diceto-camforic. Metilarea cu iodură de metil și o procedură complicată de reducere au produs acid camforic. William Perkin a publicat un alt rezumat la scurt timp după aceea. Anterior, unii compuși organici (cum ar fi ureea, de exemplu) fuseseră sintetizați în laborator, dar camforul era un produs natural în cantitate redusă și cu o cerere puternică în întreaga lume. Komppa a realizat acest lucru și a început producția industrială de camfor în Tainionkoski , Finlanda , în 1907 .
Au existat multe metode concepute pentru sinteza camforului, inclusiv cea concepută de chimistul Auguste Béhal , începând de la esența terebentinei C 10 H 16 și a lui Marcellin Berthelot , începând de la oxidarea borneolului C 10 H 18 O sau a camfenei C 10 H 16 .
Producție
Camforul poate fi produs din α-pinen , care este abundent în uleiuri de conifere și poate fi distilat din terebentină obținută ca produs al macerării chimice [6] . Cu acid acetic ca solvent și cu cataliză de către un acid puternic , α-pinenul se reorganizează ușor în camfen , care, la rândul său, suferă o rearanjare Wagner-Meerwein la cationul izobornil , care este captat de acetat care dă acetat de izobornil . Hidroliza la izobornil urmată de dehidrogenare dă camfor.
Extragerea camforului natural
Camforul natural este extras din plante adulte în vârstă de aproximativ 50 de ani. Copacii cu o circumferință de 4 metri asigură aproximativ 300 kg de camfor cristalizat. Pentru a extrage camforul într-un mod non-artizanal, dar industrial, frunzele și lemnul tocat sunt supuse distilării cu vapori de apă. Se obține un procent de 1,2-1,5% camfor și 0,5% ulei; procentele variază între vară și iarnă.
Camforul brut are de obicei multe impurități, cum ar fi apa, fierul, uleiul de camfor, nisipul, lemnul. Apa și uleiul sunt eliminate prin presiune sau prin centrifugă; apa poate fi eliminată și cu clorură de calciu sau cu var . Alte impurități sunt eliminate prin cristalizare sau sublimare . Camforul este apoi comercializat în blocuri sferice, cântărind de la 1,5 la 4 kg, alb, cristalin, semitransparent și elastic. Poate fi și sub formă de tablete (SUA), lăzi de 50-60 kg, butoaie din lemn.
Camforul obținut din Dryobalanopsul aromatic (camforul din Borneo) este rar, valoros, scump și are un gust și un miros foarte plăcut.
Biosinteza
În biosinteză , camforul este produs din piranfosfat de geranil , prin ciclizarea pirofosfatului linalol în pirofosfat borneol , urmat de hidroliza în borneol și oxidare în camfor.
Utilizări
Utilizările moderne includ camforul ca plastifiant pentru nitroceluloză , ca anti-molie, ca substanță antimicrobiană, în îmbălsămare, în artificii, explozivi, înlocuitori de piele. Camforul solid eliberează vapori care formează un strat anti-rugină și apoi sunt așezați în lăzile pentru scule pentru a proteja uneltele de rugină. [7] Cristalele de camfor sunt, de asemenea, utilizate pentru a preveni deteriorarea colecțiilor de insecte de către alte insecte mici.
Se folosește și în medicină. Camforul este absorbit rapid prin piele, produce o senzație de răcire similară cu cea a mentolului și acționează ca o substanță anestezică locală ușoară și substanță antimicrobiană . Există geluri anti-mâncărime și geluri răcoritoare care au camforul ca ingredient activ . Camforul este un ingredient activ (alături de mentol) în produsele cu aburi și este eficient ca un antitusiv. De asemenea, poate fi administrat oral în cantități mici (50 mg) pentru simptome ușoare ale inimii și oboseală. [8]
In secolul al 18 - lea, a fost folosit de Auenbrugger în tratamentul manii [9] .
Unele tradiții populare mai spun că camforul descurajează șerpii și alte reptile datorită mirosului puternic al acestuia. La fel, camforul se crede că este toxic pentru insecte și, prin urmare, este uneori folosit ca un agent de respingere. [10]
Camforul este utilizat pe scară largă în ceremoniile religioase hinduse . Hindușii se închină unei flăcări sacre generate de arderea camforului, care formează o parte importantă a multor ceremonii religioase. Camforul este folosit în sărbătorile Maha Shivaratri ale lui Shiva , zeul hindus al distrugerii și (re) creației. La fel ca înălțimea naturală, arde fără a lăsa un reziduu de cenușă, care simbolizează conștiința. Recent, majoritatea templelor din India de Sud au încetat să se aprindă cu camfor în Sancta sanctorum principal din cauza depunerilor grele de carbon , cu toate acestea în zonele deschise folosesc camfor.
Se găsește și în măștile folosite pentru a ușura pielea.
Recent, nanotuburile de carbon au fost sintetizate cu succes folosind camfor într-un proces chimic de depunere a vaporilor . [11]
Alte substanțe derivate din arbori sunt uneori vândute în mod eronat ca camfor.
Culinar
În Europa antică și medievală, camforul era folosit ca ingredient pentru dulciuri. A fost folosit și ca aromă, în pachete de tip înghețată, în China în timpul dinastiei Tang (618-907). A fost menționat într-o mare varietate de feluri de mâncare, atât sărate, cât și dulci, în cărțile de bucate medievale în arabă, cum ar fi al - Kitab al - Ṭabikh scris de ibn Sayyār al-Warrāq în secolul al X-lea [12] și o carte de bucate andaluză de Anonymous of secolul al XIII-lea [13] . De asemenea, apare în feluri de mâncare dulci și sărate într-o carte scrisă la sfârșitul secolului al XV-lea pentru sultanii din Mandu, Niʿmat-nama [14] .
Camforul este utilizat în prezent în Asia ca aromă, în special pentru dulciuri. Este utilizat pe scară largă în gătit, în special pentru deserturi, în India, unde este cunoscut sub numele de Kachha (crud / crud) Karpooram („camfor crud” în tamilă : பச்சைக் கற்பூரம்) și poate fi găsit în magazinele alimentare indiene unde este etichetat ca „camfor comestibil”.
În ceremoniile Pūjā și hinduse, camforul este ars într-o lingură ceremonială pentru interpretarea Aarti . Acest tip de camfor, de tipul cristalin alb, este vândut și în magazinele alimentare indiene. Cu toate acestea, nu este potrivit ca aliment și este periculos pentru sănătate dacă este consumat. Pentru gătit trebuie utilizat numai camforul etichetat „camfor comestibil”.
Medicament
Camforul a fost utilizat în diferite preparate pentru tuse, cum ar fi Vicks și Buckley , ca antitusiv și ca calmant local al durerii . În trecut a fost folosit și ca antispasmodic , stimulând centrele nervoase, antiseptic . Monobromata a fost utilizată pentru a trata astmul , isteria și eretismul genital de la blenoragie .
Toxicitate
Camforul este deosebit de periculos pentru copii, persoanele cu vârsta peste 55 de ani și pentru cei care iau cantități mai mult decât recomandate pentru perioade lungi de timp. În cantități mari, camforul este otrăvitor atunci când este ingerat și poate provoca convulsii , confuzie, iritabilitate, hiperactivitate neuromusculară, halucinații, greață, vărsături și amețeli. În cazuri extreme, chiar și aplicarea locală a camforului poate duce la hepatotoxicitate . [15] [16] Dozele letale la adulți sunt de 50-500 mg / kg (pe cale orală). În general, 2g provoacă toxicitate severă, iar 4g pot pune viața în pericol. Supradozajul prelungit (0,5 ml / kg greutate corporală) poate duce la comă sau leziuni renale severe.
În 1980, Administrația SUA pentru Alimente și Medicamente a plasat o limită de 11% din camforul permis în produsele de consum și a interzis total produsele etichetate ca ulei de camfor, ulei de camfor, liniment de camfor și liniment de camfor (cu excepția „uleiului esențial de camfor alb”, care nu conține cantități semnificative de camfor). Deoarece există tratamente alternative, utilizarea medicamentoasă a camforului este descurajată de FDA, cu excepția utilizărilor legate de piele, cum ar fi pulberile medicamentoase, care conțin doar cantități mici de camfor.
Reactivitate
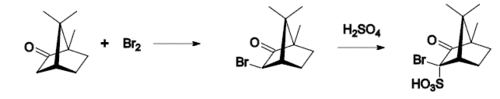
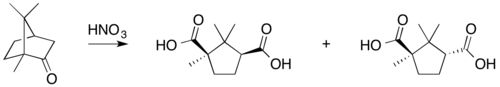
Reacțiile tipice ale camforului sunt
- oxidare cu acid azotic ,
- conversia în izonitrosocampor .
Camforul poate fi, de asemenea, redus la izoborneol folosind borohidrură de sodiu .
Notă
- ^ Fișă informativă despre camfor despre IFA-GESTIS Arhivat 16 octombrie 2019 la Arhiva Internet .
- ^ Cinnamomum camphora se găsește în Asia (Borneo, Taiwan, China și Japonia), dar este cultivată și în SUA și în țările mediteraneene
- ^ Dicționar online de etimologie
- ^ Al-Kindi , FSTC
- ^ Carte de bucate andaluză anonimă din secolul al XIII-lea , pe daviddfriedman.com . Adus pe 2 mai 2010 (arhivat din original la 23 septembrie 2015) .
- ^ acest tip de macerare corespunde termenului englez Pulping și nu Enfleurage
- ^ Sfaturi pentru magazinele de fabricare a dulapurilor , la cabinetshoptips.com . Adus la 3 mai 2010 (arhivat din original la 4 aprilie 2014) .
- ^ Agenția Națională pentru Medicamente Arhivat la 19 februarie 2009 la Internet Archive .
- ^ JMS Pearce, Leopold Auenbrugger: epilepsie indusă de camfor - remediu pentru psihoze maniacale , în Eur. Neurol. , vol. 59, 1-2, Elveția, 2008, pp. 105-7, DOI : 10.1159 / 000109581 , PMID 17934285 .
- ^ Copie arhivată ( PDF ), pe indiacare.it . Adus la 3 mai 2010 (arhivat din original la 14 iunie 2011) .
- ^ Kumar M, Ando Y, Nanotuburi de carbon din camfor: o nanotehnologie prietenoasă cu mediul , în J Phys Conf Ser. , Vol. 61, 2007, pp. 643-6, DOI : 10.1088 / 1742-6596 / 61/1/129 .
- ^ Nawal Nasrallah, Annals of the Caliphs 'Kitchen: Ibn Sayyâr al-Warrâq's Tenth-century Baghdadi Cookbook , Islamic History and Civilization, 70, Leiden, Brill, 2007, ISBN 978-0-415-35059-4 .
- ^ O carte de bucate andaluză anonimă din secolul al XIII-lea, tradusă de Charles Perry , pe daviddfriedman.com . Adus pe 2 mai 2010 (arhivat din original la 23 septembrie 2015) .
- ^ Norah Titley M., The Ni'matnama Manuscript of the Sultans of Mandu: The Sultan's Book of Delights , Routledge Studies in South Asia, London, UK, Routledge, 2004, ISBN 978-0-415-35059-4 .
- ^ Martin D, Valdez J, Boren J, Mayersohn M, Absorbția cutanată a camforului, mentolului și salicilatului de metil la om , în J Clin Pharmacol , vol. 44, nr. 10, octombrie 2004, pp. 1151–7, DOI : 10.1177 / 0091270004268409 , PMID 15342616 .
- ^ Uc A, Bishop WP, Sanders KD, Campfor hepatotoxicity , în South Med J. , vol. 93, nr. 6, iunie 2000, pp. 596-8, PMID 10881777 . Adus la 3 mai 2010 (arhivat din original la 11 mai 2012) .
Bibliografie
- Great Dictionary Encyclopedic (1934), UTET , Vol. II, p. 855
Alte proiecte
-
 Wikționarul conține dicționarul lema « camfor »
Wikționarul conține dicționarul lema « camfor » -
 Wikimedia Commons conține imagini sau alte fișiere pe camfor
Wikimedia Commons conține imagini sau alte fișiere pe camfor
linkuri externe
- camfor , pe my-personaltrainer.it .
- Autoritatea Europeană pentru Siguranța Alimentară, camfor în nutriție , pe efsa.europa.eu .
- „Camforii” Andora (Savona, Liguria) de Liguriainside.it , pe liguriainside.it .
- (RO) Camfor by Natural Medicines Comprehensive Database
- ( RO ) INCHEM IPCS (Programul internațional privind siguranța chimică)
- (EN) camfor pe botanical.com , pe botanical.com.
| Controlul autorității | NDL ( EN , JA ) 00572270 |
|---|