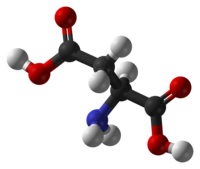
Acid aspartic
| Acid aspartic | |
|---|---|
| Numele IUPAC | |
| Acid 2-amino-1,4-butanedioic | |
| Abrevieri | |
| D. Asp | |
| Denumiri alternative | |
| Acid aspartic Acid aminosuccinic | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 4 H 7 NU 4 |
| Masa moleculară ( u ) | 133.10 |
| Aspect | solid cristalin alb |
| numar CAS | (amestec racemic Număr CAS: 617-45-8) |
| Numărul EINECS | 200-291-6 |
| PubChem | 5960 |
| DrugBank | DB00128 |
| ZÂMBETE | C(C(C(=O)O)N)C(=O)O |
| Proprietăți fizico-chimice | |
| Constanta de disociere a acidului la 293 K. | pK 1 : 1,99 PK 2 : 9,90 |
| Punctul isoelectric | 2,85 |
| Solubilitate în apă | 4 g / l la 293 K |
| Temperatură de topire | 270 ° C (543 K) |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | −973,3 |
| Informații de siguranță | |
| Fraze H | --- |
| Sfaturi P | --- [1] |
Acidul aspartic este un aminoacid folosit de ființele vii pentru sinteza proteinelor . Este indicat în mod obișnuit cu abrevierile D sau Asp și este codificat pe ARN-ul messenger de codonii GAU și GAC.
Este, de asemenea, implicat în ciclul ureei și este inclus printre aminoacizii gluconeogeni , deoarece, prin transaminare, este transformat în oxaloacetat . [2]
Istorie
Farmacistul francez Auguste-Arthur Plisson a izolat în 1827 acid aspartic după ce a reacționat asparagină , obținută din suc de sparanghel , cu hidroxid de plumb . El a numit acidul obținut „acide aspartique” (din latinescul aspăragus , „sparanghel”) acid aspartic în italiană. [3]
Ritthausen în 1868 a izolat acid aspartic dintr-o proteină hidrolizată. [3]
Structura
Este compus dintr-o grupare amino , o grupare carboxil și un lanț lateral acid ( ), care face ca molecula să fie polară . În condiții fiziologice aminoacidul apare sub formă de anion , deoarece grupările α-carboxilice și α-amino sunt încărcate negativ și pozitiv, în timp ce lanțul lateral este încărcat negativ ( ), în consecință sarcina globală a moleculei este negativă. În această formă, acidul aspartic se numește aspartat și este capabil să interacționeze electric cu alte molecule încărcate.
Forma zwitterionică este atinsă în schimb la pH acid, când gruparea amino este protonată și doar una dintre cele două grupări carboxil este deprotonată. Deoarece cele două grupări carboxil au constante de disociere a acidului diferite, este posibil să se identifice punctul izoelectric la un pH de 2,85.
Acidul aspartic, ca majoritatea aminoacizilor, este supus stereoizomerismului . Carbonul 2, numit și carbon α, este un stereocentru care transportă 4 substituenți diferiți legați ( , , Și ). În funcție de modul în care acești substituenți sunt orientați tridimensional, pot fi identificați doi enantiomeri : acidul 2 ( S ) -amino-1,4-butanedoic și acidul 2 ( R ) -amino-1,4-butanedioic. Aceste două molecule au activitate optică și, în consecință , se pot distinge acidul L-aspartic și acidul D-aspartic . Forma lor anionică posedă, de asemenea, activitate optică și, prin urmare, se recunosc reciproc: L-aspartat și D-aspartat .
Denumirile „acid aspartic” și „aspartat” înseamnă de obicei amestecurile racemice .
Acid L-aspartic
Enantiomerul L al acidului aspartic este utilizat de ființele vii ca element de construcție pentru construirea proteinelor . Este sintetizat în mod natural în corpul nostru, așa că se încadrează în acea categorie de aminoacizi neesențiali, care pot fi evitați de alimente. [4]
Un studiu a arătat că, în condiții similare celor presupuse existente pe Pământul timpuriu, cristalele de acid aspartic stângaci (enantiomerii L) s-au format mai ușor și în cantități mai mari decât cele dreptaci. Acesta ar putea fi motivul pentru care codul nostru genetic a inclus enantiomerul L și nu D. [5]
L-aspartatul acționează în creier ca un neurotransmițător excitator care stimulează receptorii NMDA , deși nu la fel de excesiv ca glutamatul . [6]
Biosinteza
În corpul uman este sintetizat prin reacția de transaminare a oxaloacetatului , un intermediar al ciclului Krebs . Reacția este catalizată de enzima aspartat transaminază , care se găsește liberă în citosolul multor celule. Transferul grupării amino din molecule precum alanina sau glutamina produce aspartat și un alfa-ceto acid . [2]
Productie industriala
Din punct de vedere industrial, acidul L-aspartic este sintetizat pornind de la acidul fumaric . Reacția implică utilizarea amoniacului și a unui catalizator enzimatic: aspartat amoniac liază , numită și aspartază. [7]
Prima utilizare a acestui catalizator datează de la un proces discontinuu [7] din 1953, care a fost apoi transformat, în 1973, într-un proces continuu pentru producerea acidului L-aspartic. Această nouă sinteză a implicat utilizarea unei coloane care conține celule E.Coli imobilizate într-o rețea de poliacrilamidă . [8] [9] Pentru a obține îmbunătățiri în proces, κ-caragenanul a fost început în 1978 ca gel de captare. [10] În 1983, totuși, au început să se utilizeze celule EAPC-7 imobilizate în χ-caragenan, eliminând, de asemenea, conversia acidului fumaric în acid L-malic . [11]
Vă urmează astfel câteva încercări de îmbunătățire a producției de acid L-aspartic: prin utilizarea E.Coli prinși în celulele poliazetidinei [12] [13] , utilizarea celulelor intacte ale unei bacterii corneforme, Brevibacterium flavum MJ- 233, cu membrană de ultrafiltrare. [14] Toate aceste procese au în comun utilizarea unui exces de amoniac pentru a încerca să deplaseze echilibrul reacției către producerea acidului L-aspartic. [7] [15]
Am încercat apoi să îmbunătățim biocatalizatorul folosit: aspartaza. Exemple sunt: prepararea unui nou microorganism din genul E.Coli , integrarea unei plasmide cu un acid dezoxiribonucleic care poartă gena pentru aspartază [16] [17] (ceea ce a condus la o sinteză mai avantajoasă a aminoacidului) și identificarea a unei aspartaze extrem de termostabile în Bacillus sp. YM55-1. [18] Studii ulterioare asupra structurii cu raze X a aspartazei de către E.Coli [19] și Bacillus sp. YM55-1 [20] au permis ingineria proteinelor să se îmbunătățească din ce în ce mai mult.
Optimizarea continuă a componentelor individuale ale procesului a asigurat că procesele bazate pe aspartază sunt printre cele mai eficiente și rentabile procese enzimatice cunoscute până în prezent. [7] [21]
Metabolism
Acidul aspartic este utilizat ca precursor în sinteza altor aminoacizi, cum ar fi asparagina , arginina , lizina , metionina , treonina și izoleucina . În afară de aceasta, este folosit pentru a sintetiza unele nucleotide . Acidul aspartic acționează și ca neurotransmițător. [22]
Procesul de biosinteză a aminoacizilor începe de la o fosforilare a aspartatului catalizată de aspartatokinază care produce aspartil-β-fosfat; din acesta din urmă se produce apoi β-aspartat-semialdehidă din care în final sunt urmate diferite căi metabolice pentru producerea de aminoacizi. [2] Sinteza alaninei implică și utilizarea acidului L-aspartic ca precursor, în acest proces Aspartatul-β-decarboxilaza este utilizat ca catalizator.
Aspartatul este degradat în oxaloacetat , care este un precursor al glucozei și din acest motiv este clasificat ca un aminoacid glucogen. [2] Reacția este o transaminare a aspartatului. Asparagina care este hidrolizată în aspartat prin L-asparaginază duce, de asemenea, la formarea oxaloacetatului. [2]
Utilizări industriale
Acidul L-aspartic este utilizat pe scară largă în nutriția parenterală și enterală ca acidifiant, ca precursor al L-alaninei și aspartamului . [7] Este, de asemenea, utilizat ca materie primă pentru sinteza stereoselectivă a diferiților compuși chimici organici chirali. [23]
Acidul poliaspartic este un polimer solubil în apă , biodegradabil al acidului aspartic, valoros în multe aplicații industriale, medicale și agricole pentru a înlocui mulți polimeri nebiodegradabili în uz. [24] [25] Aplicațiile acidului poliaspartic includ, de fapt, sisteme de tratare a apei, tratamente antimicrobiene [26] , silvicultură , exploatarea petrolului , aplicare în formulări de detergenți [27] și ca constituent al polimerilor superabsorbanți biodegradabili (SAP) , utilizat în scutece de unică folosință, produse de incontinență pentru adulți și produse de igienă feminină. [28]
Piața globală pentru acidul aspartic (care include , prin urmare: suplimente alimentare, medicamente, acid poliaspartic, aspartam, L-alanină) este de așteptat să ajungă la 101,0 milioane $ de 2022. Cererea globală de acid aspartic a fost de 35,600,000. Kilo - tone în 2012 [27] Pe de altă parte, în 1996, producția industrială de acid aspartic a fost de 7 kilograme pe an, prin intermediul enzimelor. [29]
Acid D-aspartic
Acidul D-aspartic este unul dintre principalii regulatori ai neurogenezei adulților și joacă un rol important în dezvoltarea funcției endocrine. D-Asp este prezent în țesuturile endocrine, neuroendocrine și testiculare și reglează sinteza și secreția hormonilor și spermatogeneza . Proteinele alimentare conțin, de asemenea, D-aminoacizi care sunt proveniți sau induși în mod natural prin procese care implică temperaturi ridicate, tratamente acide sau procese de fermentare . De fapt, prezența D-aminoacizilor în produsele lactate indică un tratament termic sau o contaminare microbiană. [30]
În timpul etapei embrionare a păsărilor și a vieții postnatale timpurii a mamiferelor, o creștere concentrație tranzitorie de D-Asp este prezentă în creier și retină . Acest aminoacid a fost detectat în sinaptozomi și vezicule sinaptice, unde este eliberat după stimuli chimici (ioni ( ), ionomicină ) sau electrică. Mai mult, D-Asp crește AMPc în celulele neuronale și este transportat de la fisurile sinaptice la celulele nervoase presinaptice printr-un transportor specific. Pe de altă parte, în sistemul endocrin , D-Asp este implicat în reglarea sintezei și eliberării hormonilor. De exemplu, în hipotalamusul de șobolan, crește eliberarea de gonadotropină (GnRH) și induce sinteza ARNm, oxitocină și vasopresină . În glanda pituitară , stimulează secreția următorilor hormoni: prolactină (PRL), hormon luteinizant (LH) și hormon de creștere (GH) În testicule, este prezent în celulele Leydig și este implicat în eliberarea de testosteron și progesteron . [31]
Biosinteza
Acidul D-aspartic este sintetizat în corpul nostru din acidul L-aspartic. Reacția de racemizare este catalizată de o enzimă izomerază numită: aspartat-racemază . [32]
Utilizări
D-Asp este implicat în sinteza și eliberarea testosteronului și din acest motiv se presupune că poate fi utilizat pentru creșterea testosteronului la bărbați. Studiile au arătat că D-Asp exogen crește de fapt nivelul de testosteron la animale, în timp ce studiile la om au dat rezultate inconsistente din cauza numărului mic de cercetări efectuate. [33]
Prezența acidului D-aspartic în produsele alimentare, de exemplu în brânzeturi, poate fi utilizată pentru a cuantifica orice contaminare microbiană sau orice tratament termic sau alcalin al produsului. [30]
Racemizarea acidului aspartic este unul dintre principalele tipuri de modificări covalente neenzimatice care duc la acumularea de D-Asp în țesuturile umane, dependentă de vârstă. Racemizarea are loc în timpul îmbătrânirii proteinelor și se corelează cu vârsta proteinelor de lungă durată. Racemizarea poate duce la pierderea funcției proteinelor datorită proteolizei sau datorită modificărilor structurii moleculare. Racemizarea in vivo poate crește, de asemenea, în condiții patologice. De fapt, acest proces este relevant în patogeneza bolilor bătrâneții, cum ar fi ateroscleroza , emfizemul pulmonar , presbiopia , cataracta , bolile degenerative ale cartilajului și disfuncțiile legate de vârsta creierului. [34]
Racemizarea L-aspartatului poate fi, de asemenea, utilizată pentru a estima vârsta dinților . Această metodă se bazează pe creșterea constantă legată de vârstă a cantității de acid D-aspartic din dentină , o proteină de lungă durată. [35]
Alimente care conțin acid aspartic
Mai jos sunt enumerate câteva alimente care conțin acid aspartic. Ambele forme (stereoizomerul L și D) se găsesc în alimente, deși în cantități diferite datorită activității enzimatice a aspartatului-racemazei. Pentru o listă completă, consultați sursa. [36]
| Alimente | Doza (g / 100 g) |
|---|---|
| Izolat de proteine din soia | 10.203 |
| Albus de ou uscat | 8.253 |
| Sigilați carnea | 6.887 |
| Batog uscat | 6.433 |
| Carne de balenă | 5.841 |
| Spirulina uscată | 5.793 |
| Tofu uscat | 5,298 |
| Boabe de soia | 5.112 |
| Făină de arahide | 4.123 |
| Slănină | 3,649 |
| File de vita | 3.386 |
| Arahide | 3.299 |
| Sturion afumat | 3.195 |
| Nuci | 3.096 |
| Pui | 3.021 |
Notă
- ^ foaie de acid aspartic pe [1]
- ^ a b c d e ( EN ) Voet, Donald, e Pratt, Charlotte W. ,, Fundamentals of biochemistry: life at the molecular level , Fifth edition, ISBN 9781118918401 ,OCLC 910538334 . Adus la 15 noiembrie 2018 .
- ^ a b ( EN ) Alton Meister, Biochimia aminoacizilor , volumul 1, ediția a doua, Academic Press, 1965.
- ^ (EN) PubChem, acid aspartic , pe pubchem.ncbi.nlm.nih.gov. Adus la 6 august 2021 .
- ^ (EN) Tu Lee și Yu Kun Lin, Originea vieții și cristalizarea acidului aspartic în apă în creșterea și designul cristalelor, vol. 10, nr. 4, 7 aprilie 2010, pp. 1652–1660, DOI : 10.1021 / cg901219f . Adus la 15 noiembrie 2018 .
- ^ (EN) Philip E. Chen, Matthew T. Geballe și Phillip J. Stansfeld, Caracteristici structurale ale situsului de legare a glutamatului în receptori N-metil-D-aspartat NR1 / NR2A recombinați determinați prin mutageneză direcționată către sit și modelare moleculară , în Farmacologie moleculară , vol. 67, nr. 5, 2005-5, pp. 1470–1484, DOI : 10.1124 / mol . 104.008185 . Adus la 15 noiembrie 2018 .
- ^ a b c d e ( EN ) Hughes, Andrew B., Aminoacizi, peptide și proteine în chimia organică , Wiley-VCH, © 2009-, ISBN 9783527320967 ,OCLC 436262310 . Adus la 15 noiembrie 2018 .
- ^ (EN) Ichiro Chibata, Tetsuya Tosa și Tadashi Sato, Producția continuă de acid L-aspartic , în Biochimie Aplicată și Biotehnologie, vol. 13, n. 3, 1986-12, pp. 231–240, DOI : 10.1007 / bf02798461 . Adus la 15 noiembrie 2018 .
- ^ (EN) T. Tosa, T. Sato și T. Mori, Studii de bază pentru producția continuă de acid L-aspartic de către celulele Escherichia coli imobilizate , în Microbiologie aplicată, vol. 27, n. 5, 1974-5, pp. 886–889. Adus la 30 noiembrie 2018 .
- ^ (EN) Tadashi Sato, Yutaka Nishida și Tetsuya Tosa, Imobilizarea celulelor Escherichia coli care conțin activitate aspartază cu κ-caragenan. Proprietăți enzimatice și aplicații pentru producerea acidului l-aspartic , în Biochimica et Biophysica Acta (BBA) - Enzymology , vol. 570, n. 1, 1979-09, pp. 179–186, DOI : 10.1016 / 0005-2744 (79) 90212-2 . Adus la 30 noiembrie 2018 .
- ^ (EN) Isao Umemura, Satoru Takamatsu și Tadashi Sato, Îmbunătățirea producției de acid L-aspartic folosind celule microbiene imobilizate , în Microbiologie aplicată și biotehnologie, vol. 20, nr. 5, 1984-11, pp. 291–295, DOI : 10.1007 / bf00270588 . Adus la 30 noiembrie 2018 .
- ^ (EN) Louis L. Wood și Gary J. Calton, O metodă nouă de imobilizare și utilizarea sa în producția de acid aspartic , în Bio / Technology, vol. 2, nr. 12, 1984-12, pp. 1081-1084, DOI : 10.1038 / nbt1284-1081 . Adus la 30 noiembrie 2018 .
- ^ (EN) Louis L. Wood; Gary J. Calton, Purification Engineering, Inc., Columbia, MD, IMOBILIZAREA CELULELOR CU UN PREPOLIMER POLIAZETDNE , US4732851A .
- ^ (EN) H. Yamagata, M. Terasawa și H. Yukawa, Un nou proces industrial pentru producerea acidului l-aspartic utilizând membrane de ultrafiltrare , în Catalysis Today, vol. 22, n. 3, 1994-12, pp. 621–627, DOI : 10.1016 / 0920-5861 (94) 80127-4 . Adus la 30 noiembrie 2018 .
- ^ (EN) Almuth-Sigrun Jandel, Helmut Hustedt și Christian Wandrey, Producția continuă de L-alanină din fumarat în membranele unui reactor în două etape , în European Journal of Applied Microbiology and Biotechnology, vol. 15, nr. 2, 1982, pp. 59–63, DOI : 10.1007 / bf00499507 . Adus la 30 noiembrie 2018 .
- ^ (EN) Noriyuki Nishimura, Tomoyasu Taniguchi și Saburo Komatsubara, Hyperproduction of aspartase to catabolite represive by-resistant mutant of Escherichia coli adăpostind B Multicopy ASPA și par recombinant plasmids , în Journal of Fermentation and Bioengineering, vol. 67, nr. 2, 1989-01, pp. 107-110, DOI : 10.1016 / 0922-338x (89) 90189-x . Adus la 30 noiembrie 2018 .
- ^ (EN) Masahiko Kisumi; Saburo Komatsubara; Tomoyasu Taniguchi, Tanabe Seiyaku Co., Ltd., Osaka, Japonia, METODA DE PRODUCERE A ACIDULUI LASPARTIC , US4692409A.
- ^ (EN) Yasushi Kawata, Koichi Tamura și Shigeru Yano, Purificarea și caracterizarea aspartazei termostabile din Bacillussp. YM55-1 , în Arhivele de Biochimie și Biofizică , vol. 366, nr. 1, 1999-06, pp. 40–46, DOI : 10.1006 / abbi.1999.1186 . Adus la 30 noiembrie 2018 .
- ^ (EN) Wuxian Shi, Jennifer Dunbar și Maithri MK Jayasekera, The Structure ofl-Aspartate Ammonia-Lyase fromEscherichia coli †, ‡ , în Biochimie, vol. 36, n. 30, 1997-07, pp. 9136–9144, DOI : 10.1021 / bi9704515 . Adus la 30 noiembrie 2018 .
- ^ (EN) Tomomi Fujii, Hisanobu Sakai și Yasushi Kawata, Crystal Structure of Thermostable Aspartase from Bacillus sp. YM55-1: Explorarea bazată pe structuri a siturilor funcționale din familia Aspartazei , în Journal of Molecular Biology , vol. 328, nr. 3, 2003-05, pp. 635-654, DOI : 10.1016 / s0022-2836 (03) 00310-3 . Adus la 30 noiembrie 2018 .
- ^ (EN) Bommarius, AS, Schwarm, M. și Drauz, K., Comparația diferitelor căi de proces chimioenzimatic la aminoacizi enantiomeric puri, în Chimia, vol. 55, pp. 50-59.
- ^ Tezaurul NCI , la ncit.nci.nih.gov . Adus la 6 august 2021 .
- ^ (EN) Coppola, Gary M. (Gary Mark), 1948-, Sinteza asimetrică: construirea moleculelor chirale folosind aminoacizi , Wiley, 1987, ISBN 0471828742 ,OCLC 14,212,737 . Adus la 16 noiembrie 2018 .
- ^ (EN) Sunita M. Thombre și Bhimrao Sarwade D., Synthesis and Biodegradability of polyaspartic acid: A Critical Review , în Journal of Macromolecular Science, Part A, vol. 42, n. 9, 2005-09, pp. 1299-1315, DOI : 10.1080 / 10601320500189604 . Adus la 15 noiembrie 2018 .
- ^ (EN) VL Goosey, IG Campbell și NE Fowler, Efectul impulsului de frecvență asupra economiei cursei cu scaune cu rotile în Medicină și Științe în Sport și Exercițiu, vol. 32, nr. 1, 2000-1, pp. 174–181. Adus la 15 noiembrie 2018 .
- ^ (EN) Mithil N. Kumar, K. și K. Madhusudana Varaprasad Rao, A Novel Biodegradable Green Poly (L-Aspartic Acid-Citric Acid) Copolymer for Antimicrobial Applications , Journal of Polymers and the Environment, vol. 20, nr. 1, 24 august 2011, pp. 17–22, DOI : 10.1007 / s10924-011-0335-z . Adus la 16 noiembrie 2018 .
- ^ a b ( EN ) Analiza pieței acidului aspartic după aplicație (suplimente furajere, medicamente, acid poliaspartic, aspartam, L-alanină) și prognozele pe segmente până în 2022 , pe grandviewresearch.com .
- ^ (EN) MJ Zohuriaan-Mehr, A. și H. Pourjavadi Salimi, hidrogeluri pe bază de proteine și homo poli (aminoacizi) cu proprietăți super-umflate , în Polimeri pentru tehnologii avansate, vol. 20, nr. 8, 2009-08, pp. 655-671, DOI : 10.1002 / pat.1395 . Adus la 16 noiembrie 2018 .
- ^ (EN) Masato Ikeda, Procese de producție a aminoacizilor , în Progrese în inginerie biochimică / biotehnologie, vol. 79, 2003, pp. 1–35. Adus la 15 noiembrie 2018 .
- ^ a b ( EN ) Giuseppe Genchi, O prezentare generală asupra d-aminoacizilor , în aminoacizi , vol. 49, nr. 9, 5 iulie 2017, pp. 1521–1533, DOI : 10.1007 / s00726-017-2459-5 . Adus la 15 noiembrie 2018 .
- ^ (EN) Antimo D'Aniello, acid d-aspartic: un aminoacid endogen cu un rol neuroendocrin important , în Brain Research Reviews, vol. 53, nr. 2, 2007-02, pp. 215-234, DOI : 10.1016 / j.brainresrev.2006.08.005 . Adus la 15 noiembrie 2018 .
- ^ (EN) RCSB Protein Data Bank, RCSB PDB - 5HRA: Structura cristalină a unei aspemate / glutamat racemază în complex cu D-aspartat pe www.rcsb.org. Adus la 6 august 2021 .
- ^ (EN) Farzad Roshanzamir și Seyyed Morteza Safavi, Efectele putative ale acidului D-aspartic asupra nivelurilor de testosteron din sânge: o revizuire sistematică în Jurnalul Internațional de Reproductivă Biomedicină (Yazd, Iran), vol. 15, nr. 1, 2017-1, pp. 1-10. Adus la 15 noiembrie 2018 .
- ^ (EN) RITZTIMME S și M COLLINS, Racemizarea acidului aspartic în proteinele umane , în Aging Research Reviews, vol. 1, nr. 1, 2002-02, pp. 43-59, DOI : 10.1016 / s0047-6374 (01) 00363-3 . Adus la 15 noiembrie 2018 .
- ^ (EN) S. Ohtani, Y. Yamada, I. Yamamoto, [Estimarea vârstei din dinți folosind racemizarea acidului aspartic (metodă de racemizare)] , în Nihon Hoigaku Zasshi = The Japanese Journal of Legal Medicine, vol. 54, nr. 2, 2000-8, pp. 207-218. Adus la 15 noiembrie 2018 .
- ^ a b FoodData Central , la fdc.nal.usda.gov . Adus pe 2 august 2021 .
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre acid aspartic
Wikimedia Commons conține imagini sau alte fișiere despre acid aspartic
| Controlul autorității | LCCN (EN) sh85008689 · GND (DE) 4211533-4 |
|---|