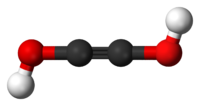
Ethindiol
| Ethindiol | |
|---|---|
| Numele IUPAC | |
| dihidroxiacetilenă | |
| Denumiri alternative | |
| Ethindiol acetilendiool | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 2 H 2 O 2 |
| Masa moleculară ( u ) | 58.0361 |
| numar CAS | |
| PubChem | 9942115 |
| ZÂMBETE | C(#CO)O |
| Proprietăți fizico-chimice | |
| Temperatura de fierbere | descompunere |
| Informații de siguranță | |
Etindiolul sau acetilendioolul este diolul acetilenei cu formula HO-C≡C-OH. Este un compus gazos instabil care se transformă prin tautomerizare în glioxal H (CO) 2 H. Molecula este singurul indiol structural posibil.
Istorie
Molecula de etindiol a fost obținută pentru prima dată de Johan K. Telrow în 1986 sub forma unui ion pozitiv în timpul analizei acidului squaric efectuată cu un spectrometru de masă . [1]
Molecula neutră a fost sintetizată nouă ani mai târziu de Günther Maier prin fotoliza acidului squaric într-o matrice izolatoare de argon solid la 10 K. [2]
Săruri
Ca toți alcoolii , etindiolul poate forma săruri alcoxi numite acetilendolați sau etoliolați cu formula generică M + (OC≡CO) 2- M + sau M 2+ (OC≡CO) 2- .
Cu toate acestea, aceste săruri sunt de obicei sintetizate prin reducerea monoxidului de carbon : etindiolatul de potasiu a fost sintetizat în 1834 de către Liebig prin reacția directă a monoxidului de carbon cu potasiul metalic: [3]
Cu toate acestea, la acea vreme, se credea că compusul era carbonil de potasiu (KCO) până când etiolatul de sodiu Na 2 C 2 O 2 a fost descris 130 de ani mai târziu (Johannis, 1893), etiolatul de bariu BaC 2 O 2 (Gunz și Mentrel , 1903), etiolatul de stronțiu (Roederer, 1906) și de litiu , rubidiu și cesiu (Pearson, 1933). [4]
Cu toate acestea, structura acestor săruri a fost definită abia în 1963 de Werner Büchner și E. Weiss .[5][6]
Acetilenediolații pot fi preparați și prin reacția monoxidului de carbon cu metalele corespunzătoare în amoniac lichid, la temperatură scăzută. [4]
Sărurile de acetilendiol reacționează violent cu oxigenul din aer, apă , halogeni , halogenuri , alcooli și orice substanță cu proprietăți acide. [7]
Complexe
Ionul etindiolat (OC≡CO) 2- poate forma complexe precum [TaH (HOC≡COH) (dmpe) 2 Cl] + Cl - (dmpe = bis (1,2-dimetilfosfin) etan ). [8] Sunt cunoscuți alți compuși de coordonare care conțin ionul etindiolat, deși nu derivă direct din etindiol. Un exemplu este diisopropoxyethin eterul (CH3) 2 HC-OC≡CO-CH (CH3) 2 și ethin di (terț-butoxi) eter (CH3) 3 COC≡COC (CH3) 3. [9]
Etindiolatul împreună cu alți cationi precum deltatul (C 3 O 3 2- ) și pătratul (C 4 O 4 2- ) se obțin prin îndepărtarea grupării CO din compușii de coordonare în care sunt conținuți. [10]
Notă
- ^ Johan K. Terlouw, Peter C. Burgers, Ben LM van Baar, Thomas Weiske și Helmut Schwarz (1986), Formarea în faza gazoasă a HO-CC-OH, H2N-CC-NH2, H2N-CC-OH și compuși înrudiți prin reducerea selectivă a cationilor lor , Chimia, volumul 40, paginile 357–359.
- ^ Günther Maier, Christine Rohr, Ethynediol: Photochemical Generation and Matrix-spectroscopic Identification ( abstract ), în Liebigs Annalen , vol. 1996, nr. 3, 2006, pp. 307-309, DOI : 10.1002 / jlac.199619960303 . Adus pe 24 august 2012 .
- ^ Justus Liebig (1834), Annalen der Chemie und Pharmacie, volumul 11, p. 182. Citat de Raymond N. Vrtis și colab. (1988), JACS p. 7564.
- ^ a b TG Pearson (1933), Carbonyls of Lithium, Rubidium and Cesium. Natura, volumul 131, pp. 166–167 (04 februarie 1933).
- ^ E. Weiss, W. Büchner, Zur Kenntnis der sogenannten «Alkalicarbonyle» I Die Kristallstruktur des Kalium-acetylendiolats, KOC≡COK. , în Helvetica Chimica Acta , vol. 46, nr. 4, 1963, pp. 1121-1127, DOI : 10.1002 / hlca . 19630460404 . Adus pe 24 august 2012 .
- ^ E. Weiss, W. Büchner, Zur Kenntnis der sogenannten Alkalicarbonyle. II. Die Kristallstrukturen des Rubidium- und Cesium-acetylendiolats, RbOC≡CORb und CsOC≡COCs. , în Zeitschrift für anorganische und allgemeine Chemie , vol. 330, nr. 5-6, 1964, pp. 251-258, DOI : 10.1002 / zaac.19643300504 . Adus pe 24 august 2012 .
- ^ Charles Kenneth Taylor (1982), Comportamentul chimic al acetilenediolaților metalelor alcaline. Teză, Universitatea de Stat din Pennsylvania; de asemenea, Memorie tehnică A642321, Laboratorul de cercetare aplicată Park University Park. 227 pagini.
- ^ Raymond N. Vrtis, C. Pulla. Rao, Simon G. Bott, Stephen J. Lippard, Sinteza și stabilizarea dihidroxiacetilenei coordonate de tantal din doi liganzi cu monoxid de carbon cuplați reductiv , în Journal of the American Chemical Society , vol. 110, nr. 22, 1988, pp. 7564–7566, DOI : 10.1021 / ja00230a062 . Adus pe 24 august 2012 .
- ^ Anna Bou, Miquel A. Pericàs, Félix Serratosa, Diisopropoxy- și di-tert-butoxyethyne , în Tetrahedron , vol. 37, n. 7, 1981, pp. 1441–1449, DOI : 10.1016 / S0040-4020 (01) 92464-0 . Adus pe 24 august 2012 .
- ^ Alistair S. Frey, F. Geoffrey N. Cloke, Peter B. Hitchcock, Iain J. Day, Jennifer C. Green, Georgina Aitken, Studii mecaniciste asupra cicloligomerizării reductive a CO de complexe U (III) Sandwich mixte; Structura moleculară a [(U (η-C 8 H 6 {Si'Pr 3 -1,4} 2 ) (η-Cp *)] 2 (μ-η 1 : η 1 -C 2 O 2 ) , în Journal of the American Chemical Society , vol. 130, nr. 42, 2008, pp. 13816–13817, DOI : 10.1021 / ja8059792 . Accesat la 24 august 2012 .