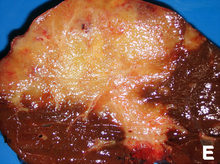
Colangiocarcinom
| Colangiocarcinom | |
|---|---|
| Micrografia unui colangiocarcinom intrahepatic (în dreapta) | |
| Specialitate | oncologie |
| Clasificare și resurse externe (EN) | |
| ICD-O | 8160/3 |
| ICD-9 -CM | 155.1 și 156.1 |
| OMIM | 615619 |
| Plasă | D018281 |
| MedlinePlus | 000291 |
| eMedicină | 277393 și 365065 |
Colangiocarcinomul este o neoplasmă malignă a arborelui biliar care provine din căile biliare interne și externe ale ficatului . Din punct de vedere morfologic, este un adenocarcinom relativ rar (cancer glandular), cu o incidență anuală de 1-2 cazuri la 100.000 înregistrate în lumea occidentală [1] , dar ratele de colangiocarcinom au crescut în întreaga lume în ultimele decenii. [2]
Principalele semne și simptome ale colangiocarcinomului includ teste anormale ale funcției hepatice, dureri abdominale, icter , scădere în greutate și, uneori, mâncărime generalizată, febră , scaun sau decolorare a urinei . Boala este diagnosticată printr-o combinație de teste de sânge, tehnici de imagistică , endoscopie și explorare chirurgicală . Apare adesea într-un stadiu avansat și acest lucru poate limita opțiunile de tratament. [3] [4] [5]
Colangiocarcinomul este considerat o boală incurabilă și letală rapid. Nu există un tratament potențial curativ în afară de intervenția chirurgicală, dar majoritatea pacienților au boală avansată, inoperabilă în momentul diagnosticului . Pacienții cu colangiocarcinom sunt în general tratați, chiar dacă nu sunt tratați, cu chimioterapie sau radioterapie , precum și îngrijiri paliative . Aceste metode sunt utilizate și ca terapie adjuvantă post-chirurgicală în cazurile în care rezecția a avut succes. Unele cercetări medicale în curs de desfășurare includ utilizarea de noi terapii vizate, cum ar fi medicamentul Erlotinib sau terapia fotodinamică . [6]
Morfologie
Colagiocarcinoamelor intrahepatic provin din non - cirotici ficatul și pot urmări spațiile portal intrahepatic creând o masă tumorală arboriform, sau pot dezvolta mase tumorale nodulilor. În orice caz, caracteristica principală este invazia limfatică și vasculară , care dă naștere la metastaze intrahepatice extinse. Se observă adenocarcinoame sclerozante histologic , moderat sau bine diferențiate, cu structuri glandulare și tubulare bine definite și căptușite cu celule epiteliale plate sau cuboidale; în consecință, tumoarea este extrem de solidă și granuloasă. Colangiocarcinoamele sunt rareori patate cu bilă, deoarece celulele epiteliului diferențiat al căilor biliare sunt incapabile să sintetizeze bila. Se pot observa variante în care elemente ale carcinomului hepatocelular și ale colangiocarcinomului sunt prezente. În aproximativ jumătate din cazuri, se observă metastaze la ganglionii limfatici regionali și metastaze hematogene la plămâni , oase (în principal vertebre ), glande suprarenale și creier . [3] [7]
semne si simptome
Cele mai frecvente indicații fizice ale colangiocarcinomului sunt testele anormale ale funcției hepatice, icterul (îngălbenirea albului ochilor sau a pielii) care apare numai atunci când canalele biliare sunt blocate de tumoră, dureri abdominale (30% - 50% cazuri) , mâncărime generalizată (66%), scădere în greutate (30% -50%), febră (până la 20%) sau modificări ale culorii scaunului sau urinei . [8] [9] Într-o anumită măsură, simptomele depind de localizarea tumorii. Pacienții cu colangiocarcinom în căile biliare extrahepatice (în afara ficatului) au mai multe șanse de a avea icter, în timp ce cei cu tumori ale tractului biliar în ficat au adesea dureri fără icter. [10]
Testele de sânge ale funcției hepatice la pacienții cu colangiocarcinom relevă adesea așa-numita „imagine obstructivă”, cu niveluri ridicate de bilirubină , fosfatază alcalină și niveluri crescute de gammaglutamiltransferază, în timp ce nivelurile de transaminaze par relativ normale. Rezultatele de laborator sugerează că această obstrucție a căilor biliare este principala cauză a icterului. [11] Valorile CA 19-9 sunt crescute în majoritatea cazurilor.
Factori de risc
Deși majoritatea pacienților nu prezintă factori de risc evident cunoscuți, un număr dintre aceștia au fost descriși pentru dezvoltarea colangiocarcinomului. Cea mai frecventă dintre acestea este colangita sclerozantă primară (PSC), o boală inflamatorie a căilor biliare, care la rândul ei este strâns asociată cu colita ulcerativă . [12] Studiile epidemiologice au sugerat că riscul de a dezvolta colangiocarcinom pentru o persoană cu PSC este de 10% -15% [13] , deși o serie de teste de autopsie au constatat rate similare de 30% la această populație. [14] Mecanismul prin care PSC crește riscul de colangiocarcinom nu este încă bine înțeles.
Alți factori de risc cunoscuți pentru colangiocarcinom includ anumite malformații congenitale ale ficatului, infecția cu paraziți hepatici Opisthorchis viverrini sau Clonorchis sinensis și expunerea la torotrast (dioxid de toriu), o substanță chimică utilizată anterior în medicină ca agent de contrast . Cu toate acestea, majoritatea pacienților cu colangiocarcinom nu au factori de risc specifici. [3] [15] [16]
Unele boli hepatice parazitare pot fi considerate factori de risc. Colonizarea ficatului de către Opisthorchis viverrini (găsită în Thailanda , Laos și Malaezia ) sau de Clonorchis sinensis (găsită în Japonia , Coreea și Vietnam ) a fost asociată cu dezvoltarea colangiocarcinomului. [17] [18] [19] Pacienți care suferă de boli hepatice cronice, fie sub formă de hepatită virală (de exemplu hepatita B sau C ), [20] [21] [22] boală alcoolică hepatică, ciroză sau alte cauze, au un risc crescut de a dezvolta colangiocarcinom. [23] [24] Infecția cu HIV a fost, de asemenea, identificată ca un potențial factor de risc pentru dezvoltarea cancerului, deși nu este clar dacă cauza este HIV în sine sau factori asociați. [23]
Anomaliile congenitale ale ficatului, cum ar fi sindromul Caroli și chisturile coledocului , au fost asociate cu un risc de 15% de a dezvolta colangiocarcinom. [25] [26] Bolile moștenite rare, cum ar fi sindromul Lynch , sunt, de asemenea, asociate cu boala. [27] [28] Prezența calculilor biliari (colelitiaza) nu este asociată în mod clar cu colangiocarcinomul. Cu toate acestea, pietrele intrahepatice, rare în Occident, dar frecvente în unele părți din Asia , au fost puternic corelate. [29] [30] [31] Expunerea la torotrast , o formă de dioxid de toriu , utilizată odată ca agent de contrast radiologic , a fost legată de dezvoltarea colangiocarcinomului, chiar și la 30-40 de ani de la expunere. Torotrasto a fost interzis în Statele Unite în 1950 , tocmai din cauza cancerigenității sale. [15] [16] .
Un studiu din 2019 a inițiat linia de cercetare legată de expunerea la azbest ca factor de risc [32] .
Fiziopatologie
Colangiocarcinomul poate afecta orice zonă a căilor biliare , în interiorul sau în afara ficatului . Tumorile care sunt localizate în canalele biliare din interiorul ficatului sunt denumite intrahepatice, cele care sunt localizate în canalele exterioare se numesc extrahepatice și, în cele din urmă, tumorile care se află în locul în care canalele biliare ies din ficat la care sunt menționate ca peri-ilar. Colangiocarcinomul care apare la joncțiunea unde se întâlnesc conductele hepatice stânga și dreapta pentru a forma canalul biliar comun poate fi denumit tumoare Klatskin . [33]
Deși se știe că colangiocarcinomul este un adenocarcinom al celulelor epiteliale care acoperă tractul biliar, celula de origine reală este necunoscută, deși studii recente au sugerat că poate rezulta dintr-o celulă stem pluripotentă hepatică. [34] [35] [36] Colangiocarcinomul se dezvoltă printr-o serie de etape, de la hiperplazia și metaplazia timpurie, până la displazia , până la dezvoltarea carcinomului, într-un proces similar cu cel observat în dezvoltarea cancerului de colon . [37] Se crede că inflamația cronică, obstrucția căilor biliare și fluxul biliar afectat rezultat pot juca un rol în această progresie. [37] [38] [39]
Histologic, colangiocarcinoamele pot varia de la nediferențiate la bine diferențiate. Acestea sunt adesea înconjurate de țesut fibrotic sau desmoplastic . Cu fibroză extinsă, poate fi dificil să se distingă colangiocarcinomul de epiteliul normal. Nu există un colorant imunohistochimic specific capabil să distingă neoplasmele maligne de cele benigne ale tractului biliar, deși colorarea pentru citokeratină, antigenul carcino-embrionar , poate ajuta la diagnostic. [40] Majoritatea cancerelor (> 90%) sunt adenocarcinoame . [41]
Diagnostic
Diagnosticul definitiv al colangiocarcinomului se obține prin examinarea țesutului , adică prin biopsie . Patologia poate fi suspectată la un pacient cu icter obstructiv. Diagnosticul poate fi o provocare la pacienții cu colangită sclerozantă primară (PSC), acești pacienți prezintă într-adevăr un risc crescut de a dezvolta colangiocarcinom, dar simptomele pot fi dificil de distins de cele ale PSC. De asemenea, la pacienții cu PSC, indicii de diagnostic, cum ar fi o masă vizibilă din tehnicile imagistice sau dilatarea căilor biliare, nu pot fi evidente. [3] [4]
Analize de sange
Nu există teste de sânge specifice care să poată diagnostica colangiocarcinomul. Nivelurile serice de antigen carcinoembrionar (CEA) și CA19-9 sunt adesea crescute la pacienți, dar nu sunt suficient de sensibile sau specifice pentru a fi utilizate ca instrument de screening general. Cu toate acestea, acestea pot fi utile împreună cu metodele imagistice în sprijinirea diagnosticului de colangiocarcinom suspectat. [42]
Imagistica abdominală

Ecografia ficatului și a tractului biliar este adesea utilizată ca modalitate inițială de imagistică la pacienții cu suspect de icter obstructiv. [43] [44] Ecografia poate identifica obstrucția și dilatarea conductelor și, în unele cazuri, poate fi suficientă pentru diagnosticarea colangiocarcinomului. [45] Tomografia computerizată (CT) poate juca, de asemenea, un rol important în diagnosticul colangiocarcinomului. [46] [47] [48]
Imagistica arborelui biliar

În timp ce imagistica abdominală poate fi utilă în diagnosticarea colangiocarcinomului, este adesea necesară imagistica directă a căilor biliare. Colangiopancreatografia endoscopică retrogradă (ERCP), este o procedură endoscopică efectuată de un gastroenterolog sau de un chirurg specializat, este utilizată pe scară largă în acest scop. Deși ERCP este o procedură invazivă, cu riscurile asociate, beneficiile sale includ capacitatea de a obține biopsii și de a pune stenturi sau de a efectua alte intervenții pentru ameliorarea obstrucției biliare. [11] Ecografia endoscopică poate fi efectuată și în momentul ERCP și poate crește precizia biopsiei. [49] Ca alternativă la ERCP, poate fi utilizată colangiografia percutană (PTC). Colangiopancreatografia prin rezonanță magnetică (MRCP) este o alternativă neinvazivă la ERCP. [50] [51] [52] Unii autori au sugerat că ar trebui să suplinească ERCP în diagnosticul cancerelor de tract biliar, deoarece poate defini mai exact tumora evitând în același timp riscurile de ERCP. [53] [54] [55]
Interventie chirurgicala
Chirurgia este singurul tratament cu intenție curativă pentru colangiocarcinom: intervenția chirurgicală constă în îndepărtarea leziunii în sine, păstrarea unei cantități adecvate de ficat funcțional cu vascularizație adecvată și în îndepărtarea ganglionilor limfatici ai pedunculului hepatic. Laparoscopia poate fi utilizată la unii pacienți prin evitarea procedurilor chirurgicale mai invazive, cum ar fi laparotomia . [5] [56] . La majoritatea pacienților cu boală amovibilă din punct de vedere tehnic, intervenția chirurgicală este prima opțiune de alegere; în unele cazuri, chiar și pacienții potențial operabili, dar cu factori prognostici slabi (afectarea ganglionilor limfatici, afectarea vasculară) sunt direcționați către un program de chimioterapie primară.
Patologie
Din punct de vedere histologic, colangiocarcinoamele se diferențiază bine până la moderat. Imunohistochimia este utilă în diagnostic și poate fi utilizată pentru a diferenția o tumoare primară de metastaze de alte tipuri de cancer gastro-intestinal. [57]
Punerea în scenă
O parte importantă a evaluării diagnostice este stadializarea , care este determinarea structurilor și organelor afectate de tumoare. Determinarea etapei ajută la definirea prognosticului și la selectarea terapiilor . Cel mai frecvent sistem este sistemul TNM în patru etape (prescurtarea pentru Tumor / Limfoganglioni / Metastaze), care implică luarea în considerare a mărimii tumorii, a numărului de ganglioni limfatici implicați și a prezenței metastazelor . [58] [59]
Cea mai importantă distincție făcută de orice sistem de stadializare este dacă tumora este sau nu limitată la căile biliare. Sunt disponibile mai multe teste pentru a evidenția o evaluare în acest sens și includ în principal tehnici de imagistică biomedicală .
Rezultatele pot fi apoi clasificate grație stadializării TNM [3] :
| stadiu | Descriere |
|---|---|
| Tx | tumoare primară nedefinibilă |
| T0 | nu există dovezi ale tumorii primare |
| Tis | tumora in situ |
| T1 | tumora limitată histologic la peretele căii biliare |
| T2 | tumora care se extinde dincolo de peretele căilor biliare |
| T3 | tumoare care invadează ficatul, vezica biliară, pancreasul și / sau o singură ramură a venei porte |
| T4 | tumora care invadează una dintre următoarele structuri: trunchiul portal principal sau ramurile sale bilateral, artera hepatică comună sau alte organe adiacente precum colonul , stomacul, duodenul sau peretele abdominal |
| Nx | ganglioni limfatici regionali nedefinibili |
| N0 | absența metastazelor în ganglionii limfatici regionali |
| N1 | prezența metastazelor în ganglionii limfatici regionali (cel puțin trei) |
| Mx | metastaze îndepărtate care nu pot fi definite |
| M0 | absența metastazelor la distanță |
| M1 | prezența metastazelor la distanță |
Etapele posibile rezultate sunt [3] :
| stadiu | Clasificare |
|---|---|
| Etapa 0: | Tis N0 M0 |
| Etapa 1A: | T1 N0 M0 |
| Etapa 1B: | T2 N0 M0 |
| Etapa 2A: | T3 N0 M0 |
| Etapa 2B: | T1, T2, T3 N1 M0 |
| Etapa 3: | T4 N (orice) M0 |
| Etapa 4: | T (orice) N (orice) M1 |
Tratament
Colangiocarcinomul este considerat o boală incurabilă și rapid fatală, cu excepția cazului în care întregul țesut tumoral poate fi complet îndepărtat (adică tăiat chirurgical). Deoarece operabilitatea tumorii poate fi evaluată numai în timpul intervenției chirurgicale, în majoritatea cazurilor [60] , pacienții sunt supuși unei intervenții chirurgicale exploratorii, cu excepția cazului în care există deja o indicație clară a inoperabilității. [11]
Terapia adjuvantă , urmată de transplantul de ficat , poate juca un rol important în tratamentul unor cazuri inoperabile. [61]
Chimioterapie și radioterapie adjuvantă
Dacă tumora poate fi îndepărtată chirurgical, pacienții pot primi chimioterapie sau radioterapie adjuvantă după operație pentru a îmbunătăți șansele de recuperare. Dacă marginile țesuturilor sunt negative (adică tumora a fost complet excizată), terapia adjuvantă are un beneficiu incert. Studiile efectuate au produs atât rezultate pozitive [62] [63], cât și negative [10] [64] [65] cu radioterapie adjuvantă. Chimioterapia adjuvantă pare a fi ineficientă la pacienții cu tumoră complet excizată. [66] Rolul chimio-radioterapiei combinate în acest context este neclar. Cu toate acestea, dacă marginile țesutului tumoral sunt pozitive, indicând faptul că tumora nu a fost complet îndepărtată prin intervenție chirurgicală, terapia adjuvantă cu radioterapie și chimioterapie este recomandată în general pe baza datelor disponibile. [67] [68]
Tratamentul bolii avansate
Majoritatea cazurilor de colangiocarcinom sunt inoperabile. [6] În acest caz, pacienții sunt de obicei tratați cu chimioterapie paliativă , cu sau fără radioterapie. Chimioterapia s-a dovedit, într-un studiu controlat randomizat, că este utilă pentru îmbunătățirea calității vieții și pentru prelungirea supraviețuirii la pacienții cu colangiocarcinom inoperabil. [69] Nu există un regim unic de chimioterapie universal utilizat și includerea în studiile clinice este adesea recomandată ori de câte ori este posibil. [69] Cei mai frecvent utilizați agenți chimioterapeutici pentru tratamentul colangiocarcinomului includ Fluorouracil cu leucovorină [70] , gemcitabina ca agent unic [71] sau gemcitabină plus cisplatină [72] , irinotecan [73] sau capecitabină [74] . Un mic studiu pilot a sugerat un posibil beneficiu al administrării Erlotinib , un inhibitor al receptorului tirozin kinazei , la pacienții cu colangiocarcinom avansat. [75]
Terapia fotodinamică , o abordare experimentală în care pacienții sunt tratați cu o lumină sensibilizantă la insulină endoscopic direct pe tumoră, s-a dovedit promițătoare în ceea ce privește îngrijirea de susținere în două studii. Cu toate acestea, rolul său exact în gestionarea colangiocarcinomului nu este încă clar. [76] [77] Cu toate acestea, sa demonstrat că terapia fotodinamică îmbunătățește supraviețuirea și calitatea vieții pacienților. [78]
Prognoză
Rezecția chirurgicală oferă singura șansă potențială de recuperare după colangiocarcinom. Pentru cazurile nerezecabile, rata de supraviețuire la 5 ani este de 0% atunci când boala este inoperabilă deoarece ganglionii limfatici distali prezintă metastaze [79] și mai puțin de 5% în general. [80] Durata mediană globală de supraviețuire este mai mică de 6 luni [81] la pacienții inoperabili și netratabili.
În cazurile în care se poate încerca abordarea chirurgicală, șansele de recuperare variază în funcție de localizarea tumorii și dacă aceasta poate fi complet sau doar parțial îndepărtată. Colangiocarcinoamele distale (cele care decurg din conducta biliară comună) sunt de obicei tratate chirurgical cu o duodenocefalopancrezectomie ; Ratele de supraviețuire pe termen lung variază de la 15% la 25%, deși un studiu a raportat o supraviețuire la cinci ani de 54% pentru pacienții fără afectare a ganglionilor limfatici. [82] Colangiocarcinoamele intrahepatice (cele care apar din căile biliare din ficat) sunt de obicei tratate cu hepatectomie parțială. Diverse studii au raportat estimări de supraviețuire post-chirurgicală variind de la 22% la 66%. Rezultatul poate depinde de implicarea ganglionilor limfatici și de completitudinea rezecției chirurgicale. [83] Colangiocarcinoamele perihilare (cele care apar în apropierea locului în care căile biliare părăsesc ficatul) sunt cele mai puțin operabile. Când este posibilă intervenția chirurgicală, acestea sunt tratate de obicei cu o abordare agresivă, care include adesea îndepărtarea vezicii biliare și a unei părți a ficatului. La pacienții cu cancer peri-ilar operabil, ratele de supraviețuire la 5 ani sunt cuprinse între 20% și 50%. [84]
Prognosticul poate fi mai rău pentru pacienții cu colangită sclerozantă primară care dezvoltă colangiocarcinom, posibil deoarece cancerul nu este detectat până când nu se află într-un stadiu avansat. [14] [85] Unele dovezi sugerează că rezultatele pot fi mai bune cu abordări chirurgicale mai agresive și cu terapie adjuvantă. [86]
Epidemiologie
|
Colangiocarcinomul este adenocarcinomul tractului biliar [88] împreună cu cancerul pancreatic (care apare de aproximativ 20 de ori mai frecvent), [89] cancerul vezicii biliare (care apare de două ori mai des) și cancerul fiolei Vater . Tratamentele și studiile clinice pentru cancerul pancreatic, fiind mult mai răspândite, sunt adesea luate ca punct de plecare pentru gestionarea colangiocarcinomului. Deși tratamentele de chimioterapie pot aduce cancerul pancreatic în remisie permanentă, nu există exemple în literatura de supraviețuire pe termen lung din medicamente și radioterapie la pacienții cu colangiocarcinom inoperabil.
Colangiocarcinomul este o formă relativ rară de cancer. În fiecare an, aproximativ 2.000 până la 3.000 de cazuri noi sunt diagnosticate în Statele Unite , ceea ce duce la o incidență anuală de 1-2 cazuri la 100.000 de persoane. [1] Examinările post- mortem au raportat o prevalență cuprinsă între 0,01% și 0,46%. [90] [91] Există o prevalență mai mare a colangiocarcinomului în Asia , care a fost atribuită unei infestări parazitare cronice endemice . Incidența colangiocarcinomului crește odată cu vârsta, iar boala este puțin mai frecventă la bărbați decât la femei (posibil datorită ratei mai mari de colangită sclerozantă primară, un factor de risc major, la bărbați). [41] Conform unor studii de autopsie, prevalența colangiocarcinomului la pacienții cu colangită sclerozantă primară ar putea ajunge la 30%. [14]
Studii multiple au documentat o creștere constantă a incidenței colangiocarcinomului intrahepatic în ultimele decenii. Au fost observate creșteri în America de Nord , Europa , Asia și Australia . [92] Motivele prezenței crescânde a acestui tip de cancer sunt neclare. O explicație ar putea fi aceea referitoare la îmbunătățirea semnificativă a tehnicilor de diagnostic. [23]
Notă
- ^ a b Landis S, Murray T, Bolden S, Wingo P, statistici despre cancer, 1998 , în CA Cancer J Clin , vol. 48, nr. 1, 1998, pp. 6–29, DOI : 10.3322 / canjclin.48.1.6 , PMID 9449931 .
- ^ Patel T, Tendințe la nivel mondial în mortalitate prin tumori maligne ale tractului biliar , în BMC Cancer , vol. 2, 2002, p. 10, DOI : 10.1186 / 1471-2407-2-10 , PMC 113759 , PMID 11991810 .
- ^ a b c d e f Colangiocarcinom [ link rupt ] , pe startoncology.net , Startoncology. Adus pe 2 ianuarie 2012 .
- ^ a b Gotthardt D, Chahoud F, Sauer P., Colangita sclerozantă primară: probleme diagnostice și terapeutice , în Endoscopy Live Berlin 2011 - Intestinal Disease Meeting , Vol. 29, Suppl 1, 2011, PMID 22104752 .
- ^ a b Weber S, DeMatteo R, Fong Y, Blumgart L, Jarnagin W,Laparoscopia în stadiula pacienții cu carcinom biliar extrahepatic: analiza a 100 de pacienți , în Ann Surg , vol. 235, nr. 3, 2002, pp. 392–9, DOI : 10.1097 / 00000658-200203000-00011 , PMC 1422445 , PMID 11882761 .
- ^ a b Vauthey J, Blumgart L, Progrese recente în gestionarea colangiocarcinoamelor , în Semin. Dis ficat. , vol. 14, n. 2, 1994, pp. 109-14, DOI : 10.1055 / s-2007-1007302 , PMID 8047893 .
- ^ Poultsides GA, Zhu AX, Choti MA, Pawlik TM., Colangiocarcinom intrahepatic , în Clinici chirurgicale din America de Nord , vol. 90, n. 4, pp. 817-837, PMID 20637950 .
- ^ Nagorney D, Donohue J, Farnell M, Schleck C, Ilstrup D, Rezultate după rezecții curative ale colangiocarcinomului , în Arch Surg , vol. 128, nr. 8, 1993, pp. 871-7; discuția 877-9, PMID 8393652 .
- ^ Cancerul căilor biliare: cauză și tratament
- ^ a b Nakeeb A, Pitt H, Sohn T, Coleman J, Abrams R, Piantadosi S, Hruban R, Lillemoe K, Yeo C, Cameron J,Colangiocarcinom. Un spectru de tumori intrahepatice, perihilare și distale , în Ann Surg , vol. 224, nr. 4, 1996, pp. 463–73; discuție 473-5, DOI : 10.1097 / 00000658-199610000-00005 , PMC 1235406 , PMID 8857851 .
- ^ a b c Mark Feldman, Lawrence S. Friedman, Lawrence J. Brandt (eds), Sleisenger și Fordtran's Gastrointestinal and Liver Disease , 8th, Saunders, o amprentă a lui Elsevier, 21 iulie 2006, pp. 1493–1496, ISBN 978-1-4160-0245-1 .
- ^ Chapman R, Factori de risc pentru carcinogeneza tractului biliar , în Ann Oncol , 10 Suppl 4, 1999, pp. 308-11, PMID 10436847 .
- ^ Studiile epidemiologice care evaluează incidența colangiocarcinomului la persoanele cu colangită sclerozantă primară includ:
- Bergquist A, Ekbom A, Olsson R, Kornfeldt D, Lööf L, Danielsson A, Hultcrantz R, Lindgren S, Prytz H, Sandberg-Gertzén H, Almer S, Granath F, Broomé U, Malignități hepatice și extrahepatice în colangita sclerozantă primară , în J Hepatol , vol. 36, n. 3, 2002, pp. 321-7, DOI : 10.1016 / S0168-8278 (01) 00288-4 , PMID 11867174 .
- Bergquist A, Glaumann H, Persson B, Broomé U, Factori de risc și prezentarea clinică a carcinomului hepatobiliar la pacienții cu colangită sclerozantă primară: un studiu caz-control , în Hepatologie , vol. 27, n. 2, 1998, pp. 311–6, DOI : 10.1002 / hep . 510270201 , PMID 9462625 .
- Burak K, Angulo P, Pasha T, Egan K, Petz J, Lindor K, Incidența și factorii de risc pentru colangiocarcinom în colangita sclerozantă primară , în Am J Gastroenterol , vol. 99, nr. 3, 2004, pp. 523-6, DOI : 10.1111 / j.1572-0241.2004.04067.x , PMID 15056096 .
- ^ a b c Rosen C, Nagorney D, Wiesner R, Coffey R, LaRusso N, Colangiocarcinom carecomplică colangita sclerozantă primară , în Ann Surg , vol. 213, nr. 1, 1991, pp. 21-5, DOI : 10.1097 / 00000658-199101000-00004 , PMC 1358305 , PMID 1845927 .
- ^ a b Sahani D, Prasad S, Tannabe K, Hahn P, Mueller P, Saini S, colangiocarcinom indus de Thorotrast: raport de caz , în Abdom Imaging , vol. 28, n. 1, 2003, pp. 72-4, DOI : 10.1007 / s00261-001-0148-y , PMID 12483389 .
- ^ a b Zhu A, Lauwers G, Tanabe K, Colangiocarcinom în asociere cu expunerea la Thorotrast , în J Hepatobiliary Pancreat Surg , vol. 11, n. 6, 2004, pp. 430–3, DOI : 10.1007/s00534-004-0924-5 , PMID 15619021 .
- ^ Watanapa P, Cholangiocarcinoma in patients with opisthorchiasis , in Br J Surg , vol. 83, n. 8, 1996, pp. 1062–64, DOI : 10.1002/bjs.1800830809 , PMID 8869303 .
- ^ Watanapa P, Watanapa W, Liver fluke-associated cholangiocarcinoma , in Br J Surg , vol. 89, n. 8, 2002, pp. 962–70, DOI : 10.1046/j.1365-2168.2002.02143.x , PMID 12153620 .
- ^ Shin H, Lee C, Park H, Seol S, Chung J, Choi H, Ahn Y, Shigemastu T, Hepatitis B and C virus, Clonorchis sinensis for the risk of liver cancer: a case-control study in Pusan, Korea , in Int J Epidemiol , vol. 25, n. 5, 1996, pp. 933–40, DOI : 10.1093/ije/25.5.933 , PMID 8921477 .
- ^ Kobayashi M, Ikeda K, Saitoh S, Suzuki F, Tsubota A, Suzuki Y, Arase Y, Murashima N, Chayama K, Kumada H, <2471::AID-CNCR7>3.0.CO;2-T Incidence of primary cholangiocellular carcinoma of the liver in Japanese patients with hepatitis C virus-related cirrhosis , in Cancer , vol. 88, n. 11, 2000, pp. 2471–7, DOI : 10.1002/1097-0142(20000601)88:11<2471::AID-CNCR7>3.0.CO;2-T , PMID 10861422 .
- ^ Yamamoto S, Kubo S, Hai S, Uenishi T, Yamamoto T, Shuto T, Takemura S, Tanaka H, Yamazaki O, Hirohashi K, Tanaka T,Hepatitis C virus infection as a likely etiology of intrahepatic cholangiocarcinoma , in Cancer Sci , vol. 95, n. 7, 2004, pp. 592–5, DOI : 10.1111/j.1349-7006.2004.tb02492.x , PMID 15245596 .
- ^ Lu H, Ye M, Thung S, Dash S, Gerber M, Detection of hepatitis C virus RNA sequences in cholangiocarcinomas in Chinese and American patients , in Chin Med J (Engl) , vol. 113, n. 12, 2000, pp. 1138–41, PMID 11776153 .
- ^ a b c Shaib Y, El-Serag H, Davila J, Morgan R, McGlynn K, Risk factors of intrahepatic cholangiocarcinoma in the United States: a case-control study , in Gastroenterology , vol. 128, n. 3, 2005, pp. 620–6, DOI : 10.1053/j.gastro.2004.12.048 , PMID 15765398 .
- ^ Sorensen H, Friis S, Olsen J, Thulstrup A, Mellemkjaer L, Linet M, Trichopoulos D, Vilstrup H, Olsen J, Risk of liver and other types of cancer in patients with cirrhosis: a nationwide cohort study in Denmark , in Hepatology , vol. 28, n. 4, 1998, pp. 921–5, DOI : 10.1002/hep.510280404 , PMID 9755226 .
- ^ Lipsett P, Pitt H, Colombani P, Boitnott J, Cameron J,Choledochal cyst disease. A changing pattern of presentation , in Ann Surg , vol. 220, n. 5, 1994, pp. 644–52, DOI : 10.1097/00000658-199411000-00007 , PMC 1234452 , PMID 7979612 .
- ^ Dayton M, Longmire W, Tompkins R, Caroli's Disease: a premalignant condition? , in Am J Surg , vol. 145, n. 1, 1983, pp. 41–8, DOI : 10.1016/0002-9610(83)90164-2 , PMID 6295196 .
- ^ Mecklin J, Järvinen H, Virolainen M, The association between cholangiocarcinoma and hereditary nonpolyposis colorectal carcinoma , in Cancer , vol. 69, n. 5, 1992, pp. 1112–4, DOI : 10.1002/cncr.2820690508 , PMID 1310886 .
- ^ Lee S, Kim M, Lee S, Jang S, Song M, Kim K, Kim H, Seo D, Song D, Yu E, Lee S, Min Y, Clinicopathologic review of 58 patients with biliary papillomatosis , in Cancer , vol. 100, n. 4, 2004, pp. 783–93, DOI : 10.1002/cncr.20031 , PMID 14770435 .
- ^ Lee C, Wu C, Chen G, What is the impact of coexistence of hepatolithiasis on cholangiocarcinoma? , in J Gastroenterol Hepatol , vol. 17, n. 9, 2002, pp. 1015–20, DOI : 10.1046/j.1440-1746.2002.02779.x , PMID 12167124 .
- ^ Su C, Shyr Y, Lui W, P'Eng F, Hepatolithiasis associated with cholangiocarcinoma , in Br J Surg , vol. 84, n. 7, 1997, pp. 969–73, DOI : 10.1002/bjs.1800840717 , PMID 9240138 .
- ^ Donato F, Gelatti U, Tagger A, Favret M, Ribero M, Callea F, Martelli C, Savio A, Trevisi P, Nardi G, Intrahepatic cholangiocarcinoma and hepatitis C and B virus infection, alcohol intake, and hepatolithiasis: a case-control study in Italy , in Cancer Causes Control , vol. 12, n. 10, 2001, pp. 959–64, DOI : 10.1023/A:1013747228572 , PMID 11808716 .
- ^ ( EN ) Grosso F, Croce A, Libener R, Mariani N, Pastormerlo M, Maconi A, Asbestos Fiber Identification in Liver From Cholangiocarcinoma Patients Living in an Asbestos Polluted Area: A Preliminary Study , su Tumori , 2019 Oct. URL consultato il 3 giugno 2020 .
- ^ KLATSKIN G, Adenocarcinoma Of The Hepatic Duct At Its Bifurcation Within The Porta Hepatis. An Unusual Tumor With Distinctive Clinical And Pathological Features , in Am J Med , vol. 38, n. 2, 1965, pp. 241–56, DOI : 10.1016/0002-9343(65)90178-6 , PMID 14256720 .
- ^ Roskams T, Liver stem cells and their implication in hepatocellular and cholangiocarcinoma , in Oncogene , vol. 25, n. 27, 2006, pp. 3818–22, DOI : 10.1038/sj.onc.1209558 , PMID 16799623 .
- ^ Liu C, Wang J, Ou Q, Possible stem cell origin of human cholangiocarcinoma , in World J Gastroenterol , vol. 10, n. 22, 2004, pp. 3374–6, PMID 15484322 .
- ^ Sell S, Dunsford H,Evidence for the stem cell origin of hepatocellular carcinoma and cholangiocarcinoma , in Am J Pathol , vol. 134, n. 6, 1989, pp. 1347–63, PMC 1879951 , PMID 2474256 .
- ^ a b Sirica A, Cholangiocarcinoma: molecular targeting strategies for chemoprevention and therapy , in Hepatology , vol. 41, n. 1, 2005, pp. 5–15, DOI : 10.1002/hep.20537 , PMID 15690474 .
- ^ Holzinger F, Z'graggen K, Büchler M, Mechanisms of biliary carcinogenesis: a pathogenetic multi-stage cascade towards cholangiocarcinoma , in Ann Oncol , 10 Suppl 4, 1999, pp. 122–6, PMID 10436802 .
- ^ Gores G, Cholangiocarcinoma: current concepts and insights , in Hepatology , vol. 37, n. 5, 2003, pp. 961–9, DOI : 10.1053/jhep.2003.50200 , PMID 12717374 .
- ^ de Groen P, Gores G, LaRusso N, Gunderson L, Nagorney D, Biliary tract cancers , in N Engl J Med , vol. 341, n. 18, 1999, pp. 1368–78, DOI : 10.1056/NEJM199910283411807 , PMID 10536130 .
- ^ a b Henson D, Albores-Saavedra J, Corle D, <1498::AID-CNCR2820700609>3.0.CO;2-C Carcinoma of the extrahepatic bile ducts. Histologic types, stage of disease, grade, and survival rates , in Cancer , vol. 70, n. 6, 1992, pp. 1498–501, DOI : 10.1002/1097-0142(19920915)70:6<1498::AID-CNCR2820700609>3.0.CO;2-C , PMID 1516001 .
- ^ Tra gli studi che hanno messo in evidenza il ruolo del dosaggio dei markers tumorali per il colangiocarcinoma (come l'antigene carcinoembrionario e il CA19-9) in pazienti affetti e non da colangite sclerosante primitiva sono compresi:
- Nehls O, Gregor M, Klump B, Serum and bile markers for cholangiocarcinoma , in Semin Liver Dis , vol. 24, n. 2, 2004, pp. 139–54, DOI : 10.1055/s-2004-828891 , PMID 15192787 .
- Siqueira E, Schoen R, Silverman W, Martin J, Rabinovitz M, Weissfeld J, Abu-Elmaagd K, Madariaga J, Slivka A, Martini J, Detecting cholangiocarcinoma in patients with primary sclerosing cholangitis , in Gastrointest Endosc , vol. 56, n. 1, 2002, pp. 40–7, DOI : 10.1067/mge.2002.125105 , PMID 12085033 .
- Levy C, Lymp J, Angulo P, Gores G, Larusso N, Lindor K, The value of serum CA 19-9 in predicting cholangiocarcinomas in patients with primary sclerosing cholangitis , in Dig Dis Sci , vol. 50, n. 9, 2005, pp. 1734–40, DOI : 10.1007/s10620-005-2927-8 , PMID 16133981 .
- Patel A, Harnois D, Klee G, LaRusso N, Gores G, The utility of CA 19-9 in the diagnoses of cholangiocarcinoma in patients without primary sclerosing cholangitis , in Am J Gastroenterol , vol. 95, n. 1, 2000, pp. 204–7, DOI : 10.1111/j.1572-0241.2000.01685.x , PMID 10638584 .
- ^ Saini S, Imaging of the hepatobiliary tract , in N Engl J Med , vol. 336, n. 26, 1997, pp. 1889–94, DOI : 10.1056/NEJM199706263362607 , PMID 9197218 .
- ^ Sharma M, Ahuja V, Aetiological spectrum of obstructive jaundice and diagnostic ability of ultrasonography: a clinician's perspective , in Trop Gastroenterol , vol. 20, n. 4, 1999, pp. 167–9, PMID 10769604 .
- ^ Bloom C, Langer B, Wilson S, Role of US in the detection, characterization, and staging of cholangiocarcinoma , in Radiographics , vol. 19, n. 5, 1999, pp. 1199–218, PMID 10489176 .
- ^ Valls C, Gumà A, Puig I, Sanchez A, Andía E, Serrano T, Figueras J, Intrahepatic peripheral cholangiocarcinoma: CT evaluation , in Abdom Imaging , vol. 25, n. 5, 2000, pp. 490–6, DOI : 10.1007/s002610000079 , PMID 10931983 .
- ^ Tillich M, Mischinger H, Preisegger K, Rabl H, Szolar D, Multiphasic helical CT in diagnosis and staging of hilar cholangiocarcinoma , in AJR Am J Roentgenol , vol. 171, n. 3, 1998, pp. 651–8, PMID 9725291 .
- ^ Zhang Y, Uchida M, Abe T, Nishimura H, Hayabuchi N, Nakashima Y, Intrahepatic peripheral cholangiocarcinoma: comparison of dynamic CT and dynamic MRI , in J Comput Assist Tomogr , vol. 23, n. 5, 1999, pp. 670–7, DOI : 10.1097/00004728-199909000-00004 , PMID 10524843 .
- ^ Sugiyama M, Hagi H, Atomi Y, Saito M, Diagnosis of portal venous invasion by pancreatobiliary carcinoma: value of endoscopic ultrasonography , in Abdom Imaging , vol. 22, n. 4, 1997, pp. 434–8, DOI : 10.1007/s002619900227 , PMID 9157867 .
- ^ Schwartz L, Coakley F, Sun Y, Blumgart L, Fong Y, Panicek D, Neoplastic pancreaticobiliary duct obstruction: evaluation with breath-hold MR cholangiopancreatography , in AJR Am J Roentgenol , vol. 170, n. 6, 1998, pp. 1491–5, PMID 9609160 .
- ^ Zidi S, Prat F, Le Guen O, Rondeau Y, Pelletier G,Performance characteristics of magnetic resonance cholangiography in the staging of malignant hilar strictures , in Gut , vol. 46, n. 1, 2000, pp. 103–6, DOI : 10.1136/gut.46.1.103 , PMC 1727781 , PMID 10601064 .
- ^ Lee M, Park K, Shin Y, Yoon H, Sung K, Kim M, Lee S, Kang E, Preoperative evaluation of hilar cholangiocarcinoma with contrast-enhanced three-dimensional fast imaging with steady-state precession magnetic resonance angiography: comparison with intraarterial digital subtraction angiography , in World J Surg , vol. 27, n. 3, 2003, pp. 278–83, DOI : 10.1007/s00268-002-6701-1 , PMID 12607051 .
- ^ Yeh T, Jan Y, Tseng J, Chiu C, Chen T, Hwang T, Chen M, Malignant perihilar biliary obstruction: magnetic resonance cholangiopancreatographic findings , in Am J Gastroenterol , vol. 95, n. 2, 2000, pp. 432–40, DOI : 10.1111/j.1572-0241.2000.01763.x , PMID 10685746 .
- ^ Freeman M, Sielaff T, A modern approach to malignant hilar biliary obstruction , in Rev Gastroenterol Disord , vol. 3, n. 4, 2003, pp. 187–201, PMID 14668691 .
- ^ Szklaruk J, Tamm E, Charnsangavej C, Preoperative imaging of biliary tract cancers , in Surg Oncol Clin N Am , vol. 11, n. 4, 2002, pp. 865–76, DOI : 10.1016/S1055-3207(02)00032-7 , PMID 12607576 .
- ^ Callery M, Strasberg S, Doherty G, Soper N, Norton J, Staging laparoscopy with laparoscopic ultrasonography: optimizing resectability in hepatobiliary and pancreatic malignancy , in J Am Coll Surg , vol. 185, n. 1, 1997, pp. 33–9, PMID 9208958 .
- ^ ( DE ) Länger F, von Wasielewski R, Kreipe HH, [The importance of immunohistochemistry for the diagnosis of cholangiocarcinomas] , in Pathologe , vol. 27, n. 4, 2006, pp. 244–50, DOI : 10.1007/s00292-006-0836-z , PMID 16758167 .
- ^ Sobin LH, Gospodarowicz MK, Wittekind Ch., TNM Classification of Malignant Tumors , Oxford, Wiley-Blackwell, 2009, ISBN 978-1-4443-3241-4 .
- ^ ( EN ) Stadiazione: Domande & Risposte" a cura dell'Istituto Nazionale dei Tumori Americano , su cancer.gov . URL consultato il 2 gennaio 2012 .
- ^ Su C, Tsay S, Wu C, Shyr Y, King K, Lee C, Lui W, Liu T, P'eng F,Factors influencing postoperative morbidity, mortality, and survival after resection for hilar cholangiocarcinoma , in Ann Surg , vol. 223, n. 4, 1996, pp. 384–94, DOI : 10.1097/00000658-199604000-00007 , PMC 1235134 , PMID 8633917 .
- ^ Heimbach JK, Gores GJ, Haddock MG, et al., Predictors of disease recurrence following neoadjuvant chemoradiotherapy and liver transplantation for unresectable perihilar cholangiocarcinoma, Transplantation. 2006 Dec 27;82(12):1703-7.
- ^ Todoroki T, Ohara K, Kawamoto T, Koike N, Yoshida S, Kashiwagi H, Otsuka M, Fukao K, Benefits of adjuvant radiotherapy after radical resection of locally advanced main hepatic duct carcinoma , in Int J Radiat Oncol Biol Phys , vol. 46, n. 3, 2000, pp. 581–7, DOI : 10.1016/S0360-3016(99)00472-1 , PMID 10701737 .
- ^ Alden M, Mohiuddin M, The impact of radiation dose in combined external beam and intraluminal Ir-192 brachytherapy for bile duct cancer , in Int J Radiat Oncol Biol Phys , vol. 28, n. 4, 1994, pp. 945–51, DOI : 10.1016/0360-3016(94)90115-5 , PMID 8138448 .
- ^ González González D, Gouma D, Rauws E, van Gulik T, Bosma A, Koedooder C, Role of radiotherapy, in particular intraluminal brachytherapy, in the treatment of proximal bile duct carcinoma , in Ann Oncol , 10 Suppl 4, 1999, pp. 215–20, PMID 10436826 .
- ^ Pitt H, Nakeeb A, Abrams R, Coleman J, Piantadosi S, Yeo C, Lillemore K, Cameron J,Perihilar cholangiocarcinoma. Postoperative radiotherapy does not improve survival , in Ann Surg , vol. 221, n. 6, 1995, pp. 788–97; discussion 797–8, DOI : 10.1097/00000658-199506000-00017 , PMC 1234714 , PMID 7794082 .
- ^ Takada T, Amano H, Yasuda H, Nimura Y, Matsushiro T, Kato H, Nagakawa T, Nakayama T, Is postoperative adjuvant chemotherapy useful for gallbladder carcinoma? A phase III multicenter prospective randomized controlled trial in patients with resected pancreaticobiliary carcinoma , in Cancer , vol. 95, n. 8, 2002, pp. 1685–95, DOI : 10.1002/cncr.10831 , PMID 12365016 .
- ^ ( EN ) National Comprehensive Cancer Network (NCCN) guidelines on evaluation and treatment of hepatobiliary malignancies ( PDF ), su nccn.org . URL consultato il 13 marzo 2007 .
- ^ ( EN ) Junji Furuse, Tadahiro Takada, Masaru Miyazaki, Shuichi Miyakawa, Kazuhiro Tsukada, Masato Nagino, Satoshi Kondo, Hiroya Saito, Toshio Tsuyuguchi and Koichi Hirata, et al., Guidelines for chemotherapy of biliary tract and ampullary carcinomas [ collegamento interrotto ] , in Journal of Hepato-Biliary-Pancreatic Surgery , vol. 15, n. 1, pp. 55-62, PMID 18274844 .
- ^ a b Glimelius B, Hoffman K, Sjödén P, Jacobsson G, Sellström H, Enander L, Linné T, Svensson C, Chemotherapy improves survival and quality of life in advanced pancreatic and biliary cancer , in Ann Oncol , vol. 7, n. 6, 1996, pp. 593–600, PMID 8879373 .
- ^ Choi C, Choi I, Seo J, Kim B, Kim J, Kim C, Um S, Kim J, Kim Y, Effects of 5-fluorouracil and leucovorin in the treatment of pancreatic-biliary tract adenocarcinomas , in Am J Clin Oncol , vol. 23, n. 4, 2000, pp. 425–8, DOI : 10.1097/00000421-200008000-00023 , PMID 10955877 .
- ^ Park J, Oh S, Kim S, Kwon H, Kim J, Jin-Kim H, Kim Y, Single-agent gemcitabine in the treatment of advanced biliary tract cancers: a phase II study , in Jpn J Clin Oncol , vol. 35, n. 2, 2005, pp. 68–73, DOI : 10.1093/jjco/hyi021 , PMID 15709089 .
- ^ Giuliani F, Gebbia V, Maiello E, Borsellino N, Bajardi E, Colucci G, Gemcitabine and cisplatin for inoperable and/or metastatic biliary tree carcinomas: a multicenter phase II study of the Gruppo Oncologico dell'Italia Meridionale (GOIM) , in Ann Oncol , 17 Suppl 7, 2006, pp. vii73–vii77, DOI : 10.1093/annonc/mdl956 , PMID 16760299 .
- ^ Bhargava P, Jani C, Savarese D, O'Donnell J, Stuart K, Rocha Lima C, Gemcitabine and irinotecan in locally advanced or metastatic biliary cancer: preliminary report , in Oncology (Williston Park) , vol. 17, 9 Suppl 8, 2003, pp. 23–6, PMID 14569844 .
- ^ Knox J, Hedley D, Oza A, Feld R, Siu L, Chen E, Nematollahi M, Pond G, Zhang J, Moore M, Combining gemcitabine and capecitabine in patients with advanced biliary cancer: a phase II trial , in J Clin Oncol , vol. 23, n. 10, 2005, pp. 2332–8, DOI : 10.1200/JCO.2005.51.008 , PMID 15800324 .
- ^ Philip P, Mahoney M, Allmer C, Thomas J, Pitot H, Kim G, Donehower R, Fitch T, Picus J, Erlichman C, Phase II study of erlotinib in patients with advanced biliary cancer , in J Clin Oncol , vol. 24, n. 19, 2006, pp. 3069–74, DOI : 10.1200/JCO.2005.05.3579 , PMID 16809731 .
- ^ Ortner M, Caca K, Berr F, Liebetruth J, Mansmann U, Huster D, Voderholzer W, Schachschal G, Mössner J, Lochs H, Successful photodynamic therapy for nonresectable cholangiocarcinoma: a randomized prospective study , in Gastroenterology , vol. 125, n. 5, 2003, pp. 1355–63, DOI : 10.1016/j.gastro.2003.07.015 , PMID 14598251 .
- ^ Zoepf T, Jakobs R, Arnold J, Apel D, Riemann J, Palliation of nonresectable bile duct cancer: improved survival after photodynamic therapy , in Am J Gastroenterol , vol. 100, n. 11, 2005, pp. 2426–30, DOI : 10.1111/j.1572-0241.2005.00318.x , PMID 16279895 .
- ^ Gut Liver. 2010 Sep;4(Suppl. 1):S62-S66. Epub 2010 Sep 10. Photodynamic Therapy for Cholangiocarcinoma. Talreja JP, Kahaleh M. PMID 21103297
- ^ Yamamoto M, Takasaki K, Yoshikawa T, Lymph Node Metastasis in Intrahepatic Cholangiocarcinoma , in Japanese Journal of Clinical Oncology , vol. 29, n. 3, 1999, pp. 147–150, DOI : 10.1093/jjco/29.3.147 , PMID 10225697 .
- ^ Farley D, Weaver A, Nagorney D, "Natural history" of unresected cholangiocarcinoma: patient outcome after noncurative intervention , in Mayo Clin Proc , vol. 70, n. 5, 1995, pp. 425–9, DOI : 10.4065/70.5.425 , PMID 7537346 .
- ^ Grove MK, Hermann RE, Vogt DP, Broughan TA, Role of radiation after operative palliation in cancer of the proximal bile ducts , in Am J Surg , vol. 161, n. 4, 1991, pp. 454–458, DOI : 10.1016/0002-9610(91)91111-U , PMID 1709795 .
- ^ Studi dei risultati chirurgici del colangiocarcinoma distale includono:
- Nakeeb A, Pitt H, Sohn T, Coleman J, Abrams R, Piantadosi S, Hruban R, Lillemoe K, Yeo C, Cameron J,Cholangiocarcinoma. A spectrum of intrahepatic, perihilar, and distal tumors , in Ann Surg , vol. 224, n. 4, 1996, pp. 463–73; discussion 473–5, DOI : 10.1097/00000658-199610000-00005 , PMC 1235406 , PMID 8857851 .
- Nagorney D, Donohue J, Farnell M, Schleck C, Ilstrup D, Outcomes after curative resections of cholangiocarcinoma , in Arch Surg , vol. 128, n. 8, 1993, pp. 871–7; discussion 877–9, PMID 8393652 .
- Jang J, Kim S, Park D, Ahn Y, Yoon Y, Choi M, Suh K, Lee K, Park Y,Actual Long-term Outcome of Extrahepatic Bile Duct Cancer After Surgical Resection , in Ann Surg , vol. 241, n. 1, 2005, pp. 77–84, PMC 1356849 , PMID 15621994 .
- Bortolasi L, Burgart L, Tsiotos G, Luque-De León E, Sarr M, Adenocarcinoma of the distal bile duct. A clinicopathologic outcome analysis after curative resection , in Dig Surg , vol. 17, n. 1, 2000, pp. 36–41, DOI : 10.1159/000018798 , PMID 10720830 .
- Fong Y, Blumgart L, Lin E, Fortner J, Brennan M, Outcome of treatment for distal bile duct cancer , in Br J Surg , vol. 83, n. 12, 1996, pp. 1712–5, DOI : 10.1002/bjs.1800831217 , PMID 9038548 .
- ^ Tra gli studi dei risultati operatori di colangiocarcinomi intraepatici sono annoverati:
- Nakeeb A, Pitt H, Sohn T, Coleman J, Abrams R, Piantadosi S, Hruban R, Lillemoe K, Yeo C, Cameron J,Cholangiocarcinoma. A spectrum of intrahepatic, perihilar, and distal tumors , in Ann Surg , vol. 224, n. 4, 1996, pp. 463–73; discussion 473–5, DOI : 10.1097/00000658-199610000-00005 , PMC 1235406 , PMID 8857851 .
- Lieser M, Barry M, Rowland C, Ilstrup D, Nagorney D, Surgical management of intrahepatic cholangiocarcinoma: a 31-year experience , in J Hepatobiliary Pancreat Surg , vol. 5, n. 1, 1998, pp. 41–7, DOI : 10.1007/PL00009949 , PMID 9683753 .
- Valverde A, Bonhomme N, Farges O, Sauvanet A, Flejou J, Belghiti J, Resection of intrahepatic cholangiocarcinoma: a Western experience , in J Hepatobiliary Pancreat Surg , vol. 6, n. 2, 1999, pp. 122–7, DOI : 10.1007/s005340050094 , PMID 10398898 .
- Nakagohri T, Asano T, Kinoshita H, Kenmochi T, Urashima T, Miura F, Ochiai T, Aggressive surgical resection for hilar-invasive and peripheral intrahepatic cholangiocarcinoma , in World J Surg , vol. 27, n. 3, 2003, pp. 289–93, DOI : 10.1007/s00268-002-6696-7 , PMID 12607053 .
- Weber S, Jarnagin W, Klimstra D, DeMatteo R, Fong Y, Blumgart L, Intrahepatic cholangiocarcinoma: resectability, recurrence pattern, and outcomes , in J Am Coll Surg , vol. 193, n. 4, 2001, pp. 384–91, DOI : 10.1016/S1072-7515(01)01016-X , PMID 11584966 .
- ^ Tra le stime sulla sopravvivenza post-chirurgica di pazienti operati per colangiocarcinoma periilare sono compresi i seguenti studi:
- Burke E, Jarnagin W, Hochwald S, Pisters P, Fong Y, Blumgart L,Hilar Cholangiocarcinoma: patterns of spread, the importance of hepatic resection for curative operation, and a presurgical clinical staging system , in Ann Surg , vol. 228, n. 3, 1998, pp. 385–94, DOI : 10.1097/00000658-199809000-00011 , PMC 1191497 , PMID 9742921 .
- Tsao J, Nimura Y, Kamiya J, Hayakawa N, Kondo S, Nagino M, Miyachi M, Kanai M, Uesaka K, Oda K, Rossi R, Braasch J, Dugan J,Management of Hilar Cholangiocarcinoma: Comparison of an American and a Japanese Experience , in Ann Surg , vol. 232, n. 2, 2000, pp. 166–74, DOI : 10.1097/00000658-200008000-00003 , PMC 1421125 , PMID 10903592 .
- Chamberlain R, Blumgart L, Hilar cholangiocarcinoma: a review and commentary , in Ann Surg Oncol , vol. 7, n. 1, 2000, pp. 55–66, DOI : 10.1007/s10434-000-0055-4 , PMID 10674450 .
- Washburn W, Lewis W, Jenkins R, Aggressive surgical resection for cholangiocarcinoma , in Arch Surg , vol. 130, n. 3, 1995, pp. 270–6, PMID 7534059 .
- Nagino M, Nimura Y, Kamiya J, Kanai M, Uesaka K, Hayakawa N, Yamamoto H, Kondo S, Nishio H, Segmental liver resections for hilar cholangiocarcinoma , in Hepatogastroenterology , vol. 45, n. 19, 1998, pp. 7–13, PMID 9496478 .
- Rea D, Munoz-Juarez M, Farnell M, Donohue J, Que F, Crownhart B, Larson D, Nagorney D, Major hepatic resection for hilar cholangiocarcinoma: analysis of 46 patients , in Arch Surg , vol. 139, n. 5, 2004, pp. 514–23; discussion 523–5, DOI : 10.1001/archsurg.139.5.514 , PMID 15136352 .
- Launois B, Reding R, Lebeau G, Buard J, Surgery for hilar cholangiocarcinoma: French experience in a collective survey of 552 extrahepatic bile duct cancers , in J Hepatobiliary Pancreat Surg , vol. 7, n. 2, 2000, pp. 128–34, DOI : 10.1007/s005340050166 , PMID 10982604 .
- ^ Kaya M, de Groen P, Angulo P, Nagorney D, Gunderson L, Gores G, Haddock M, Lindor K, Treatment of cholangiocarcinoma complicating primary sclerosing cholangitis: the Mayo Clinic experience , in Am J Gastroenterol , vol. 96, n. 4, 2001, pp. 1164–9, DOI : 10.1111/j.1572-0241.2001.03696.x , PMID 11316165 .
- ^ Nakeeb A, Tran K, Black M, Erickson B, Ritch P, Quebbeman E, Wilson S, Demeure M, Rilling W, Dua K, Pitt H, Improved survival in resected biliary malignancies , in Surgery , vol. 132, n. 4, 2002, pp. 555–63; discission 563–4, DOI : 10.1067/msy.2002.127555 , PMID 12407338 .
- ^ Khan S, Taylor-Robinson S, Toledano M, Beck A, Elliott P, Thomas H, Changing international trends in mortality rates for liver, biliary and pancreatic tumours , in J Hepatol , vol. 37, n. 6, 2002, pp. 806–13, DOI : 10.1016/S0168-8278(02)00297-0 , PMID 12445422 .
- ^ Colangiocarcinoma , su fondazionefegato.it , Fondazione Italiana per la Ricerca in Epatologia. URL consultato il 2 gennaio 2011 .
- ^ http://seer.cancer.gov/csr/1975_2005/results_single/sect_01_table.01.pdf
- ^ Vauthey J, Blumgart L, Recent advances in the management of cholangiocarcinomas , in Semin Liver Dis , vol. 14, n. 2, 1994, pp. 109–14, DOI : 10.1055/s-2007-1007302 , PMID 8047893 .
- ^ Cancer Statistics Home Page - National Cancer Institute
- ^ Numerosi studi indipendenti hanno documentato una crescita stazionaria nel tasso di incidenza mondiale del colangiocarcinoma; tra gli studi più rilevanti citiamo:
- Patel T, Worldwide trends in mortality from biliary tract malignancies , in BMC Cancer , vol. 2, 2002, p. 10, DOI : 10.1186/1471-2407-2-10 , PMC 113759 , PMID 11991810 .
- Patel T, Increasing incidence and mortality of primary intrahepatic cholangiocarcinoma in the United States , in Hepatology , vol. 33, n. 6, 2001, pp. 1353–7, DOI : 10.1053/jhep.2001.25087 , PMID 11391522 .
- Shaib Y, Davila J, McGlynn K, El-Serag H, Rising incidence of intrahepatic cholangiocarcinoma in the United States: a true increase? , in J Hepatol , vol. 40, n. 3, 2004, pp. 472–7, DOI : 10.1016/j.jhep.2003.11.030 , PMID 15123362 .
- West J, Wood H, Logan R, Quinn M, Aithal G,Trends in the incidence of primary liver and biliary tract cancers in England and Wales 1971–2001 , in Br J Cancer , vol. 94, n. 11, 2006, pp. 1751–8, DOI : 10.1038/sj.bjc.6603127 , PMC 2361300 , PMID 16736026 .
- Khan S, Taylor-Robinson S, Toledano M, Beck A, Elliott P, Thomas H, Changing international trends in mortality rates for liver, biliary and pancreatic tumours , in J Hepatol , vol. 37, n. 6, 2002, pp. 806–13, DOI : 10.1016/S0168-8278(02)00297-0 , PMID 12445422 .
- Welzel T, McGlynn K, Hsing A, O'Brien T, Pfeiffer R, Impact of classification of hilar cholangiocarcinomas (Klatskin tumors) on the incidence of intra- and extrahepatic cholangiocarcinoma in the United States , in J Natl Cancer Inst , vol. 98, n. 12, 2006, pp. 873–5, DOI : 10.1093/jnci/djj234 , PMID 16788161 .
Bibliografia
- DeVita, Hellman, Lawrence, DeVita, Hellman, and Rosenberg's Cancer: Principles & Practice of Oncology , 8ª ed., Lippincott Williams & Wilkins, 2008, ISBN 978-0-7817-7207-5 .
- Gianni Bonadonna, Gioacchino Robustelli Della Cuna, Pinuccia Valgussa, Medicina oncologica , 8ª ed., Milano, Elsevier Masson, 2007, ISBN 978-88-214-2814-2 .
- Robbins e Cotran, Le basi patologiche delle malattie , 7ª ed., Torino-Milano, Elsevier Masson, 2008, ISBN 978-88-85675-53-7 .
- Giorgio Cittadini, Diagnostica per immagini e radioterapia , ECIG, 2008, ISBN 978-88-7544-138-8 .
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su colangiocarcinoma
Wikimedia Commons contiene immagini o altri file su colangiocarcinoma
Collegamenti esterni
- ( EN ) Linee Guida del British Medical Journal per il colangiocarcinoma
- ( EN ) studio italiano relativo all'eterogeneità genetica dei colangiocarcinomi pubblicato dall' IRCC di Candiolo
- ( EN ) studio BINGO , su asco.org . URL consultato il 15 ottobre 2011 (archiviato dall' url originale il 12 ottobre 2011) .
- Chirurgia Epatobiliare, Ospedale San Raffaele, Milano https://www.hsr.it/strutture/ospedale-san-raffaele/chirurgia-epatobiliare