Distribuție Maxwell-Boltzmann
| Distribuție Maxwell-Boltzmann | |
|---|---|
Funcția de densitate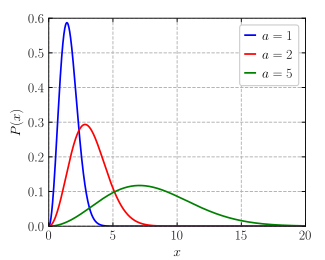 | |
Funcția de distribuție | |
| Parametrii | |
| A sustine | |
| Funcția de densitate | |
| Funcția de distribuție | , unde este Este funcția de eroare |
| Valorea estimata | |
| Modă | |
| Varianța | |
| Indicele de asimetrie | |
| Curios | |
| Entropie | |
Distribuția Maxwell-Boltzmann este o funcție de distribuție a particulelor cu o anumită energie, într-un sistem care respectă legile fizicii clasice : asigură adică probabilitatea ca o particulă să aibă o „ energie între și Sau o viteză cuprinsă între Și .
Presupunerea fundamentală care stă la baza acestei distribuții este că componentele particulelor sistemului se disting , că sistemul este liniar, izotrop și că procesele statistice de la baza stării sistemului pentru a respecta statisticul Markov . În termeni fizici, se spune atunci că sistemul este termalizat complet. Acest lucru se întâmplă, de exemplu, dacă frecvența coliziunilor din sistem (care, de exemplu, poate fi un gaz ) este suficient de mare în comparație cu timpii proceselor pe care doriți să le analizați.
Când cade prima ipoteză, de exemplu în mecanica cuantică , distribuția lui Maxwell-Boltzmann nu mai este valabilă și apar în locul a două tipuri de distribuții diferite, cunoscute sub numele de distribuția lui Fermi-Dirac și Bose-Einstein .
Când ipotezele despre liniaritate, izotropie sau statistici Markov cad, distribuția Maxwell-Boltzmann este variată în diferite moduri, în funcție de proprietățile sistemului. În acest al doilea caz, nu există un tratament organic complet, dar există diverse teorii care ne permit să tratăm anumite cazuri particulare. Mai jos va fi explicat cazul sistemelor slab haotice , adică acele sisteme care în teoria haosului nu sunt ergodice , dar sunt caracterizate de regiuni ordonate cufundate în cele mai haotice regiuni.
fundal
Această distribuție a fost introdusă pentru prima dată de fizicul Maxwell , dar a ajuns la celebritate datorită studiului și a înțelegerilor lui Ludwig Boltzmann privind utilizarea sa pentru mecanica statistică .
Este expus sub deducția clasică, furnizată de Boltzmann dintr-o coloană de gaz supusă gravitației.
Model simplu

Luați în considerare o coloană de gaz sub influența gravitației [1] : înălțimea vei avea presiune Unde este legea lui Stevin :
Adică, prin descompunerea densității masei în densitatea numărului și a mediului de masă molecular :
Ecuația constitutivă a unui gaz ideal este:
- .
unde temperatura absolută este aici exprimată în unități de energie (în sistemul internațional , în jouli , pentru înmulțirea valorii constantei Boltzmann ). În condiții izotermale avem această lege a proporționalității în distribuțiile spațiale:
.
Apoi se ajunge la „ ecuația diferențială parțială :
care este atribuibil unei ecuații a valorii proprii pentru gradient : vectorul de undă , valoarea proprie a gradientului, pentru acest caz corespunde raportului:
.
Într - o dimensiune spațială (o coloană de gaz, în care este altitudinea barometrică ), puteți vedea ecuația ca o ecuație diferențială obișnuită de primul ordin :
- .
Acesta din urmă are soluția clasică de descompunere exponențială :
- .
Această lege poate fi în cele din urmă re-exprimată, ținând cont de faptul că „ energia potențială a coloanei este:
Prin urmare, densitatea în coloană variază în funcție de factor :
- .
Inversând această relație, energia potențială a câmpului poate fi reconstituită din distribuția câmpului de densitate a gazului:
- .
Modelul statistic
Având în vedere un sistem format din particule totale cu energie totală
se presupune că distribuția de echilibru este cea mai probabilă și cea la care concurează valoarea maximă a ponderii statistice . Dacă în aceste condiții are loc o variație infinitesimală a distribuției, amintind că:
- ,
adică sub forma logaritmică
și restricția că nici numărul total de particule și nici energia totală a sistemului nu se schimbă, ajungem la:
- .
Deoarece are legătură cu valori mari (de exemplu, o cantitate de particule egală cu valoarea numerică a constantei Avogadro ), puteți aplica aproximarea „ Stirling ”:
- ,
obținând astfel:
- .
Ținând cont în același timp de ecuațiile care constrâng fluctuațiile de distribuție, adică
este posibil să abordăm problema folosind metoda multiplicatorilor Lagrange care introduc coeficienții Și . Prin atribuirea acestor doi coeficienți o valoare astfel încât, de exemplu, termenii Și ecuaţie
sunt nule, atunci impunem pur și simplu că suma termenilor din cu este egal cu zero. Care este deci echivalent cu starea generală:
- ,
care se poate exprima și sub forma exponențială
cu constant.
Identificarea cu modelul fizic al coloanei de gaz supuse gravitației, permite derivarea relației , În cazul în care temperatura este măsurată în unități de energie (în sistemul internațional , în jouli ) sau, echivalent, , unde este este temperatura absolută , măsurată în unități de energie (de exemplu, în jouli ).
Caz unidimensional
Adesea, în cazuri practice, este mai bine să exprimăm densitatea particulelor în funcție de viteza particulelor. În acest paragraf temperatura absolută Se măsoară în unități de energie, astfel încât să nu apară constanta Boltzmann . Prin urmare, definim distribuția unidimensională a vitezei în direcție : acesta este, este probabilitatea ca componenta vitezei de -a lungul este între Și . Din legea conservării energiei, avem o particulă cu viteză poate ajunge până la o înălțime:
- .
din care se obține diferențierea . Acestea sunt chiar moleculele care ating nivelul , dar nu și nivelul deoarece nu au suficientă energie cinetică pentru ao face. Diferențierea legii exponențiale pentru densitate obținem:
- ,
și, folosind relația care leagă înălțimea atinsă a accelera , noi obținem:
- .
Ca prin definiție , obținem asta
- .
Prin definirea mediei modulului de viteză ca , obținem că:
- ,
unde este este o constantă de normalizare adecvată. În practică, distribuția vitezei într-o direcție este o amplitudine gaussiană : aceasta înseamnă că mișcarea particulelor este lungă Este complet haotic (ipoteza haosului molecular ) și distanța pătratică medie pe care o particulă o parcurge în direcția este proporțională cu temperatura sistemului.
Pentru a obține valoarea constantei, distribuția trebuie normalizată la unitate, adică expresia pentru este integrată pe un domeniu infinit (apoi ne întoarcem la acest aspect):
- .
Pentru a găsi integralul utilizând proprietățile integralelor funcției Gamma , cu schimbarea variabilelor , pentru a obține în cele din urmă distribuția normalizată corect pe întreaga axă reală:
- .
Momente ale distribuției unidimensionale
Una dintre pietrele de temelie ale gândirii lui Boltzmann este că cantitățile măsurabile în lumea macroscopică (adică cantitatea termodinamică ca temperatură și presiune ) pot fi obținute cu operații medii ale cantităților microscopice, utilizând funcția de distribuție: așa cum se spune în statistici , folosind metoda momentelor .
Este interesant în acest moment să ne întrebăm care sunt momentele distribuției unidimensionale, adică cantitățile:
- .
cu arbitrar, unde chiar am remarcat că integrarea se realizează pe un domeniu infinit.
Din considerații simple de paritate a funcției integrand, obținem că pentru număr întreg ciudat: pentru orice eventualitate , aceasta înseamnă pur și simplu că viteza medie în direcție este nulă (consecință a ipotezei haosului molecular).
Dacă în schimb este chiar întreg, integralul este rezolvat folosind una dintre integralele care definesc funcția Gamma :
- .
Folosind schimbarea obișnuită a variabilelor pe care le obținem că momentele -alea sunt
- .
Rezultatul este următorul: deși distribuția este definită pe un domeniu infinit, toate momentele de viteză sunt finite. Aceasta înseamnă în special că deplasarea pătrată medie a unei particule este diferită de zero chiar și la distanțe infinite (ceea ce implică un conflict cu dinamica sistemului): în realitate, toate distribuțiile reale sunt trunchiate: vom reveni la acest punct mai târziu.
În special, al doilea moment (viteza pătrată medie în direcția ) este dată de expresia generală din cauză :
- ,
acesta este:
- ,
sau, în termeni de energie cinetică medie:
- .
Aceasta din urmă este faimoasa lege a temperaturii identității cu „media sistemului de energie cinetică ”.
Deducerea distribuției complete
Deducerea distribuției tridimensionale complete este relativ simplă, dacă se presupune că sistemul este izotrop , și anume că mișcarea particulelor nu are direcții preferențiale. În aceste ipoteze, distribuția completă este produsul distribuțiilor unidimensionale pe axele unice Și :
Expresia poate fi simplificată folosind modulul de viteză Și folosind elementul volum în coordonate sferice , și integrarea pe coordonatele unghiulare:
- .
Ultima expresie este expresia clasică a distribuției. Vedem imediat asta în dimensiunea nu este mai mult decât o gaussiană : odată cu creșterea distribuției temperaturii se lărgește, dar maximul se deplasează în același timp spre valori de viteză mai mari.
În ceea ce privește al doilea moment, viteza pătrată medie se obține folosind independența mișcărilor din cele trei axe Și :
- , [2]
sau, în termeni de energie cinetică medie (totală) a sistemului:
- ,
adică de trei ori energia cinetică medie pentru fiecare direcție de mișcare. Acest rezultat este în acord cu teorema echipartizării energiei .
Generalizând ceea ce s-a găsit pentru distribuția unidimensională, se poate deduce că momentele succesive ale distribuției complete (tridimensionale) sunt date de:
Aceasta înseamnă că, de exemplu, pentru momente uniforme avem:
- , ,
si asa mai departe.
Sisteme reale
Deducerea distribuției lui Maxwell-Boltzmann este una dintre cele mai elegante și mai strălucite demonstrații ale fizicii : este de fapt singura distribuție analitică care permite (într-un sistem clasic), într-un mod relativ simplu, să conecteze mărimi termodinamice și microscopice dinamica. Din acest motiv, este utilizat pe scară largă în toate domeniile fizicii aplicate până la punctul de a uita adesea care sunt ipotezele care stau la baza demonstrației. Ignorarea acestor ipoteze duce deseori la întâlnirea abaterilor de la datele experimentale, atribuibile faptului că sistemele reale sunt adesea mult mai complexe.
Principalele ipoteze utilizate sunt următoarele:
Ipoteza stochastică
Presupuneri că sistemul respectă ipoteza haosului molecular . Aceasta implică distribuția vitezei în orice direcție, atât Gaussiană : adică particulele nu au o direcție preferențială de mișcare. Dacă acest lucru este adevărat în cazul unui gaz perfect , nu este întotdeauna adevărat pentru toate sistemele. De fapt, în mecanică puteți fi rezolvat într-un mod analitic, prin „ ecuația Newton ”, doar sisteme relativ simple, cum ar fi sistemul cu două corpuri . Există, de asemenea, unele sisteme haotice care pot fi tratate analitic în teoria haosului , ca bazinul Sinaiului și „ atractivul lui Lorenz : uneori le vorbești despre haosul determinist. Cu toate acestea, caracteristica acestor sisteme este că sunt caracterizate de câteva grade de libertate.
Pentru sistemele reale, care sunt caracterizate în general de un număr mare de grade de libertate , este dificil de găsit o punte simplă care să lege comportamentul microscopic dinamic de comportamentul macroscopic al termodinamicii : simplificarea adoptată de Boltzmann este tocmai aceea de a aduce numărul de grade de libertate la infinit și presupunem că mișcarea particulelor este stocastică . Acest lucru este în general destul de bine verificat: de exemplu, numărul de particule conținute într-un metru cub d ' aer este , ceea ce justifică această presupunere.
Cu toate acestea, pentru unele sisteme, ipoteza stocastică nu funcționează bine: atunci când numărul de grade de libertate este mare, dar nu infinit, comportamentul sistemului poate fi intermediar între cel al unui sistem previzibil (cum ar fi sistemele teoriei haosului ) și haos molecular. Adică, pot exista unele zone de haos slab imersate într-un stochastic mediu. Un exemplu tipic este cel al plasmelor imersate în câmpuri magnetice haotice aproape de pragul ergodicității . În astfel de cazuri, aveți nevoie de distribuții diferite (de exemplu, distribuția lui Lévy ), dar adesea acestea nu sunt analitice și complică foarte mult calculele.
Ipoteza izotropiei
Dacă există direcții preferențiale de mișcare, distribuția globală nu mai depinde doar de modulul vitezei, ci și de poziție [3] .
Ipoteza unui sistem infinit
După cum s-a văzut mai sus, distribuția Maxwell-Boltzmann este definită pe întreaga axă reală. În realitate, niciun sistem nu este infinit, ci are o dimensiune finită: totuși, pentru ca deducția să aibă sens, spațiul trebuie că o particulă poate călători într-un timp este suficient de mic în comparație cu dimensiunea generală a sistemului . Adică, în formule, limita trebuie să se aplice:
- .
În cazul Maxwell-Boltzmann avem asta
- .
prin urmare, limita merge la zero pentru temperaturi rezonabile: aceasta înseamnă că dimensiunea saltului elementar pe care o poate face o particulă trebuie să fie încă mică în comparație cu sistemul. Dacă acest lucru nu se face, există abateri importante la distribuție, denumite generic subdifuziune sau superdifuziune [4] .
Ipoteza unui sistem markovian
O ipoteză de bază în tratamentul termodinamic este că proprietățile coliziunilor dintre particule nu depind de istoricul anterior al particulelor (adică de modul în care a fost atinsă coliziunea), ci doar de condițiile instantanee din momentul coliziunii. Această ipoteză poate cădea, de exemplu, dacă distanța medie dintre două coliziuni este de ordinul lungimii de undă a particulei De Broglie : în acest caz, aceasta din urmă trebuie tratată ca o undă conform regulilor mecanicii cuantice . Prin urmare, nu mai este posibilă neglijarea fenomenelor de interferență între diferitele evenimente de împrăștiere și ipoteza procesului Markov cade. De asemenea, puteți apărea situații, cum ar fi cea a localizării Anderson , în care procesele de difuzie necesare termalizării sistemului sunt interzise și astfel statisticile Boltzmann încetează să se afirme.
Aplicații
Biofizică
În neuroștiințe , ele descriu adesea mecanismele de deschidere și închidere a canalelor ionice printr-o funcție simplificată de Boltzmann atunci când acestea sunt dependente de potențialul membranei . Prin urmare, formula utilizată este:
- ,
unde este
- este potențialul membranei ,
- este conductivitatea electrică ionică asociată canalelor, în funcție de potențialul membranelor,
- este conductivitatea maximă,
- Jumătate din potențialul de activare este potențialul de membrană pentru care jumătate din canale sunt deschise,
- este dependența de deschiderea canalelor în raport cu schimbarea potențialului.
Distribuția Boltzmann este utilizată aici pentru a descrie rezultatele experimentale obținute din măsurarea patch-clamp a curenților de membrană și, astfel, pentru a determina proprietățile diferitelor categorii de curenți transmembranari. Parametrii Și sono determinanti per la modellizzazione informatica delle proprietà elettriche di una cellula nervosa .
Note
- ^ ( EN ) Questa deduzione si può trovare in John D. McGervey, Introduction to Modern Physics , seconda edizione, Academic Press, San Diego, CA, 1983, pp. 6-9. ISBN 0-12-483560-0 .
- ^ Meccanica e termodinamica, Mencuccini-Silvestrini .
- ^ ( EN ) Una trattazione completa nel libro di Radu Balescu, Statistical Dynamics: Matter Out of Equilibrium , World Scientific Publishing Company (giugno 1997). ISBN 1-86094-046-3 .
- ^ ( EN ) I problemi relativi alla definizione di una distribuzione che leghi la termodinamica alla dinamica di un sistema realistico di dimensioni finite è un argomento di frontiera: un articolo di rassegna degli ultimi risultati nel campo è GM Zaslavsky, Chaos, fractional kinetics and anomalous transport , Physics Reports 371 (2002), pp. 461-580.
Voci correlate
- Distribuzione di Boltzmann
- Legge di Boltzmann
- Funzione di partizione (meccanica statistica)
- Distribuzione di Maxwell-Jüttner
Collegamenti esterni
- ( EN ) Distribuzione di Maxwell-Boltzmann , su Enciclopedia Britannica , Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 27341 |
|---|









































































































