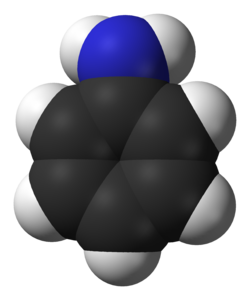
Anilină
| Anilină | |
|---|---|
| Numele IUPAC | |
| anilină | |
| Abrevieri | |
| Ph-NH2 | |
| Denumiri alternative | |
| fenilamina aminobenzen benzenamina | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 6 H 7 N |
| Masa moleculară ( u ) | 93.13 |
| Aspect | lichid incolor (galben până la maro dacă este impur) |
| numar CAS | |
| Numărul EINECS | 200-539-3 |
| PubChem | 6115 |
| DrugBank | DB06728 |
| ZÂMBETE | C1=CC=C(C=C1)N |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1,03 |
| Constanta de disociere de baza la 293 K. | 3,81 × 10 −10 |
| Solubilitate în apă | 36 g / l la 293 K |
| Temperatură de topire | −6,2 ° C (266,9 K) |
| Temperatura de fierbere | 184 ° C (457 K) |
| Δ eb H 0 (kJ mol −1 ) | 47.3 |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | 31.6 |
| C 0 p, m (J K −1 mol −1 ) | 191,9 |
| Informații de siguranță | |
| Punct de flacără | 76 ° C (349 K) |
| Limite de explozie | 1,2 - 11% vol. |
| Temperatură de autoaprindere | 540 ° C (813 K) |
| Simboluri de pericol chimic | |
     | |
| Pericol | |
| Fraze H | 351 - 341 - 331 - 311 - 301 - 372 - 318 - 317 - 400 |
| Sfaturi P | 273 - 280 - 308 + 313 - 302 + 352 - 305 + 351 + 338 - 309 + 310 [1] |
Anilina , cunoscută și sub numele de fenilamină sau aminobenzen , este un compus aromatic cu formula brută C 6 H 7 N. Este o amină primară a cărei structură este cea a unui benzen , în care un atom de hidrogen a fost înlocuit cu un grup NH 2 . La temperatura camerei apare ca un lichid incolor atunci când este foarte pur. Având în vedere ușurința cu care se oxidează în aer, anilina tinde să se întunece în timp până devine neagră.
Istorie
Anilina a fost izolată pentru prima dată în 1826 de către Otto Unverdorben prin distilarea produselor de descompunere ale indigo . Inițial a fost numită cristalină .
În 1834 F. Runge a izolat din gudron o substanță capabilă să producă o culoare albastră intensă prin tratarea cu var și a botezat-o cianol .
În 1841 CJ Fritzsche a dat numele de anilină uleiului obținut prin tratarea indigo cu potasiu caustic . Și-a luat numele de la planta Indigofera anil , din care derivă indigo. La rândul său, anil derivă din sanscrita nīla , albastru închis și nīlā , planta indigo. În același timp, chimistul rus Nikolai Nikolaevič Zinin a descoperit că prin reducerea nitrobenzenului se obține un compus bazic pe care l-a numit benzidam .
În cele din urmă, August Wilhelm von Hofmann, în 1855, a dovedit identitatea acestor preparate, toate atribuibile unei singure substanțe, denumită anilină sau fenilamină .
Prima producție de anilină la scară industrială a fost utilizată ca intermediar în sinteza mauveinei , un colorant violet descoperit în 1856 de William Henry Perkin . Se folosește și pentru „infernul negru”, un colorant pentru piele folosit de cizmari.
Sinteză
Anilina poate fi făcută din benzen în două etape. Benzenul este mai întâi nitrat , adică reacționează cu un amestec de acizi nitric și sulfurici concentrați pentru a da nitrobenzen printr-o reacție de substituție electrofilă . Apoi nitrobenzenul este redus la anilină prin reacția cu diverși reactivi reducători; printre care hidrogen în prezența unui catalizator sau a unui metal ( fier , zinc sau staniu ) în prezența acizilor .
Mulți derivați de anilină pot fi sintetizați în mod similar.
Proprietăți chimice și reactivitate
Anilina este o substanță otrăvitoare cu posibile efecte cancerigene (fraza de risc R40). Este un lichid uleios cu miros caracteristic și aspect incolor, cu toate acestea în timp se oxidează și produce impurități rășinoase roșii-maronii. Arde ușor cu flacără mare, fumurie. Chimic este o bază slabă. Aminele aromatice, cum ar fi anilina, sunt în general mai puțin bazice decât aminele alifatice, acest lucru se datorează faptului că dubletul de electroni al atomului de azot este parțial împărțit cu inelul aromatic prin rezonanță și, prin urmare, este mai puțin disponibil pentru a fi transferat speciilor chimice acide .
- Anilina reacționează cu acizi puternici pentru a da săruri de aniliniu C 6 H 5- NH 3 + care, în general, se descompun la încălzire, eliberând amoniac ; ea , de asemenea , reacționează cu acil halogenuri , cum ar fi clorura de acetil CH3COCI, sau cu acizi carboxilici într - un mediu de deshidratare pentru a da amide . Anilinele amide sunt adesea numite anilide ; CH3 - CO-NH-C 6 H 5, de exemplu, este acetanilida . [2]
- Prin reacția cu ioduri de alchil , anilina formează amine secundare și terțiare; prin fierbere cu sulfură de carbon dă sulfocarbanilidă ( difeniltiourea , CS (NHC 6 H 5 ) 2 ) care poate fi descompusă în fenil tiocianat C 6 H 5 CNS și trifenilguanidină C 6 H 5 N = C (NHC 6 H 5 ) 2 .
- La fel ca fenolul , și anilina suferă cu ușurință reacții de substituție electrofilă pe inelul aromatic în poziția para și orto . Prin reacția cu acidul sulfuric la 180 ° C dă acid sulfanilic p -NH 2 -C 6 H 4 -SO 3 H ale cărui amide formează clasa sulfonamidelor , medicamente antibacteriene utilizate în mod obișnuit la începutul secolului XX .
- Anilina și derivații săi substituiți pe inelul aromatic reacționează ușor cu acidul azotat pentru a da sărurile de diazoniu corespunzătoare; prin ele -NH2 gruparea de anilină poate fi transformată în alte grupe funcționale , cum ar fi -OH, -CN sau un halogen sau compuși de colorare, numit diazo coloranți, pot fi sintetizați.
- Cu acroleina anilina reacționează în conformitate cu sinteza Skraup după cum urmează:
- Anilina este oxidat atât pe gruparea -NH2 și pe inelul aromatic; într-un mediu alcalin oxidarea anilinei produce azobenzen ; cu acid arsenic se obține colorantul violet al anilinei , cu acid cromic se transformă în chinona corespunzătoare, în timp ce prin oxidare cu clorați în prezența sărurilor metalice, în special vanadiu , se obține colorantul negru pentru anilină .
- Oxidarea cu acid clorhidric și clorat de potasiu dă cloranil ; oxidarea cu permanganat de potasiu în soluție neutră îl transformă în nitrobenzen , în soluție alcalină îl oxidează în azobenzen, amoniac și acid oxalic , în soluție acidă îl transformă în negru de anilină.
- Reacția cu acidul hipocloros dă 4-aminofenol și 4-amino-difenilamină .
Eseuri
Anilina și sărurile sale pot fi identificate într-o soluție apoasă prin adăugarea a câteva picături de soluție saturată de hipoclorit de calciu ; se obține colorarea.
Utilizări
Valoarea comercială a anilinei este legată de versatilitatea sa ca intermediar în sintezele chimice industriale ale produselor precum medicamente, auxiliare și coloranți.
Din 1858 anilina a fost materia primă utilizată în producția a sute de substanțe colorante, inclusiv fuchsină , safranină , indigo și multe altele.
Industrial, anilina este produsă prin reducerea nitrobenzenului cu fier și acid clorhidric, purificându-l ulterior prin distilare cu abur.
Anilina a fost considerată inițial un propulsor de rachetă, dar a fost abandonată din cauza temperaturii ridicate de topire
Efecte asupra sănătății
Anilina este unul dintre primii agenți cancerigeni umani recunoscuți. [3] Ludwig Rehn, în 1895, a asociat incidența cancerului de vezică urinară cu expunerea lucrătorilor din industria germană a coloranților artificiali. [3] Provoacă în principal cancerul vezicii urinare, precum și cancerul de rinichi, piele, ficat și sânge. Molecula nu este cancerigenă ca atare, dar devine ca urmare a metabolizării sale în ficat prin procese de hidroxilare de către enzime dependente de citocromul P450 (lanțul oxidativ al microsomilor). Principalii derivați ai anilinei sunt para-amino-fenol și 2,4-dioxi-anilină; la rândul lor, acestor intermediari li se cere să sufere reacții de oxidare-reducere pentru a fi transformate în chinonele lor respective: para-iminochinonă și 2-hidroxi-para-iminochinonă.
Aceste ultime molecule, foarte reactive (electrofile), reacționează prompt cu reziduuri proteice specifice și cu acizi nucleici, stabilind o legătură covalentă. În cazul proteinelor, aceste enzime pot fi permanent inactivate și trebuie degradate. În cazul acizilor nucleici, în special al ADN-ului , au loc interacțiuni covalente cu bazele de guanină și adenină , reacții care duc atât la legături încrucișate între helicile ADN, cât și la rupturile acestora. În funcție de genele implicate și de localizarea lor, pot exista modificări variabile ale fenotipului celular, de exemplu, modificările genelor supresoare tumorale pot face celula mai supusă transformărilor neoplazice.
Notă
- ^ foaie informativă anilină pe IFA-GESTIS Arhivat 16 octombrie 2019 la Arhiva Internet .
- ^(RO) IUPAC Gold Book, "anilides"
- ^ a b ( EN ) Imaginația epidemiologică: un cititor - 1994, Pagina 77 | Biblioteca de cercetare online: Questia , la www.questia.com . Adus la 15 august 2017 .
Bibliografie
- ( EN ) Klaus Weissermel, Hans-Jürgen Arpe, Charlet R. Lindley, Industrial organic chimie , ediția a IV-a, Wiley-VCH, 2003, pp. 376-379, ISBN 3-527-30578-5 .
Alte proiecte
-
 Wikționarul conține dicționarul lema « anilină »
Wikționarul conține dicționarul lema « anilină » -
 Wikimedia Commons conține imagini sau alte fișiere pe anilină
Wikimedia Commons conține imagini sau alte fișiere pe anilină
linkuri externe
- ( EN ) Aniline / Aniline (altă versiune) , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
| Controlul autorității | Tezaur BNCF 30854 · LCCN (EN) sh85005157 · GND (DE) 4142482-7 · BNF (FR) cb12359525w (data) |
|---|