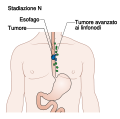
Carcinomul esofagului
| Carcinomul esofagului | |
|---|---|
| Un adenocarcinom în tractul de joncțiune gastroesofagian | |
| Specialitate | oncologie |
| Clasificare și resurse externe (EN) | |
| OMIM | 133239 |
| MedlinePlus | 000283 |
| eMedicină | 277930 și 368206 |
| Sinonime | |
| Carcinom esofagian | |
Carcinomul esofagului este o formă de neoplasm malign (tumoră) care afectează esofagul . [1] Simptomele includ deseori dificultăți la înghițire și scăderea în greutate. Alte simptome pot include durere la înghițire , o voce răgușită, ganglioni limfatici umflați în jurul claviculei , o tuse uscată și, eventual, tuse sau vărsături însoțite de sânge ( hemoptizie și, respectiv, hematemeză ). [2] [3]
Cele două subtipuri principale ale bolii sunt carcinomul cu celule scuamoase al esofagului, care este cel mai frecvent în lumea în curs de dezvoltare și cel mai frecvent adenocarcinom esofagian din lumea dezvoltată. [1] Cele mai frecvente cauze ale tipului de celule scuamoase sunt fumatul , alcoolul , băuturile foarte calde și o dietă destul de slabă, în timp ce cauzele adenocarcinomului sunt de obicei fumul de tutun, obezitatea și refluxul acid. [4]
Boala este diagnosticată grație unei biopsii făcute cu un endoscop . [5] Prevenirea include renunțarea la fumat și o dietă sănătoasă. [1] [2] Tratamentul variază în funcție de stadiul tumorii și de localizarea acesteia, evaluând, de asemenea, starea generală a pacientului și așteptările acestuia. Tumorile mici cu celule scuamoase localizate pot fi tratate numai prin intervenție chirurgicală și cu speranța unui prognostic favorabil. În majoritatea celorlalte cazuri, chimioterapia , cu sau fără radioterapie , este utilizată împreună cu intervenția chirurgicală. [5] În prezența unei boli extinse sau dacă persoana în cauză nu poate fi supusă unei operații chirurgicale, se solicită adesea îngrijiri paliative . [5] Datorită diagnosticului, care de obicei ajunge la un stadiu avansat, prognosticul este adesea slab și ratele de supraviețuire la 5 ani sunt cuprinse între aproximativ 13% și 18%. [1] [4] [6]
Începând din 2012, cancerul esofagian a fost al optulea cel mai frecvent cancer la nivel mondial, cu 456.000 de cazuri noi înregistrate în cursul anului [1] și aproximativ 400.000 de decese (87,7% letalitate), cifră mai mare decât 1990 când s-au înregistrat aproximativ 345.000 de decese. [1] [7] Datele epidemiologice variază foarte mult între țări și aproximativ jumătate din cazuri apar în China . Se estimează că este de trei ori mai frecventă la bărbați decât la femei. [1]
fundal
Primele descoperiri legate de acest carcinom datează din secolul al XIX-lea; prima operație chirurgicală pentru îndepărtarea tumorii a fost efectuată în 1913 .
Epidemiologie

nu există date
mai puțin de 3
3-6
6-9
9-12
12-15
15-18
18–21
21-24
24-27
27-30
30–35
peste 35
Cancerul esofagului este răspândit în întreaga lume, cu o incidență mai mare în țările asiatice (mai precis, în China și Mongolia ) și în Africa de Sud-Est, în special în Malawi și Africa de Sud . În toate aceste țări, numărând ambele sexe, incidența (ratele standardizate la populația lumii) depășește 15 cazuri la 100.000 de locuitori. În Europa, cele mai afectate țări sunt Regatul Unit , Olanda și Irlanda , dar cu rate mai mici decât în Asia și Africa, ajungând la 6 cazuri la 100.000 de locuitori. În Italia , cancerul esofagian este mai frecvent în nord-estul țării, cu o incidență medie de 2 cazuri la 100.000 de locuitori. Tumorile esofagului afectează în principal bărbații (70%). Cancerul esofagului este un cancer de vârstă avansată, cu rate de incidență care cresc treptat de la vârsta de 50 de ani, până la vârf între 70 și 80 de ani [9] .
Evoluția temporală a acestei tumori prezintă semne de scădere, în special în țările mai dezvoltate.
În Statele Unite ale Americii s-a observat că această tendință are o tendință diferită de histotip: în timp ce carcinomul cu celule scuamoase a fost cel mai răspândit, în ultimii douăzeci de ani ai secolului al XX-lea s-a observat o scădere a incidenței sale atât la populația neagră iar în cel alb, în timp ce incidența adenocarcinomului esofagian a crescut, în special la bărbații albi. Acest fenomen răspunde unor motive care sunt încă neclare. [10] În Italia, cancerul esofagian este în continuă scădere, în special la bărbați, dar histotipul scuamos continuă să predomine, ceea ce reprezintă aproximativ 60% din toate cazurile de cancer esofagian [11] .
Tipologie
În funcție de epiteliul de origine, există două tipuri de carcinom esofagian.
- Carcinom cu celule scuamoase , originar din celulele epiteliale ale trotuarului. Se găsește în treimea inferioară, mijlocie și superioară a esofagului. Inițial apare ca o depresiune apoi se dezvoltă sub formă vegetativă. Acesta reprezintă aproximativ 50% din cazuri.
- Adenocarcinom , care apare adesea din epiteliul cilindric al esofagului Barrett , în special în esofagul terminal (acest tip histologic crește în ultima perioadă).
Simptomatologie
De obicei, simptomele importante nu apar până când tumora nu a infiltrat mai mult de 60% din circumferința tubului esofagian, moment în care poate fi considerată deja într-un stadiu avansat. [12] Debutul simptomelor este de obicei cauzat de îngustarea esofagului cauzată de prezența obstructivă a masei tumorale. [13]
Primul și cel mai frecvent simptom este de obicei dificultatea de a înghiți ( disfagie ), care apare adesea inițial cu alimente solide și apoi cu alimente mai moi și lichide. [2] Există, de asemenea, durere la înghițire ( odinofagie ). [2] Pierderea în greutate este adesea un simptom destul de timpuriu pentru cazurile de carcinom cu celule scuamoase, deși de obicei nu este pentru adenocarcinom. [14] Cu toate acestea, este obișnuit să suferiți o pierdere substanțială în greutate din cauza apetitului redus și a malnutriției . [15] Durerea în spatele sternului sau în zona din jurul stomacului este adesea percepută ca arsuri la stomac. Un alt semn poate fi o tuse neobișnuit de răgușită, datorită masei tumorale care afectează nervul laringian recurent .
Prezența tumorii poate perturba contracțiile normale ale esofagului la înghițire. Acest lucru poate duce la greață și vărsături , insuficiență alimentară și tuse. [12] Există, de asemenea, posibilitatea de a dezvolta pneumonie de aspirație , datorită alimentelor care intră în căile respiratorii prin fistule care se pot dezvolta între esofag și trahee . [12] [16] Primele semne ale acestei complicații grave pot fi tusea în timp ce beți sau mâncați. [17] Suprafața tumorii poate fi fragilă și sângeroasă , provocând vărsături de sânge și anemie cu deficit de fier . Compresia structurilor locale apare în boala avansată, ducând la probleme cum ar fi obstrucția căilor respiratorii superioare și sindromul venei cave superioare . Poate apărea hipercalcemie (exces de calciu în sânge). [12]
Dacă cancerul s-a răspândit în altă parte, pot apărea simptome legate de boala metastatică . Locurile comune de răspândire includ ganglionii limfatici supraclaviculari, ficatul , plămânii și oasele . [12] Metastazele hepatice pot provoca icter și umflături abdominale ( ascită ). Metastazele pulmonare pot duce la insuficiență respiratorie cauzată de excesul de lichid din jurul plămânilor ( revărsat pleural ) și dispnee , printre alte simptome.
Etiologie
Cele două tipuri principale de cancer esofagian (adică carcinomul cu celule scuamoase și adenocarcinomul) au factori de risc distincti. [14] Carcinomul cu celule scuamoase este mai mult legat de stilul de viață, cum ar fi fumatul și alcoolul . [18] Adenocarcinomul a fost în schimb legat de efectele pe termen lung ale refluxului gastroesofagian . [18] Cu toate acestea, fumul de tutun este un factor de risc pentru ambele tipuri. [14] În plus, ambele sunt mai frecvente la bărbați și la cei cu vârsta peste 60 de ani. [19]
Carcinom cu celule scuamoase
Cei doi factori principali de risc pentru carcinomul cu celule scuamoase ale esofagului sunt tutunul ( afumat sau mestecat) și băuturile alcoolice. [1] Combinația de tutun și alcool are un puternic efect sinergic. [20] Unele date sugerează că aproximativ jumătate din cazuri se datorează tutunului și aproximativ o treime alcoolului, în timp ce peste trei sferturi din cazuri la bărbați se datorează combinației celor două. [1] Riscurile asociate alcoolului par a fi legate de metabolitul aldehidei sale și de mutațiile unor enzime conexe. [14] Astfel de variante metabolice sunt relativ frecvente în Asia . [1]
Nivelurile ridicate de expunere dietetică la nitrozamine (compuși chimici care pot fi găsiți atât în fumul de tutun, cât și în unele produse alimentare) par să aibă un factor de risc relevant. [14] Alimentele nefavorabile par să implice expunerea la nitrozamine prin salcam și carne la grătar, legume murate și un aport redus de alimente proaspete în dietă. [1] Alți factori asociați includ deficiențe nutriționale, stare socioeconomică scăzută și igienă orală precară. [14] Mestecarea nucilor de areca este un factor de risc major în Asia. [21]
Adenocarcinom
Acest tip de cancer esofagian apare de aproximativ 7 până la 10 ori mai des la bărbați decât la femei. [22] Acest dezechilibru poate fi legat de caracteristicile și interacțiunile altor factori de risc cunoscuți, inclusiv refluxul acidului esofagian și obezitatea . [22] [23]

Efectele erozive pe termen lung ale refluxului acid (o afecțiune foarte frecventă, cunoscută și sub numele de boală de reflux gastroesofagian ) au fost puternic asociate cu acest tip de cancer. [24] O afecțiune de acest tip pe o perioadă lungă de timp poate induce o schimbare a tipului de țesut din porțiunea inferioară a esofagului ca răspuns la eroziunea căptușelii sale solzoase. [24] Acest fenomen, cunoscut sub numele de esofag Barrett , pare să apară cu aproximativ 20 de ani mai târziu la femei decât la bărbați, posibil din cauza factorilor hormonali . [24] [25] Riscul dezvoltării adenocarcinomului în prezența esofagului Barrett nu este dovedit, în trecut această corelație fusese supraestimată. [1]
Obezitatea și excesul de greutate par a fi asociate cu un risc crescut. [26] Asocierea cancerului esofagian cu obezitatea pare să fie mai puternică decât cu orice alt cancer, deși motivele pentru acest lucru rămân neclare. [24] Obezitatea abdominală pare să aibă o relevanță deosebită și în cazul bolii de reflux esofagian și a esofagului Barrett. [24] Acest tip de obezitate este caracteristic bărbaților. [24]
Deși prezența Helicobacter pylori , care afectează mai mult de jumătate din populația lumii, este un factor de risc important pentru cancerul de stomac , pare a fi asociată cu o reducere de 50% a probabilității de a dezvolta adenocarcinom esofagian. [27] [28] Explicația biologică a acestui efect protector este oarecum incertă. [28] O posibilă explicație este că unele tulpini de H. pylori reduc acidul din stomac, reducând astfel daunele cauzate de boala de reflux esofagian. [29] Scăderea ratei de H. pylori la populațiile occidentale în ultimele decenii a fost propusă ca una dintre explicațiile pentru creșterea simultană a adenocarcinomului esofagian. Scăderea se datorează unei igiene mai bune, de exemplu printr-o refrigerare mai mare a alimentelor și grupuri familiale mai puțin aglomerate. [27]
Hormonii feminini pot avea, de asemenea, un efect protector, deoarece adenocarcinomul esofagian nu numai că este mult mai puțin frecvent la femei, dar se dezvoltă mai târziu în viață decât la bărbați. Deși studiile multor factori de reproducere nu au produs o imagine clară, riscul pare să scadă pentru mamele care au alăptat . [27]
Fumatul de tutun crește riscul, dar riscul crescut pentru adenocarcinomul esofagian este mic în comparație cu cel pentru carcinomul cu celule scuamoase. [27]
Condiții conexe
- Cancerele de cap și gât sunt asociate cu tumori din regiunea înconjurătoare, inclusiv carcinoamele cu celule scuamoase esofagiene, din cauza expunerii regionale pe termen lung a cancerigenului . [30] [31]
- Un istoric de radioterapie pentru alte afecțiuni toracice este un factor de risc pentru adenocarcinomul esofagian. [14]
- Leziunea corozivă a esofagului din cauza înghițirii accidentale sau intenționate a substanțelor caustice este un factor de risc pentru carcinomul cu celule scuamoase. [1]
- Tiloza cu cancer esofagian este o boală familială rară care a fost legată de o mutație a genei RHBDF2: este o îngroșare a pielii și un risc ridicat de carcinom cu celule scuamoase. [1] [32]
- Acalazia (adică lipsa reflexelor involuntare în esofag după înghițire) pare a fi un factor de risc pentru ambele tipuri majore de cancer esofagian, cel puțin la bărbați, din cauza stagnării alimentelor și băuturilor. [33]
- Sindromul Plummer-Vinson (o boală rară care implică membranele esofagiene) este, de asemenea, un factor de risc. [1]
- Există unele dovezi care sugerează o posibilă asociere cauzală între papilomavirusul uman (HPV) și carcinomul cu celule scuamoase al esofagului. [34] [35]
- Există dovezi limitate care să susțină o corelație între boala celiacă și cancerul esofagian. [33]
Diagnostic
Boala trebuie suspectată în prezența simptomelor specifice. O neoplazie ocluzivă poate fi suspectată în urma unei serii de raze X ale esofagului după administrarea unei mese de bariu ca agent de contrast , diagnosticul se face în urma unei esofagogastroduodenoscopie ( endoscopie ), care constă în trecerea unui tub flexibil echipat cu fibră optică lumină și o cameră care permite examinarea peretelui esofagian. Biopsiile prelevate din leziuni suspecte sunt apoi supuse examinării histologice pentru a observa semne de malignitate.
Sunt necesare teste suplimentare pentru a evalua răspândirea ( metastază ) a tumorii. Tomografia computerizată (CT) a pieptului, abdomenului și bazinului poate evalua dacă s-a răspândit în țesuturile adiacente sau în organele îndepărtate (în special ficatul și ganglionii limfatici ). Sensibilitatea unei scanări CT este limitată de capacitatea sa de a detecta mase (de exemplu, ganglioni limfatici umflați sau organe implicate) în general mai mari de 1 cm. Tomografia cu emisie de pozitroni (PET) poate fi utilizată pentru a estima amploarea bolii și este considerată mai precisă decât CT singură. Ecografia esofagiană endoscopică poate oferi unele informații cu privire la nivelul invaziei tumorale și la posibila răspândire în ganglionii limfatici regionali.
Localizarea tumorii este de obicei măsurată prin distanța de la dinți. Esofagul este împărțit în mod obișnuit în trei părți în scopul determinării locației. Adenocarcinoamele tind să apară mai aproape de stomac și carcinoamele cu celule scuamoase lângă gât, dar pot apărea oriunde în esofag.
Punerea în scenă
Stadializarea se bazează pe sistemul de clasificare TNM care clasifică cantitatea de invazie tumorală (T), implicarea ganglionilor limfatici (N) și prezența metastazelor la distanță (M). [14]
| stadiu | Clasificare |
|---|---|
| Etapa I: | tumora se găsește numai în mucoasă |
| Etapa II: | rămâne limitat în straturile peretelui esofagului |
| Etapa III: | invadează alte țesături |
| Etapa IV: | unde tumora s-a metastazat , cel mai avansat stadiu. |
Tratament

Se recomandă ca tratamentul să fie gestionat de o echipă multidisciplinară care acoperă diferitele specialități implicate. [36] [37] Trebuie asigurată o nutriție adecvată, precum și o îngrijire dentară eficientă. Factorii care influențează deciziile de tratament includ stadializarea tumorii și histologia , împreună cu starea generală a persoanei și orice alte afecțiuni medicale. [14]
În general, tratamentul cu intenție curativă este fezabil numai în cazurile de boală localizată, fără metastaze la distanță. În astfel de cazuri, poate fi luată în considerare o abordare combinată care implică o intervenție chirurgicală . Cancerele difuze sau recurente sunt gestionate prin îngrijiri paliative . În acest caz, chimioterapia poate fi utilizată pentru a extinde supraviețuirea, în timp ce tratamente precum radioterapia sau stenting-ul pot fi utilizate pentru ameliorarea simptomelor și facilitarea înghițirii. [14]
Interventie chirurgicala
O tumoare esofagiană de tip adenocarcinom în stadiul său incipient poate fi tratată prin îndepărtarea chirurgicală a esofagului total sau parțial ( esofagectomie ). Cu toate acestea, această intervenție chirurgicală este deosebit de dificilă, cu un risc relativ ridicat de mortalitate sau dificultăți postoperatorii. Beneficiile intervenției chirurgicale sunt mai puțin clare pentru cazurile de carcinom cu celule scuamoase în stadiu primar. Există o serie de opțiuni chirurgicale care fac adesea obiectul discuției. [36] [38] [39] Pe lângă caracteristicile și localizarea tumorii, alți factori de decizie includ starea pacientului și tipul de intervenție chirurgicală cu care echipa chirurgicală este cel mai obișnuit. Calitatea probabilă a vieții după operație este un factor relevant. [40] Rezultatele chirurgicale sunt de obicei mai bune în centrele mari unde astfel de proceduri sunt efectuate mai frecvent. [38] Dacă cancerul s-a răspândit în alte părți ale corpului, esofagectomia tinde să nu fie recomandată. [38]
Disecția endoscopică a submucoasei este o procedură care implică îndepărtarea tumorilor mici care implică doar mucoasa sau mucoasa esofagului. [41]
Esofagectomia este îndepărtarea unui segment al esofagului; deoarece acest lucru scurtează lungimea esofagului rămas, un alt segment al tractului digestiv este deplasat prin cavitatea toracică și interpus. Se face de obicei cu stomacul sau o parte a intestinului gros ( colon ) sau jejunul . Reconectarea stomacului la un esofag scurtat se numește anastomoză esofagogastrică . [38]
Esofagectomia se poate efectua folosind mai multe metode. Alegerea metodei chirurgicale depinde de caracteristicile și localizarea tumorii și de preferința chirurgului. [38] Prima decizie, referitoare la punctul de intrare, este între o procedură transhiatală și una transtoracică. Abordarea transhiatală este mai recentă și evită necesitatea deschiderii pieptului: chirurgul intră printr-o incizie în abdomenul inferior și alta în gât. Partea inferioară a esofagului este eliberată de țesuturile din jur și tăiată după cum este necesar. Stomacul este apoi împins prin hiatusul esofagian (gaura în care esofagul trece prin diafragmă ) și se alătură părții superioare rămase a esofagului. [38]
Abordarea transtoracică tradițională presupune accesul prin piept, cu numeroase variații. Abordarea toracică standard constă în deschiderea atât a cavităților abdominale, cât și a celei toracice, tehnica în două etape Ivor-Lewis (numită și Lewis-Tanner) implică o laparotomie inițială și construirea unui tub gastric, urmată de o toracotomie dreaptă pentru îndepărtarea tumorii și creează o anastomoză esofagogastrică. Abordarea McKeown în trei pași adaugă o a treia incizie în gât pentru a completa anastomoza cervicală. Abordările recente, numite esofagectomii extinse, constau în îndepărtarea în bloc a mai multor țesuturi înconjurătoare, inclusiv a ganglionilor limfatici. [38]
Dacă pacientul nu poate înghiți alimente, se poate introduce un stent esofagian pentru a menține brevetul esofagului; stentul poate ajuta, de asemenea, la ocluzia fistulelor. Un tub nazogastric poate fi necesar pentru a continua hrănirea în timp ce cancerul este tratat, iar unii pacienți necesită o gastrostomie (o gaură în piele care oferă acces direct la stomac). Aceste două soluții sunt deosebit de importante dacă pacientul tinde să aspire mâncare sau salivă în căile respiratorii, predispunându-l la pneumonie de aspirație .
Chimioterapie și radioterapie

Chimioterapia depinde de tipul de cancer, dar tinde să fie cisplatină (sau carboplatină și oxaliplatină ) la fiecare trei săptămâni cu fluorouracil (5-FU) continuu sau la fiecare trei săptămâni. În studii mai recente, adăugarea de epirubicină a arătat rezultate mai bune. [42] Chimioterapia poate fi administrată după intervenție chirurgicală ( terapie adjuvantă , adică pentru a reduce riscul de recurență), înainte de operație ( terapie neoadjuvantă ) sau dacă intervenția chirurgicală nu este posibilă. Începând cu 2014, există studii în curs de desfășurare pentru a evalua diferite combinații de medicamente pentru chimioterapie. [43]
Radioterapia poate fi utilizată înainte, în timpul sau după chimioterapie sau intervenție chirurgicală și uneori exclusiv pentru controlul simptomelor. La pacienții cu boală localizată, dar cu contraindicații chirurgicale, radioterapia radicală poate fi utilizată cu intenție curativă. [44]
Prognoză
În general, prognosticul este destul de rău, deoarece majoritatea pacienților prezintă boală avansată la diagnostic. Până la apariția primelor simptome (cum ar fi dificultăți la înghițire), tumora a progresat deja. Rata generală de supraviețuire pe cinci ani înregistrată în Statele Unite este de aproximativ 15%, majoritatea oamenilor murind în primul an de diagnostic. [45] Cele mai recente date de supraviețuire pentru Anglia și Țara Galilor (pacienți diagnosticați în 2007) arată că doar unul din zece pacienți va supraviețui cancerului esofagian timp de cel puțin zece ani. [46]
Notă
- ^ a b c d e f g h i j k l m n o Montgomery, EA și colab., Oesophageal Cancer , în Stewart, BW; Wild, CP (ed.), World Cancer Report 2014 , Organizația Mondială a Sănătății, 2014, pp. 528-543, ISBN 92-832-0429-8 .
- ^ a b c d Ferri, FF (editat de), Tumori esofagiene , în consilierul clinic al lui Ferri 2013 , Philadelphia, PA, Mosby (Elsevier), 2012, pp. 389–391, ISBN 978-0-323-08373-7 .
- ^ Fișele statistice SEER: Cancer esofagian , pe Institutul Național al Cancerului . Adus la 18 iunie 2014 .
- ^ a b Zhang, HZ, Jin, GF și Shen, HB,Diferențe epidemiologice în cancerul esofagian între populațiile asiatice și occidentale. , în revista chineză de cancer , vol. 31, n. 6, iunie 2012, pp. 281-6, DOI : 10.5732 / cjc.011.10390 , PMC 3777490 , PMID 22507220 .
- ^ a b c Stahl, M, Mariette, C, Haustermans, K, Cervantes, A, Arnold, D și ESMO Guidelines Working, Group, Cancer esofagian: ESMO Clinical Practice Guidelines for diagnostic, treatment and follow-up. , în Annals of oncology: jurnal oficial al Societății Europene pentru Oncologie Medicală / ESMO , 24 Suppl 6, oct 2013, pp. vi51-6, DOI : 10.1093 / annonc / mdt342 , PMID 24078662 .
- ^ editat de David Schottenfeld, Joseph F. Fraumeni, Jr.; editori asociați, Graham A. Colditz, Jonathan M. Samet, Alice S. Whittemore, Cancer epidemiology and prevent , 3rd, Oxford, Oxford University Press, 2006, p. 697, ISBN 978-0-19-974797-9 .
- ^ R Lozano, M Naghavi, K Foreman, S Lim, K Shibuya, V Aboyans, J Abraham, T Adair și R Aggarwal, Mortalitatea globală și regională din 235 cauze de deces pentru 20 de grupe de vârstă în 1990 și 2010: o analiză sistematică pentru Global Burden of Disease Study 2010 , în Lancet , vol. 380, n. 9859, 15 decembrie 2012, pp. 2095–128, DOI : 10.1016 / S0140-6736 (12) 61728-0 , PMID 23245604 .
- ^ Estimările țării OMS privind bolile și leziunile , Organizația Mondială a Sănătății , 2009. Accesat la 11 noiembrie 2009 .
- ^ Ferlay J, Shin HR, Bray F, Forman D, Mathers C și Parkin DM. GLOBOCAN 2008 v1.2, Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 10 [Internet]. Lyon, Franța: Agenția Internațională pentru Cercetarea Cancerului; 2010.
- ^ Harrison - Principiile medicinii interne - McGraw-Hill
- ^ Grupul de lucru AIRTUM - Tumori în Italia, Raport 2006. Epidemiologie și prevenire, 30 ianuarie-februarie 2006 supliment 2
- ^ a b c d și Robert J Mayer, Gastrointestinal Tract Cancer , în Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo J. (eds), principiile lui Harrison de medicină internă , vol. 1, 18, New York, McGraw-Hill Medical Publishing Division, 2008, pp. 764-5, ISBN 978-0-07-174889-6 .
- ^ Adam S Cheifetz, Alphonso Brown, Michael Curry și Alan C Moss, Oxford American Handbook of Gastroenterology and Hepatology , Oxford University Press, 2011, p. 106, ISBN 978-0-19-983012-1 .
- ^ a b c d e f g h i j Pennathur A, Gibson MK, Jobe BA, Luketich JD, carcinom esofagian, în Lancet , vol. 381, nr. 9864, februarie 2013, pp. 400-12, DOI : 10.1016 / S0140-6736 (12) 60643-6 , PMID 23374478 .
- ^ Tadataka Yamada, Manual de gastroenterologie , John Wiley & Sons, 2011, pp. 1590-1, ISBN 978-1-4443-5941-1 .
- ^ Enzinger PC, Mayer RJ, Cancer esofagian ( PDF ), în N. Engl. J. Med. , Vol. 349, n. 23, 2003, pp. 2241–52, DOI : 10.1056 / NEJMra035010 , PMID 14657432 (arhivat din original la 14 iulie 2014) .
- ^ Hans Gerdes și Mark K Ferguson, Paliația cancerului esofagian , în Posner, Mitchell C; Vokes, Everett E; Weichselbaum, Ralph R (eds), Cancer of the Upper Gastrointestinal Tract , PMPH-SUA, 2002, p. 184, ISBN 978-1-55009-101-4 .
- ^ a b P Lao-Sirieix, C Caldas și RC Fitzgerald, Predispoziție genetică la cancerul gastro-esofagian , în Opinia curentă în Genetică și dezvoltare , vol. 20, nr. 3, iunie 2010, pp. 210–7, DOI : 10.1016 / j.gde.2010.03.002 , PMID 20347291 .
- ^ Tobias JS, Hochhauser D, Cancer and its management , 6, 2013, p. 254, ISBN 1-118-71325-7 .
- ^ A Prabhu, KO Obi și JH Rubenstein, Efectele sinergice ale consumului de alcool și tutun asupra riscului de carcinom cu celule scuamoase esofagiene: o meta-analiză , în The American Journal of Gastroenterology , vol. 109, nr. 6, iunie 2014, pp. 822–7, DOI : 10.1038 / ajg.2014.71 , PMID 24751582 .
- ^ S Akhtar, masticarea nucilor de areca și riscul de carcinom cu celule scuamoase esofagiene la asiatici: o meta-analiză a studiilor caz-control , în Cauze și control al cancerului , vol. 24, n. 2, februarie 2013, pp. 257–65, DOI : 10.1007 / s10552-012-0113-9 , PMID 23224324 .
- ^ a b Rutegård M, Lagergren P, Nordenstedt H, Lagergren J, Oesophageal adenocarcinoma: the new epidemic in men? , in Maturitas , vol. 69, n. 3, luglio 2011, pp. 244–8, DOI :10.1016/j.maturitas.2011.04.003 , PMID 21602001 .
- ^ Merry AH, Schouten LJ, Goldbohm RA, van den Brandt PA, Body Mass Index, height and risk of adenocarcinoma of the oesophagus and gastric cardia: a prospective cohort study , 2007, DOI : 10.1136/gut.2006.116665 , PMID 17337464 .
- ^ a b c d e f PJ de Jonge, M van Blankenstein, WM Grady e EJ Kuipers, Barrett's oesophagus: epidemiology, cancer risk and implications for management , in Gut , vol. 63, n. 1, gennaio 2014, pp. 191–202, DOI : 10.1136/gutjnl-2013-305490 , PMID 24092861 .
- ^ Lagergren J, Bergström R, Lindgren A, Nyrén O, Symptomatic gastroesophageal reflux as a risk factor for esophageal adenocarcinoma , in N. Engl. J. Med. , vol. 340, n. 11, 1999, pp. 825-31, PMID 10080844 .
- ^ Turati F, Tramacere I, La Vecchia C, Negri E, A meta-analysis of body mass index and esophageal and gastric cardia adenocarcinoma , in Annals of Oncology , vol. 24, n. 3, marzo 2013, pp. 609–17, DOI : 10.1093/annonc/mds244 , PMID 22898040 .
- ^ a b c d J Lagergren e P Lagergren, Recent developments in esophageal adenocarcinoma , in CA: a Cancer Journal for Clinicians , vol. 63, n. 4, 2013, pp. 232–48, DOI : 10.3322/caac.21185 , PMID 23818335 .
- ^ a b GW Falk, Risk factors for esophageal cancer development ( PDF ), in Surgical Oncology Clinics of North America , vol. 18, n. 3, luglio 2009, pp. 469–85, DOI : 10.1016/j.soc.2009.03.005 , PMID 19500737 .
- ^ Randall E Harris, Epidemiology of Esophageal Cancer , in Epidemiology of Chronic Disease: Global Perspectives , Burlington, MA, Jones & Bartlett Publishers, 2013, pp. 157–161, ISBN 978-0-7637-8047-0 .
- ^ Priante AV, Castilho EC, Kowalski LP, Second primary tumors in patients with head and neck cancer , in Current Oncology Reports , vol. 13, n. 2, aprile 2011, pp. 132–7, DOI : 10.1007/s11912-010-0147-7 , PMID 21234721 .
- ^ ( DE ) Scherübl H, Steinberg J, Schwertner C, Mir-Salim P, Stölzel U, de Villiers EM, 'Field cancerization' im oberen Aerodigestivtrakt [ Coincidental squamous cell cancers of the esophagus, head, and neck: risk and screening ] , in HNO , vol. 56, n. 6, giugno 2008, pp. 603–8, DOI : 10.1007/s00106-007-1616-7 , PMID 17928979 .
- ^ Tylosis with esophageal cancer , su rarediseases.info.nih.gov , Genetic and Rare Diseases Information Center (GARD) – NIH, 18 gennaio 2013. URL consultato il 16 agosto 2014 .
- ^ a b O Nyrén e HO Adami, Esophageal Cancer , in Adami, HO; Hunter DJ; Trichopoulos D (a cura di), Textbook of Cancer Epidemiology , Volume 1, Oxford University Press, 2008, p. 224, ISBN 978-0-19-531117-4 .
- ^ Syrjänen KJ, HPV infections and oesophageal cancer , in J. Clin. Pathol. , vol. 55, n. 10, 2002, pp. 721–8, PMID 12354793 . PMC 1769774
- ^ Liyanage SS, Rahman B, Ridda I, Newall AT, Tabrizi SN, Garland SM, Segelov E, Seale H, Crowe PJ, Moa A, Macintyre CR, The aetiological role of human papillomavirus in oesophageal squamous cell carcinoma: a meta-analysis , in Plos One , vol. 8, n. 7, 2013, pp. e69238, DOI : 10.1371/journal.pone.0069238 , PMC 3722293 , PMID 23894436 .
- ^ a b Jeffrey S. Tobias e Daniel Hochhauser, Cancer and its Management , 6th, 2010, p. 257, ISBN 1-118-71325-7 .
- ^ Berry , p. S292
- ^ a b c d e f g Ch 79, "Treatment" , in DeVita, Hellman, and Rosenberg's Cancer: Cancer: Principles & Practice of Oncology , 9th, Lippincott Williams & Wilkins, 2011, ISBN 978-1-4511-0545-2 . Online edition, with updates to 2014
- ^ MF Berry, Esophageal cancer: staging system and guidelines for staging and treatment. , in Journal of thoracic disease , vol. 6, Suppl 3, maggio 2014, pp. S289–97, PMID 24876933 .
- ^ Parameswaran R, McNair A, Avery KN, Berrisford RG, Wajed SA, Sprangers MA, Blazeby JM, The role of health-related quality of life outcomes in clinical decision making in surgery for esophageal cancer: a systematic review , in Annals of Surgical Oncology , vol. 15, n. 9, settembre 2008, pp. 2372–9, DOI : 10.1245/s10434-008-0042-8 , PMID 18626719 .
- ^ Wang KK, Prasad G, Tian J,Endoscopic mucosal resection and endoscopic submucosal dissection in esophageal and gastric cancers , in Curr. Opin. Gastroenterol. , vol. 26, n. 5, settembre 2010, pp. 453–8, DOI : 10.1097/MOG.0b013e32833e4712 , PMC 3215503 , PMID 20703112 .
- ^ Ross P, Nicolson M, Cunningham D, et al., Prospective randomized trial comparing mitomycin, cisplatin, and protracted venous-infusion fluorouracil (PVI 5-FU) With epirubicin, cisplatin, and PVI 5-FU in advanced esophagogastric cancer , in Journal of clinical oncology , vol. 20, n. 8, aprile 2002, pp. 1996–2004, DOI : 10.1200/JCO.2002.08.105 , PMID 11956258 .
- ^ Yamasaki M, Miyata H, Miyazaki Y, et al. , Perioperative therapy for esophageal cancer , in Gen Thorac Cardiovasc Surg , vol. 62, n. 9, settembre 2014, pp. 531–40, DOI : 10.1007/s11748-014-0458-y , PMID 25065567 .
- ^ Dai Y, Li C, Xie Y, et al. , Interventions for dysphagia in oesophageal cancer , in Cochrane Database Syst Rev , vol. 10, 2014, pp. CD005048, DOI : 10.1002/14651858.CD005048.pub4 , PMID 25354795 .
- ^ Polednak AP, Trends in survival for both histologic types of esophageal cancer in US surveillance, epidemiology and end results areas , in Int. J. Cancer , vol. 105, n. 1, maggio 2003, pp. 98–100, DOI : 10.1002/ijc.11029 , PMID 12672037 .
- ^ Cancer Research UK , http://www.cancerresearchuk.org/cancer-info/cancerstats/types/oesophagus/survival/ .
Bibliografia
- Joseph C. Segen,Concise Dictionary of Modern Medicine , New York, McGraw-Hill, 2006, ISBN 978-88-386-3917-3 .
- Douglas M. Anderson, A. Elliot Michelle, Mosby's medical, nursing, & Allied Health Dictionary sesta edizione , New York, Piccin, 2004, ISBN 88-299-1716-8 .
- Anacleto Peracchia, Okolicsanyi Lajos, Roncoroni Luigi, Malattie dell'apparato gastrointestinale, 3ª edizione , Milano, McGraw-Hill, 2004, ISBN 88-386-2386-4 .
Voci correlate
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su carcinoma dell'esofago
Wikimedia Commons contiene immagini o altri file su carcinoma dell'esofago
Collegamenti esterni
- ( EN ) Informazioni sul tumore , su mayoclinic.org .
- ( EN ) Sito MedlinePlus , su nlm.nih.gov .
- ( EN ) Sito GLOBOCAN , su globocan.iarc.fr .
- Sito AIRTUM , su registri-tumori.it .
- Informazioni sui tumori dell'esofago , su centroesofagopadova.org .
| Controllo di autorità | LCCN ( EN ) sh85044858 · GND ( DE ) 4132808-5 · NDL ( EN , JA ) 00572161 |
|---|