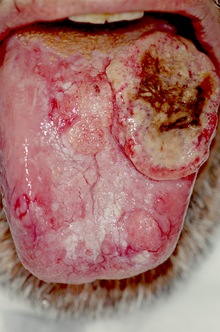
Cancer la gură
| Cancer la gură | |
|---|---|
 Imagine histologică a unui carcinom scuamos bine diferențiat în gură, colorare hematoxilină-eozină | |
| Tip | Malign |
| Celula de origine | Epiteliul oral |
| Factori de risc | · Fumatul · Alcool · Alimentare · Imunodeficiență |
| Incidenţă | 4,0 / 100 000 (global) 3,1 / 100 000 (Italia) |
| Vârsta medie la diagnostic | peste 50 de ani |
| Raportul M: F | 2: 1 |
| Clasificare și resurse externe | |
| ICD - 9 -CM | ( EN ) 140 - 146 |
| ICD - 10 | ( RO ) C00 - C06 |
Termenul de carcinom al gurii sau carcinom oral se referă la setul de neoplasme maligne care provin din țesuturile epiteliale care acoperă cavitatea bucală . Prin urmare, neoplasmele benigne ( papiloame , lipoame , angioame ) și neoplasmele maligne de origine neepitelială ( melanoame , tumori ale glandei salivare, sarcoame ) care pot apărea uneori în cavitatea bucală, nu intră în această categorie. La fel, formularele secundare nu sunt incluse.
Cancerul oral reprezintă mai mult de 90% din toate tumorile maligne ale gurii [1] . Afectează mai frecvent vârsta de peste cincizeci de ani și bărbații într-o măsură mai mare decât femeile, într-un raport de aproximativ 2: 1. Principalii factori de risc sunt fumatul și abuzul de alcool [2] . De departe cel mai frecvent tip histologic este carcinomul cu celule scuamoase sau celulele scuamoase.
În etapele inițiale, aspectul este o leziune superficială mică de culoare roșie sau albă ( eritroplakie sau leucoplakie ) sau o ulcerație care nu tinde să se vindece spontan. Uneori poate avea aspectul unei leziuni infiltrative nodulare, sub forma unei îngroșări mai mult sau mai puțin regulate detectate pe margini, care tinde să se ulcereze superficial, dar o formă de creștere exofitică sau papilară nu este neobișnuită. În unele cazuri, poate prezenta mai mult de unul dintre aceste aspecte în același timp. Tendința predominantă este de creștere locală invazivă, cu implicare rapidă a ganglionilor limfatici , dar frecvență scăzută a metastazelor la distanță .
Cele mai frecvente simptome sunt senzația de consistență crescută a mucoasei afectate, ulterior durerea , inițial sub formă de arsură ușoară, dar înrăutățită, care în timp poate fi însoțită de umflarea ganglionilor limfatici , dificultăți de înghițire și dificultăți de vorbire . Principalul test de diagnostic este biopsia .
Terapia pentru acest tip de tumoare implică utilizarea unei intervenții chirurgicale sau radioterapice , în funcție de loc, în timp ce în leziunile mai avansate cele două tehnici sunt utilizate în combinație, uneori cu chimioterapie de susținere. Prognosticul este în medie bun, dar depinde în mare măsură de amploarea bolii în momentul diagnosticului , astfel încât diagnosticarea precoce este esențială.
Epidemiologie
Cancerul oral și de buze ocupă locul al cincisprezecelea la nivel mondial ca o incidență relativă a tuturor tipurilor de cancer (2,1% din toate tipurile de cancer), cu o cifră (standardizată în funcție de vârstă) de 4,0 cazuri noi pe an la 100 000 de locuitori, valori care diferă semnificativ între bărbați și femei , pentru un raport orientativ de aproximativ 2: 1. De fapt, atinge locul al unsprezecelea în rândul bărbaților cu o valoare de 5,5 cazuri la 100.000 de locuitori (2,7% din totalul neoplasmelor) și al șaptesprezecelea în rândul femeilor (2,5 cazuri la 100.000, 1,5%). Rata mortalității este de 1,9 decese la 100.000 de locuitori și chiar și în acest caz bărbații depășesc numărul femeilor cu un factor de aproximativ 2: 1 (2,7 față de 1,2 decese la 100.000 de locuitori) [3] . În comparație cu datele anchetelor anterioare (2002), este posibil să se observe o ușoară scădere atât a incidenței, cât și a datelor privind mortalitatea, la ambele sexe [4] .
Distribuția globală a acestei patologii variază considerabil atât în ceea ce privește valorile absolute, cât și cele relative, cu un vârf în unele țări din Asia de Sud și din Europa Central-Estică [5] , legat de difuzarea pe scară largă a comportamentelor de risc precum fumatul, abuzul de alcool și mestecarea paan (betel), ajungând pe locul trei în India ca incidență relativă printre toate neoplasmele [6] . Cele mai puțin răspândite țări sunt cele din Africa și America de Sud [7] .
În Italia, cancerul oral și al buzelor are o incidență medie de 3,1 cazuri noi pe an la 100 000 de locuitori (standardizat în funcție de vârstă), ceea ce îl plasează pe locul douăzeci dintre toate neoplasmele din Italia [8] . Împărțind datele după sex, există 4,1 cazuri noi la 100.000 de locuitori bărbați pe an [9] și 2,1 la femei [10] , cu un raport între cele două sexe de puțin sub 2: 1. Rata anuală a mortalității este de 1,1 persoane la 100.000 de locuitori [11] , de aproape trei ori mai mare la bărbați (1,5) [12] decât la femei (0,6) [13] . Analizând datele din anii trecuți (perioada 1986-1997), este posibil să se observe o tendință spre o apropiere treptată a datelor de incidență și mortalitate între bărbați și femei [14] .
Datele epidemiologice arată clar legătura acestui neoplasm cu vârsta în creștere, ceea ce duce la o incidență care, pornind de la cifra (globală) de 0,1 cazuri la 100.000 de locuitori din grupa de vârstă 0-14 ani, crește treptat până la atingerea nivelului maxim de 23,4 în grupa de vârstă peste 75 de ani [15] .
Etiologie
Unii factori de risc s-au dovedit a fi deosebit de semnificativi pentru această formă de neoplasm [16] [17] . Dintre acestea, utilizarea tutunului este deosebit de importantă, atât în formele care implică arderea și mestecarea, cât și abuzul de alcool , care reprezintă aproximativ trei sferturi din toate cazurile de cancer oral în țările în care aceste obiceiuri reprezintă principala sursă de risc [ 1] [18] . În țările din Orientul Mijlociu și în Asia de Sud, obiceiul larg răspândit de a mesteca voluptuos anumite amestecuri de legume (paan și qāt) pare să implice, de asemenea, niveluri foarte ridicate de risc. Alți factori care ar putea fi corelați cu creșterea incidenței tumorilor orale sunt infecțiile virale HPV, unii factori legați de obiceiurile de dietă și igienă, situațiile de imunodeficiență atât dobândită, cât și congenitală și prezența unor patologii care par a fi promotori ai neoplaziei. , din acest motiv clasificat de OMS drept condiții precanceroase. Familiarizarea a fost, de asemenea, pusă sub semnul întrebării de unele studii ca posibil factor de risc [19] .
Tutun

Legătura dintre fumat , în diferitele sale forme, și cancerul oral a fost bine cunoscută de ceva timp și s-a demonstrat prin numeroase studii epidemiologice [20] . Fumatul în special este considerat prima cauză a cancerului oral vreodată, iar reconcilierea treptată a incidenței și a mortalității între cele două sexe pare să fie legată tocmai de răspândirea acestui obicei și la femei, unde pare capabil să se dezvăluie chiar mai dăunătoare decât în rândul bărbaților [21] . Obiceiul fumatului de țigări , mai puțin corelat cu tumorile căilor respiratorii și plămânilor inferiori decât țigările, deoarece este însoțit de o inhalare mai mică de fum, pare să implice în schimb un risc mai mare pentru căile respiratorii superioare , în primul rând cavitatea bucală. , tocmai datorită obiceiului de a reține mai mult fum în gură. Nivelurile de risc detectate sunt de șapte până la zece ori mai mari decât la nefumători și sunt legate de numărul de trabucuri fumate și de nivelul de inhalare a fumului [22] [23] . Probleme similare sunt legate de utilizarea conductei [24] . Utilizarea la unele populații (predominant la femei) a fumatului cu partea aprinsă din gură a fost la rândul ei corelată cu o incidență mai mare a bolilor orale, care pare să implice și căldura ca factor de risc [25] [26] . Utilizarea tutunului pentru mestecat a fost de asemenea raportată de ceva timp în legătură cu o creștere a riscului de cancer oral [27] , conform unor studii într-un mod la fel de semnificativ în comparație cu modalitățile care implică arderea acestuia, sau chiar mai mare [28] [29] .
Alcoolism
Corelația dintre consumul de alcool și cancerul oral este documentată de numeroase studii, atât singure, cât și în legătură cu fumatul, două obiceiuri care, de obicei, tind să se însoțească reciproc, fapt care se dovedește a fi capabil să sporească foarte mult acțiunea de promovare a cancerului. [28 ] [30] . Legătura dintre abuzul de alcool și diferitele tipuri de cancer este cunoscută de ceva timp, atât de mult încât băuturile alcoolice sunt incluse de IARC în prima clasă de risc, chiar dacă modalitățile în care se dezvoltă efectul oncogen nu au fost încă pe deplin clarificate. ., deoarece etanolul nu s-a dovedit a avea acțiune mutagenă directă . Au fost propuse diferite efecte directe sau indirecte care pot explica mecanismele prin care se produce această acțiune [31] . Cu toate acestea, studii recente par să limiteze importanța acțiunii directe în cazul cancerului oral, susținând în schimb o acțiune potențială aproape exclusivă în asociere cu fumatul [32] [33] . Legătura dintre neoplasmele orale și apele de gură care conțin alcool nu a fost confirmată [34] [35] .
Paan (Betel) și qāt

A rezultat obiceiul foarte comun în țările asiatice de a mesteca paan (mai cunoscut de noi sub numele uneia dintre componente, betel), un amestec vegetal care conține unele molecule aparținând clasei de alcaloizi cu efect comparabil cu cel al nicotinei . să fie puternic corelată cu incidența mare a acestei tumori în regiunile sud-estice [36] . Paan este preparat în mod tradițional amestecând nuca de areca și frunzele betelului ( Piper betel ), o bază care în diferitele regiuni prezintă numeroase variații [37] [38] , inclusiv adăugarea tutunului, obicei care pare capabil să se amplifice în special acțiunea cancerigenă, precum și asocierea cu alte surse de risc [39] .
Chiar și obiceiul larg răspândit în unele țări arabe de a mesteca frunze qāt , conținând o substanță alcaloidă cu efect euforic similar cu cel al amfetaminelor , a fost legat de prezența neoplasmelor orale [40] .
HPV
Asocierea dintre papilomavirus (HPV) și carcinom este bine cunoscută pentru zonele genitale ( cancer de col uterin ), în special în ceea ce privește unele tulpini specifice (16, 18), capabile să producă proteine cu efect de promovare a tumorii, efecte în produc schimbări chiar și pe termen lung. Un rol similar al HPV în raport cu tumorile orofaringelui pare acum suficient demonstrat [41] [42] , în timp ce studiile recente par să reducă considerabil implicarea la debutul oral [43] [44] .
Dietă
Legătura dintre cancerul oral și obiceiurile alimentare s-a dovedit deosebit de semnificativă în ceea ce privește unele tipuri de alimente, în analogie cu ceea ce s-a găsit pentru alte tipuri de cancer ale sistemului digestiv . În special, mai multe studii au evidențiat rolul fructelor și legumelor proaspete ca alimente capabile să contracareze apariția bolii [45] [46] , precum și un rol protector legat de consumul regulat de cafea [47] [48] . Consumul de carne procesată sa dovedit a fi un factor de risc semnificativ [49] , în timp ce consumul de alimente bogate în fibre nu sa dovedit a fi deosebit de important [50] .
Imunodeficiență
Se cunoaște rolul scăderii activității sistemului imunitar în promovarea cancerului. Chiar și în gură, unele afecțiuni care pot slăbi capacitățile normale ale sistemului imunitar al organismului par a fi corelate semnificativ cu un risc crescut de cancer. Acest lucru a fost observat în legătură cu terapiile anti- respingere [51] , boala grefă versus gazdă și bolile imunosupresoare precum SIDA și se crede că chiar și în cazul HPV, limfoepiteliomul legat de virusul Epstein -Barr și unele patologii congenitale care interferează cu buna funcționare a sistemului imunitar (vezi mai jos condițiile precanceroase), mecanismul imunosupresor este unul dintre principalii factori ai promovării oncogene. Acest lucru ar putea fi confirmat de corelația găsită între nivelul substanțelor imunosupresoare și progresia neoplazică la subiecții bolnavi [52] .
Igiena orală și patologiile dentare
Asocierea dintre o igienă orală deficitară sau prezența stimulilor iritativi (proteze incongruente sau leziuni carioase și patologie parodontală ) și cancerul oral este frecvent observată clinic [53] . Prezența frecventă simultană a sănătății orale și a obiceiurilor slabe, cum ar fi fumatul și alcoolismul, implicate la rândul lor în procesul de promovare a tumorii, au făcut totuși foarte dificilă stabilirea unei corelații sigure pe baze statistice. Cu toate acestea, studii recente par să susțină ipoteza unei asocieri între carcinom și boala parodontală [54] [55] .
Condiții precanceroase
Unele condiții patologice au fost corelate semnificativ cu dezvoltarea cancerului oral. Potrivit OMS, bolile cu cel mai mare risc sunt: lichen plan oral, în special în forma sa erozivă, fibroză submucoasă orală , lupus eritematos sistemic , xeroderma pigmentară , disfagie cu deficit de fier sau sindrom Plummer-Vinson , epidermoliză buloasă și discheratoză congenită [56]. ] . În prezența acestor patologii, se recomandă o evaluare periodică a stării de sănătate a mucoasei bucale.
Patogenie
La fel ca în majoritatea cazurilor de cancer, procesul patogenetic care duce la dezvoltarea neoplasmului ( carcinogeneza ) nu este încă pe deplin înțeles. Teoria care găsește în prezent cel mai mult credit este cea cu mai multe etape, care prevede o acumulare treptată de alterări capabile să acționeze asupra mecanismelor care mențin echilibrul celulelor ( homeostazie ), provocând ca efect final o proliferare incontrolabilă și, în cazul a formelor maligne, acțiunea agresivă față de țesuturile înconjurătoare, ale căror celule pot fi la rândul lor implicate în procesul patologic [57] . Începutul transformării ar fi expunerea la un factor promotor capabil să modifice structura cromozomială a unei singure celule, atât acționând la nivel structural, cât și modificându-i expresia [58] . În general, există multe gene care, atunci când sunt activate ( oncogene ) sau blocate în funcția lor obișnuită de protecție ( gene supresoare tumorale ), pot împinge o celulă spre transformarea neoplazică. În cazul neoplasmelor orale, au fost identificate numeroase anomalii genetice recurente [59] [60] , în special ștergerea unor regiuni specifice ale anumitor cromozomi , modificări ale secvențelor care afectează expresia proteinei p53 , a unor cicline și a CKD înrudită enzime, K-Ras , Notch [61] și numeroase alte oncogene și supresoare tumorale [62] [63] [64] . Unii mediatori implicați în procesele de angiogeneză , un mecanism esențial în creșterea tumorii, par, de asemenea, să joace un rol important [65] .
Leziuni precanceroase
Conform modelului care prezice o progresie treptată către patologia neoplazică, există unele condiții ale mucoasei bucale care au fost corelate semnificativ cu o evoluție de acest tip și, prin urmare, se recomandă monitorizarea în scopul interceptării sale timpurii. Conform unor studii, aproximativ 70% din cancerele orale se dezvoltă din aceste condiții predispozante [66] . Potrivit OMS, cheilita actinică , leucoplakia și eritroplakia pot fi considerate leziuni precanceroase, distingându-le de condițiile precanceroase, deoarece, spre deosebire de acestea din urmă, sunt leziuni localizate în zonele orale și au condus în mod specific la dezvoltarea patologiei neoplazice în acest sediu [56] . Monitorizarea progresiei către tabloul neoplazic necesită examinarea biopsiei , în căutarea modificărilor histologice și citologice capabile să prezică sau nu această apariție. În acest sens, a fost propusă și uneori utilizată o clasificare care măsoară gradul de displazie observabilă (OED) și, prin urmare, nivelul de pericol potențial. Carcinomul in situ , în care gradul de displazie atinge cel mai înalt grad, dar fără ca atipia să fi depășit membrana bazală , este considerat ca etapa de frontieră între leziunea precanceroasă și neoplazia adevărată. Predictivitatea limitată arătată prin această metodă [67] și dificultatea de a obține uniformitatea rezultatelor [68] au condus totuși la căutarea unor indicatori mai specifici, bazate pe investigații cromozomiale sau markeri genetici specifici [69] , cu rezultate promițătoare, dar nu încă suficient de fiabil [70] .
Cheilita actinică este o formă de hiperkeratoză a epiteliului porțiunii exterioare a buzelor și apare ca o pată ridicată de culoare variabilă, mai frecvent pe buza inferioară și este strâns legată de expunerea la soare.
Termenul de leucoplazie sau leucoplasie se referă la o leziune de culoare deschisă prezentă pe suprafața membranelor mucoase care nu poate fi corelată cu alte patologii [71] . Prin urmare, este o entitate clinică, nu ușor de identificat cu precizie, care poate include diferite entități patologice în conformitate cu autorii și care a văzut schimbarea criteriilor de definiție de-a lungul timpului [72] . De asemenea, din punct de vedere histopatologic, aspectele pot varia foarte mult, cu o prevalență a imaginii hiperkeratozei , asociată cu diferite niveluri de displazie [73] . Leziunea poate fi uniformă sau alternată cu zone erozive care indică un pericol mai mare de evoluție malignă (eritroleucoplacie), cu o variantă numită leucoplacie verucoasă, considerată la rândul ei cu un risc ridicat de transformare neoplazică [74] . Cauzele apariției pot fi multe, printre care cele mai frecvente sunt fumatul și unele obiceiuri proaste. De obicei asimptomatic, prevede terapia chirurgicală numai în formele cu cel mai mare risc, în special în cazul unui aspect neomogen, în timp ce în cele mai frecvente forme este prevăzută monitorizarea, și eventual biopsia periodică, pentru a evalua gradul de displazie atins. Cu toate acestea, eficacitatea acestor abordări pentru prevenirea dezvoltării unei forme maligne pare a fi discutabilă [75] .
Eritroplakia sau eritroplazia este definită ca o leziune eritematoasă roșie care nu are legătură cu alte patologii [73] . De obicei de dimensiuni mici, apare de obicei în zone cu un nivel mai scăzut de keratinizare; poate prezenta aspecte de omogenitate mai mare sau mai mică și este adesea legată de obiceiuri proaste, cum ar fi fumatul și alcoolismul. Prezintă cel mai mare risc de transformare neoplazică, atât de mult încât este considerată leziunea predispozantă prin excelență [76] .
Anatomie patologică
Clasificare histologică
Diferitele tipuri de carcinoame se disting printr-o clasificare bazată pe recunoașterea histologică. În conformitate cu OMS [77] , următoarele histotipuri sunt clasificate ca neoplasme maligne orale de origine epitelială :
- Carcinom cu celule scuamoase sau scuamoase
- Carcinom scuamos verucos sau verucos
- Carcinom scuamos bazaloid
- Carcinom scuamos papilar
- Carcinom cu celule scuamoase cu fus
- Carcinom acantolitic cu celule scuamoase
- Carcinomul adenocvamos
- Carcinom cuniculatum
- Limfoepiteliom
Dacă tumorile orale includ și cele ale porțiunii externe a buzelor, este, de asemenea, necesar să se includă carcinomul bazocelular , un neoplasm în special legat de expunerea la soare, care este, prin urmare, practic inexistent în localizarea intraorală.
Carcinom cu celule scuamoase
Este de departe cel mai frecvent tip, contribuind în formele sale mai mult sau mai puțin diferențiate la 90% din toate cazurile de carcinom oral [78] . Histologic în primele etape se caracterizează prin proliferarea celulelor epiteliale , de formă poligonală, dispuse în cuiburi sau extensii care se proiectează dincolo de membrana bazală . Sunt observabile diferite grade de transformare, cu prezența keratinizării mai mult sau mai puțin marcate, nuclee de formă neregulată, alungite și hipercromatice. Celulele se pot uni uneori pentru a forma perle de cornee sau celule gigantice multi-nucleare și se pot recunoaște punți intercelulare ( desmosomi ), asemănătoare cu aspectul spinilor, de unde și denumirea pe scară largă a carcinomului cu celule scuamoase. În formele mai puțin diferențiate, polimorfismul celular crește, până la a nu mai permite recunoașterea caracterelor definibile ale celulei epiteliale de pornire, precum și numărul mitozelor observabile, aspectele keratinizării anormale și punțile intercelulare. dispărea. Frecvent diferitele aspecte pot coexista, ceea ce face dificilă clasificarea diferitelor grade de diferențiere. Invazia țesutului conjunctiv implică reorganizarea sa treptată sub forma unei strome capabile să susțină creșterea neoplazică [79] . Prezența infiltratului limfocitar este frecventă și într-o formă organizată și pare a fi asociată cu un prognostic mai favorabil [80] . Leziunea neoplazică tinde de obicei spre agresivitate locală, cu invazia rapidă a structurilor înconjurătoare, atât a țesuturilor moi, cât și a țesuturilor osoase, și a metastazelor către ganglionii limfatici de referință. Pe de altă parte, metastazele îndepărtate de sânge sunt rare.
Carcinom scuamos verucos
O variantă a carcinomului cu celule scuamoase, este al doilea tip cel mai frecvent și se caracterizează prin celule bine diferențiate, câteva perle excitate și mitoză redusă și o tendință scăzută de a trece prin membrana bazală , un comportament care uneori poate face diagnostic prin biopsie complicată.lăsând îndoiala unei leziuni precanceroase sau benigne simple. Cu toate acestea, depășirea membranei bazale este însoțită de o reacție inflamatorie intensă a straturilor submucoase inferioare. Denumirea neoplasmului se datorează apariției macroscopice a unei leziuni exofitice papilo-verucoase, cu o suprafață foarte neregulată și consistentă, rar ulcerată și se caracterizează printr-o tendință scăzută de metastazare și, prin urmare, un prognostic favorabil. Localizarea tipică este pe mucoasa bucală și pe gingii . Având în vedere apariția leziunilor, a fost sugerată o legătură cu HPV, dar acest lucru nu a fost încă confirmat [81] .
Carcinom bazaloid
Formă rară și agresivă, tipică podelei orale, dar care poate afecta și zona orofaringiană . Histologic se remarcă prin prezența simultană a celulelor tipice carcinomului scuamos, uneori cu aspecte de keratinizare, amestecate cu structurile de cuib caracteristice carcinomului bazocelular , cu celule de dimensiuni mici, dar cu nuclei voluminoși, și uneori prezența perifericului tipic dispunerea palisadei celulelor [82] . Prognosticul nu pare să difere de cel al carcinomului scuamos [83] .
Carcinom scuamos papilar
Varianta de carcinom scuamos care prezintă macroscopic aspect tipic exofit-papilar, tendință moderată a celulelor neoplazice de a depăși stratul bazal și prognostic favorabil, chiar dacă are o tendință marcată de recidivă .
Carcinom cu celule fusiforme
De asemenea, numit carcinom sarcomatoid sau pseudosarcom, deoarece aspectul histologic simulează cel al sarcomului adevărat, datorită prezenței celulelor alungite care alcătuiesc corpul principal al tumorii, într-o imagine care prezintă totuși aspecte ale amestecului cu celulele tipice ale carcinomului solzos , amestecat cu atipii celulare, ceea ce face ca identificarea să nu fie ușoară [84] . Aspectul macroscopic este adesea al unei leziuni polipoide exofitice care tinde să se ulcereze. Comportamentul nu este deosebit de agresiv, dar cu variații notabile. Cu toate acestea, metastazele la distanță nu sunt frecvente.
Carcinomul adenocvamos
Variantă foarte rară care combină aspectele carcinomului scuamos cu cele tipice adenocarcinomului , cu agresivitate ridicată și prognostic sever [85] .
Limfoepiteliom
De asemenea, numit carcinom limfoepitelial Epstein-Barr, datorită asocierii frecvente cu virusul Epstein-Barr , este o formă rară de carcinom (deci de origine epitelială, în ciuda numelui), în care aspectele histologice ale grupurilor de celule poligonale sau nediferențiate cu nucleele foarte cromatice sunt asociate cu o prezență masivă a infiltrării limfocitare . Macroscopic apare ca o masă infiltrantă care tinde spre invazie în profunzime, mai degrabă decât spre suprafață și este localizată de obicei în zonele în care țesutul limfatic este cel mai prezent sau în structurile care alcătuiesc inelul Waldeyer , deci la granița dintre cavitatea bucală și orofaringe .
Profil clinic
Semnele și simptomele cancerului la gură în stadiile incipiente pot fi foarte ușoare, dacă nu chiar absente. Leziunea din etapele inițiale se poate prezenta ca o mică ulcerație care nu tinde spre vindecare spontană sau poate evolua dintr-o leziune de tip eritroplastic sau leucoplasic , iar singurul simptom poate fi o ușoară arsură sau durere la stimulul mecanic. Uneori, un aspect exofit-papilar sau polipoid , sau infiltrativ-nodular, de consistență dură și cu margini ușor ridicate, poate avea deja un aspect de la început. În acest caz, simptomul va fi cel al senzației de variație a consistenței sau prezenței masei solide. În unele cazuri, diferitele aspecte pot coexista sau pot apărea în diferite zone (leziuni sincrone). Simptomul dureros poate apărea destul de târziu și într-o formă ușoară și intermitentă, sau sub formă de arsură , și apoi se poate agrava, ajungând la niveluri extrem de ridicate. În raport cu aceasta și datorită implicării mușchilor linguali, pot exista disfagii , dificultăți și / sau dureri la vorbire și, uneori, sângerări spontane sau cauzate de traume. În cazul extinderii la raioanele orofaringiene și nazofaringiene ar putea exista dureri ale urechii și în cele mai grave cazuri poate duce la dificultăți de respirație . Alte simptome legate de extensia locală, dacă există invazia structurilor osoase, vor fi mobilitatea și pierderea ulterioară a dinților din cauza distrugerii țesuturilor de susținere și parestezia sau anestezia nervilor prin compresie, în special nervul alveolar inferior, în caz de invazie a canalului în care rulează.
Implicarea ganglionilor limfatici , vizibilă ca umflarea ganglionilor limfatici , afectează aproximativ 40% dintre pacienții cu cancer oral în momentul diagnosticului [86] și poate fi precoce în unele cazuri și nu de puține ori poate fi primul simptom al patologiei neoplazice. . Cu toate acestea, acest simptom nu va fi neapărat legat întotdeauna de metastază, deoarece uneori este reacția specifică la prezența neoplasmului în locul original. I linfonodi interessati dipendono dalla sede di insorgenza della lesione, venendo solitamente colpiti per primi i tributari, che raccolgono il drenaggio linfatico dalla sede di partenza. Nel caso di localizzazione anteriore (labbra, pavimento anteriore della bocca e porzione anteriore della lingua) i linfonodi coinvolti in via primaria sono i sottomentali e sottomandibolari, mentre nelle zone orali posteriori ( palato , trigoni retromolari) possono essere coinvolti i linfonodi periauricolari e parotidei. Successivamente vengono interessati i distretti cervicali inferiori, in successione, ma sono comunque possibili salti di stazioni linfonodali, o localizzazioni controlaterali, soprattutto nel caso di neoplasie poste vicino alla linea mediana.
La disseminazione a distanza per via ematica è invece meno frequente e di solito tardiva, quindi solitamente correlata ad una stadiazione del tumore originario già molto avanzata. L'organo più comunemente coinvolto è il polmone [1] .
Profilo diagnostico
Esami di laboratorio e strumentali
L'esame obiettivo può solo individuare la presenza di uno stato di alterazione della normale struttura delle mucose, prestandosi ad un variabilità interpretativa eccessiva [87] , ei sistemi diagnostici a bassa invasività finora proposti non sembrano a loro volta aver ancora raggiunto un livello di efficacia soddisfacente [88] [89] [90] .

Ad oggi quindi il prelievo tramite biopsia viene ancora considerato il gold standard [91] [92] , permettendo tramite l'esame istologico del campione raccolto la determinazione delle modificazioni cellulari (citologia) e dell'alterazione della morfologia tissutale (istologia) tipiche della patologia neoplastica. In particolare trova maggiore indicazione la tecnica incisionale, a meno di trovarsi di fronte a lesioni di piccole dimensioni, ben delimitate. La biopsia escissionale, infatti, nel caso frequente di lesioni infiltranti comporta il facile rischio di non comprendere totalmente la lesione neoplastica, aumentando nel caso di conferma della presenza di malignità il pericolo di disseminazione e una maggiore difficoltà nell'identificare i margini della lesione nel successivo intervento chirurgico. Il prelievo bioptico deve comprendere anche una parte di tessuto sano, e nel caso di lesioni di aspetto ampio e non uniforme, è consigliabile un prelievo multiplo, per non incorrere in falsi negativi. L'uso di una tecnica di colorazione vitale , ad esempio con il blu di toluidina, proposto a suo tempo come metodica diagnostica ma rivelatosi poco adatto allo scopo, può in alcuni casi aiutare a definire meglio i limiti del prelievo, particolarmente nel caso di lesioni in cui predomina l'aspetto atrofico su quello ipercheratosico.

L'uso della diagnostica per immagini nel caso dei carcinomi orali non risulta utile per la diagnosi primaria, ma è fondamentale per determinarne la stadiazione, monitorando il livello di progressione locale ea distanza, per stabilire l'efficacia delle terapie, e per escludere la comparsa di nuove manifestazioni della patologia nel tempo. La semplice indagine radiografica bidimensionale ha valore molto limitato. L'uso della tomografia computerizzata (CT) ottiene migliori risultati, anche grazie alle nuove tecnologie di ricostruzione tridimensionale, ma non permette una buona visualizzazione dei tessuti molli, a meno di usare mezzi di contrasto specifici. La Risonanza Magnetica (RMN) permette una miglior visuale dei tessuti molli, avendo raggiunto nella sua ultima versione ( DWI ) un buon livello di risoluzione [93] . La tomografia a emissione di positroni o PET è l'esame principale per la determinazione di eventuale disseminazione metastatica, usando allo scopo dei radiotraccianti , principalmente il fluorodesossiglucosio , che viene assorbito in quantità molto maggiore dai tessuti tumorali rispetto alle cellule sane, venendo poi rilevato dal sensore della macchina, anche se con una definizione non molto elevata. Nuove apparecchiature, combinando le tecnologie PET e CT, permettono di unire i pregi di entrambe le metodiche, ottenendo così i migliori risultati possibili a livello di definizione e risposta diagnostica. Malgrado questo, il livello di precisione raggiunto non sembra ancora sufficiente per orientare in modo sicuro la scelta terapeutica [94] [95] .
Diagnosi differenziale
Vista la grande variabilità di aspetti con cui il carcinoma orale può manifestarsi, sono numerose le patologie orali che pongono necessità di diagnosi differenziale con la patologia neoplastica, il che spiega la difficoltà nel riuscire ad effettuare una diagnosi precoce.
La lesione iniziale limitata di aspetto ulcerante andrà prima di tutto differenziata dalle comuni lesioni da decubito , da ustione o da traumatismo, frequenti soprattutto nei portatori di protesi mobili , e dalle comuni ulcere di origine erpetica o aftosa . In questi casi è considerata valida la regola delle due settimane, per cui qualunque lesione ulcerata che non guarisce spontaneamente in massimo 15 giorni, dopo aver eliminato le possibili cause quando presenti, richiederà una diagnosi più approfondita, tramite biopsia.
La candidosi orale o mughetto , soprattutto nella sua forma erosiva o eritomatosa, ma anche nelle sue forme di lesione chiara (pseudomembranosa), può simulare gli aspetti di una lesione neoplastica iniziale, o di lesione precancerosa. Un trattamento antifungino topico, accompagnato da sciacqui con bicarbonato permetterà l'eliminazione della patologia, qualora di origine micotica.
Alcune lesioni di origine infettiva acute o croniche legate a patologie dentarie (parodontiti, osteiti), soprattutto se associate a stati di immunodepressione, possono in casi rari assumere caratteri di aggressività locale tali da porre il sospetto di lesioni neoplastiche. Un problema simile si può presentare per le osteonecrosi da bifosfonati . La storia clinica dei pazienti raccolta con una corretta anamnesi dovrebbe essere sufficiente per eliminare il dubbio.
Altre lesioni ulcerative di aspetto simile a quella neoplastica, di tipo persistente, sono quelle da sifilide , ma solo la lesione iniziale (sifiloma primario), che può durare parecchie settimane, può creare problemi di diagnosi differenziale, in quanto le lesioni secondarie e terziarie (gomme) si presentano in un quadro molto più ampio.
Il papilloma a cellule squamose, la più comune neoplasia benigna orale, così come l'affine condiloma da HPV , può creare allarme per l'aspetto di escrescenza sessile o peduncolata in grado talvolta di ulcerarsi in seguito a traumatismo, ma queste neoformazioni rimangono tipicamente di piccole dimensioni, presentando rivestimento epiteliale solitamente integro e crescita molto lenta. La trasformazione maligna è molto rara ma possibile, per cui se ne consiglia il monitoraggio periodico o, in caso di traumatismo frequente, l'escissione. Altre neoplasie benigne dei tessuti molli come il fibroma o il raro tumore a cellule granulose, di origine neurogena, possono richiedere l'esame istologico per eliminare il dubbio diagnostico.
La sialometaplasia necrotizzante è una lesione degenerativa acuta a carico delle ghiandole salivari minori di incerta origine (probabilmente ischemica), che compare come un nodulo che evolve in ulcerazione superficiale. Il dolore può essere variabile, e la risoluzione avviene spontaneamente nell'arco di alcune settimane [96] .
Per quanto riguarda la cresta gengivale , zona comunque di non frequente localizzazione del carcinoma orale, la lesione benigna più comune in grado di indurre allarme è l' epulide , piccola neoformazione fibrosa polipoide di varia origine e aspetto istologico, tipicamente associata ad un dente, quasi sempre asintomatica.
La glossite rombica mediana , entità patologica oggi considerata una particolare forma di candidosi cronica, si manifesta come arrossamento o lesione rilevata al centro della lingua , poco o per niente sintomatica, non sanguinante. Istologicamente si osserva ipercheratosi associata ad un modesto grado di alterazione della normale struttura tissutale, ma senza aspetti di malignità. Può essere associata all'uso di spray contenenti corticosteroidi per il trattamento di patologie respiratorie su base allergica.
Diagnosi precoce
La presenza di un gran numero di patologie a carattere benigno in grado di confondersi con la neoplasia nei suoi primi stadi, quando è scarsamente sintomatica, è una delle cause principali della diagnosi tardiva tipica di questa forma di tumore. Per superare questo problema, sono state proposte diverse tecniche diagnostiche di rapida esecuzione ea minor tasso di impegno per paziente e medico allo scopo di poter essere utilizzate come screening [97] [98] . Tra le più promettenti, la citologia esfoliativa (cytobrush) nelle sue varie versioni [99] [100] , i coloranti vitali [101] , l'uso di particolari fonti di emissioni luminose in grado di visualizzare zone di mucosa con caratteristiche anomale tramite reazioni di chemioluminescenza o autofluorescenza [102] e, come sviluppo recente, test salivari e marker molecolari [103] [104] [105] [106] . Nonostante i continui miglioramenti apportati nel tempo allo scopo di eliminare i problemi di sensibilità e specificità delle varie metodiche, allo stato attuale non sembrano esistere le condizioni per certificarne un uso routinario o per programmi di screening su larga scala [107] [108] [109] [110] [111] .
Stadiazione
La classificazione di questi tumori utilizza una specifica codifica TNM per quantificare l'estensione locale e l'eventuale diffusione linfonodale ea distanza della neoplasia, e per creare una scala di gradazione (stadiazione) utile per indirizzare l'approccio terapeutico [112] [113] . Per quanto riguarda la tipologia istologica più frequente, quella a cellule squamose, viene anche utilizzata una classificazione di gravità legata al livello di differenziazione cellulare ( grading ), che però si è rivelata poco significativa a livello prognostico, in quanto una notevole percentuale di queste neoplasie non presenta omogeneità istologica. Per superare questo problema, sono state proposte delle sistematiche di classificazione meno legate al giudizio soggettivo, come quella di Anneroth, che assegna un punteggio da 1 a 4 a sei differenti parametri istologici, per poi ottenere il valore del grading attraverso un punteggio finale complessivo, con risultati effettivamente più validi [114] .
| Stadio | Descrizione |
|---|---|
| TX | Tumore primitivo non definibile |
| T0 | Non segni di tumore primitivo |
| Tis | Tumore in situ (non invasivo) |
| T1 | Dimensione massima < 2 cm di diametro |
| T2 | Dimensione massima compresa tra i 2 e 4 cm di diametro |
| T3 | Dimensione massima > 4 cm senza invasione delle strutture adiacenti |
| T4a (labbra) | Invasione delle strutture adiacenti (osso corticale, nervo alveolare inferiore, pavimento della bocca, pelle) |
| T4a (cavità orale) | Invasione delle strutture adiacenti (osso corticale, muscoli della lingua, seno mascellare, pelle) |
| T4b (labbra e cavità orale) | Invasione delle strutture adiacenti (spazi masticatori, spazi pterigoidei, base del cranio; inglobamento carotide interna) |
| NX | Metastasi linfonodali non definibili |
| N0 | Metastasi linfonodali non rilevabili |
| N1 | Metastasi in singolo linfonodo omolaterale, < 3 cm |
| N2 | Metastasi come specificato da N2a,b,c |
| N2a | Metastasi in singolo linfonodo omolaterale con dimensione maggiore tra 3 e 6 cm |
| N2b | Metastasi in più linfonodi omolaterali, nessuno dei quali di dimensione > 6 cm |
| N2c | Metastasi in più linfonodi bilaterali o controlaterali, nessuno dei quali di dimensione > 6 cm |
| N3 | Metastasi linfonodali di dimensione > 6 cm |
| MX | Metastasi a distanza non rilevabili |
| M0 | Assenza di metastasi a distanza |
| M1 | Presenza di metastasi a distanza |
| Stadio 0 | Tis N0 M0 |
|---|---|
| Stadio I | T1 N0 M0 |
| Stadio II | T2 N0 M0 |
| Stadio III | T1,T2 N1 M0 |
| T3 N0,N1 M0 | |
| Stadio IVa | T1-3 N2 M0 |
| T4a N0-2 M0 | |
| Stadio IVb | T1-4 N3 M0 |
| T4b N1-3 M0 | |
| Stadio IVc | T1-4 N1-3 M1 |
| Grado | Descrizione |
|---|---|
| GX: | Livello di differenziazione non definibile |
| Grado 1: | Ben differenziato < 25% cellule non differenziate |
| Grado 2: | Moderatamente differenziato < 50% cellule non differenziate |
| Grado 3: | Scarsamente differenziato < 75% cellule non differenziate |
| Grado 4: | Indifferenziato (anaplastico) > 75% cellule non differenziate |
Terapia
La scelta terapeutica per il carcinoma orale dipende principalmente dalla stadiazione del tumore al momento della diagnosi [115] . Negli stadi precoci, con lesione limitata, la terapia di scelta è quella chirurgica , a bassa invasività. Con la progressione e l'espansione locale (S I-II), la scelta può variare tra chirurgia e radioterapia , entrambi considerate ugualmente valide, a seconda delle sedi coinvolte. Con la progressione in S III-IV diventa indicato l'uso combinato delle due tecniche, associando anche la chemioterapia di supporto [116] . Questa può essere utilizzata sia successivamente all'intervento primario ( terapia adiuvante ) che in via preventiva (terapia neoadiuvante), approccio sulla cui utilità non esiste accordo [117] [118] . Il tentativo di sostituire nei casi avanzati l'approccio chirurgico con tecniche meno demolitive, allo scopo di preservare organi delicati e di difficile ricostruzione, non sembra al momento fornire risultati promettenti [119] .
Nella tecnica chirurgica, l'intervento di asportazione richiede necessariamente un'escissione con margini sufficientemente ampi della lesione [120] , a cui molto spesso si associa lo svuotamento linfonodale , fasi sempre accompagnate dal necessario esame istologico dei reperti [121] . La tecnica del linfonodo sentinella proposta per limitare la necessità dello svuotamento linfonodale della zona cervicale, è allo studio, e sembra poter offrire una valida guida nella scelta dell'estensione della procedura [122] [123] . In passato gli interventi più estesi erano pesantemente lesivi per la qualità della vita dei pazienti, comportando notevoli deficit funzionali e spesso anche estetici. Le moderne tecniche di microchirurgia ricostruttiva, implantologia e chirurgia estetica , applicate in molti casi contestualmente all'intervento di asportazione della massa tumorale [124] [125] , o pianificate in seconda fase [126] , permettono oggi di diminuire sensibilmente queste problematiche, consentendo un recupero mediamente soddisfacente dal punto di vista funzionale ed estetico [127] [128] [129] . Quando necessario, possono essere utilizzate protesi mobili individuali [130] [131] . Per il recupero di una corretta funzione fonatoria , della deglutizione e respirazione , viene inoltre utilizzato il supporto dello specialista in logopedia [132] .
La radioterapia può essere del tipo a sorgente esterna, il cui utilizzo è stato implementato grazie alle nuove tecnologie, in grado di raggiungere un livello di precisione sempre più elevato (IMRT o radioterapia a intensità modulata) [133] , oppure del tipo interno ( brachiterapia ) [134] [135] , o una combinazione delle due [136] [137] . Come per la chirurgia, anche la radioterapia può prevedere l'associazione con un trattamento farmacologico [136] [138] .
Di recente hanno fatto la loro comparsa una nuova categoria di farmaci basati su meccanismi di tipo selettivo ( targeted therapy ), nati dalle scoperte nel campo della biologia molecolare delle cellule tumorali. Nel caso della neoplasia orale, prevede l'uso di un anticorpo monoclonale ( cetuximab ) che ha come bersaglio il recettore del fattore di crescita dell'epidermide (EGFR), da solo o in associazione alla radioterapia ea chemioterapici classici come il cisplatino e il fluorouracile [139] . Alcuni studi sembrano però mettere in dubbio il rapporto costo/beneficio di questo approccio [140] .
Una nuova strategia terapeutica in fase avanzata di sperimentazione è la terapia genica . I primi studi giunti alla fase clinica sull'uomo sono orientati verso una delle alterazioni più comuni, quella della proteina p53 [141] .
Prognosi
La prognosi per questa tipologia di tumori si assesta in media su un valore di poco superiore al 50% di sopravvivenza a 5 anni [72] [142] [143] , dato che però varia in maniera sensibile rispetto ad alcuni parametri. Tra tutti il più importante è la precocità della diagnosi, a cui è strettamente correlato il profilo TNM della neoplasia al momento della diagnosi stessa [144] [145] [146] . In particolare il livello di coinvolgimento linfonodale sembra essere un indicatore particolarmente significativo [147] .
| Stadio | Labbra | Lingua | Pavimento della bocca | Gengive e altre sedi |
|---|---|---|---|---|
| I | 96% | 71% | 73% | 81% |
| II | 83% | 59% | 60% | 62% |
| III | 57% | 47% | 36% | 45% |
| IV | 48% | 37% | 30% | 40% |
Altri elementi in grado di influire sulla prognosi sono la posizione della lesione nel cavo orale, con una prognosi peggiore per i tumori della lingua rispetto alla localizzazione orale e delle labbra [149] , il grado di differenziazione cellulare (grading), e l' istotipo [150] . In conseguenza alle scoperte nel campo della patogenesi tumorale sono in corso numerosi studi su marker o altri fattori che potrebbero rivelarsi utili ai fini prognostici [151] [152] [153] .
Nel caso di pazienti in età pediatrica, i tassi di sopravvivenza non sembrano discostarsi da quelli dell'età adulta [154] .
Prevenzione
Visto lo stretto legame tra precocità della diagnosi e prospettive di guarigione, e la scarsa conoscenza di questa forma di neoplasia tra la popolazione [155] e gli stessi medici ed odontoiatri , da alcuni anni sono state attivate delle campagne mirate allo scopo di aumentare la consapevolezza sui pericoli e le cause che possono condurre alla comparsa della patologia (prevenzione primaria), e sulla necessità di non sottovalutare alcuni tipi di lesioni orali quando non tendono alla guarigione spontanea in tempi brevi, recandosi presso il proprio dentista di fiducia per un controllo (prevenzione secondaria). L' OMS ha creato a tal fine delle linee guida all'interno del proprio programma globale per la promozione della salute orale, in modo da indirizzare le iniziative dei paesi più a rischio [18] .
In Italia un progetto in tale senso è stato avviato nel 2009 dalla Federazione Nazionale Ordini Medici Chirurghi e Odontoiatri (FNOMCeO) [156] , individuando una specifica strategia d'azione (approccio tetra), basata sull'informazione degli operatori sanitari più presenti sul territorio, odontoiatri, medici di base e igienisti dentari, e creando una più stretta collaborazione tra questi e le strutture pubbliche del servizio sanitario nazionale meglio attrezzate per la diagnostica e il trattamento avanzato di questa patologia [157] .
Un'altra iniziativa è stata avviata su base volontaria da parte della maggior organizzazione di dentisti italiani, l' Andi , sempre allo scopo di intercettare in fase precoce la malattia e informare sui rischi e necessità di controlli in caso di presenza di segni premonitori [158] . In particolare, nel mese designato, solitamente a maggio, viene organizzata una giornata dedicata all'informazione e alla sensibilizzazione denominata "Oral Cancer Day", offrendo per un periodo prestabilito visite gratuite mirate specificatamente alla ricerca dei segni di patologia o di condizioni precancerose presso i dentisti partecipanti [159] .
Note
- ^ a b c ( EN ) aa. vv. , Tumours of the Oral Cavity and Oropharynx , in Pathology and Genetics of Head and Neck Tumours ( PDF ), IARC Scientific Publication, 2005, pp. 163-181, ISBN 92-832-2417-5 . URL consultato il 4 ottobre 2013 (archiviato dall' url originale il 24 settembre 2015) .
- ^ ( EN ) Shukla S, Shukla S, Oral cancer-curse, cure and challenge , in Indian J Surg , vol. 74, n. 6, Springer, dicembre 2012, pp. 437-439, DOI : 10.1007/s12262-012-0769-0 , PMID 24293895 , PMC 3537986 .
- ^ ( EN ) Fact stats-world , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Parkin DM, Bray F, Ferlay J, Pisani P, Global cancer statistics, 2002 , in CA Cancer J Clin. , vol. 55, n. 2, John Wiley & Sons, Mar-Apr 2005, pp. 74-108, DOI : 10.3322/canjclin.55.2.74 , PMID 15761078 . URL consultato il 15 febbraio 2013 .
- ^ ( EN ) Incidence/Mortality > Dual multi-bar chart: populations/sexes by cancer 20 highest in the world , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) India estimated cancer incidence, all ages: both sexes , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Jemal A, et al , Global cancer statistics , in CA Cancer J Clin , vol. 61, n. 2, John Wiley & Sons, Mar-Apr 2011, pp. 69-90, DOI : 10.3322/caac.20107 , PMID 21296855 . URL consultato il 30 gennaio 2013 .
- ^ ( EN ) Italy (2012) estimated cancer incidence, all ages: both sexes , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Italy (2012) estimated cancer incidence, all ages: male , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Italy (2012) estimated cancer incidence, all ages: female , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Italy (2012) estimated cancer mortality, all ages: both sexes , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Italy (2012) estimated cancer mortality, all ages: male , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Italy (2012) estimated cancer mortality, all ages: female , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Analisi e interpretazioni per sede tumorale i dati dei registri tumori 1986-1997 ( PDF ), in Gli andamenti temporali della patologia oncologica in Italia: i dati dei Registri tumori (1986-1997) , Associazione italiana dei registri tumori (AIRTUM). URL consultato il 12 febbraio 2013 .
- ^ ( EN ) World- Both Sexes estimated incidence by age , in Globocan 2012 , International Agency for research on Cancer-WHO. URL consultato l'11 maggio 2014 .
- ^ ( EN ) Zygogianni AG, et al , Oral squamous cell cancer: early detection and the role of alcohol and smoking , in Head Neck Oncology , vol. 3, n. 2, 6 gennaio 2011, DOI : 10.1186/1758-3284-3-2 , PMC 3022893 .
- ^ ( EN ) Rosenquist K, Risk factors in oral and oropharyngeal squamous cell carcinoma: a population-based case-control study in southern Sweden , in Swed Dent J Suppl , n. 179, 2005, pp. 1-66, PMID 16335030 .
- ^ a b ( EN ) Petersen PE, Oral cancer prevention and control-the approach of the World Health Organization ( PDF ), in Oral Oncology , vol. 45, n. 4-5, Apr-Marzo 2009, pp. 454-460, DOI : 10.1016/j.oraloncology.2008.05.023 , PMID 18804412 . URL consultato il 2 febbraio 2013 .
- ^ ( EN ) Foulkes WD, et al , Familial risks of squamous cell carcinoma of the head and neck: retrospective case-control study , in BMJ , vol. 313, n. 7059, British Medical Association, 21 settembre 1996, pp. 716-721, PMID 8819440 , PMC 2352110 .
- ^ ( EN ) Johnson N, Tobacco use and oral cancer: a global perspective , in J Dent Educ , vol. 65, n. 4, American Dental Education Association, aprile 2001, pp. 328-339, PMID 11336118 . URL consultato il 14 febbraio 2013 (archiviato dall' url originale il 25 febbraio 2015) .
- ^ ( EN ) Freedman ND, et al , Prospective investigation of the cigarette smoking-head and neck cancer association by sex , in Cancer , vol. 110, n. 7, American Cancer Society, 1º ottobre 2007, pp. 1593-1601, DOI : 10.1002/cncr.22957 , PMID 17724671 .
- ^ ( EN ) Cancer Control and Population Sciences, Cigars: Health Effects and Trends ( PDF ), in Smoking and Tobacco Control Monographs , vol. 9, National Cancer Institute, 1998, pp. 120-127. URL consultato il 2 febbraio 2013 (archiviato dall' url originale il 7 febbraio 2017) .
- ^ ( EN ) Chang CM, et al , Systematic review of cigar smoking and all cause and smoking related mortality , in BMC Public Health , vol. 15, n. 1, BioMed Central, 24 aprile 2015, p. 390, DOI : 10.1186/s12889-015-1617-5 , PMID 25907101 , PMC 4408600 .
- ^ ( EN ) Henley SJ, et al , Association between exclusive pipe smoking and mortality from cancer and other diseases , in J Natl Cancer Inst , vol. 96, n. 11, Oxford University Press, 2 giugno 2004, pp. 853-861, DOI : 10.1093/jnci/djh144 , PMID 15173269 .
- ^ ( EN ) Gupta PC, Meht FS, Pindborg J, Mortality among reverse chutta smokers in south India ( PDF ), in British Medical Journal (Clin Res Ed) , vol. 289, n. 6449, 6 ottobre 1984, pp. 865-866, PMID 6434115 , PMC 1443430 . URL consultato il 2 febbraio 2013 .
- ^ ( EN ) Alvarez Gómez GJ, et al. , Reverse smokers's and changes in oral mucosa. Department of Sucre, Colombia ( PDF ), in Med Oral Patol Oral Cir Bucal , vol. 13, n. 2, 1º gennaio 2008, pp. E 1-8, PMID 18167472 . URL consultato il 2 febbraio 2013 .
- ^ ( EN ) The World Health Organization IARC Expert Group, Tobacco Habits other than Smoking;Betel-Quid and Areca-Nut Chewing; and some Related Nitrosamines ( PDF ), in IARC Monographs on the Evaluation of Carcinogenic Risks to Humans , vol. 37, IARC Press, 1985, pp. 89-140. URL consultato il 26 aprile 2015 .
- ^ a b ( EN ) Znaor A, et al , Independent and combined effects of tobacco smoking, chewing and alcohol drinking on the risk of oral, pharyngeal and esophageal cancers in Indian men , in int J Cancer , vol. 105, n. 5, John Wiley & Sons, 10 luglio 2003, pp. 681-686, DOI : 10.1002/ijc.11114 , PMID 12740918 . URL consultato il 10 febbraio 2013 .
- ^ ( EN ) Khan Z, Tönnies J, Müller S, Smokeless tobacco and oral cancer in South Asia: a systematic review with meta-analysis , in J Cancer Epidemiol , vol. 2014, Hindawi, 2014, p. 394696, DOI : 10.1155/2014/394696 , PMID 25097551 , PMC 4109110 .
- ^ ( EN ) Takezaki T, et al , Tobacco, alcohol and dietary factors associated with the risk of oral cancer among Japanese , in Jpn J Cancer Res , vol. 87, n. 6, John Wiley & Sons, giugno 1996, pp. 555-562, DOI : 10.1111/j.1349-7006.1996.tb00259.x , PMID 8766517 .
- ^ ( EN ) Boffetta P, Hashibe M, Alcohol and cancer ( PDF ), in Lancet Oncol , vol. 7, n. 2, Elsevier, febbraio 2006, pp. 149-156, PMID 16455479 . URL consultato il 20 gennaio 2013 (archiviato dall'url originale il 19 aprile 2013) .
- ^ ( EN ) Hashibe M, et al , Interaction between tobacco and alcohol use and the risk of head and neck cancer: pooled analysis in the International Head and Neck Cancer Epidemiology Consortium , in Cancer Epidemiol Biomarkers Prev , vol. 18, n. 2, American Association for Cancer Research, febbraio 2009, pp. 541-550, DOI : 10.1158/1055-9965.EPI-08-0347 , PMID 19190158 , PMC 3051410 .
- ^ ( EN ) Ferreira Antunes JL, et al , Joint and independent effects of alcohol drinking and tobacco smoking on oral cancer: a large case-control study , in PLOS One , vol. 8, n. 7, PLOS, 10 luglio 2013, p. e68132, DOI : 10.1371/journal.pone.0068132 , PMID 23874521 , PMC 3707956 .
- ^ ( EN ) Lachenmeier DW, Alcohol-containing mouthwash and oral cancer--can epidemiology prove the absence of risk? , in Ann Agric Environ Med , vol. 19, n. 3, 2012, pp. 609-610, PMID 23020065 . URL consultato il 15 febbraio 2013 .
- ^ ( EN ) Gandini S, et al , Mouthwash and oral cancer risk quantitative meta-analysis of epidemiologic studies , in Ann Agric Environ Med , vol. 19, n. 2, 2012, pp. 173-180, PMID 22742785 . URL consultato il 15 febbraio 2013 .
- ^ ( EN ) The World Health Organization IARC Expert Group, Betel-quid and Areca-nut Chewing and Some Areca-nut-derived Nitrosamines ( PDF ), in IARC Monographs on the Evaluation of Carcinogenic Risks to Humans , vol. 87, IARCPress, 2004. URL consultato il 26 aprile 2015 .
- ^ ( EN ) Sharan RN, et al , Association of betel nut with carcinogenesis: revisit with a clinical perspective , in PLOS One , vol. 7, n. 8, PLOS, 2012, p. e42759, DOI : 10.1371/journal.pone.0042759 , PMID 22912735 , PMC 3418282 .
- ^ ( EN ) Little MA, et al , The reasons for betel-quid chewing scale: assessment of factor structure, reliability, and validity , in BMC Oral Health , vol. 14, Springer Science+Business Media, 3 giugno 2014, p. 62, DOI : 10.1186/1472-6831-14-62 , PMID 24889863 , PMC 4059468 .
- ^ ( EN ) Petti S, Masood M, Scully C, The magnitude of tobacco smoking-betel quid chewing-alcohol drinking interaction effect on oral cancer in South-East Asia. A meta-analysis of observational studies , in PLOS One , vol. 8, n. 11, PLOS, 18 novembre 2013, p. e78999, DOI : 10.1371/journal.pone.0078999 , PMID 24260143 , PMC 3832519 .
- ^ ( EN ) The impact of qat-chewing on health: a re-evaluation , su al-bab.com , The British-Yemeni Society, agosto 2005. URL consultato il 26 aprile 2015 (archiviato dall' url originale il 7 giugno 2010) .
- ^ ( EN ) Gan LL, et al , Prevalence of human papillomavirus infection in oral squamous cell carcinoma: a case-control study in Wuhan, China , in Asian Pac J Cancer Prev , vol. 15, n. 14, National Cancer Center of Korea, Editorial Office, 2014, pp. 5861-5865, DOI : 10.7314/APJCP.2014.15.14.5861 , PMID 25081714 .
- ^ ( EN ) Khode SR, et al. , Exploring the link between human papilloma virus and oral and oropharyngeal cancers , in J Cancer Res Ther , vol. 10, n. 3, Wolters Kluwer, luglio-settembre 2014, pp. 492-498, DOI : 10.4103/0973-1482.138213 , PMID 25313727 .
- ^ ( EN ) Poling JS, et al. ,Human papillomavirus (HPV) status of non-tobacco related squamous cell carcinomas of the lateral tongue , in Oral Oncol , vol. 50, n. 4, Elsevier, aprile 2014, pp. 306-310, DOI : 10.1016/j.oraloncology.2014.01.006 , PMID 24485566 , PMC 3972491 .
- ^ ( EN ) Rushatamukayanunt P, et al , Lack of association between high-risk human papillomaviruses and oral squamous cell carcinoma in young Japanese patients , in Asian Pac J Cancer Prev , vol. 15, n. 10, National Cancer Center of Korea, 2014, pp. 4135-4141, DOI : 10.7314/APJCP.2014.15.10.4135 , PMID 24935359 .
- ^ ( EN ) Pavia M., et al , Association between fruit and vegetable consumption and oral cancer: a meta-analysis of observational studies , in Am J Clin Nutr. , vol. 83, n. 5, The American Society for Nutrition, maggio 2006, pp. 1126-1134, PMID 16685056 . URL consultato il 26 gennaio 2013 .
- ^ ( EN ) Bravi F, et al , Foods, nutrients and the risk of oral and pharyngeal cancer , in Br J Cancer , vol. 109, n. 11, Nature Publishing Group, 26 novembre 2013, pp. 2904-2910, DOI : 10.1038/bjc.2013.667 , PMID 24149181 , PMC 3844916 .
- ^ ( EN ) Galeone C, et al , Coffee and tea intake and risk of head and neck cancer: pooled analysis in the international head and neck cancer epidemiology consortium , in Cancer Epidemiol Biomarkers Prev , vol. 19, n. 7, American Association for Cancer Research, 6 luglio 2010, pp. 1723-1736, DOI : 10.1158/1055-9965.EPI-10-0191 , PMID 20570908 , PMC 3047460 .
- ^ ( EN ) Hildebrand JS, et al , Coffee, tea, and fatal oral/pharyngeal cancer in a large prospective US cohort , in Am J Epidemiol , vol. 177, n. 1, Oxford University Press, 1º gennaio 2013, pp. 50-58, DOI : 10.1093/aje/kws222 , PMID 23230042 .
- ^ ( EN ) Xu J, et al , Meat consumption and risk of oral cavity and oropharynx cancer: a meta-analysis of observational studies , in PLOS One , vol. 9, n. 4, PLOS, 15 aprile 2014, p. e95048, DOI : 10.1371/journal.pone.0095048 , PMID 24736706 , PMC 3988178 .
- ^ ( EN ) Lam TK, et al , Dietary fiber and grain consumption in relation to head and neck cancer in the NIH-AARP Diet and Health Study , in cancer causes Control , vol. 22, n. 10, Springer Science+Business Media, ottobre 2011, pp. 1405-1414, DOI : 10.1007/s10552-011-9813-9 , PMID 21785948 , PMC 3215506 .
- ^ ( EN ) Öhman J, et al ,Oral and lip cancer in solid organ transplant patients--a cohort study from a Swedish Transplant Centre , in Oral Oncol , vol. 51, n. 2, Elsevier, febbraio 2015, pp. 146-150, DOI : 10.1016/j.oraloncology.2014.11.007 , PMID 25497104 .
- ^ ( EN ) Kubota E, Kurokawa H, Katsuki T, Evaluation of the serum level of immunosuppressive substance in oral cancer patients ( abstract ), in J Oral Maxillofac Surg , vol. 49, n. 2, Elsevier, febbraio 1991, pp. 121-126, DOI : 10.1016/0278-2391(91)90097-6 , PMID 1990088 . URL consultato il 17 febbraio 2013 .
- ^ ( EN ) Rotundo LD, et al , Are recurrent denture-related sores associated with the risk of oral cancer? A case control study , in Rev Bras Epidemiol , vol. 16, n. 3, ABRASCO, settembre 2013, pp. 705-715, DOI :10.1590/S1415-790X2013000300014 , PMID 24896283 .
- ^ ( EN ) Moergel M, et al , Chronic periodontitis and its possible association with oral squamous cell carcinoma - a retrospective case control study , in Head Face Med , vol. 9, BioMed Central, 9 dicembre 2013, p. 39, DOI : 10.1186/1746-160X-9-39 , PMID 24321243 , PMC 4029401 .
- ^ ( EN ) Wen BW, et al , Cancer risk among gingivitis and periodontitis patients: a nationwide cohort study , in QJM , vol. 107, n. 4, Oxford University Press, aprile 2014, pp. 283-290, DOI : 10.1093/qjmed/hct248 , PMID 24336850 .
- ^ a b ( EN ) A digital manual for the early diagnosis of oral neoplasia , su screening.iarc.fr , International Agency for Research on Cancer-WHO. URL consultato il 27 gennaio 2013 .
- ^ ( EN ) Rivera C, Venegas B, Histological and molecular aspects of oral squamous cell carcinoma (Review) , in Oncol Lett , vol. 8, n. 1, Spandidos Publications, luglio 2014, pp. 7-11, DOI : 10.3892/ol.2014.2103 , PMID 24959211 , PMC 4063640 .
- ^ ( EN ) Gupta B, Johnson NW, Emerging and established global life-style risk factors for cancer of the upper aero-digestive tract , in Asian Pac J Cancer Prev , vol. 15, n. 15, 2014, pp. 5983-5991, DOI : 10.7314/APJCP.2014.15.15.5983 , PMID 25124561 .
- ^ ( EN ) Martin CL, et al , Chromosomal imbalances in oral squamous cell carcinoma. Examination of 31 cell lines and review of the literature , in Oral Oncol , vol. 44, n. 4, Elsevier, agosto 2007, pp. 369-382, PMID 17681875 , PMC 2362065 .
- ^ ( EN ) Jurel SK, et al , Genes and oral cancer , in Indian J Hum Genet , vol. 20, n. 1, Wolters Kluwer, gennaio 2014, pp. 4-9, DOI : 10.4103/0971-6866.132745 , PMID 24959008 , PMC 4065477 .
- ^ ( EN ) Yoshida R, et al , The pathological significance of Notch1 in oral squamous cell carcinoma , in Lab Invest , vol. 93, n. 10, Nature Publishing Group, ottobre 2013, pp. 1068-81, DOI : 10.1038/labinvest.2013.95 , PMID 23938602 .
- ^ ( EN ) Perez-Ordoñez B, Beauchemin M, Jordan RCK, Molecular biology of squamous cell carcinoma of the head and neck , in J Clin Pathol , vol. 59, n. 5, Association of Clinical Pathologists-BMJ Group, maggio 2006, pp. 445-453, PMID 16644882 , PMC 1860277 .
- ^ ( EN ) India Project Team of the International Cancer Genome Consortium, Mutational landscape of gingivo-buccal oral squamous cell carcinoma reveals new recurrently-mutated genes and molecular subgroups , in Nat Commun , vol. 4, Nature Publishing Group, 2013, p. 2873, DOI : 10.1038/ncomms3873 , PMID 24292195 , PMC 3863896 .
- ^ ( EN ) Bundela S, Sharma A, Bisen PS, Potential therapeutic targets for oral cancer: ADM, TP53, EGFR, LYN, CTLA4, SKIL, CTGF, CD70 , in PLOS One , vol. 9, n. 7, PLOS, 16 luglio 2014, p. e102610, DOI : 10.1371/journal.pone.0102610 , PMID 25029526 , PMC 4110113 .
- ^ ( EN ) Jung S, et al , Analysis of angiogenic markers in oral squamous cell carcinoma-gene and protein expression , in Head Face Med , vol. 11, Springer, 5 giugno 2015, p. 19, DOI : 10.1186/s13005-015-0076-7 , PMID 26044849 , PMC 4461981 .
- ^ ( EN ) Tanaka T, Ishigamori R, Understanding Carcinogenesis for Fighting Oral Cancer , in J Oncol , vol. 2011, Hindawi, 2011, p. 603740, DOI : 10.1155/2011/603740 , PMID 21772845 , PMC 3136173 . URL consultato il 17 febbraio 2013 .
- ^ ( EN ) Dost F, et al , Malignant transformation of oral epithelial dysplasia: a real-world evaluation of histopathologic grading , in Oral Surg Oral Med Oral Pathol Oral Radiol , vol. 117, n. 3, Elsevier, marzo 2014, pp. 279-290, DOI : 10.1016/j.oooo.2013.09.017 , PMID 22549675 .
- ^ ( EN ) Manchanda A, Shetty DC, Reproducibility of grading systems in oral epithelial dysplasia , in Med Oral Patol Oral Cir Bucal , vol. 17, n. 6, 1º novembre 2012, pp. e935-942, DOI : 10.4317/medoral.17749 , PMID 22549675 , PMC 3505713 .
- ^ ( EN ) Yang Y, et al , Progress risk assessment of oral premalignant lesions with saliva miRNA analysis , in BMC Cancer , 13numero=, Springer, 19 marzo 2013, p. 129, DOI : 10.1186/1471-2407-13-129 , PMID 23510112 , PMC 3637283 .
- ^ ( EN ) Abdulmajeed AA, Farah CS, Gene Expression Profiling for the Purposes of Biomarker Discovery in Oral Potentially Malignant Lesions: A Systematic Review , in Clin Med Insights Oncol , vol. 7, Libertas Academica, 31 ottobre 2013, pp. 279-290, DOI : 10.4137/CMO.S12950 , PMID 24250244 , PMC 3825664 .
- ^ ( EN ) Leukoplakia , su screening.iarc.fr , International Agency for Research on Cancer-WHO. URL consultato il 17 febbraio 2013 .
- ^ a b ( EN ) Neville BW, Day TA, Oral cancer and precancerous lesions , in CA Cancer J Clin , vol. 52, n. 4, John Wiley & Sons, luglio-Ago 2002, pp. 195-215, DOI : 10.3322/canjclin.52.4.195 , PMID 12139232 . URL consultato il 17 febbraio 2013 .
- ^ a b ( EN ) Messadi DV, Diagnostic aids for detection of oral precancerous conditions , in Int J Oral Sci , vol. 5, n. 2, Nature Publishing Group, giugno 2013, pp. 59-65, DOI : 10.1038/ijos.2013.24 , PMID 23743617 , PMC 3707069 .
- ^ ( EN ) Farah CS, et al , Oral cancer and oral potentially malignant disorders , in Int J Dent , vol. 2014, Hindawi Publishing Corporation, 2014, p. 853479, DOI : 10.1155/2014/853479 , PMID 24891850 , PMC 4033498 .
- ^ ( EN ) van der Waal I, Oral potentially malignant disorders: is malignant transformation predictable and preventable? , in Med Oral Patol Oral Cir Bucal , vol. 19, n. 4, 1º luglio 2014, pp. e386-390, DOI : 10.4317/medoral.20205 , PMID 24905952 , PMC 4119315 .
- ^ ( EN ) Reichart PA, Philipsen HP, Oral erythroplakia--a review ( PDF ) ( abstract ), in Oral Oncol , vol. 3841, n. 6, Elsevier, luglio 2005, pp. 551-561, PMID 15975518 . URL consultato il 17 febbraio 2013 .
- ^ ( EN ) WHO histological classification of tumours of the oral cavity and oropharynx , su screening.iarc.fr , International Agency for Research on Cancer-WHO. URL consultato il 27 gennaio 2013 .
- ^ ( EN ) Sixto-Requeijo R, et al , An analysis of oral biopsies extracted from 1995 to 2009, in an oral medicine and surgery unit in Galicia (Spain) , in Med Oral Patol Oral Cir Bucal , vol. 17, n. 1, 1º gennaio 2012, pp. e16-22, DOI : 10.4317/medoral.17143 , PMID 21743423 , PMC 3448179 .
- ^ ( EN ) George J, Narang RS, Rao NN, Indian J Dent Res , vol. 23, n. 6, Wolters Kluwer, novembre dicembre 2012, p. 842, DOI : 10.4103/0970-9290.111291 , PMID 23649085 , https://oadoi.org/10.4103/0970-9290.111291 .
- ^ ( EN ) Wirsing AM, et al , Characterisation and prognostic value of tertiary lymphoid structures in oral squamous cell carcinoma , in BMC Cancer , vol. 14, BioMed Central, 23 agosto 2014, p. 38, DOI : 10.1186/1472-6890-14-38 , PMID 25177210 , PMC 4148494 .
- ^ ( EN ) Samman M, et al , Next-generation sequencing analysis for detecting human papillomavirus in oral verrucous carcinoma , in Oral Surg Oral Med Oral Pathol Oral Radiol , vol. 118, n. 1, Elsevier, luglio 2014, pp. 117-125.e1, DOI : 10.1016/j.oooo.2014.03.018 , PMID 24908602 .
- ^ ( EN ) Xie S, et al , Basaloid squamous cell carcinoma of the maxillary gingiva: A case report and review of the literature , in Oncol Lett , vol. 8, n. 3, Spandidos Publications, settembre 2014, pp. 1287-1290, DOI : 10.3892/ol.2014.2318 , PMID 25120708 , PMC 4114586 .
- ^ ( EN ) Hanemann JA, et al , Expression of E-cadherin and β-catenin in basaloid and conventional squamous cell carcinoma of the oral cavity: are potential prognostic markers? , in BMC Cancer , vol. 14, BioMed Central, 3 giugno 2014, p. 395, DOI : 10.1186/1471-2407-14-395 , PMID 24893577 , PMC 4049437 .
- ^ ( EN ) Reyes M, et al , Sarcomatoid (spindle cell) carcinoma of tongue: a report of two cases , in Case Rep Dent , vol. 2015, Hindawi Publishing Corporation, 2015, p. 780856, DOI : 10.1155/2015/780856 , PMID 25785207 , PMC 4346690 .
- ^ ( EN ) Ishida M, et al , Adenosquamous carcinoma of the tongue: a case report with review of the literature , in Int J Clin Exp Pathol , vol. 7, n. 4, e-Century Publishing Corporation, 15 marzo 2014, pp. 1809-13, PMID 24817985 , PMC 4014269 .
- ^ ( EN ) Noguti J, et al , Metastasis from oral cancer: an overview , in Cancer Genomics Proteomics , vol. 9, n. 5, International Institute of Anticancer Research, sett-ott 2012, pp. 329-335, PMID 22990112 . URL consultato il 16 febbraio 2013 .
- ^ ( DE ) Awan Kh, Oral Cancer: Early Detection is Crucial , in J Int Oral Health , vol. 6, n. 5, International Society of Preventive and Community Dentistry, settembre 2014, pp. i-ii, PMID 25395811 , PMC 4229841 .
- ^ ( EN ) Patton LL, Epstein JB, Kerr AR, Adjunctive techniques for oral cancer examination and lesion diagnosis: a systematic review of the literature , in J Am Dent Assoc , vol. 139, n. 7, American Dental Association, luglio 2008, pp. 896-905, PMID 18594075 . URL consultato il 16 febbraio 2013 .
- ^ ( EN ) Kazanowska K, Hałoń A, Radwan-Oczko M,The role and application of exfoliative cytology in the diagnosis of oral mucosa pathology - contemporary knowledge with review of the literature ( PDF ), in Adv Clin Exp Med , vol. 23, n. 1, marzo-aprile 2014, pp. 299-305, PMID 24913123 . URL consultato il 14 giugno 2015 .
- ^ ( EN ) Ujaoney S, et al , Evaluation of chemiluminescence, toluidine blue and histopathology for detection of high risk oral precancerous lesions: A cross-sectional study , in BMC Clin Pathol , vol. 12, BioMed Central, 12 marzo 2012, p. 6, DOI : 10.1186/1472-6890-12-6 , PMID 22410295 , PMC 3315728 .
- ^ ( DE ) Hullmann M, et al , Oral cytology: historical development, current status, and perspectives , in Mund Kiefer Gesichtschir , vol. 11, n. 1, Springer Science+Business Media, gennaio 2007, pp. 1-9, PMID 17177045 .
- ^ ( EN ) Carreras-Torras C, Gay-Escoda C, Techniques for early diagnosis of oral squamous cell carcinoma: Systematic review , in Med Oral Patol Oral Cir Bucal , vol. 20, n. 3, 1º maggio 2015, pp. e305-315, DOI : 10.4317/medoral.20347 , PMID 25662554 .
- ^ ( EN ) Gődény M, Prognostic factors in advanced pharyngeal and oral cavity cancer; significance of multimodality imaging in terms of 7th edition of TNM , in Cancer Imaging , vol. 14, Springer, 28 aprile 2014, p. 15, DOI : 10.1186/1470-7330-14-15 , PMID 25608735 , PMC 4331821 .
- ^ ( EN ) Schöder H, et al , 18F-FDG PET/CT for detecting nodal metastases in patients with oral cancer staged N0 by clinical examination and CT/MRI , in J Nucl Med , vol. 47, n. 5, Society of Nuclear Medicine and Molecular Imaging, maggio 2006, pp. 755-762, PMID 16644744 . URL consultato il 16 febbraio 2013 .
- ^ ( EN ) Ng SH, et al , 18F-FDG PET and CT/MRI in oral cavity squamous cell carcinoma: a prospective study of 124 patients with histologic correlation , in J Nucl Med , vol. 46, n. 7, Society of Nuclear Medicine and Molecular Imaging, luglio 2005, pp. 1136-1143, PMID 16000282 . URL consultato il 16 febbraio 2013 .
- ^ ( EN ) Uppal N, Baliga M, Necrotizing sialometaplasia: A rare lesion that mimics oral cancer clinically and histopathologically , in Otolaryngol Pol , vol. 68, n. 3, Elsevier, maggio-giugno 2014, pp. 154-156, DOI : 10.1016/j.otpol.2013.07.004 , PMID 24837912 .
- ^ ( EN ) Masthan KM, et al , Advanced diagnostic aids in oral cancer , in Asian Pac J Cancer Prev , vol. 13, n. 8, National Cancer Center, 2012, pp. 3573-3576, DOI : 10.7314/APJCP.2012.13.8.3573 , PMID 23098535 .
- ^ ( EN ) Omar E, Current concepts and future of noninvasive procedures for diagnosing oral squamous cell carcinoma--a systematic review , in Head Face Med , vol. 11, n. 1, Springer, 25 marzo 2015, p. 6, DOI : 10.1186/s13005-015-0063-z , PMID 25889859 , PMC 4396078 .
- ^ ( EN ) Gupta S, et al , Clinical correlative study on early detection of oral cancer and precancerous lesions by modified oral brush biopsy and cytology followed by histopathology , in J Cancer Res Ther , vol. 10, n. 2, Wolters Kluwer, aprile-giugno 2014, pp. 232-238, DOI : 10.4103/0973-1482.136539 , PMID 25022371 .
- ^ ( EN ) Reddy SP, Ramani P, Nainani P, Confocal microscopy and exfoliative cytology , in J Oral Maxillofac Pathol , vol. 17, n. 2, Wolters Kluwer, maggio 2013, pp. 217-221, DOI : 10.4103/0973-029X.119746 , PMID 24250082 , PMC 3830230 .
- ^ ( EN ) Riaz A, et al , Methylene blue as an early diagnostic marker for oral precancer and cancer , in Springerplus , vol. 2, n. 1, Springer, dicembre 2013, p. 95, DOI : 10.1186/2193-1801-2-95 , PMID 23524482 , PMC 3602613 .
- ^ ( EN ) Mendes SF, et al , Techniques for precancerous lesion diagnosis , in J Oncol , vol. 59, n. 5, Hindawi Publishing Corporation, 13 gennaio 2011, pp. 445-453, DOI : 10.1155/2011/326094 , PMID 21318165 , PMC 3026985 .
- ^ ( EN ) Prasad G, McCullough M, Chemokines and cytokines as salivary biomarkers for the early diagnosis of oral cancer , in Int J Dent , vol. 2013, Hindawi, 2013, p. 813756, DOI : 10.1155/2013/813756 , PMID 24376459 , PMC 3860143 .
- ^ ( EN ) Shah S, Kaur M, Biomarkers and chemopreventives in oral carcinogenesis and its prevention , in J Oral Maxillofac Pathol , vol. 18, n. 1, Wolters Kluwer, gennaio 2014, pp. 69-76, DOI : 10.4103/0973-029X.131914 , PMID 24959040 , PMC 4065451 .
- ^ ( EN ) Cheng YS, Rees T, Wright J, A review of research on salivary biomarkers for oral cancer detection , in Clin Transl Med , vol. 3, n. 1, Springer, 24 febbraio 2014, p. 3, DOI : 10.1186/2001-1326-3-3 , PMID 24564868 , PMC 3945802 .
- ^ ( EN ) Yang Y, et al , Quantitative Proteomic Analysis of Oral Brush Biopsies Identifies Secretory Leukocyte Protease Inhibitor as a Promising, Mechanism-Based Oral Cancer Biomarker , in PLOS One , vol. 9, n. 4, PLOS, 18 aprile 2014, p. e95389, DOI : 10.1371/journal.pone.0095389 , PMID 24748380 , PMC 3991667 .
- ^ ( EN ) Hanken H, et al , The detection of oral pre- malignant lesions with an autofluorescence based imaging system (VELscope™) - a single blinded clinical evaluation , in Head Face Med , vol. 9, Springer, 23 agosto 2013, p. 23, DOI : 10.1186/1746-160X-9-23 , PMID 23967796 , PMC 3851797 .
- ^ ( EN ) Shashidara R, Sreeshyla HS, Sudheendra US, Chemiluminescence: a diagnostic adjunct in oral precancer and cancer: a review , in J Cancer Res Ther , vol. 10, n. 3, Wolters Kluwer, luglio-settembre 2014, pp. 487-491, DOI : 10.4103/0973-1482.138215 , PMID 25313726 .
- ^ ( EN ) Brocklehurst P, et al , Screening programmes for the early detection and prevention of oral cancer ( abstract ), in Cochrane Database Syst Rev , vol. 11, 19 novembre 2013, p. CD004150, DOI : 10.1002/14651858.CD004150.pub4 , PMID 24254989 .
- ^ ( EN ) Kujan O, Sloan P, Dilemmas of oral cancer screening: an update , in Asian Pac J Cancer Prev , vol. 14, n. 5, National Cancer Center, 2013, pp. 3369-3373, DOI : 10.7314/APJCP.2013.14.5.3369 , PMID 23803131 .
- ^ ( EN ) Olson CM, et al , Screening for Oral Cancer: A Targeted Evidence Update for the US Preventive Services Task Force [Internet] , in Evidence Syntheses , vol. 102, Agency for Healthcare Research and Quality, aprile 2013, PMID 23617014 .
- ^ ( EN ) TNM classification of carcinomas of the oral cavity , su screening.iarc.fr , International Agency for Research on Cancer-WHO. URL consultato il 17 gennaio 2013 .
- ^ ( EN ) Snehal G. Patel, Jatin P Shah, TNM Staging of Cancers of the Head and Neck: Striving for Uniformity Among Diversity ( PDF ), in CA: A Cancer Journal for Clinicians , vol. 55, John Wiley & Sons, luglio 2005, pp. 242-258, PMID 16020425 . URL consultato il 15 gennaio 2013 (archiviato dall' url originale il 3 febbraio 2013) .
- ^ ( EN ) Akhter M, et al , A study on histological grading of oral squamous cell carcinoma and its co-relationship with regional metastasis , in J Oral Maxillofac Pathol , vol. 15, n. 2, Wolters Kluwer, maggio 2011, pp. 168-176, DOI : 10.4103/0973-029X.84485 , PMID 22529575 , PMC 3329698 .
- ^ ( EN ) Treatment options for oral cavity and oropharyngeal cancer by stage , su cancer.org , American Cancer Society. URL consultato il 7 febbraio 2013 .
- ^ ( EN ) Huang SH, O'Sullivan B, Oral cancer: Current role of radiotherapy and chemotherapy , in Med Oral Patol Oral Cir Bucal , vol. 18, n. 2, 5 febbraio 2013, pp. e233-240, DOI : 10.4317/medoral.18772 , PMID 23385513 , PMC 3613874 .
- ^ ( EN ) Kessler P, et al , Neoadjuvant and adjuvant therapy in patients with oral squamous cell carcinoma Long-term survival in a prospective, non-randomized study ( abstract ), in Br J Oral Maxillofac Surg , vol. 46, n. 1, Elsevier, gennaio 2008, pp. 1-5, DOI : 10.1016/j.bjoms.2007.08.006 , PMID 17931758 . URL consultato il 20 gennaio 2013 .
- ^ ( EN ) Bossi P, et al , Preoperative chemotherapy in advanced resectable OCSCC: long-term results of a randomized phase III trial , in Ann Oncol , vol. 25, n. 2, Oxford University Press, febbraio 2014, pp. 462-466, DOI : 10.1093/annonc/mdt555 , PMID 24401930 .
- ^ ( EN ) Chinn SB, et al , Efficacy of induction selection chemotherapy vs primary surgery for patients with advanced oral cavity carcinoma , in JAMA Otolaryngol Head Neck Surg , vol. 140, n. 2, American Medical Association, febbraio 2014, pp. 134-142, DOI : 10.1001/jamaoto.2013.5892 , PMID 24370563 , PMC 4103099 .
- ^ ( EN ) Cankovic M, et al , The histological characteristics of clinically normal mucosa adjacent to oral cancer , in J Cancer Res Ther , vol. 9, n. 2, Wolters Kluwer, aprile-giugno 2013, pp. 240-244, DOI : 10.4103/0973-1482.113365 , PMID 23771366 .
- ^ ( EN ) Ravi SB, Annavajjula S, Surgical margins and its evaluation in oral cancer: a review , in J Clin Diagn Res , vol. 8, n. 9, JCDR Research and Publications, settembre 2014, pp. ZE01-5, DOI :10.7860/JCDR/2014/9755.4836 , PMID 25386547 , PMC 4225999 .
- ^ ( EN ) Ravi SB, et al , Long term results of sentinel lymph node biopsy in early oral squamous cell carcinoma , in Onco Targets Ther , vol. 6, Dove Press, 25 giugno 2013, pp. 799-802, DOI : 10.2147/OTT.S43446 , PMID 23836993 , PMC 3699346 .
- ^ ( EN ) Bassi KK, et al , The first and second echelon sentinel lymph node evaluation in oral cancer , in Indian J Surg , vol. 75, n. 5, Springer, ottobre 2013, pp. 377-382, DOI : 10.1007/s12262-012-0497-5 , PMID 24426480 , PMC 3824774 .
- ^ ( EN ) George RK, Krishnamurthy A, Microsurgical free flaps: Controversies in maxillofacial reconstruction , in Ann Maxillofac Surg , vol. 3, n. 1, Wolters Kluwer, gennaio 2013, pp. 72-79, DOI : 10.4103/2231-0746.110059 , PMID 23662264 , PMC 3645616 .
- ^ ( EN ) Singh S, Singh RK, Pandey M, Nasolabial flap reconstruction in oral cancer , in World J Surg Oncol , vol. 10, Springer, 30 ottobre 2012, p. 227, DOI : 10.1186/1477-7819-10-227 , PMID 23110587 , PMC 3544680 .
- ^ ( EN ) Romeo U, et al , Soft tissue management and prosthetic rehabilitation in a tongue cancer patient , in Case Rep Dent , vol. 2013, Hindawi, 2013, p. 475186, DOI : 10.1155/2013/475186 , PMID 24319601 , PMC 3844260 .
- ^ ( EN ) Azuma M, et al , Mandibular reconstruction using plates prebent to fit rapid prototyping 3-dimensional printing models ameliorates contour deformity , in Head Face Med , vol. 10, Springer, 23 ottobre 2014, p. 45, DOI : 10.1186/1746-160X-10-45 , PMID 25338640 , PMC 4213462 .
- ^ ( EN ) Deshmukh A, et al , Tongue flap revisited , in J Cancer Res Ther , vol. 9, n. 2, Wolters Kluwer, aprile-giugno 2013, pp. 215-218, DOI : 10.4103/0973-1482.113354 , PMID 23771361 .
- ^ ( EN ) Wang X, et al , Functional tongue reconstruction with the anterolateral thigh flap , in World J Surg Oncol , vol. 11, Springer, 25 novembre 2013, p. 303, DOI : 10.1186/1477-7819-11-303 , PMID 24274671 , PMC 3879093 .
- ^ ( EN ) Mantri SS, et al , Scope of prosthodontic services for patients with head and neck cancer , in Indian J Cancer , vol. 49, n. 1, Wolters Kluwer, gennaio-marzo 2012, pp. 39-45, DOI : 10.4103/0019-509X.98917 , PMID 22842167 .
- ^ ( EN ) Fierz J, Hallermann W, Mericske-Stern R, Patients with oral tumors. Part 1: Prosthetic rehabilitation following tumor resection , in Schweiz Monatsschr Zahnmed , vol. 123, n. 2, 2013, pp. 91-105, PMID 23512240 . URL consultato il 2 giugno 2015 .
- ^ ( EN ) Tarsitano A, et al , Functional results of microvascular reconstruction after hemiglossectomy: free anterolateral thigh flap versus free forearm flap , in Acta Otorhinolaryngol Ital , vol. 33, n. 6, Pacini Editore, dicembre 2013, pp. 374-379, PMID 24376292 , PMC 3870442 .
- ^ ( EN ) Studer G, et al , Follow up after IMRT in oral cavity cancer: update , in Radiat Oncol , n. 7, Bio Med Central, 11 giugno 2012, p. 84, DOI : 10.1186/1748-717X-7-84 , PMID 22686297 , PMC 3488022 .
- ^ ( EN ) Yamazaki H, et al , High dose rate brachytherapy for oral cancer , in J Radiat Res , vol. 54, n. 1, Oxford University Press, gennaio 2013, pp. 1-17, DOI : 10.1093/jrr/rrs103 , PMID 23179377 , PMC 3534285 .
- ^ ( EN ) Liu Z, Huang S, Zhang D, High dose rate versus low dose rate brachytherapy for oral cancer--a meta-analysis of clinical trials , in PLOS One , vol. 8, n. 6, PLOS, 10 giugno 2013, p. e65423, DOI : 10.1371/journal.pone.0065423 , PMID 23762369 , PMC 3677879 .
- ^ a b ( EN ) Matsumoto K, et al , Treatment outcome of high-dose-rate interstitial radiation therapy for patients with stage I and II mobile tongue cancer , in Jpn J Clin Oncol , vol. 43, n. 10, Oxford University Press, ottobre 2013, pp. 1012-1017, DOI : 10.1093/jjco/hyt108 , PMID 23906605 .
- ^ ( EN ) Unetsubo T, et al , High-dose-rate brachytherapy using molds for lip and oral cavity tumors , in Radiat Oncol , vol. 10, n. 1, Oxford University Press, 8 aprile 2015, p. 81, DOI : 10.1186/s13014-015-0390-z , PMID 25888772 .
- ^ ( EN ) Tano T, et al , Immunochemoradiotherapy for patients with oral squamous cell carcinoma: augmentation of OK-432-induced helper T cell 1 response by 5-FU and X-ray irradiation , in Neoplasia , vol. 15, n. 7, Neoplasia Press, luglio 2013, pp. 805-814, PMID 23814492 , PMC 3689243 .
- ^ ( EN ) Vermorken JB, et al , Platinum-based chemotherapy plus cetuximab in head and neck cancer , in N Engl J Med , vol. 359, n. 11, Massachusetts Medical Society, 11 settembre 2008, pp. 1116-1127, DOI : 10.1056/NEJMoa0802656 , PMID 18784101 .
- ^ ( EN ) Hannouf MB, et al , Cost-effectiveness of adding cetuximab to platinum-based chemotherapy for first-line treatment of recurrent or metastatic head and neck cancer , in PLOS ONE , vol. 7, n. 6, Public Library of Science, 20 giugno 2012, pp. e38557, DOI : 10.1371/journal.pone.0038557 , PMID 22745668 , PMC 3379991 .
- ^ ( EN ) Li Y, et al , Selective intra-arterial infusion of rAd-p53 with chemotherapy for advanced oral cancer: a randomized clinical trial , in BMC Med , vol. 12, BioMed Central, 30 gennaio 2014, p. 16, DOI : 10.1186/1741-7015-12-16 , PMID 24479409 , PMC 3922639 .
- ^ ( EN ) Wolff KD, Follmann M, Nast A, The diagnosis and treatment of oral cavity cancer , in Dtsch Arztebl Int , vol. 109, n. 48, Deutscher Arzte-Verlag GmbH, novembre 2012, pp. 829-835, DOI : 10.3238/arztebl.2012.0829 , PMID 23248713 , PMC 3523261 .
- ^ ( EN ) Wang B, et al , The recurrence and survival of oral squamous cell carcinoma: a report of 275 cases , in Chin J Cancer , vol. 32, n. 11, Springer, novembre 2013, pp. 614-618, DOI : 10.5732/cjc.012.10219 , PMID 23601241 , PMC 3845544 .
- ^ ( EN ) Kreppel M, et al , Prognostic value of the sixth edition of the UICC's TNM classification and stage grouping for oral cancer ( abstract ), in J Surg Oncol , vol. 102, n. 5, John Wiley & Sons, 1º ottobre 2010, pp. 443-449, DOI : 10.1002/jso.21547 , PMID 20872947 . URL consultato l'11 febbraio 2013 .
- ^ ( EN ) de Araújo RF Jr, et al , Prognostic significance of the anatomical location and TNM clinical classification in oral squamous cell carcinoma ( PDF ), in Med Oral Patol Oral Cir Bucal , vol. 13, n. 6, 1º giugno 2008, pp. E344-347, PMID 17931758 . URL consultato l'11 febbraio 2013 .
- ^ ( EN ) Fan Y, et al , Survival analysis of oral squamous cell carcinoma in a subgroup of young patients , in Asian Pac J Cancer Prev , vol. 15, n. 20, 2014, pp. 8887-8891, DOI : 10.7314/APJCP.2014.15.20.8887 , PMID 25374224 .
- ^ ( EN ) Patel SG, et al , Lymph node density in oral cavity cancer: results of the International Consortium for Outcomes Research , in Br J Cancer , vol. 109, n. 8, Nature Publishing Group, 15 ottobre 2013, pp. 2087-2095, DOI : 10.1038/bjc.2013.570 , PMID 24064974 , PMC 3798966 .
- ^ ( EN ) aa.vv. , SEER Survival Monograph: Cancer Survival Among Adults: US SEER Program, 1988-2001, Patient and Tumor Characteristics ( PDF ), NHI, 2007, p. 15.
- ^ ( EN ) Sopravvivenza: i dati dei Registri tumori ( PDF ), in I tumori in Italia - Rapporto 2007 , Associazione italiana dei registri tumori (AIRTUM). URL consultato il 12 febbraio 2013 (archiviato dall' url originale il 16 aprile 2015) .
- ^ ( EN ) Pereira MC, Oliveira DT, Landman G, Kowalski LP, Histologic subtypes of oral squamous cell carcinoma: prognostic relevance ( PDF ), in J Can Dent Assoc , vol. 73, n. 4, Canadian Dental Association, maggio 2007, pp. 339-344, PMID 17484800 . URL consultato l'11 febbraio 2013 .
- ^ ( EN ) Sharma M, et al , Molecular changes in invasive front of oral cancer , in J Oral Maxillofac Pathol , vol. 17, n. 2, Wolters Kluwer, maggio 2013, pp. 240-247, DOI : 10.4103/0973-029X.119740 , PMID 24250086 , PMC 3830234 .
- ^ ( EN ) Jadhav KB, Gupta N, Clinicopathological prognostic implicators of oral squamous cell carcinoma: need to understand and revise , in N Am J Med Sci , vol. 5, n. 12, Wolters Kluwer, dicembre 2013, pp. 671-679, DOI : 10.4103/1947-2714.123239 , PMID 24404549 , PMC 3877528 .
- ^ ( EN ) Hsin CH, et al , High level of plasma matrix metalloproteinase-11 is associated with clinicopathological characteristics in patients with oral squamous cell carcinoma , in PLOS ONE , vol. 9, n. 11, Public Library of Science, 25 novembre 2014, pp. e113129, DOI : 10.1371/journal.pone.0113129 , PMID 25423087 , PMC 4244114 .
- ^ ( EN ) Morris LG, Ganly I,Outcomes of oral cavity squamous cell carcinoma in pediatric patients , in Oral Oncol , vol. 46, n. 4, Elsevier, aprile 2010, pp. 292-296, DOI : 10.1016/j.oraloncology.2010.01.015 , PMID 20188621 , PMC 2889246 .
- ^ ( EN ) Panzarella V, et al , Diagnostic delay in oral squamous cell carcinoma: the role of cognitive and psychological variables , in Int J Oral Sci , vol. 6, n. 1, Nature Publishing Group, marzo 2014, pp. 39-45, DOI : 10.1038/ijos.2013.88 , PMID 24287962 , PMC 3967306 .
- ^ I dentisti sentinella dichiarano guerra al cancro della bocca , su portale.fnomceo.it , FNOMCeO. URL consultato il 1º febbraio 2013 (archiviato dall' url originale il 7 marzo 2016) .
- ^ Lo Muzio L, Il carcinoma orale progetto di prevenzione primaria e secondaria per operatori sanitari odontoiatrici “tacco” (tetra azione contro cancro orale) ( PDF ), su omco.pd.it , FNOMCeO. URL consultato il 1º febbraio 2013 .
- ^ Le iniziative di ANDI e Fondazione ANDI a tutela della salute orale , su fondazioneandi.org , Fondazione ANDI Onlus. URL consultato il 18 gennaio 2013 .
- ^ Oral Cancer Day , su oralcancerday.it , Associazione Nazionale Dentisti Italiani. URL consultato il 16 luglio 2013 (archiviato dall' url originale il 23 luglio 2013) .
Bibliografia
- Stanley L. Robbins, Ramzi S. Cotran; Vinay Kumar, La basi patologiche delle malattie , II, 4ª ed., Padova, Piccin, 1992 [1989] , pp. 937-938, ISBN 88-299-1083-X .
- Bruno De Michelis, Remo Modica; Giorgio Re, Clinica Odontostomatologica , Edizioni Minerva Medica, 1992, pp. 339-348, ISBN 88-7711-146-1 .
- Fabrizio Montagna, Giuseppe Ferronato; Franco Martinelli, Patologia orale orientata per problemi: diagnosi differenziale e terapia , Edizioni Promoass, 2000, pp. 63-68, 324, ISBN 88-87109-02-8 .
- Vito Terribile Wiel Marin, Lezioni di Anatomia Patologica Odontostomatologica , Cleup editrice, 1992, pp. 81-93, ISBN 88-7178-163-5 .
- Stella Blandamura Piazza, Elementi di citologia del cavo orale , Cleup editrice, 1993, pp. 58-63, ISBN 88-7178-212-7 .
Voci correlate
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su carcinoma della bocca
Wikimedia Commons contiene immagini o altri file su carcinoma della bocca
Collegamenti esterni
- Faq sul cancro orale a cura della Società Italiana di Patologia e Medicina Orale (SIPMO) , su sipmo.it .
- AIRC – Associazione Italiana Ricerca sul cancro: Tumore alla bocca , su airc.it .
- ( EN ) - Tumore orale nel sito del National Cancer Institute , su cancer.gov .
- ( EN ) - Tumore orale nel sito dei Centers for Disease Control and Prevention
- ( EN ) - sito della Oral Cancer Foundation, associazione non profit americana , su oralcancerfoundation.org .
| Controllo di autorità | LCCN ( EN ) sh92005236 · GND ( DE ) 4040733-0 · NDL ( EN , JA ) 00575602 |
|---|