Disecția aortică
| Disecția aortică | |
|---|---|
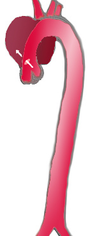
| Disecția aortei descendente (3), care începe de la subclavia stângă, până la aorta abdominală (4). Aorta ascendentă (1) și arcada aortică (2) nu sunt afectate. | |
| Specialitate | Chirurgie vasculară |
| Clasificare și resurse externe (EN) | |
| ICD-9 -CM | 441,0 |
| ICD-10 | I71.0 |
| OMIM | 607086 |
| MedlinePlus | 000181 |
| eMedicină | 756835 |
| GeneReviews | Prezentare generală |
| Sinonime | |
| Disecția aortică Disecția aortei Disecția aortei | |
Disecția sau disecția aortică este o boală vasculară relativ rară, împovărată de mortalitate ridicată dacă nu este tratată cu o intervenție chirurgicală de urgență. [1] Apare atunci când o leziune a stratului interior al aortei permite curgerea sângelui între straturile peretelui aortic, forțându-i să se separe. În acest fel, se produce alunecarea tunicii intime a vazei odată cu formarea unui al doilea lumen numit „lumen fals”. [2] În majoritatea cazurilor, disecția este asociată cu apariția durerii toracice anterioare (dar uneori spate) bruste și severe, adesea descrisă de pacienți ca durere de rupere. [3] [4] Mulți pacienți raportează alte simptome precum vărsături , transpirații abundente și amețeli . Alte simptome pot apărea din scăderea fluxului sanguin către alte organe: simptomele neurologice apar relativ frecvent, inclusiv accident vascular cerebral , [5] [6] [7] sau ischemie mezenterică . [8] [9] Disecția aortică poate duce rapid la moarte din cauza fluxului sanguin insuficient către inimă sau a unei rupturi a aortei în sine. Disecția aortică este mai frecventă la persoanele cu antecedente de hipertensiune arterială , unele afecțiuni ale țesutului conjunctiv care afectează peretele vaselor de sânge și cauzează slăbirea structurală (cum ar fi sindromul Marfan , [10] [11] la cei cu valvă aortică bicuspidă și la subiecți care au suferit anterior o intervenție chirurgicală pe inimă. [2] Traumatisme majore, fumatul de tutun , consumul de cocaină , [12] [13] sarcina , [14] Un diagnostic de anevrism aortic toracic, vasculită care implică arterele și niveluri anormale de lipide sunt toate asociate cu o risc crescut. [3] Diagnosticul este suspectat pe baza simptomelor pacientului și confirmat prin efectuarea de imagini radiologice (ecografie abdominală sau tomografie abdominală sau RMN : aceste teste sunt utilizate nu numai pentru confirmarea diagnosticului, ci și pentru o mai bună definiție a locului și a amplorii a disecției. Principalii factori de disecție sunt Stanford tip A (implicarea primei părți a aortei) și tip B (absența implicării). [3]
Prevenirea bolii se bazează pe un control bun al tensiunii arteriale și încetarea fumatului. Tratamentul disecției aortice depinde de ce parte a aortei a fost implicată. Chirurgia este de obicei necesară pentru disecțiile care implică prima parte a aortei; dimpotrivă, disecțiile care nu implică aorta ascendentă pot fi tratate și cu medicamente care reduc tensiunea arterială și ritmul cardiac, cu excepția cazului în care apar complicații . Tratamentul chirurgical poate fi efectuat în aer liber (cu o incizură care implică deschiderea pieptului) sau recurgând la o reparație endovasculară a anevrismului (se introduce o proteză vasculară în sacul anevrismului care trece prin artera femurală).
Disecția aortică este un eveniment relativ rar și are loc la o rată estimată de 3 la 100.000 de persoane pe an. [3] [2] Este mai frecvent la bărbați decât la femele. [3] De obicei, vârsta la diagnostic este de 63 de ani, aproximativ 10% din cazuri apărând înainte de vârsta de 40 de ani. [2] Fără tratament, aproximativ jumătate dintre persoanele cu morfologie de tip A mor în decurs de trei zile și aproximativ 10% dintre persoanele cu morfologie de tip B mor în decurs de o lună.
Clasificare
 |  |  | |
| Procent | 60% | 10-15% | 25-30% |
| Tipologie | DeBakey I | DeBakey II | DeBakey III |
| Stanford A (Proximal) | Stanford B (Distal) | ||
Diferite sisteme de clasificare au fost utilizate pentru a descrie disecția aortică. O clasificare frecvent utilizată se bazează pe criteriul temporal, adică durata apariției simptomelor înainte de prezentare: disecțiile aortice sunt etichetate ca hiperacute (durata <24 ore), acute (2-7 zile), subacute (8-30 zile) și cronice (> 30 de zile). [15] Alte sisteme de clasificare utilizate în mod obișnuit se bazează pe locația anatomică în care apare această patologie (în special aorta ascendentă sau descendentă). Sistemul Stanford este probabil cel mai frecvent utilizat astăzi, deoarece este mai adaptat la managementul pacienților.
- DeBakey
Sistemul DeBakey (numit după chirurgul cardiac toracic Michael E. DeBakey) oferă o descriere anatomică a disecției aortice. Acesta clasifică disecția pe baza locului în care este localizată ruptura intimă originală și pe baza întinderii disecției (localizarea în aorta ascendentă sau descendentă sau implicarea atât aortei ascendente, cât și descendente. [16]
- Tipul I - apare în aorta ascendentă și se extinde (implică aorta ascendentă, arcada aortică și aorta toracică). Este observat cel mai adesea la pacienții cu vârsta sub 65 de ani și este cea mai mortală formă a bolii.
- Tipul II - își are originea și se limitează la aorta ascendentă
- Tipul III - implică aorta descendentă distală până la originea arterei subclaviene. Cel mai adesea observat la pacienții vârstnici cu ateroscleroză și hipertensiune arterială.
- Tipul IIIa - limitat la aorta toracică descendentă
- Tipul IIIb - implică aorta toracică și abdominală
- Stanford
Clasificarea Stanford este împărțită în două grupe, A și B, în funcție de implicarea sau nu aortei ascendente. [17]
- Tipul A - (proximal sau ascendent) este implicată aorta ascendentă și / sau arcada aortică, putându-se extinde spre aorta descendentă. Include tipurile DeBakey I și II.
- Tipul B - (distală sau descendentă) aorta descendentă este implicată distal până la artera subclaviană stângă cu sau fără extensie distală. Include tipul DeBakey III.
- Descriptiv
- Proximal - DeBakey tip I și II și Stanford tip A
- Distal - DeBakey de tip III și Stanford de tip B.
Clasificarea Stanford este utilă în următoarea practică clinică: de fapt, disecțiile ascendente de aorta de tip A necesită, în general, tratament chirurgical primar; spre deosebire de disecțiile de tip B, tratamentul farmacologic (morfină, beta-blocante și vasodilatatoare arteriale) este în general rezervat, cel puțin inițial, în timp ce intervenția chirurgicală este rezervată pentru orice complicații. Motivul reparării chirurgicale a disecțiilor de tip A este că disecțiile ascendente aortice implică adesea valva aortică, care, după ce și-a pierdut suportul suspensiv, împinge spre rădăcina aortică, provocând astfel insuficiență aortică. Valva trebuie astfel resuspendată și repoziționată corespunzător, precum și repararea deseori a leziunilor care afectează artera coronară. În plus, zona implicată în disecție este îndepărtată și înlocuită cu o grefă Dacron, pentru a preveni apariția unei disecții suplimentare. În cele din urmă, trebuie avut în vedere faptul că disecțiile de tip B rareori au o evoluție mai bună, din punctul de vedere al mortalității, dacă sunt supuse unei intervenții chirurgicale, cu excepția cazului în care există rupturi sau compromisuri ale altor organe, de exemplu rinichii. Aproximativ 70% din disecții apar în tractul ascendent, care este, de asemenea, cel mai periculos punct pentru supraviețuirea pacientului.
Simptomatologie
Aproximativ 96% dintre subiecții cu disecție aortică vin la medic acuzând o durere severă cu debut brusc, adesea în deplină stare de bine (așa-numita durere „lovitură de pumnal”). [18] [19] Durerea poate fi descrisă ca o senzație de rupere, înjunghiere sau ascuțită. 17% dintre indivizi simt că durerea se mișcă pe măsură ce disecția se extinde de-a lungul aortei (denumită durere toracică „migratoare”). Localizarea durerii este asociată cu localizarea disecției. Durerea toracică anterioară sau precordială este asociată cu disecția care implică aorta ascendentă , în timp ce durerea interscapulară (dorsală) este asociată cu disecția aortică care afectează aorta descendentă . Dacă durerea este de natură pleuritică, poate sugera pericardită acută cauzată de sângerări în sacul pericardic . Aceasta este o eventualitate deosebit de periculoasă și trebuie să ne temem de apariția iminentă a tamponării cardiace acute. Tamponarea pericardică este cea mai frecventă cauză de deces prin disecție aortică. [20] În timp ce durerea poate fi confundată cu durerea asociată în mod tipic cu sindromul coronarian acut (infarct miocardic), disecția aortică nu este de obicei asociată cu alte semne care sugerează infarctul miocardic (de exemplu, ECG . Cu toate acestea, în evoluția bolii este posibil ca simptomele să sugereze de insuficiență cardiacă congestivă poate apărea.
Mai rar, dar este posibil ca unii indivizi să nu prezinte durere sau mai des să fie paucisimptomatici: acești subiecți au, în general, disecție aortică cronică.
Simptomele mai puțin frecvente care pot fi observate în contextul disecției aortice includ insuficiența cardiacă congestivă menționată anterior (7%), sincopa (9%), accident vascular cerebral (6%), neuropatie ischemică periferică, paraplegie și stop cardiac . [21] Dacă o persoană cu disecție aortică a prezentat un episod de sincopă, în aproximativ 50% din cazuri se datorează sângerării din sacul pericardic, care a provocat tamponarea pericardică.
Complicațiile neurologice ale disecției aortice (cum ar fi accident vascular cerebral sau plegie) se datorează de obicei implicării uneia sau mai multor artere care alimentează o anumită zonă a sistemului nervos central .
Dacă disecția se extinde la sinusul coronarian , se poate stabili o afecțiune a ischemiei miocardice care, dacă nu este tratată imediat, ar putea duce la infarct miocardic . Un alt semn util în scop diagnostic, deși destul de inconstant, este un murmur din insuficiența aortică (atribuibil modificării hemodinamice stabilite în aorta).
Dacă disecția aortică implică aorta abdominală, este posibil ca și unele dintre ramurile acestui vas să fie compromise. În disecțiile aortice abdominale, compromiterea uneia sau a ambelor artere renale apare în 5-8% din cazuri, în timp ce ischemia mezenterică (ischemia intestinului) apare la aproximativ 3% dintre subiecți. [8] [9]
Tensiune arteriala
Pacienții cu disecție aortică au adesea antecedente de hipertensiune arterială. Tensiunea arterială a subiecților care prezintă disecție acută aortică este destul de variabilă și tinde să fie mai mare la persoanele care au disecție distală. La subiecții cu disecție aortică proximală, aproximativ 36% prezintă hipertensiune, în timp ce 25% prezintă hipotensiune. Disecția proximală aortică tinde să fie mai asociată cu slăbirea peretelui vascular datorită degenerescenței chistice mediale. La cei cu disecție aortică distală (tip B), 60-70% prezintă hipertensiune, în timp ce 2-3% prezintă tensiune arterială scăzută. [22]
Hipotensiunea arterială severă la momentul prezentării pacientului într-un centru medical este un indicator pronostic serios. De obicei, este asociat cu o situație de tamponadă pericardică, insuficiență aortică severă sau ruptură aortei. Măsurarea exactă a tensiunii arteriale este importantă. Pseudohipotensiunea (o măsurare falsă a tensiunii arteriale) poate apărea din cauza implicării arterei brahiocefalice (care alimentează brațul drept) sau a arterei subclaviene stângi (care alimentează brațul stâng).
Insuficiență aortică
Insuficiența aortică (AI) apare la 50% și până la 66% din disecțiile ascendente aortice: la nivel auscultator, murmurul diastolic datorat insuficienței aortice este audibil în aproximativ 32% din disecțiile proximale. Volumul zgomotului depinde de tensiunea arterială, deci este posibil să nu fie audibil în caz de tensiune arterială scăzută. Există mai multe cauze posibile pentru apariția insuficienței aortice (AI) în caz de disecție aortică ascendentă. Disecția poate dilata inelul supapei aortice, astfel încât clapetele supapei să nu se mai poată juxtapune. Un alt mecanism posibil este acela că disecția se poate extinde în rădăcina aortică și poate provoca detașarea clapetelor supapei. Un alt mecanism posibil este asociat cu o lacerare intimă mare: în acest caz clapeta intimă poate prolabora în tractul de ieșire al ventriculului stâng, provocând o intimă intimă în valva aortică și împiedicând astfel închiderea corectă a supapei.
Infarct miocardic
Infarctul miocardic apare la 1-2% din disecțiile aortice. Cauza infarctului este de obicei implicarea arterelor coronare , care alimentează inima cu sânge oxigenat, în disecție. Artera coronariană dreaptă este implicată mai des decât artera coronară stângă. Dacă infarctul miocardic este tratat cu terapie trombolitică, mortalitatea crește cu peste 70%, în principal din cauza sângerărilor care apar în sacul pericardic și provoacă tamponare cardiacă. Deoarece persoanele cu disecție aortică se prezintă adesea în camera de urgență cu simptome similare cu cele ale unui infarct miocardic, medicul de urgență trebuie să fie atent pentru a pune diagnosticul corect înainte de a începe tratamentul specific pentru infarct, deoarece regimul de tratament pentru această patologie poate fi letal pentru o persoană care are în schimb disecție aortică.
Revărsat pleural
Un revărsat pleural (adică o colecție de lichid în spațiul pleural, între plămâni și peretele toracic sau diafragma ) poate fi prezent la persoanele cu disecție aortică și se datorează atât sângelui care poate rezulta dintr-o ruptură tranzitorie a aortei. Și pentru colectarea fluidului secundar unei reacții inflamatorii în jurul aortei. În cazul în care se dezvoltă un revărsat pleural din cauza disecției aortice, acest lucru apare mai frecvent în toracele stâng decât în toracele drept.
Etiologie
Disecția aortică este asociată cu hipertensiune arterială (aproximativ 72-80% dintre persoanele cu disecție aortică au antecedente de hipertensiune arterială) și multe tulburări ale țesutului conjunctiv. O formă de vasculită (un proces inflamator care afectează o arteră) poate fi uneori, deși rar, asociată cu disecția aortică. Această boală într-o minoritate de cazuri poate fi, de asemenea, rezultatul unui traumatism toracic. Utilizarea drogurilor ilicite cu stimulente (de exemplu, cocaină [12] [13] și metamfetamină ) reprezintă un factor de risc suplimentar modificabil pentru disecția aortică. Acest lucru pare a fi asociat cu fumul de tutun la unele persoane.
O valvă aortică bicuspidă (o formă rară de anomalie cardiovasculară congenitală care implică valva aortică) se găsește la 7-14% dintre persoanele care au disecție aortică. Acești indivizi sunt deosebit de predispuși să dezvolte disecția aortei ascendente. Riscul de disecție la subiecții cu valvă aortică bicuspidă nu este asociat cu gradul de stenoză valvulară.
Anumite tulburări ale țesutului conjunctiv, cum ar fi sindromul Marfan , [10] [11] sindromul Ehlers-Danlos , [23] și sindromul Loeys-Dietz cresc riscul de disecție aortică. [22] În mod similar, unele vasculite, cum ar fi arterita lui Takayasu, arterita cucelule uriașe , poliarterita nodoză și boala Behçet, au fost asociate cu posibilitatea dezvoltării unei disecții aortice ulterioare. [22] [15] Sindromul Marfan se găsește la 5-9% dintre persoanele care au avut disecție aortică. În acest subgrup, incidența la persoanele tinere a crescut. Persoanele cu sindrom Marfan tind să aibă anevrisme aortice și sunt mai predispuse la disecții aortice proximale. [10]
Alte sindroame congenitale precum Turner , [24] [25] și Noonan , [26] sunt, de asemenea, asociate cu un risc crescut de disecție aortică, de obicei după dilatarea rădăcinii aortice.
Traumatismele toracice care pot implica disecția aortică pot fi împărțite în două grupe, diferențiate prin cauză: traumatism toracic închis (observat frecvent după un accident auto) și traumatism toracic iatrogen (asociat cu proceduri de cardiologie chirurgicală sau intervențională). Cauzele iatrogene includ traume care apar în timpul procedurilor de cateterism cardiac sau legate de umflarea unui balon intra-aortic.
Disecția aortică poate fi o consecință tardivă a chirurgiei cardiace. Aproximativ 18% dintre persoanele cu disecție acută aortică au un istoric personal de intervenție chirurgicală pe cord deschis. Persoanele supuse înlocuirii valvei aortice pentru regurgitația aortică prezintă un risc deosebit, deoarece regurgitația aortică implică un flux sanguin crescut în aorta ascendentă. Acest lucru poate provoca dilatarea și slăbirea pereților aortei ascendente.
Sifilisul în faza terțiară poate provoca disecția aortică.
Fiziopatologie
Ca toate celelalte artere, aorta este alcătuită din trei straturi, intima, mediile și adventitia. Intima este în contact direct cu sângele din interiorul vasului și constă în principal dintr-un strat de celule endoteliale care se sprijină pe o membrană bazală ; tunica media este alcătuită în principal din țesut conjunctiv și muscular și vasul este protejat la exterior de tunica accidentală, care include și țesutul conjunctiv. [27] În disecția aortică, sângele intră în intim și intră în stratul mediu. Presiunea ridicată rupe țesutul suport al tunicii media prin unlaminarea celor două treimi interne și împărțirea acestora de adventitia, adică de treimea suport externă. [28] Acest eveniment se poate propaga de-a lungul lungimii aortei pe o distanță variabilă, înainte sau înapoi. Disecțiile care se propagă către bifurcația iliacă (adică în urma fluxului sanguin) se numesc disecții anterograde și cele care se propagă către rădăcina aortică (opusă fluxului sanguin) sunt numite disecții retrograde. Lacrima inițială apare de obicei la o distanță de 100 mm de valva aortică: ca urmare, disecția retrogradă poate compromite cu ușurință pericardul și poate duce la un hemopericard. Disecțiile anterogradelor se pot propaga către bifurcația iliacă a aortei, pot rupe peretele aortic sau se recanalizează în lumenul intravascular, ducând la o aortă „dublă”. Aorta cu două țevi scade presiunea fluxului sanguin și, prin urmare, reduce riscul de rupere. Dacă disecția aortică se rupe, hemoragia apare într-o cavitate corporală: prognosticul depinde de locul afectat de ruptură. Sunt posibile atât rupturi retroperitoneale cât și pericardice.
Evenimentul inițial în disecția aortică este o ruptură în mucoasa intimă a aortei. Datorită presiunilor ridicate din vas, sângele este capabil să pătrundă în tunica mijlocie în punctul de lacerare. Forța sângelui care reușește să pătrundă în sutana din mijloc face ca lacerarea să se extindă. Sângele se deplasează prin tonicul mediu creând un lumen fals: lacrima se extinde de obicei distal (departe de inimă), dar se poate extinde atât proximal, cât și în ambele direcții (adevăratul lumen este canalul normal de sânge din aortă). Separarea lumenului fals de lumenul adevărat este reprezentată de un strat de țesut intim cunoscut sub numele de lamboul intim.
Marea majoritate a disecțiilor aortice își au originea cu o ruptură intimă fie în aorta ascendentă (65%), arcada aortică (10%), fie doar distală de ligamentul arterial în aorta toracică descendentă (20%). De îndată ce sângele începe să curgă în lumenul fals, pot apărea lacrimi secundare în interior. Prin aceste lacerații secundare, sângele poate intra din nou în lumenul adevărat. Deși nu este întotdeauna clar de ce apare o lacrimă intimă, de multe ori implică degenerarea colagenului și elastinei, care sunt constituenții fundamentali ai tunicii mediale. Această situație este cunoscută sub numele de necroză chistică medială și este mai frecvent asociată cu sindromul Marfan, precum și cu sindromul Ehlers-Danlos.
În aproximativ 13% din disecțiile aortice, nu există dovezi ale unei rupturi intime. În aceste cazuri, evenimentul declanșator este considerat a fi un hematom intramural (probabil cauzat de sângerări în mass-media). Deoarece nu există o legătură directă între lumenul adevărat și lumenul fals în aceste cazuri, diagnosticarea unei disecții aortice utilizând arteriografie (aortografie) este dificilă dacă cauza este un hematom intramural.
Epidemiologie
Stabilirea incidenței disecției aortice într-o anumită populație este adesea dificilă, deoarece multe cazuri sunt diagnosticate numai după deces (ceea ce poate fi adesea atribuit unei alte cauze). De fapt, în cazul disecției aortice, diagnosticul greșit nu este neobișnuit. Disecția aortică afectează aproximativ 2,0-3,5 persoane din 100.000 de oameni în fiecare an. Studiile epidemiologice efectuate în Suedia sugerează că incidența disecției aortice poate fi în creștere. [29] Subiecții de sex masculin sunt mai frecvent afectați decât femeile: 65% din totalul persoanelor cu disecție aortică sunt de fapt bărbați. Vârsta medie la diagnostic este de aproximativ 63 de ani. [27] Dacă sunt luate în considerare femeile cu vârsta sub 40 de ani, jumătate din toate disecțiile aortice apar în timpul perioadei de sarcină (de obicei în al treilea trimestru sau în perioada postpartum timpurie). [30] [31] În general, disecția aortică apare la aproximativ 0,6% din sarcini.
Factori de risc
Factorii nemodificabili includ vârsta și bolile congenitale, cum ar fi valva aortică bicuspidă, sindromul Turner și bolile țesutului conjunctiv, cum ar fi sindromul Marfan . [10] [11] Factorii de risc modificabili (adică tratabili) sunt anevrismul ascendent al aortei toracice (pentru ateroscleroză , sifilis , traume și alte cauze), ateroscleroza și dislipidemia , fumatul și hipertensiunea arterială.
Cauzele morții
Moartea apare ca urmare a șocului după ruperea aortei și sângerări interne severe.
Riscul de rupere fulminant începe de la 40% la apariția simptomelor și crește cu 1% la fiecare oră; în termen de 24 de ore, riscul este mai mare de 60%.
Diagnostic
Disecția aortică este una dintre cele mai provocatoare situații de urgență din domeniul cardiologiei. Diagnosticul este adesea provocator, deoarece necesită utilizarea unor proceduri lungi și care necesită mult timp, care nu sunt întotdeauna disponibile în fiecare spital. [32] Deși colectarea unui istoric medical bun de la subiect poate fi puternic indicativă a disecției aortice, diagnosticul nu poate fi întotdeauna pus pe baza istoricului clinic și a rezultatelor examinării fizice numai. Diagnosticul de confirmare apare adesea numai după vizualizarea lamboului intim după imagistica radiologică. Pe de altă parte, rata ridicată a mortalității bolii (în special în faza acută) necesită o clarificare rapidă a diagnosticului (de obicei prin ecocardiografie transesofagiană, o tomografie toracică cu mediu de contrast iodat sau un RMN. Ultrasunete de înaltă frecvență) o capacitate de rezoluție ridicată datorită apropierii anatomice a aortei de esofag care permite realizarea unor imagini bune. Alte teste care pot fi utilizate includ o aortogramă sau o angiografie cu rezonanță magnetică a aortei. sensibil și specific în diagnosticul disecției aortice.
În general, alegerea tehnicii imagistice se bazează pe disponibilitatea modalității de testare în spital, stabilitatea pacientului și sensibilitatea și specificitatea examenului.
Suspiciune inițială
Orice durere bruscă severă din spate, piept sau abdomen, pentru care nu se poate găsi nicio altă explicație plauzibilă, trebuie să ducă la suspiciunea de disecție aortică sau anevrism aortic. În special dacă există alte constatări, de exemplu constatarea hipertensiunii arteriale (49% dintre pacienții cu disecție aortică), a unei presiuni diferențiale marcate (31%), a unui murmur diastolic (28%) sau a deficitelor neurologice focale (17%) suspiciunea de disecție aortică devine mai consistentă și există obligația de a efectua investigații suplimentare pentru a clarifica originea problemei.
D-dimer
Unii medici din procesul de evaluare a diagnosticului consideră utilă măsurarea nivelului de dimer D în sânge. Această determinare are valoare doar ca o predicție negativă, adică pentru a exclude o posibilă disecție: un nivel sub 500 ng / ml poate fi de fapt considerat un test împotriva diagnosticului de disecție aortică. [33] Cu toate acestea, se consideră că această abordare se aplică numai în cazurile considerate a fi cu „risc scăzut” și dacă este efectuată în termen de 24 de ore de la apariția simptomelor. [34] [35] Cu toate acestea, Asociația Americană a Inimii nu recomandă utilizarea acestui test în procesul de diagnostic, deoarece dovezile încă lipsesc. [36]
Raze x la piept

Radiografia toracică poate demonstra o modificare a morfologiei aortei toracice, care poate fi suspectată pentru disecția aortică. Clasic, constatarea unei extinderi mediastinale cu debut nou la radiografie este o constatare a sensibilității moderate pentru detectarea disecției ascendente aortice. Din păcate, această constatare este de specificitate scăzută, deoarece multe alte condiții pot provoca mărirea aparentă a mediastinului.
Alte descoperiri radiografice asociate cu disecția sunt:
- „Semnul calciului”: radiologul descrie o separare a intimei calcificate de marginea aortică externă de peste 10 mm.
- Revărsat pleural: este mai frecvent în disecțiile descendente ale aortei și este de obicei localizat pe partea stângă.
- Alte constatări: obliterarea butonului aortic, depresia bronhiului principal stâng, pierderea benzii paratraheale și deviația traheală.
Important, aproximativ 12-20% din disecțiile aortice sunt nedetectabile cu radiografia toracică; pertanto, una radiografia del torace "normale" non esclude la dissecazione aortica. Se vi è un alto sospetto clinico, può essere giustificato un test di imaging più sensibile (angio-TAC, angio-RMN oppure un'ecografia transesofagea).
Angio Tomografia computerizzata
L'angiografia con tomografia computerizzata è un test rapido e non invasivo che fornisce un'accurata valutazione tridimensionale dell'aorta e più in generale dell'albero arterioso. Queste immagini sono prodotte acquisendo molto rapidamente strati molto sottili del torace e dell'addome, affidando quindi a un sistema computerizzato la loro ricombinazione volta alla creazione di sezioni trasversali. Per delineare l'aorta con la precisione necessaria per effettuare una diagnosi corretta, è necessario iniettare un materiale di contrasto iodato in una vena periferica. Un'apposita apparecchiatura a pompa (iniettore automatico) inietta la quantità di mezzo di contrasto prestabilita e nei tempi opportuni. In sostanza si ha una gestione in tempo reale della modulazione del flusso di contrasto, in sincronia con le scansioni tomografiche del macchinario TAC. Questo tipo di scansione è programmata per acquisire le immagini quando il contrasto penetra nell'aorta. Le scansionei quindi proseguono man mano che il contrasto fluisce attraverso il vaso. La tecnica ha una sensibilità variabile dal 96 al 100% e una specificità dal 96 al 100%. Sfortunatamente l'angio-TAC spesso non è in grado di identificare il sito preciso ove è avvenuta la rottura intimale. Un'ulteriore svantaggio è dato dalla necessità di ricorrere a materiale di contrasto iodato.
Risonanza magnetica
La risonanza magnetica (RMN) può essere utilizzata dia per fare diagnosi che per una migliore valutazione della dissecazione aortica, con una sensibilità del 98% e una specificità del 98%. Un esame RMN dell'aorta comporta una ricostruzione tridimensionale dell'aorta, che consente al medico di determinare la posizione della lesione intimale, il coinvolgimento di eventuali altri vasi e ramificazioni, e di individuare eventuali lacerazioni secondarie. È un test non invasivo, non richiede l'uso di materiale di contrasto iodato e può rilevare e quantificare il grado di insufficienza aortica.
Lo svantaggio di questa modalità di imaging è soprattutto legato al fatto che la disponibilità dell'esame è ancora riservata ad un numero limitato di centri ospedalieri (spesso è disponibile solo in pochi ospedali di grandi dimensioni); inoltre le scansioni in risonanza magnetica richiedono tempi di esecuzione relativamente lunghi. L'esame presenta anche alcune controindicazioni specifiche. A causa dei campi magnetici ad alta intensità che vengono utilizzati durante l'esecuzione della risonanza magnetica, l'esame è controindicato nei soggetti con protesi metalliche. Un ulteriore problema è dato dal fatto che il paziente deve essere posizionato all'interno di un tubo di scansione di diametro di 60 cm, che può provocare un senso di oppressione e di claustrofobia.
Ecocardiografia
Dobbiamo distinguere tra ecocardiografia transtoracica - TTE (che identifica in modo affidabile una dissecazione dell'aorta ascendente) e l'ecocardiogramma transesofageo - TEE. Quest'ultimo è un tipo di esame relativamente affidabile nella diagnosi di dissecazione aortica, con una sensibilità fino al 98% e una specificità fino al 97%. L'esame permette di visualizzare un flap intimale flottante nel lume aortico: ovviamente è necessario verificare l'immagine in più proiezioni per essere certi che quella visualizzata non sia una falsa immagine (ad esempio un riverbero). È diventata una delle modalità di imaging più utilizzate per eseguire diagnosi in caso di sospetta dissecazione aortica. Si tratta infatti di un esame relativamente non invasivo (anche se nella modalità transesofagea richiede comunque che la sonda di ecocardiografia sia inserita nell'esofago del paziente, il quale si trova così ad ingoiarla). L'esame è particolarmente utile nella valutazione dell'insufficienza aortica, in caso di dissecazione aortica ascendente, per determinare se e quanto siano coinvolti gli osti (le origini) delle arterie coronarie. L'ecocardiogramma transesofageo può essere eseguito, in soggetti che cooperano, senza ricorrere alla sedazione; tuttavia la maggior parte dei centri, per un maggiore comfort del paziente, preferisce ricorrere ad una sedazione blanda (ad esempio 1-2 mg di midazolam ). Tra gi svantaggi dell'ecocardiografia TEE deve essere considerata l'incapacità di visualizzare l'aorta ascendente distale (il tratto iniziale dell'arco aortico) e l'aorta addominale discendente, la parte di vaso che decorre al di sotto dello stomaco. Un TEE può essere tecnicamente difficile da eseguire in soggetti con stenosi o varici esofagee.
Aortogramma
Un aortogramma prevede il posizionamento di un catetere nell'aorta e l'iniezione di materiale di contrasto durante l'esecuzione di radiografie dell'aorta. La procedura rientra più in generale fra le procedure arteriogarfiche ed è anche nota come aortografia. In un passato recente era considerata il gold standard diagnostico, ma oggigiorno è stata soppiantata da altre modalità di imaging meno invasive.
Trattamento
In una dissecazione acuta, la scelta del trattamento dipende dalla sede in cui si verifica lo scollamento delle tonache. Nel caso di dissecazione di Stanford di tipo A (coinvolgimento dell'aorta ascendente), il trattamento chirurgico è superiore al trattamento medico. Nel caso di dissecazione di Stanford di tipo B (coinvolgimento dell'aorta distale - incluse le dissezioni aortiche addominali), il trattamento medico è preferibile rispetto a quello chirurgico. Il rischio di morte dovuto a dissecazione aortica è più alto nelle prime ore dopo l'inizio della dissecazione e diminuisce in seguito. Per questo motivo, le strategie terapeutiche differiscono a seconda che ci si trovi di fronte a una dissecazione acuta rispetto a una dissezione cronica. Si ricorda che una dissecazione acuta è, per definizione, un evento per il quale il paziente si presenta all'attenzione del medico entro le prime due settimane. Se un soggetto riesce a sopravvivere a questo periodo finestra, la sua prognosi è migliore. Circa il 66% di tutte le dissezioni si presenta in fase acuta. Le persone che si presentano due settimane dopo l'inizio della dissecazione sono considerate affette da dissecazione aortica cronica. Questi individui in un certo qual modo si sono auto-selezionati, in quanto sopravvissuti all'episodio acuto e possono quindi essere trattati con terapia farmacologica, purché clinicamente ed emodinamicamente stabili.
Trattamento medico (farmacologico)
La dissecazione aortica si presenta generalmente come un'emergenza ipertensiva: ne consegue che l'obiettivo principale del trattamento medico è il rigoroso controllo della pressione arteriosa. Il trattamento iniziale deve infatti tendere ad arrestare la progressione dell'ematoma dissecante. La pressione sanguigna target dovrebbe essere una pressione arteriosa media (MAP) compresa tra i 60 ed i 75 mmHg o una pressione arteriosa anche più bassa, se tollerata dal paziente. La riduzione della pressione arteriosa con la quale il paziente si presenta alla valutazione medica deve avvenire gradualmente, e le diminuzioni iniziali non dovrebbero essere superiori al 20% circa della pressione basale. Un altro obiettivo fondamentale del trattamento iniziale è la riduzione della cosiddetta forza di taglio dP/dt (cioè della forza di espulsione del sangue dal ventricolo sinistro ). La gestione a lungo termine di ogni tipo di stress (fisico, emotivo e psicologico) è importante per ottenere un buon controllo della pressione arteriosa.
I farmaci betabloccanti sono il trattamento di prima linea per i pazienti con dissecazione aortica acuta e cronica. Nella dissecazione acuta, sono generalmente preferiti gli agenti ad azione rapida, in quanto possono essere somministrati per via endovenosa e presentano dosaggi più facili da regolare (ad esempio si ricorre all' esmololo , propranololo o labetalolo ). I farmaci vasodilatatori , ad esempio il nitroprussiato di sodio possono essere presi in considerazione per alcuni pazienti con pressione arteriosa estremamente alta, ma non dovrebbero mai essere utilizzati da soli, poiché spesso stimolano un aumento riflesso (e non desiderabile) della frequenza cardiaca . I farmaci calcio-antagonisti possono essere utilizzati nel trattamento della dissecazione aortica, in particolare se esiste una controindicazione all'uso dei betabloccanti. I bloccanti dei canali del calcio che vengono generalmente utilizzati sono il verapamil e il diltiazem , a causa dei loro effetti combinati vasodilatatori e inotropi negativi.
Se un paziente con dissecazione aortica si presenta con un'ipertensione arteriosa refrattaria (cioè un'ipertensione persistente nonostante il ricorso alle dosi massime previste di ben tre diverse classi di agenti antipertensivi), è necessario sospettare che la dissecazione aortica abbia coinvolto anche le arterie renali.
Trattamento chirurgico
Le indicazioni per il trattamento chirurgico della dissecazione aortica comprendono una dissecazione aortica prossimale acuta e una dissecazione aortica distale acuta ma gravata da una o più complicanze. Le complicanze che devono essere prese in considerazione includono la compromissione di un organo vitale, una rottura o l'imminente rottura dell'aorta, la dissecazione retrograda con coinvolgimento dell'aorta ascendente e una storia personale di sindrome di Marfan o sindrome di Ehlers-Danlos.
L'obiettivo nella gestione chirurgica della dissecazione aortica è quello di asportare i segmenti dell'aorta più gravemente danneggiati e di impedire l'ulteriore ingresso di sangue nel falso lume (sia nella zona di lacerazione intimale originaria, che in qualsiasi zona di lacerazione secondaria lungo il decorso del vaso). È tecnicamente possibile eseguire l'escissione della lesione intimale, tuttavia questo tipo di intervento non cambia in modo significativo la mortalità. Ricorrere ad un particolare tipo di trattamento piuttosto che ad un altro dipende dal segmento o tratto di aorta coinvolto. Alcuni trattamenti possibili comprendono:
- Chirurgia aortica “a cielo aperto” con sostituzione della sezione danneggiata di aorta e sua sostituzione con un innesto a tubo (spesso in materiale di dacron ) purché si possa escludere qualsiasi tipo di danno a carico della valvola aortica.
- Procedura di Bentall-De Bono: sostituzione della sezione d'aorta danneggiata e sostituzione della valvola aortica. [37]
- Procedura di David - sostituzione della sezione danneggiata dell'aorta e reimpianto della valvola aortica [38]
- Riparazione aortica endovascolare toracica: una procedura chirurgica minimamente invasiva, solitamente associata a un trattamento medico continuo.
- Sostituzione della sezione d'aorta danneggiata con un connettore vascolare ad anello senza suture-rinforzo con innesto di Dacron: il connettore vascolare ad anello è un anello di titanio usato come stent nell'innesto vascolare per ottenere una rapida anastomosi senza ricorrere a suture. Due solchi sulla superficie dell'anello servono per il fissaggio dell'innesto vascolare e dell'aorta. I nastri utilizzati per ancorarsi all'anello forniscono una superficie di contatto più ampia rispetto ai punti tradizionali, quindi comportano la realizzazione di anastomosi più forti e risultati chirurgici migliori.
Poiché il falso lume potrebbe aver ostruito altri tronchi arteriosi emergenti, spesso si rende necessario, contestualmente all'intervento chirurgico per la dissecazione vera e propria, anche un intervento di rivascolarizzazione per eliminare l'ostruzione in questi vasi attigui, e ciò al fine di risolvere la cattiva perfusione di molti organi vicini.
Un certo numero di condizioni e di comorbilità aumentano il rischio chirurgico di intervento di riparazione nei pazienti colpiti da una dissecazione aortica. Queste condizioni includono quanto segue:
- Valutazione preoperatoria prolungata (ampio periodo temporale prima della scelta dell'intervento chirurgico)
- Età avanzata
- Presenza di comorbilità (ad esempio una malattia coronaria )
- Rottura di aneurisma
- Tamponamento cardiaco
- Shock
- Storia pregressa di infarto del miocardio
- Storia di insufficienza renale (sia acuta che cronica )
Follow up
Il follow-up a lungo termine nelle persone che sopravvivono alla dissecazione aortica comporta un rigoroso controllo della pressione arteriosa. Il rischio di una rottura tardiva di un aneurisma aortico è 10 volte più alto nei soggetti con ipertensione arteriosa non controllata, rispetto ai soggetti con una pressione sistolica inferiore a 130 mmHg. Pertanto l'ipertensione non controllata rimane il fattore di rischio trattabile più significativo nella dissecazione aortica. [39] Il rischio di morte è più alto nei primi due anni dopo l'evento acuto, ed i pazienti dovrebbero essere seguiti strettamente durante questo periodo di tempo. Circa il 29% delle morti tardive dopo l'intervento chirurgico è dovuto alla rottura di un aneurisma dissecante. Inoltre, esiste una rilevante incidenza (calcolata tra il 17% e il 25%) di formazione di un nuovo aneurisma, tipicamente dovuta alla dilatazione del falso lume residuo. Questi nuovi aneurismi hanno maggiori probabilità di rottura, per il fatto che sono costituiti da pareti più sottili. Molti medici suggeriscono imaging seriale dell'aorta, e la risonanza magnetica (RMN) è la tecnica di imaging preferita.
Prevenzione
Tra i fattori di rischio riconosciuti per la dissecazione aortica, l'ipertensione, i livelli anormalmente alti di lipidi (ad esempio il colesterolo) nel sangue e il fumo di tabacco, sono tutti considerati fattori di rischio prevenibili. Si raccomanda di intervenire chirurgicamente a riparare un ingrossamento dell'aorta ascendente dovuto a un aneurisma con una dimensione superiore a 6 cm per ridurre il rischio di dissecazione. L'intervento chirurgico può essere raccomandato quando la dimensione è superiore a 4,5 cm se la persona è affetta da una delle diverse patologie del tessuto connettivo oppure una storia familiare di rottura dell'aorta.
Note
- ^ Sono a rischio di dissezione aortica ? , in la Repubblica , 2 ottobre 2018, p. 55.
- ^ a b c d Criado FJ,Aortic dissection: a 250-year perspective , in Tex Heart Inst J , vol. 38, n. 6, 2011, pp. 694–700, PMC 3233335 , PMID 22199439 . URL consultato il 22 marzo 2018 .
- ^ a b c d e Nienaber CA, Clough RE, Management of acute aortic dissection , in Lancet , vol. 385, n. 9970, February 2015, pp. 800–11, DOI : 10.1016/S0140-6736(14)61005-9 , PMID 25662791 . URL consultato il 22 marzo 2018 .
- ^ White A, Broder J, Mando-Vandrick J, Wendell J, Crowe J, Acute aortic emergencies--part 2: aortic dissections , in Adv Emerg Nurs J , vol. 35, n. 1, 2013, pp. 28–52, DOI : 10.1097/TME.0b013e31827145d0 , PMID 23364404 . URL consultato il 22 marzo 2018 .
- ^ Gaul C, Dietrich W, Erbguth FJ, Neurological symptoms in aortic dissection: a challenge for neurologists , in Cerebrovasc. Dis. , vol. 26, n. 1, 2008, pp. 1–8, DOI : 10.1159/000135646 , PMID 18511865 . URL consultato il 22 marzo 2018 .
- ^ Gaul C, Dietrich W, Friedrich I, Sirch J, Erbguth FJ,Neurological symptoms in type A aortic dissections , in Stroke , vol. 38, n. 2, February 2007, pp. 292–7, DOI : 10.1161/01.STR.0000254594.33408.b1 , PMID 17194878 . URL consultato il 22 marzo 2018 .
- ^ Walma RA, Vermeij FH, Bakker S, [Neurological signs in aortic dissection] , in Ned Tijdschr Geneeskd , vol. 157, n. 38, 2013, pp. A6259, PMID 24330794 . URL consultato il 22 marzo 2018 .
- ^ a b Orihashi K, Mesenteric ischemia in acute aortic dissection , in Surg. Today , vol. 46, n. 5, May 2016, pp. 509–16, DOI : 10.1007/s00595-015-1193-4 , PMID 26024781 . URL consultato il 22 marzo 2018 .
- ^ a b Kamman AV, Yang B, Kim KM, Williams DM, Michael Deeb G, Patel HJ, Visceral Malperfusion in Aortic Dissection: The Michigan Experience , in Semin. Thorac. Cardiovasc. Surg. , vol. 29, n. 2, 2017, pp. 173–178, DOI : 10.1053/j.semtcvs.2016.10.002 , PMID 28823323 . URL consultato il 22 marzo 2018 .
- ^ a b c d Cook JR, Ramirez F, Clinical, diagnostic, and therapeutic aspects of the Marfan syndrome , in Adv. Exp. Med. Biol. , vol. 802, 2014, pp. 77–94, DOI : 10.1007/978-94-007-7893-1_6 , PMID 24443022 . URL consultato il 23 marzo 2018 .
- ^ a b c Murdoch JL, Walker BA, Halpern BL, Kuzma JW, McKusick VA, Life expectancy and causes of death in the Marfan syndrome , in N. Engl. J. Med. , vol. 286, n. 15, April 1972, pp. 804–8, DOI : 10.1056/NEJM197204132861502 , PMID 5011789 . URL consultato il 23 marzo 2018 .
- ^ a b Stankowski RV, Kloner RA, Rezkalla SH, Cardiovascular consequences of cocaine use , in Trends Cardiovasc. Med. , vol. 25, n. 6, August 2015, pp. 517–26, DOI : 10.1016/j.tcm.2014.12.013 , PMID 25657055 . URL consultato il 23 marzo 2018 .
- ^ a b Singh A, Khaja A, Alpert MA, Cocaine and aortic dissection , in Vasc Med , vol. 15, n. 2, April 2010, pp. 127–33, DOI : 10.1177/1358863X09358749 , PMID 20233907 . URL consultato il 23 marzo 2018 .
- ^ Wanga S, Silversides C, Dore A, de Waard V, Mulder B, Pregnancy and Thoracic Aortic Disease: Managing the Risks , in Can J Cardiol , vol. 32, n. 1, January 2016, pp. 78–85, DOI : 10.1016/j.cjca.2015.09.003 , PMID 26604124 . URL consultato il 23 marzo 2018 .
- ^ a b Lech C, Swaminathan A, Abdominal Aortic Emergencies , in Emerg. Med. Clin. North Am. , vol. 35, n. 4, November 2017, pp. 847–867, DOI : 10.1016/j.emc.2017.07.003 , PMID 28987432 . URL consultato il 23 marzo 2018 .
- ^ Debakey ME, Henly WS, Cooley DA, Morris GC, Crawford ES, Beall AC, Surgical management of dissecting aneurysms of the aorta , in J. Thorac. Cardiovasc. Surg. , vol. 49, January 1965, pp. 130–49, PMID 14261867 .
- ^ Daily PO, Trueblood HW, Stinson EB, Wuerflein RD, Shumway NE, Management of acute aortic dissections , in Ann. Thorac. Surg. , vol. 10, n. 3, September 1970, pp. 237–47, PMID 5458238 .
- ^ Slater EE, DeSanctis RW, The clinical recognition of dissecting aortic aneurysm , in Am. J. Med. , vol. 60, n. 5, May 1976, pp. 625–33, DOI : 10.1016/0002-9343(76)90496-4 , PMID 1020750 . URL consultato il 25 marzo 2018 .
- ^ Spittell PC, Spittell JA, Joyce JW, Tajik AJ, Edwards WD, Schaff HV, Stanson AW, Clinical features and differential diagnosis of aortic dissection: experience with 236 cases (1980 through 1990) , in Mayo Clin. Proc. , vol. 68, n. 7, July 1993, pp. 642–51, DOI : 10.1016/s0025-6196(12)60599-0 , PMID 8350637 . URL consultato il 25 marzo 2018 .
- ^ ( EN ) Isselbacher EM, Cigarroa JE, Eagle KA, Cardiac tamponade complicating proximal aortic dissection. Is pericardiocentesis harmful? , in Circulation , vol. 90, n. 5, November 1994, pp. 2375–8, PMID 7955196 . URL consultato il 2 agosto 2021 (archiviato dall' url originale il 27 marzo 2018) .
- ^ Sheikh AS, Ali K, Mazhar S, Acute aortic syndrome , in Circulation , vol. 128, n. 10, September 2013, pp. 1122–7, DOI : 10.1161/CIRCULATIONAHA.112.000170 , PMID 24002714 . URL consultato il 25 marzo 2018 .
- ^ a b c Alfson DB, Ham SW, Type B Aortic Dissections: Current Guidelines for Treatment , in Cardiol Clin , vol. 35, n. 3, August 2017, pp. 387–410, DOI : 10.1016/j.ccl.2017.03.007 , PMID 28683909 . URL consultato il 25 marzo 2018 .
- ^ Meester JAN, Verstraeten A, Schepers D, Alaerts M, Van Laer L, Loeys BL,Differences in manifestations of Marfan syndrome, Ehlers-Danlos syndrome, and Loeys-Dietz syndrome , in Ann Cardiothorac Surg , vol. 6, n. 6, November 2017, pp. 582–594, DOI : 10.21037/acs.2017.11.03 , PMC 5721110 , PMID 29270370 . URL consultato il 23 marzo 2018 .
- ^ Turtle EJ, Sule AA, Webb DJ, Bath LE, Aortic dissection in children and adolescents with Turner syndrome: risk factors and management recommendations , in Arch. Dis. Child. , vol. 100, n. 7, July 2015, pp. 662–6, DOI : 10.1136/archdischild-2014-307080 , PMID 25573747 . URL consultato il 23 marzo 2018 .
- ^ Bondy CA, Aortic dissection in Turner syndrome , in Curr. Opin. Cardiol. , vol. 23, n. 6, November 2008, pp. 519–26, PMC 2692924 , PMID 18839441 . URL consultato il 23 marzo 2018 .
- ^ Shachter N, Perloff JK, Mulder DG, Aortic dissection in Noonan's syndrome (46 XY turner) , in Am. J. Cardiol. , vol. 54, n. 3, August 1984, pp. 464–5, PMID 6465040 .
- ^ a b Hiratzka LF, Bakris GL, Beckman JA, Bersin RM, Carr VF, Casey DE, Eagle KA, Hermann LK, Isselbacher EM, Kazerooni EA, Kouchoukos NT, Lytle BW, Milewicz DM, Reich DL, Sen S, Shinn JA, Svensson LG, Williams DM, 2010 ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM guidelines for the diagnosis and management of patients with Thoracic Aortic Disease: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, American Association for Thoracic Surgery, American College of Radiology, American Stroke Association, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of Thoracic Surgeons, and Society for Vascular Medicine , in Circulation , vol. 121, n. 13, April 2010, pp. e266–369, DOI : 10.1161/CIR.0b013e3181d4739e , PMID 20233780 . URL consultato il 26 marzo 2018 .
- ^ Das M., Mahnken AH and Wildberger JE, “Dual Energy: CTA Aorta” in Seidensticker PR and Hofmann LK (eds.), Dual Source CT Imaging , Springer Medizin Verlag, Heidelberg, 2008. ISBN 978-3-540-77602-4 .
- ^ Olsson C, Thelin S, Ståhle E, Ekbom A, Granath F, Thoracic aortic aneurysm and dissection: increasing prevalence and improved outcomes reported in a nationwide population-based study of more than 14,000 cases from 1987 to 2002 , in Circulation , vol. 114, n. 24, December 2006, pp. 2611–8, DOI : 10.1161/CIRCULATIONAHA.106.630400 , PMID 17145990 . URL consultato il 26 marzo 2018 .
- ^ Yuan SM, Postpartum aortic dissection , in Taiwan J Obstet Gynecol , vol. 52, n. 3, September 2013, pp. 318–22, DOI : 10.1016/j.tjog.2013.06.003 , PMID 24075366 . URL consultato il 26 marzo 2018 .
- ^ Immer FF, Bansi AG, Immer-Bansi AS, McDougall J, Zehr KJ, Schaff HV, Carrel TP, Aortic dissection in pregnancy: analysis of risk factors and outcome , in Ann. Thorac. Surg. , vol. 76, n. 1, July 2003, pp. 309–14, PMID 12842575 . URL consultato il 26 marzo 2018 .
- ^ Ohle R, Kareemi HK, Wells G, Perry JJ, Clinical Examination for Acute Aortic Dissection: A Systematic Review and Meta-analysis , in Acad Emerg Med , December 2017, DOI : 10.1111/acem.13360 , PMID 29265487 . URL consultato il 27 marzo 2018 .
- ^ Shimony A, Filion KB, Mottillo S, Dourian T, Eisenberg MJ, Meta-analysis of usefulness of d-dimer to diagnose acute aortic dissection , in Am. J. Cardiol. , vol. 107, n. 8, April 2011, pp. 1227–34, DOI : 10.1016/j.amjcard.2010.12.027 , PMID 21296332 . URL consultato il 27 marzo 2018 .
- ^ Asha SE, Miers JW, A Systematic Review and Meta-analysis of D-dimer as a Rule-out Test for Suspected Acute Aortic Dissection , in Ann Emerg Med , vol. 66, n. 4, October 2015, pp. 368–78, DOI : 10.1016/j.annemergmed.2015.02.013 , PMID 25805111 . URL consultato il 27 marzo 2018 .
- ^ Bossone E, Suzuki T, Eagle KA, Weinsaft JW, Diagnosis of acute aortic syndromes : imaging and beyond , in Herz , vol. 38, n. 3, May 2013, pp. 269–76, DOI : 10.1007/s00059-012-3710-1 , PMID 23263244 . URL consultato il 27 marzo 2018 .
- ^ Lo BM, An evidence-based approach to acute aortic syndromes , in Emerg Med Pract , vol. 15, n. 12, December 2013, pp. 1–23; quiz 23–4, PMID 24804329 . URL consultato il 27 marzo 2018 .
- ^ Bentall H, De Bono A, A technique for complete replacement of the ascending aorta , in Thorax , vol. 23, n. 4, July 1968, pp. 338–9, PMID 5664694 . URL consultato il 24 marzo 2018 .
- ^ David TE, Armstrong S, Ivanov J, Feindel CM, Omran A, Webb G, Results of aortic valve-sparing operations , in J. Thorac. Cardiovasc. Surg. , vol. 122, n. 1, July 2001, pp. 39–46, DOI : 10.1067/mtc.2001.112935 , PMID 11436035 . URL consultato il 24 marzo 2018 .
- ^ Howard DP, Banerjee A, Fairhead JF, Perkins J, Silver LE, Rothwell PM, Population-based study of incidence and outcome of acute aortic dissection and premorbid risk factor control: 10-year results from the Oxford Vascular Study , in Circulation , vol. 127, n. 20, May 2013, pp. 2031–7, DOI : 10.1161/CIRCULATIONAHA.112.000483 , PMID 23599348 . URL consultato il 24 marzo 2018 .
Bibliografia
- Joseph C. Sengen, Concise Dictionary of Modern Medicine , New York, McGraw-Hill, ISBN 978-88-386-3917-3 .
- Harrison, Principi di Medicina Interna (il manuale - 16ª edizione) , New York - Milano, McGraw-Hill, 2006, ISBN 88-386-2459-3 .
- Hurst, Il Cuore (il manuale - 11ª edizione) , Milano, McGraw-Hill, 2006, ISBN 978-88-386-2388-2 .
- Eugene Braunwald, Malattie del cuore (7ª edizione) , Milano, Elsevier Masson, 2007, ISBN 978-88-214-2987-3 .
Voci correlate
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su dissecazione aortica
Wikimedia Commons contiene immagini o altri file su dissecazione aortica





