Pentafluorură de bismut
| Pentafluorură de bismut | |
|---|---|
| Numele IUPAC | |
| pentafluorură de bismut | |
| Denumiri alternative | |
| fluorură de bismut (V) | |
| Caracteristici generale | |
| Formula moleculară sau brută | BiF 5 |
| Masa moleculară ( u ) | 303,97 |
| Aspect | solid cristalin alb |
| numar CAS | |
| Numărul EINECS | 232-125-3 |
| PubChem | 123260 |
| ZÂMBETE | [F-].[F-].[F-].[F-].[F-].[BiH3+3] e [F-].[F-].[F-].[F-].[F-].[Bi+5] |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 5.40 |
| Solubilitate în apă | reacție violentă |
| Temperatură de topire | 154,4 ° C (427,6 K) [1] |
| Temperatura de fierbere | 230 ° C (503 K) [1] |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
  | |
| Fraze H | 272, 314 |
| Sfaturi P | 220, 280, 305 + 351 + 338, 310 |
Pentafluorura de bismut este compusul anorganic cu formula BiF 5 . În condiții normale, este un solid cristalin alb, inodor. În acest compus, bismutul este în starea de oxidare +5. Este un oxidant puternic și un fluoror foarte puternic, dar nu este de uz comun.
fundal
După câteva încercări nereușite de sinteză în soluție apoasă , [2] BiF 5 a fost descris pentru prima dată în 1940 de Hans von Wartenberg (1880-1960). [3]
Caracteristici structurale și fizice
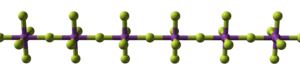
În stare solidă BiF 5 are o structură polimerică, formată din lanțuri liniare de octaedre BiF 6 conectate prin liganzii F în poziția trans . [1] [4] O structură analogă este prezentă în α- UF 5 . Trifluorura de bismut , BiF 3 , este în schimb un compus ionic cu o structură asemănătoare YF 3 . [1]
Sinteză
BiF 5 poate fi preparat prin reacția trifluorurii de bismut și a fluorului la 500 ° C: [2]
- BiF 3 + F 2 → BiF 5
Alternativ, trifluorura de clor la 350 ° C poate fi utilizată ca agent de fluorurare: [5]
- BiF 3 + ClF 3 → BiF 5 + ClF
Reactivitate
BiF 5 este cel mai reactiv dintre pentafluoruri din grupul 15 elemente . Este un oxidant puternic și un fluorinator foarte energic. Reacționează violent cu apă formând ozon și difluorură de oxigen . La temperatura camerei reacționează violent și cu iod și sulf . La temperaturi peste 50 ° C, fluorează hidrocarburile, transformându-le în fluorocarburi . La 150 ° C oxidează UF 4 la UF 6 . La 180 ° C fluoruri Br 2 la BrF 3 și BrF 5 și Cl 2 la ClF . [1]
BiF 5 reacționează, de asemenea, cu fluorurile metalelor alcaline, MF, pentru a forma hexafluorobismutați, M [BiF 6 ], care conțin anionul [BiF 6 ] - , [6] și heptafluorobismutați, M 2 [BiF 7 ], care conțin l 'anion [BiF 7 ] 2− . Acesta din urmă are structura bipiramidică pe bază de pentagon. [7]
Informații de siguranță
BiF 5 este disponibil comercial. Este un compus foarte reactiv și periculos care provoacă arsuri la nivelul pielii, mucoaselor și ochilor. Ca oxidant poate agrava un incendiu. Reacționează violent cu apa. Nu există date care să indice proprietăți cancerigene. Nu există date privind ecotoxicitatea. [8]
Notă
- ^ a b c d e Greenwood și Earnshaw (1997)
- ^ a b Fischer și Rudzitis 1959
- ^ von Wartenberg 1940
- ^ Hebecker 1971
- ^ Popov și colab. 1989
- ^ Holleman și Wiberg 2001
- ^ Housecroft și Sharpe 2008
- ^ Sigma Aldrich, Fișa tehnică de siguranță a pentafluorurii de bismut
Bibliografie
- J. Fischer și E. Rudzitis, Prepararea, proprietățile și reacțiile pentafluorurii de bismut , în J. Am. Chem. Soc. , Vol. 81, nr. 24, 1959, pp. 6375-6377, DOI : 10.1021 / ja01533a009 . Adus la 20 februarie 2012 .
- NN Greenwood și A. Earnshaw, Chimia elementelor , ediția a II-a, Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4 .
- C. Hebecker, Zur Kristallstruktur von Wismutpentafluorid , în Z. anorg. Anexă Chem. , vol. 384, nr. 2, 1971, pp. 111-114.
- AF Holleman și E. Wiberg, Chimie anorganică , San Diego, Academic Press, 2001, ISBN 0-12-352651-5 .
- CE Housecroft și AG Sharpe, Chimie anorganică , ediția a 3-a, Harlow (Anglia), Pearson Education Limited, 2008, ISBN 978-0-13-175553-6 .
- AI Popov, AV Scharabarin, VF Sukhoverkhov, NA Tchumaevsky, Sinteza și proprietățile antimonului pentavalent și fluorurilor de bismut , în Z. anorg. Anexă Chem. , vol. 576, nr. 1, 1989, pp. 242-254, DOI : 10.1002 / zaac.19895760128 . Adus la 20 februarie 2012 .
- H. von Wartenberg, Über einige höhere Fluoride (PbF 4 , CeF 4 , BiF 5 ) , în Z. anorg. Anexă Chem. , vol. 244, n. 4, 1940, pp. 337–347, DOI : 10.1002 / zaac.19402440401 . Adus la 20 februarie 2012 .