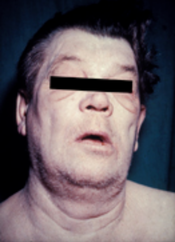
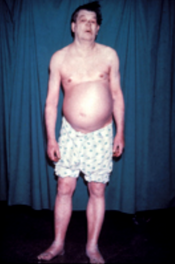
Hipotiroidism
| Hipotiroidism | |
|---|---|
| Formula chimică a tiroxinei , a cărei lipsă provoacă simptomele hipotiroidismului | |
| Specialitate | endocrinologie |
| Clasificare și resurse externe (EN) | |
| Plasă | D007037 |
| MedlinePlus | 000353 |
| eMedicină | 122393 |
Hipotiroidismul sau insuficiența tiroidiană este un sindrom clinic al sistemului endocrin rezultat dintr-un deficit de hormoni tiroidieni ( triiodotironină și tetraiodotironină sau tiroxină) produse de tiroidă și care implică o reducere generalizată a tuturor proceselor metabolice din organism. [1]
Această tulburare endocrină poate provoca o serie de simptome precum oboseală , toleranță slabă la frig și creștere în greutate. La copii, hipotiroidismul duce la întârzieri în creștere și dezvoltare intelectuală. Diagnosticul de hipotiroidism, atunci când este suspectat, poate fi confirmat prin teste de sânge care măsoară nivelul hormonului stimulator al tiroidei (TSH) și al nivelului de tiroxină.
La nivel global, deficitul alimentar de iod este cea mai frecventă cauză a hipotiroidismului. La populațiile care se bucură de o dietă corectă , cea mai frecventă cauză este tiroidita Hashimoto , o boală autoimună . Cauzele mai puțin frecvente includ: tratamentul anterior cu iod radioactiv , leziunea hipotalamusului sau a hipofizei anterioare , administrarea anumitor medicamente , lipsa unei tiroide funcționale la naștere sau intervenția chirurgicală anterioară a tiroidei.
Hipotiroidismul poate fi bine tratat cu levotiroxină , a cărei doză este ajustată pe baza simptomelor și a normalizării nivelurilor de tiroxină și TSH. În țările occidentale, hipotiroidismul apare la 0,3% -0,4% dintre indivizi. Boala poate afecta și animalele, în special câinii [2] , și cu o incidență mai mică și pisicile sau caii . [3]
fundal

Corelația dintre tiroidă și mixedem a fost găsită spre sfârșitul secolului al XIX-lea, când s-a observat o îmbunătățire a simptomelor la persoanele sau animalele cărora li s-a îndepărtat tiroida și a fost înlocuită cu țesutul tiroidian animal. [4] Iodul a fost descoperit în algele marine în 1811 de Bernard Courtois și aportul său a fost asociat cu dimensiunea gușei în 1820 de Jean-Francois Coindet . [5] În 1852, Gaspard Adolphe Chatin a propus că gușa endemică se datorează aportului insuficient de iod și Eugen Baumann și-a demonstrat prezența în țesutul tiroidian în 1896. [5]
În 1891, medicul englez George Redmayne Murray a injectat subcutanat un extract de tiroidă de oaie [6] la scurt timp după înlocuirea acestuia cu o formulare orală. [4] [7] Tiroxina purificată a fost introdusă în 1914, iar tiroxina sintetică a devenit disponibilă în 1930, deși extractul de tiroidă animală uscată a rămas pe scară largă. Liothyronina a fost identificată în 1952. [4]
Epidemiologie
În contextul lucrărilor științifice care au analizat epidemiologia hipotiroidismului, studiul populației județului Whickham din Marea Britanie , efectuat timp de două decenii începând cu mijlocul anilor 1970, care a furnizat date de referință pentru țările occidentale, subliniind o prevalența hipotiroidismului spontan la femei egală cu 7,7% (care devine 9,3% dacă se includ cazuri de hipotiroidism iatrogen ) și la bărbați egală cu 1,3%. [8]
Aceste date au fost ulterior confirmate de o altă lucrare epidemiologică semnificativă, studiul NHANES III, efectuat pe peste 17.000 de locuitori din Statele Unite în anii 1988-1994, care a arătat o prevalență a hipotiroidismului egală cu 4,6% în întreaga populație luată în considerare. Acest ultim studiu a demonstrat, de asemenea, în mod clar că marea majoritate a hipotiroidismelor găsite este de fapt reprezentată de forme subclinice (4,3% din cazuri), adică pauci-simptomatice și caracterizate biochimic prin creșterea TSH singură. Pe de altă parte, doar o minoritate dintre hipotiroidismele găsite este semnificativă clinic (0,3% din cazuri) și se caracterizează în special prin creșterea TSH și reducerea FT3 și FT4. [9]
În lume există aproximativ un miliard de persoane cu deficit de iod. Cu toate acestea, nu se știe cât de des rezultă acest lucru hipotiroidism. [10] În studii ample efectuate pe populații din țările occidentale cu iod suficient în dietă, hipotiroidismul evident a fost detectat la 0,3-0,4% dintre indivizi. [11] Dintre acestea, 80% au un nivel de TSH sub pragul de 10 mIU / L, care este considerat a fi pragul pentru tratament. [12] Copiii cu hipotiroidism subclinic recuperează adesea funcția tiroidiană normală și doar un procent mic dezvoltă o formă clinică. [13]
Femeile sunt mai susceptibile de a suferi de această afecțiune decât bărbații. În studiile populației, femeile s-au dovedit a avea șapte ori mai multe șanse decât bărbații să aibă niveluri de TSH peste 10 mU / L. [11] În fiecare an, între 2 și 4% dintre persoanele cu hipotiroidism subclinic vor progresa către hipotiroidismul complet. Riscul este mai mare la pacienții cu anticorpi peroxidazei tiroidiene. [11] [12] Se estimează că hipotiroidismul subclinic implică aproximativ 2̬% dintre copii. La adulți, hipotiroidismul subclinic este mai frecvent la vârstnici și caucazieni . [14] Există o rată mult mai mare de tulburări tiroidiene, hipotiroidismul fiind cel mai frecvent la persoanele cu sindrom Down [15] [16] și sindromul Turner . [15]
O formă foarte severă de hipotiroidism și mixedem comă sunt afecțiuni foarte rare, cu o incidență estimată de 0,22 cazuri pe milion de persoane pe an. [17] Majoritatea cazurilor apar la femeile cu vârsta peste 60 de ani, deși se poate întâmpla în orice moment al vieții. [17]
Majoritatea cazurilor de hipotiroidism sunt de natură primară. Hipotiroidismul central sau secundar afectează cu un raport cuprins între 1: 20.000 și 1: 80.000 din populație sau aproximativ una din fiecare mie de persoane care suferă deja de hipotiroidism. [18]
semne si simptome
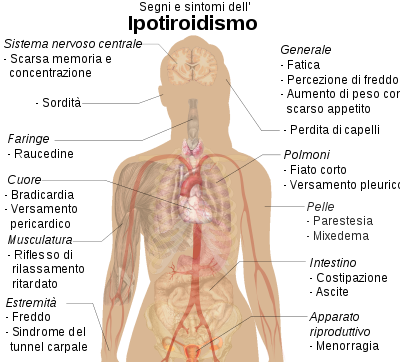
Persoanele cu hipotiroidism se dovedesc adesea asimptomatice sau au doar simptome ușoare. Numeroase semne și simptome sunt asociate cu hipotiroidismul și pot fi legate de cauza sau efectele de bază ale deficitului de hormoni tiroidieni. [19] [20] Tiroidita lui Hashimoto se poate prezenta cu prezența strumei (gușa) din cauza unei glande tiroide mărită. [19] [21]
Apetitul pacientului este afectat, oboseală ușoară, ritm cardiac scăzut, scăderea libidoului , uneori creștere în greutate, constipație , amorțeală mentală, somnolență excesivă în timpul zilei (pacientul poate dormi 10-14 ore pe zi), amorțeală musculară care vede mușchii să se relaxeze lent după contracție, metabolizarea redusă a tuturor glandelor endocrine cu dezechilibrele rezultate, menoragia și polimenoreea sau fluxurile menstruale excesive sau excesiv de frecvente. Uneori poate fi găsită hipoglicemie reactivă (o scădere a zahărului din sânge după o masă bogată în carbohidrați , cu simptome precum somnolență și anxietate). [22]
Tabloul clinic al hipotiroidismului se repetă identic în diferitele forme etiologice [1] . Insuficiența tiroidiană se caracterizează prin progresul unei reduceri funcționale destul de nespecifice care implică organismul în ansamblu și severitatea este proporțională cu deficitul hormonal [23] . Prezentarea clinică este, însă, puternic condiționată de vârsta pacientului: în timp ce la vârstnici manifestările clinice tind să fie mai nuanțate, în vârstă de dezvoltare, alături de semnele periferice ale deficitului de tiroxină, există și semne ale unui statut și intelectual. , care sunt mai mari cu cât boala a apărut mai devreme [1] .
Reducerea progresivă a proceselor metabolice implică întregul organism și are ca rezultat o producție redusă de căldură, cu consecința intoleranței la frig și într-un metabolism redus al glicozaminoglicanilor (GAG), care, prin urmare, tind să se acumuleze și, fiind marcat hidrofil , să readucă apa, explicând îngroșarea, cu edem neimprimant, a pielii și a subcutanatului (mai evidentă în corespondența cu regiunile orbitale și pretibiale), până la imaginea izbitoare a mixedemului. Infiltrarea mixedematoasă a limbii și a corzilor vocale , pe de altă parte, este responsabilă pentru vocea răgușită caracteristică a pacientului hipotiroidian. Reducerea activităților metabolice conduce, de asemenea, la o tendință de uscăciune și fragilitate a pielii, a părului și a unghiilor (tipică este căderea sprâncenelor în corespondență cu treimea lor externă) și la o culoare cenușie-gălbuie a pielii (datorită hipercarotenemiei ) [23] .
Cu toate acestea, în ceea ce privește efectele endocrinologice , hipotiroidismul implică, la femei, modificări ale ciclului menstrual, de la oligomenoree la amenoree sau hiperpolimenoree și un risc crescut de avort , în timp ce la bărbați poate exista o reducere a libidoului și a potenței sexuale. Nivelurile ridicate deTRH pot exercita, de asemenea, o acțiune stimulatoare asupra secreției de prolactină care, împreună cu clearance-ul metabolic redus al prolactinei în sine tipic subiectului hipotiroidian, poate provoca hiperprolactinemie și galactoree , care regresează rapid odată cu începerea terapiei de substituție cu hormon tiroidian. Din punct de vedere metabolic, însă, scăderea consumului de oxigen, cheltuielile energetice bazale și utilizarea substraturilor metabolice duc la scăderea poftei de mâncare, o tendință de creștere în greutate și modificări ale structurii lipidelor , în special o creștere a colesterolului total. ,LDL și trigliceride [23] . În cursul hipotiroidismului există, de asemenea, o absorbție lentă a glucozei intestinale și există o motilitate intestinală redusă, cu o consecință a tendinței la constipație.
În ceea ce privește, în schimb, efectele asupra sistemului cardiovascular , deficitul de tiroxină are ca rezultat un efect inotrop și cronotrop negativ, cu o reducere consecventă a ritmului cardiac și a ritmului cardiac , o creștere a rezistenței vasculare periferice, cu o reducere a presiunii diferențiale și a țesutului. perfuzie. În cele mai avansate stări, acumularea de mucopolizaharide favorizează formarea revărsatului pericardic și pleural și există o implicare mixedematoasă a musculaturii , inclusiv a căilor respiratorii, cu o consecință a tendinței de hipoxie și hipercapnie . Implicarea sistemului muscular duce adesea la rigiditate și sensibilitate și, în confirmarea acestei miopatii , se găsesc adesea niveluri ridicate de GOT și CPK . [1] În ceea ce privește, în schimb, efectele hematologice, în hipotiroidism există adesea o reducere a eritropoiezei (pentru ajustarea necesității scăzute de oxigen periferic), cu anemie moderată în consecință [1]
Principalele semne și simptome sunt rezumate în următorul tabel:
| Simptome [19] | Semne [19] |
|---|---|
| Oboseală | Piele uscată și aspră |
| Senzație de frig | Rece la capete |
| Memorie slabă și concentrare | Mixedem |
| Constipație | Pierderea parului |
| Creșterea în greutate cu apetit slab | Ritm cardiac lent |
| Respirație scurtă | Edemul membrelor |
| Voce ragusita | Relaxarea întârziată a reflexelor tendinoase |
| Menoragie (și oligomenoree ) | Sindromul de tunel carpian |
| Parestezie | Revărsat pleural , ascită , revărsat pericardic |
| Lipsa auzului |
O întârziere a relaxării după testul reflex al tendonului gleznei este un semn distinctiv al hipotiroidismului și este asociată cu severitatea deficitului hormonal. [11]
Coma din cauza mixedemului
Coma de Mixedem este o afecțiune rară, dar care pune viața în pericol, din cauza unei afecțiuni foarte severe a hipotiroidismului. Se poate întâmpla la cei cu hipotiroidism atunci când dezvoltă alte afecțiuni, dar poate coincide și cu prima prezentare a afecțiunii. Coma de Mixedem se caracterizează prin temperaturi corporale foarte scăzute, dar nu este însoțită de frisoane , confuzie, bătăi lente ale inimii și depresie respiratorie. Pot exista semne fizice sugestive de hipotiroidism, cum ar fi modificări ale pielii sau limba mărită . [17]
Sarcina
Chiar și hipotiroidismul ușor sau subclinic poate provoca afectarea fertilității și un risc crescut de avort spontan . [24] Hipotiroidismul în timpul sarcinii timpurii, chiar și sub formă ușoară sau asimptomatică, poate crește riscul de preeclampsie , nașterea unui copil cu tulburări cognitive și deces perinatal. [24] [25] Femeile experimentează hipotiroidism la 0,3-0,5% din sarcini. [25]
Pediatrie
Deoarece hormonii tiroidieni sunt indispensabili pentru neuronogeneză, migrație neuronală, mielinizare, sinaptogeneză și neurotransmisie, se determină o afecțiune a dezvoltării neuronale afectate. [26]
Sugarii cu hipotiroidism pot avea greutate și înălțime normale la naștere (deși capul poate fi mai mare decât se aștepta și fontanelul posterior deschis). Unii pot prezenta somnolență, tonus muscular scăzut , plâns răgușit, dificultăți de hrănire, constipație , limbă mărită, hernie ombilicală , piele uscată, temperatură corporală redusă și icter . [15] Gușa este rară, deși se poate dezvolta mai târziu la copiii care au o glandă tiroidă care nu produce hormon tiroidian funcțional. [15] Gușa se poate dezvolta și la copiii care cresc în locuri cu deficit de iod. [27] Creșterea și dezvoltarea normală pot fi întârziate, iar lipsa tratamentului poate duce la un handicap mental ( IQ cu 6 până la 15 puncte mai mic în cazurile severe). Alte probleme includ următoarele: dificultăți în coordonarea mișcărilor ( ataxie ), tonus muscular redus, strabism , scăderea duratei de atenție și întârzierea dobândirii abilităților verbale. [15]
Screeningul neonatal este important, având în vedere impactul grav deja asupra stadiilor incipiente ale dezvoltării fizice și mentale a copilului și face posibilă inițierea promptă (în termen de două săptămâni de la naștere) a terapiei de substituție cu levotiroxină în cazul unei descoperiri. În Italia, hipotiroidismul congenital afectează aproximativ 1 nou-născut din 2.000, iar screening-ul este obligatoriu conform Legii din 5 februarie 1992, nr. 104 , în domeniul medicinei preventive. [28] [29] [30] [31]
Hipotiroidismul neonatal sau congenital este cauzat de malformații ale glandei, defecte ale sistemului de reglare sau sinteză a hormonilor tiroidieni, trecerea placentară a receptorilor TSH care blochează anticorpii de la mamă la făt sau expunerea la deficit de iod.
În timpurile ulterioare, este adesea o patologie dobândită ca urmare a tiroiditei autoimune sau a îndepărtării glandei. [29] [30] [31] Simptomele hipotiroidismului la copii și adolescenți mai mari pot include oboseală, intoleranță la frig, somnolență excesivă în timpul zilei, slăbiciune musculară, constipație, întârziere a creșterii, paloare , creșterea părului corporal , perioade menstruale neregulate la fete și întârziere pubertate . Semnele pot include relaxarea întârziată a reflexului tendonului gleznei și bătăile inimii lente . [15] Gușa poate fi prezentă cu o glandă tiroidă complet mărită. [15] Cu toate acestea, uneori doar o parte a glandei tiroide este mărită și poate avea un caracter nodulos. [32]
Etiologie
Hipotiroidismul se datorează funcției inadecvate a glandei în sine (hipotiroidism primar) sau nivelurilor insuficiente de hormon stimulator tiroidian (hipotiroidism central). [11] [33] Hipotiroidismul primar este de aproximativ o mie de ori mai frecvent decât hipotiroidismul central. [18]
Deficitul de iod este cea mai frecventă cauză a hipotiroidismului primar și a gușei endemice la nivel mondial. [4] [11] În zonele planetei cu iod suficient în dietă, hipotiroidismul se datorează cel mai frecvent unei boli autoimune , tiroidita Hashimoto ( tiroidita cronică autoimună). [4] [11] Hashimoto poate fi asociat cu gușa. Se caracterizează prin infiltrarea glandei tiroide de către limfocitele T și anticorpi împotriva antigenelor tiroidiene specifice, cum ar fi iodura peroxidază , tiroglobulina și receptorul TSH . [11]
După ce o femeie naște, în aproximativ 5% din cazuri va dezvolta tiroidită postpartum care poate apărea până la nouă luni de la naștere. [34] Aceasta se caracterizează printr-o perioadă scurtă de hipertiroidism urmată de o perioadă de hipotiroidism. Între 20% și 40% dintre aceștia rămân hipotiroidieni permanent. [34]
Tiroidita autoimună este asociată cu alte boli mediate de imunitate, cum ar fi diabetul zaharat de tip 1 , anemia pernicioasă , miastenia gravis , boala celiacă , artrita reumatoidă și lupusul eritematos sistemic . [11] Poate să apară ca parte a sindromului polendocrin autoimun (tip 1 și tip 2). [11]
| grup | Cauze |
|---|---|
| Hipotiroidism primar [11] | Lipsa de iod (țări în curs de dezvoltare), tiroidită autoimună, tiroidectomie anterioară, terapie radioiodică anterioară, radioterapie cu fascicul extern anterior la gât Medicamente: stabilizatori ai dispoziției pe bază de săruri de litiu , amiodaronă , interferon- alfa, inhibitori ai tirozin kinazei, cum ar fi sunitinib |
| Hipotiroidism central [18] | Leziuni compresive ale hipofizei ( adenom hipofizar , craniofaringiom , meningiom , gliom , chistul pungii Rathke , metastază , sindrom sella gol , anevrism cerebral al arterei carotide interne ), intervenții chirurgicale sau radioterapie a hipofizei, medicamente, traume, boli vasculare ( hipofiză) apoplexie , sindromul Sheehan , hemoragie subarahnoidiană ), boli autoimune (autoimune hipofizită , sindroame poliglandulare), boli infiltrative (supraabundență de fier din cauza hemocromatoza sau talasemie , sarcoidoza , Langerhans histiocitoza cu celule ), condiții congenitale și infecții ( tuberculoza ) micoze , sifilis ) |
| Hipotiroidism congenital [35] | Disgeneză tiroidiană (75%), dismorfogeneză tiroidiană (20%), anticorpi materni sau aport radioactiv de iod Sindroame: mutații (în locusul complex GNAS , PAX8 , TTF-1 / NKX2-1 , TTF-2 / FOXE1 ), sindrom Pendred (asociat cu pierderea auzului senzorial neural ) |
Patogenie
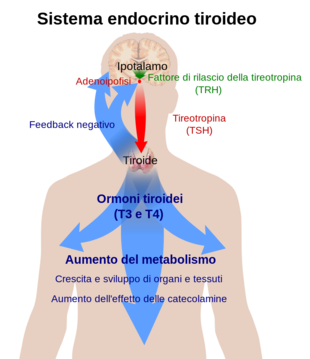
Hormonul tiroidian este necesar pentru funcționarea normală a corpului. Când este sănătoasă, glanda tiroidă secretă în principal tiroxină (T 4 ), care este convertită, în alte organe, în triiodotironină (T 3 ) datorită acțiunii catalizatoare a enzimei iodotironin-deiodinazei seleniu- dependente . [36] Triiodotironina se leagă de receptorul hormonului tiroidian prezent în nucleul celular, unde stimulează exprimarea anumitor gene și, prin urmare, producerea de proteine specifice. [37] Mai mult, hormonul se leagă de integrina αvβ3 pe membrana celulară prin stimularea antiportului sodiu-hidrogen și a anumitor procese, cum ar fi formarea vaselor de sânge și creșterea celulelor. [37] În sânge , aproape tot hormonul tiroidian (99,97%) este legat de proteinele plasmatice , cum ar fi globulina care leagă tiroxina ; numai hormonul tiroidian liber nelegat este biologic activ. [11]
Tiroida este singura sursă de hormon tiroidian din organism. Pentru producția sa este nevoie de iod și tirozină . Iodul este preluat din fluxul sanguin și încorporat în moleculele de tiroglobulină . Procesul este controlat de hormonul stimulator al tiroidei (TSH, tirotropina), care este secretat de hipofiza . Deficitul de iod sau deficitul de TSH poate determina scăderea producției de hormoni tiroidieni. [33]
Axa hipotalamus-hipofiză-tiroidă joacă un rol cheie în menținerea nivelurilor hormonilor tiroidieni în limite normale. Producția de TSH din hipofiza anterioară este stimulată la rândul său dehormonul care eliberează tirotropina (TRH), care este eliberat din hipotalamus . Producția de TSH și TRH scade tiroxina prin intermediul unui proces de feedback negativ . TRH insuficient, care este rar, poate duce la deficit de TSH și, prin urmare, la producția insuficientă de hormoni tiroidieni. [33]
Mai rar, hipotiroidismul se poate datora rezistenței periferice la hormonii tiroidieni din cauza deficitului de receptor sau post-receptor. Modificările genetice ale genelor care codifică NIS ( simporter de iodură de sodiu ) și pendrin pot determina producția redusă de hormoni tiroidieni. [1]
Sarcina duce la modificări semnificative în fiziologia hormonului tiroidian. Tiroida crește în dimensiune cu aproximativ 10%, producția de tiroxină crește cu 50% și crește cererea de iod. Multe femei au încă funcția tiroidiană normală, dar dacă au dovezi imunologice de autoimunitate tiroidiană (dovadă fiind prezența autoanticorpilor ) sau sunt deficiente în iod, vor dezvolta simptome de hipotiroidism înainte sau după naștere. [38]
Diagnostic
Testarea în laborator a nivelurilor hormonilor stimulatori tiroidieni este considerată cea mai bună metodă inițială pentru diagnosticarea hipotiroidismului. O a doua evaluare după câteva săptămâni este în general necesară ca confirmare. [39] Cu toate acestea, aceste niveluri pot fi modificate pentru alte boli, iar testarea TSH la persoanele internate nu este recomandată, cu excepția cazului în care se suspectează puternic disfuncția tiroidiană. [11] Un nivel ridicat de TSH indică faptul că tiroida nu produce suficient hormon tiroidian, iar nivelurile libere de T4 sunt adesea măsurate și. [11] [32] Măsurarea T 3 nu este recomandată în cazurile de hipotiroidism. [11] Există o serie de scale de evaluare a simptomelor de hipotiroidism care oferă un anumit grad de obiectivitate, dar sunt totuși un instrument limitat pentru diagnostic. [1] [11]
| TSH | T 4 | Interpretare |
|---|---|---|
| Normal | Normal | Funcția tiroidiană normală |
| Înalt | Bas | Hipotiroidism deplin |
| Normal / scăzut | Bas | Hipotiroidism central |
| Înalt | Normal | Hipotiroidismul subclinic |
Multe cazuri de hipotiroidism sunt asociate cu o creștere ușoară a creatin kinazei și a enzimelor hepatice din sânge. În mod normal, aceste valori revin la normal atunci când hipotiroidismul este tratat complet. [11] Nivelurile de colesterol , lipoproteine cudensitate mică și lipoproteine (a) pot fi, de asemenea, crescute. [11] Impactul hipotiroidismului subclinic asupra parametrilor lipidici este totuși mai puțin bine definit. [27]
O formă foarte severă de hipotiroidism și mixedem comă sunt asociate de obicei cu niveluri scăzute de sodiu din sânge și cu o creștere a hormonului antidiuretic , precum și cu insuficiență renală acută . [17]
Un diagnostic de hipotiroidism fără, la palpare , noduli sau mase detectabile în glanda tiroidă nu necesită imagistică tiroidiană. [39] Prezența anticorpilor împotriva iodurii peroxidazei face mai probabil ca nodulii tiroidieni să fie cauzați de tiroidită autoimună, dar, dacă există dubii, poate fi indicată biopsia acului . [11]
Dacă nivelul TSH este normal sau scăzut, iar nivelul T 4 fără ser este scăzut, imaginea indică hipotiroidismul central (secreția insuficientă de TSH sau TRH de către hipofiză sau hipotalamus ). Pot exista și alte caracteristici ale hipopituitarismului, cum ar fi anomalii ale ciclului menstrual și insuficiența suprarenală . De asemenea, poate exista prezența unei mase hipofizare, cum ar fi cefalee și tulburări vizuale. Hipotiroidismul central ar trebui investigat în continuare pentru a determina cauza de bază. [18] [39]
Hipotiroidismul subclinic
În hipotiroidismul primar evident, nivelurile TSH sunt crescute, în timp ce nivelurile T 4 și T 3 sunt scăzute. TSH crește de obicei după scăderea nivelului T 4 și T 3 . Hipotiroidismul subclinic este o formă mai ușoară de hipotiroidism caracterizată printr-un nivel crescut de TSH seric, dar cu un nivel normal de tiroxină liberă. [12] [14] Prezentarea hipotiroidismului subclinic este variabilă, iar semnele și simptomele clasice ale hipotiroidismului nu pot fi observate. [14] Dintre indivizii cu hipotiroidism subclinic, un procent va dezvolta hipotiroidism evident în fiecare an. La cei cu anticorpi detectabili împotriva peroxidazei tiroidiene (TPO) acest lucru apare în 4,3% din cazuri, în timp ce la cei fără anticorpi detectabili apare în 2,6% din cazuri. [11] Cei cu hipotiroidism subclinic și anticorpi TPO detectabili care nu necesită tratament ar trebui să facă un test de funcție tiroidiană mai repetat (de exemplu anual) decât cei care nu au anticorpi. [39]
Sarcina
Sarcina duce la modificări semnificative în fiziologia hormonului tiroidian. Glanda crește în dimensiune cu 10%, producția de tiroxină crește cu 50% și crește nevoia de iod . Molte donne presentano una funzionalità tiroidea normale, ma possono avere la prova immunologica della autoimmunità tiroidea (come evidenziato dalla presenza di autoanticorpi) o sono carenti di iodio, e sviluppare i segni dell'ipotiroidismo prima o dopo il parto . [38]
In gravidanza, i livelli di tiroxina libera possono essere inferiori a quelli previsti, a causa del maggiore legame con le globuline leganti tiroxina e una diminuzione del legame con l' albumina . Per la diagnosi essi devono essere corretti per lo stadio della gravidanza [11] oppure devono essere considerati i livelli complessivi di tiroxina. [11] I valori di TSH possono anche essere inferiori al normale (in particolare nel primo trimestre di gestazione). [11] [38]
In gravidanza, l'ipotiroidismo subclinico è definito come un TSH tra i 2,5 ei 10 mIU/l con un normale livello di tiroxina, mentre le donne con un TSH sopra 10 mIU/l sono considerati casi di ipotiroidismo conclamato anche se il livello tiroxina è normale. [38] La presenza degli anticorpi anti TPO possono essere importanti nel prendere decisioni sul trattamento e pertanto dovrebbe essere determinata nelle donne con test di funzionalità tiroidea anormale. [11]
La determinazione degli anticorpi TPO può essere considerata come parte della valutazione in seguito ad aborto spontaneo ricorrente . [11] Tuttavia questa raccomandazione non è accettata universalmente [40] e la presenza di anticorpi anti perossidasi tiroidea non può predire anti-tiroide non può predire l'esito futuro. [41]
Endocrinopatie con effetti comuni con l'ipotiroidismo
Alcuni dei sintomi dell'ipotiroidismo (quali ad esempio astenia , aumento di peso, perdita di massa muscolare e della libido , depressione ) sono comuni ad altre endocrinopatie altrettanto diffuse quali ad esempio l' ipogonadismo (carenza di testosterone ) e la sindrome di Cushing . Se si sospetta ipotiroidismo è sempre bene verificare anche i livelli di ACTH , GH , fattore di crescita insulino-simile , cortisolo (plasmatico e urinario), LH , FSH , testosterone libero e totale.
Prevenzione
L'ipotiroidismo può essere evitato con l'aggiunta dello iodio agli alimenti di uso comune. L'adozione di questa misura come intervento di sanità pubblica ha permesso di eliminare l'ipotiroidismo endemico infantile nei paesi dove prima era frequente. Oltre a promuovere il consumo di alimenti ricchi di iodio, come i latticini e il pesce, molti paesi sono intervenuti con la iodizzazione universale del sale (USI). [42] Grazie agli incoraggiamenti della Organizzazione mondiale della sanità [43] , 130 paesi hanno un programma USI e il 70% della popolazione mondiale riceve sale iodato. In alcuni paesi, il sale iodato viene aggiunto al pane. [42] Nonostante ciò, la carenza di iodio è ricomparsa in alcuni paesi occidentali come risultato dei tentativi di ridurre il consumo del sale. [42]
Le donne incinte e che allattano , il cui fabbisogno di iodio è più elevato, possono sperimentarne una mancanza. [42] Si raccomanda pertanto l'assunzione di una dose giornaliera di 250 mg. Siccome molte donne non raggiungono questo obiettivo dalla sola alimentazione, l' American Thyroid Association raccomanda un supplemento di 150 mcg giornaliero da prendere per os . [38] [44]
Trattamento
Terapia ormonale sostitutiva
La terapia dell'ipotiroidismo si basa sulla somministrazione di ormone tiroideo, con lo scopo di ristabilire e mantenere una condizione di eutiroidismo, normalizzando le concentrazioni sieriche di TSH e T 4 libero. Il trattamento avviene mediante somministrazione di tiroxina sintetica a lunga durata d'azione, nota come levotiroxina (L-tiroxina). [11] [20] Nei giovani e nelle persone con ipotiroidismo manifesto ma altrimenti sane, una dose completa può essere assunta immediatamente. Negli anziani e in coloro che soffrono di malattie cardiache, si raccomanda una dose iniziale più bassa per evitare una sopra integrazione e il rischio di complicanze. [11] [33] Dosi inferiori possono essere sufficienti in coloro con ipotiroidismo subclinico, mentre le persone con ipotiroidismo centrale possono richiederne una più elevata rispetto alla dose media. [11]
I livelli ematici di tiroxina e di TSH libero vengono monitorati per determinare se la dose sia sufficiente. Questo viene fatto da 4 a 8 settimane dopo l'inizio del trattamento o quando vi è un cambiamento del dosaggio della levotiroxina. Una volta che il dosaggio adeguato è stato stabilito, i test possono essere ripetuti dopo 6 e poi 12 mesi, salvo se si presenta un cambiamento dei sintomi. [11] Negli individui con ipotiroidismo centrale o secondario, la misurazione di TSH non è un indicatore affidabile per la sostituzione ormonale e le decisioni su trattamento si basano principalmente sul livello di T 4 libero. [11] [18] Nelle formulazioni in compresse è consigliato assumere la levotiroxina da 30 a 60 minuti prima della colazione o quattro ore dopo i pasti [11] in quanto alcune sostanze, come il calcio, possono inibirne l'assorbimento. [45] Tale problema viene parzialmente superato dall'introduzione di formulazioni liquide in soluzione orale, che hanno permeazione fino al 30% più rapida e riducono il rischio di interazione con cibi e bevande assunte in tempi ravvicinati al farmaco. [46] [47] [48] [49]
Non vi è alcun modo diretto per aumentare la secrezione di ormone tiroideo dalla tiroide. [20]
Nel paziente adulto le dosi di T 4 con cui iniziare un trattamento sostitutivo, oscillano tra 1 µg/kg/die, nel caso dell'ipotiroidismo sub-clinico, e 1,6 µg/kg/die, nel caso dell'ipotiroidismo conclamato, soprattutto se il paziente è tireoprivo. Tuttavia la posologia va adattata sulla base dei valori di TSH (determinato con metodo di 3ª generazione) raggiunti, con l'obiettivo terapeutico di riportarli nei limiti della norma. L'obiettivo terapeutico, una volta iniziata la terapia sostitutiva, dovrebbe essere quello di mantenere il TSH nel range di 0,5-2 μU/ml[50] .
Liotironina

L'aggiunta della liotironina (T 3 sintetico) alla levotiroxina è una strategia suggerita come misura per controllare meglio i sintomi, ma tuttavia ciò non è stato confermato da studi al riguardo. [4] [20] [51] Nel 2007, la British Thyroid Association ha dichiarato che la terapia combinata con T 4 e T 3 ha portato ad un più alto tasso di effetti collaterali ea nessun vantaggio rispetto al T 4 da solo. [20] [52] Allo stesso modo, le linee guida statunitense scoraggiano la terapia combinata, proprio per mancanza di prove certe, anche se riconoscono che alcuni casi abbiano tratto beneficio da questo approccio. [11] Il trattamento con la sola liotironina non è suffragato da abbastanza studi al riguardo ed inoltre, a causa della sua breve emivita , deve essere assunta più frequentemente. [11]
Estratto di tiroide animale
La somministrazione di estratto animale, più comunemente da suini, di tiroide essiccata [20] è una terapia di combinazione, contenente forme di T 4 e T 3 . [20] Inoltre essa contiene calcitonina (un ormone prodotto dalla tiroide e coinvolto nella regolazione dei livelli di calcio), T 1 e T 2 . Questi elementi non sono presenti nei farmaci sintetici. [53] Questo approccio una volta era il trattamento fondamentale, ma al 2013 esso non è supportato da sufficienti prove al riguardo. [4] [20] La British Thyroid Association e le linee guida professionali statunitensi ne scoraggiano l'uso. [11] [52]
Ipotiroidismo subclinico
Vi sono poche prove se vi sia un beneficio dal trattamento dell'ipotiroidismo subclinico e se questo compensa i rischi correlati. Un ipotiroidismo subclinico non trattato può essere associato ad un modesto aumento del rischio di malattia coronarica. [54] Una review sistematica del 2007 non ha trovato alcun beneficio dalla sostituzione dell'ormone tiroideo ad eccezione di "alcuni parametri dei profili lipidici e della funzionalità ventricolare sinistra". [55]
A partire dal 2008, la comunità scientifica internazionale si è orientata sul considerare non richiedenti trattamento le persone con TSH inferiore ai 10 μU/ml. [11] [12] [56] Le linee guida statunitensi raccomandano che il trattamento sia comunque considerato per un livello di TSH compreso tra 4,5 e 10 μU/ml nelle persone con sintomi di ipotiroidismo, anticorpi contro perossidasi tiroidea rilevabili, una storia di malattia cardiaca o che hanno un rischio aumentato di incorrerci. [11]
Coma da mixedema
I casi di coma da mixedema richiedono solitamente il ricovero in terapia intensiva , il trattamento delle problematiche relative alla respirazione, il controllo della temperatura corporea, della pressione sanguigna e dei livelli di sodio. La ventilazione artificiale può rendersi necessaria, come la somministrazione di liquidi, di vasopressori e di corticosteroidi (per una eventuale insufficienza surrenalica che può verificarsi con l'ipotiroidismo). La correzione accurata dei bassi livelli di sodio può essere realizzata con soluzioni saline ipertoniche o antagonisti dei recettori della vasopressina. [17] Per un rapido trattamento dell'ipotiroidismo, la levotiroxina o la liotironina possono essere somministrate per via endovenosa , in particolare se il livello di coscienza è troppo basso perché il farmaco possa essere ingoiato in maniera sicura. [17]
Gravidanza
Alle donne con ipotiroidismo noto che affrontano una gravidanza , si raccomanda che i livelli sierici di TSH siano strettamente monitorati. La levotiroxina deve essere utilizzata per mantenere i livelli di TSH entro il range normale per il primo trimestre. Il range normale per il primo trimestre è inferiore a 2,5 mIU/L e per il secondo e per il terzo trimestre è inferiore a 3,0 mIU/L. [20] [38] Il trattamento deve essere guidato dai livelli di totali di tiroxina e non da quelli di tiroxina libera. I risultati dovrebbero essere interpretati secondo il range di riferimento appropriato per quella fase della gravidanza. [11] La dose di levotiroxina abituale solitamente deve essere aumentata dopo che la gravidanza è confermata. [11] [33] [38]
Le donne con anticorpi anti-TPO che cercano di rimanere incinte (naturalmente o tramite procreazione assistita ) possono richiedere la supplementazione di ormone tiroideo, anche se il livello di TSH è normale. Ciò è particolarmente vero se hanno avuto aborti precedenti o hanno avuto ipotiroidismo in passato. [11] L'assunzione di levotiroxina integrativa può ridurre il rischio di parto pretermine e la possibilità di incorrere in aborto spontaneo. [57] Tale raccomandazione è più forte nelle donne in gravidanza con ipotiroidismo subclinico (definito come TSH tra i 2,5 ei 10 mIU/l) che sono anti-TPO positive, in considerazione del rischio di ipotiroidismo manifesto. Se viene presa la decisione di non procedere al trattamento, si raccomanda un attento monitoraggio della funzionalità tiroidea (ogni 4 settimane nelle prime 20 settimane di gravidanza). [11] [38] Se non risulta anti-TPO positiva, il trattamento per l'ipotiroidismo subclinico non è attualmente raccomandato. [38]
Negli animali

Nella pratica veterinaria, i cani sono le specie più frequentemente colpite da ipotiroidismo. La maggior parte dei casi si verifica per un ipotiroidismo primario, di cui due tipi sono riconosciuti: tiroidite linfocitica, che è probabilmente di origine autoimmune e porta alla distruzione e alla fibrosi della ghiandola tiroidea, e l'atrofia idiopatica che porta ad una progressiva sostituzione della ghiandola con tessuto adiposo . [58] [59] Spesso si presentano letargia , intolleranza al freddo, affaticamento nell'esercizio e un aumento di peso. Inoltre, cambiamenti nella pelle e problematiche legate alla fertilità sono frequenti, nonché una serie di altri sintomi. [59] I segni di mixedema possono essere notati nei cani, soprattutto con pieghe della pelle sulla fronte e talvolta si hanno anche casi di coma da mixedema. [58] La diagnosi può essere confermata da analisi del sangue; la sola valutazione clinica può portare a sovradiagnosi. [58] [59] La tiroidite linfocitaria è associata al rilevamento di anticorpi anti-tireoglobulina, anche se ciò avviene ad uno stadio avanzato della malattia. [59] Il trattamento consiste nella somministrazione sostitutiva dell'ormone tiroideo. [58]
Gatti e cavalli sono meno comunemente colpiti, così come altri grandi animali domestici. Nei gatti l'ipotiroidismo è di solito il risultato di altre cure mediche, come la chirurgia o la radioterapia. Nei cavalli più giovani, casi di ipotiroidismo congenito sono stati rilevati principalmente in Canada occidentale e sono stati correlati con la dieta del genitore femmina. [58]
Distiroidismo
Vi è poi una condizione nella quale convivono, apparentemente paradossalmente, in proporzione variabile, i sintomi sia dell'ipotiroidismo sia quelli dell'ipertiroidismo, condizione probabilmente causata dallo squilibrio in senso reciprocamente opposto dei diversi tipi di ormoni tiroidei. Qualora si sospetti una patologia tiroidea, questa apparente incoerenza nei vari sintomi contrapposti può indurre in diagnosi errate, in tal caso si parla di distiroidismo.
Note
- ^ a b c d e f g E. Puxeddu, F. Santeusanio, Trattato di Medicina Interna, fondato da Paolo Larizza, Volume III, Malattie delle ghiandole endocrine, del metabolismo e della nutrizione, a cura di Paolo Brunetti e Fausto Santeusanio; Piccin Nuova Libraria, 2011. ( ISBN 978-88-299-2111-9 )
- ^ Emanuele Peccioli, La tiroide negli animali e le patologie ad essa collegate , su peccioliveterinario.it , 10 settembre 2016.
- ^ Raffaella Lauretta, Problemi alla tiroide del gatto: ipotiroidismo e ipertiroidismo , su amoreaquattrozampe.it .
- ^ a b c d e f g Chakera, AJ; Pearce, SH; Vaidya, B,Treatment for primary hypothyroidism: current approaches and future possibilities (Review), in Drug Design, Development and Therapy , vol. 6, 2012, pp. 1-11, DOI : 10.2147/DDDT.S12894 , PMC 3267517 , PMID 22291465 .
- ^ a b AM Leung, Braverman, LE; Pearce, EN, History of US iodine fortification and supplementation , in Nutrients , vol. 4, n. 11, 13 novembre 2012, pp. 1740-6, DOI : 10.3390/nu4111740 , PMC 3509517 , PMID 23201844 .
- ^ GR Murray,Note on the Treatment of Myxoedema by Hypodermic Injections of an Extract of the Thyroid Gland of a Sheep , in British Medical Journal , vol. 2, n. 1606, 10 ottobre 1891, pp. 796-7, DOI : 10.1136/bmj.2.1606.796 , PMC 2273741 , PMID 20753415 .
- ^ EL Fox,A Case of Myxoedema Treated by Taking Extract of Thyroid by the Mouth , in British Medical Journal , vol. 2, n. 1661, 29 ottobre 1892, p. 941, DOI : 10.1136/bmj.2.1661.941 , PMC 2421284 , PMID 20753901 .
- ^ MP. Vanderpump, WM. Tunbridge; JM. French; D. Appleton; D. Bates; F. Clark; J. Grimley Evans; DM. Hasan; H. Rodgers; F. Tunbridge, The incidence of thyroid disorders in the community: a twenty-year follow-up of the Whickham Survey. , in Clin Endocrinol (Oxf) , vol. 43, n. 1, luglio 1995, pp. 55-68, PMID 7641412 .
- ^ JG. Hollowell, NW. Staehling; WD. Flanders; WH. Hannon; EW. Gunter; CA. Spencer; LE. Braverman, Serum TSH, T(4), and thyroid antibodies in the United States population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III). , in J Clin Endocrinol Metab , vol. 87, n. 2, febbraio 2002, pp. 489-99, DOI : 10.1210/jcem.87.2.8182 , PMID 11836274 .
- ^ Cooper, DS; Braverman LE (a cura di), Werner & Ingbar's the thyroid : a fundamental and clinical text , 10th, Philadelphia, Wolters Kluwer/Lippincott Williams & Wilkins Health, 12 luglio 2012, p. 552, ISBN 1-4511-2063-X .
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an JR Garber, Cobin, RH; Gharib, H; Hennessey, JV; Klein, I; Mechanick, JI; Pessah-Pollack, R; Singer, PA; Woeber, KA for the American Association of Clinical Endocrinologists and the American Thyroid Association Taskforce on Hypothyroidism in Adults, Clinical Practice Guidelines for Hypothyroidism in Adults ( PDF ), in Thyroid , vol. 22, n. 12, dicembre 2012, pp. 1200-1235, DOI : 10.1089/thy.2012.0205 , PMID 22954017 . URL consultato il 2 marzo 2014 (archiviato dall' url originale il 14 gennaio 2016) .
- ^ a b c d V. Fatourechi, Subclinical Hypothyroidism: An Update for Primary Care Physicians (Review), in Mayo Clinic Proceedings , vol. 84, n. 1, 2009, pp. 65–71, DOI : 10.4065/84.1.65 , PMC 2664572 , PMID 19121255 .
- ^ A Monzani, Prodam, F; Rapa, A; Moia, S; Agarla, V; Bellone, S; Bona, G, Endocrine disorders in childhood and adolescence. Natural history of subclinical hypothyroidism in children and adolescents and potential effects of replacement therapy: a review , in European Journal of Endocrinology , vol. 168, n. 1, Jan 2013, pp. R1–R11, DOI : 10.1530/EJE-12-0656 , PMID 22989466 (archiviato dall' url originale il 1º gennaio 2014) .
- ^ a b c Bona, G; Prodam, F; Monzani, A,Subclinical hypothyroidism in children: natural history and when to treat (Review), in Journal of Clinical Research in Pediatric Endocrinology , 5 Suppl 1, n. 4, 2013, pp. 23-8, DOI : 10.4274/jcrpe.851 , PMC 3608012 , PMID 23154159 .
- ^ a b c d e f g D Counts, Varma, SK, Hypothyroidism in children , in Pediatrics in Review , vol. 30, n. 7, 2009 Jul, pp. 251-8, DOI : 10.1542/pir.30-7-251 , PMID 19570923 .
- ^ Malt, EA; Dahl, RC; Haugsand, TM; et al. , Health and disease in adults with Down syndrome (Review), in Tidsskrift for Den Norske Legeforening , vol. 133, n. 3, febbraio 2013, pp. 290-4, DOI : 10.4045/tidsskr.12.0390 , PMID 23381164 .
- ^ a b c d e f J Klubo-Gwiezdzinska, Wartofsky, L, Thyroid emergencies , in Medical Clinics of North America , vol. 96, n. 2, marzo 2012, pp. 385-403, DOI : 10.1016/j.mcna.2012.01.015 , PMID 22443982 .
- ^ a b c d e Persani, L, Clinical review: Central hypothyroidism: pathogenic, diagnostic, and therapeutic challenges (Review), in The Journal of Clinical endocrinology and Metabolism , vol. 97, n. 9, settembre 2012, pp. 3068-78, DOI : 10.1210/jc.2012-1616 , PMID 22851492 . URL consultato il 2 marzo 2014 (archiviato dall' url originale il 7 gennaio 2014) .
- ^ a b c d e DL Longo, Fauci, AS; Kasper, DL; Hauser, SL; Jameson, JL; Loscalzo, J, 341: disorders of the thyroid gland , in Harrison's principles of internal medicine. , 18th, New York, McGraw-Hill, 2011, ISBN 0-07-174889-X .
- ^ a b c d e f g h i Khandelwal D, Tandon N, Overt and subclinical hypothyroidism: who to treat and how (Review), in Drugs , vol. 72, n. 1, gennaio 2012, pp. 17-33, DOI : 10.2165/11598070-000000000-00000 , PMID 22191793 .
- ^ Führer D, Bockisch A, Schmid KW, Euthyroid goiter with and without nodules--diagnosis and treatment. , in Dtsch Arztebl Int , vol. 109, n. 29-30, luglio 2012, pp. 506-15, DOI : 10.3238/arztebl.2012.0506 , PMC 3441105 , PMID 23008749 .
- ^ Hofeldt FD, Dippe S, Forsham PH, Diagnosis and classification of reactive hypoglycemia based on hormonal changes in response to oral and intravenous glucose administration , in Am. J. Clin. Nutr. , vol. 25, n. 11, novembre 1972, pp. 1193-201, PMID 5086042 .
- ^ a b c Fabrizio Monaco, Malattie della tiroide , SEU, 2007, ISBN 978-88-89548-57-8 .
- ^ a b van den Boogaard, E; Vissenberg, R; Land, JA et al. , Significance of (sub)clinical thyroid dysfunction and thyroid autoimmunity before conception and in early pregnancy: a systematic review (Review), in Human Reproduction Update , vol. 17, n. 5, 2011, pp. 605-19, DOI : 10.1093/humupd/dmr024 , PMID 21622978 .
- ^ a b Vissenberg, R; van den Boogaard, E; van Wely, M et al. , Treatment of thyroid disorders before conception and in early pregnancy: a systematic review (Review), in Human Reproduction Update , vol. 18, n. 4, luglio 2012, pp. 360-73, DOI : 10.1093/humupd/dms007 , PMID 22431565 .
- ^ Fredric E. Wondisford, Sally Radovick Clinical Management of Thyroid Disease. Saunders Elsevier, 2009.
- ^ a b EN Pearce, Update in lipid alterations in subclinical hypothyroidism , in The Journal of Clinical endocrinology and Metabolism , vol. 97, n. 2, Feb 2012, pp. 326-33, DOI : 10.1210/jc.2011-2532 , PMID 22205712 . URL consultato il 28 marzo 2014 (archiviato dall' url originale il 1º gennaio 2014) .
- ^ Roberto Gastaldi, Ipotiroidismo congenito: lo screening neonatale , su tiroide.com . URL consultato il 21 marzo 2017 .
- ^ a b Andrew Calabria, Hypothyroidism in Infants and Children , Merck manual professional version.
- ^ a b Brown RS., Disorders of the Thyroid Gland in Infancy, Childhood and Adolescence. , PMID 25905261 .
- ^ a b Grüters A, Krude H., Detection and treatment of congenital hypothyroidism. , in Nat Rev Endocrinol , vol. 2, n. 8, 2011 Oct 18, pp. 104-13, DOI : 10.1038/nrendo.2011.160 , PMID 22009163 .
- ^ a b Brown, RS,Autoimmune thyroiditis in childhood (Review), in Journal of Clinical Research in Pediatric Endocrinology , 5 Suppl 1, n. 4, 2013, pp. 45-9, DOI : 10.4274/jcrpe.855 , PMC 3608006 , PMID 23154164 .
- ^ a b c d e Gaitonde, DY; Rowley, KD; Sweeney, LB, Hypothyroidism: an update (Review), in American Family Physician , vol. 86, n. 3, agosto 2012, pp. 244-51, PMID 22962987 .
- ^ a b Stagnaro-Green, A, Approach to the patient with postpartum thyroiditis (Review), in The Journal of Clinical endocrinology and Metabolism , vol. 97, n. 2, febbraio 2012, pp. 334-42, DOI : 10.1210/jc.2011-2576 , PMID 22312089 . URL consultato il 17 aprile 2014 (archiviato dall' url originale l'8 aprile 2020) .
- ^ Donaldson, M; Jones, J,Optimising outcome in congenital hypothyroidism; current opinions on best practice in initial assessment and subsequent management (Review), in Journal of Clinical Research in Pediatric Endocrinology , 5 Suppl 1, n. 4, 2013, pp. 13-22, DOI : 10.4274/jcrpe.849 , PMC 3608009 , PMID 23154163 .
- ^ AL Maia, Goemann, IM; Meyer, EL; Wajner, SM, Type 1 iodothyronine deiodinase in human physiology and disease: Deiodinases: the balance of thyroid hormone , in Journal of Endocrinology , vol. 209, n. 3, 17 marzo 2011, pp. 283-297, DOI : 10.1530/JOE-10-0481 , PMID 21415143 .
- ^ a b SY Cheng, Leonard, JL; Davis, PJ,Molecular aspects of thyroid hormone actions , in Endocrine Reviews , vol. 31, n. 2, Apr 2010, pp. 139-70, DOI : 10.1210/er.2009-0007 , PMC 2852208 , PMID 20051527 .
- ^ a b c d e f g h i A Stagnaro-Green, Abalovich, M; Alexander, E; Azizi, F; Mestman, J; Negro, R; Nixon, A; Pearce, EN; Soldin, OP; Sullivan, S; Wiersinga, W; American Thyroid Association Taskforce on Thyroid Disease During Pregnancy and Postpartum, Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and postpartum , in Thyroid , vol. 21, n. 10, Oct 2011, pp. 1081-125, DOI : 10.1089/thy.2011.0087 , PMC 3472679 , PMID 21787128 .
- ^ a b c d So, M; MacIsaac, RJ; Grossmann M, Hypothyroidism , in Australian Family Physician , vol. 41, n. 8, agosto 2012, pp. 556-62, PMID 23145394 .
- ^ The Practice Committee of the American Society for Reproductive Medicine, Evaluation and treatment of recurrent pregnancy loss: a committee opinion , in Fertility and Sterility , vol. 98, n. 5, novembre 2012, pp. 1103-1111, DOI : 10.1016/j.fertnstert.2012.06.048 , PMID 22835448 .
- ^ Regan, L ; Backos M; Rai, R, The investigation and treatment of couples with recurrent first-trimester and second-trimester miscarriage ( PDF ), su Green-top Guideline No. 17 , London, Royal College of Obstetricians and Gynaecologists, 19 maggio 2011. URL consultato il 26 dicembre 2013 (archiviato dall' url originale il 31 dicembre 2013) .
- ^ a b c d K Charlton, Skeaff, S, Iodine fortification , in Current Opinion in Clinical Nutrition and Metabolic Care , vol. 14, n. 6, novembre 2011, pp. 618-624, DOI : 10.1097/MCO.0b013e32834b2b30 , PMID 21892078 .
- ^ World Health Organization, UNICEF, ICCIDD, Assessment of iodine deficiency disorders and monitoring their elimination ( PDF ), 3rd, Geneva, World Health Organization, 2008, ISBN 978-92-4-159582-7 .
- ^ Public Health Committee of the American Thyroid Association, Becker, DV; Braverman, LE; Delange, F; Dunn, JT; Franklyn, JA; Hollowell, JG; Lamm, SH; Mitchell, ML; Pearce, E; Robbins, J; Rovet, JF, Iodine supplementation for pregnancy and lactation-United States and Canada: recommendations of the American Thyroid Association , in Thyroid , vol. 16, n. 10, Oct 2006, pp. 949-51, DOI : 10.1089/thy.2006.16.949 , PMID 17042677 .
- ^ Cascorbi, I,Drug interactions--principles, examples and clinical consequences (Review), in Deutsches Ärzteblatt International , vol. 109, 33–34, agosto 2012, pp. 546-55, DOI : 10.3238/arztebl.2012.0546 , PMC 3444856 , PMID 23152742 .
- ^ Morelli S, Reboldi G, Moretti S, Menicali E, Avenia N, Puxeddu E., Timing of breakfast does not influence therapeutic efficacy of liquid levothyroxine formulation. , in Endocrine , vol. 3, n. 52, Jun 2016, DOI : 10.1007/s12020-015-0788-2 , PMID 26537478 .
- ^ Cappelli C, Pirola I, Daffini L, Formenti A, Iacobello C, Cristiano A, Gandossi E, Agabiti Rosei E, Castellano M., A Double-Blind Placebo-Controlled Trial of Liquid Thyroxine Ingested at Breakfast: Results of the TICO Study. , in Thyroid , vol. 2, n. 26, Feb 2016, pp. 197-202, DOI : 10.1089/thy.2015.0422. .
- ^ Brancato D, Scorsone A, Saura G, Ferrara L, Di Noto A, Aiello V, Fleres M, Provenzano V., Comparison of TSH Levels with Liquid Formulation Versus Tablet Formulations of Levothyroxine in the Treatment of Adult Hypothyroidism. , in Endocr Pract , vol. 7, n. 20, Jul 2014, pp. 657-62.
- ^ Negro R, Valcavi R, Agrimi D, Toulis KA., Levothyroxine liquid solution versus tablet for replacement treatment in hypothyroid patients. , in Endocr Pract , vol. 9, n. 20, Sep 2014, pp. 901-6.
- ^ Wartofsky L, Dickey RA. The evidence for a narrower thyrotropin reference range is compelling. J Clin Endocrinol Metab. 2005 Sep;90(9):5483-8.
- ^ Escobar-Morreale, HF; Botella-Carretero, JI; Escobar del Rey, F; Morreale de Escobar, G, Treatment of hypothyroidism with combinations of levothyroxine plus liothyronine (Review), in The Journal for Clinical Endocrinology and Metabolism , vol. 90, n. 8, agosto 2005, pp. 4946-54, DOI : 10.1210/jc.2005-0184 , PMID 15928247 . URL consultato il 17 aprile 2014 (archiviato dall' url originale il 13 febbraio 2013) .
- ^ a b British Thyroid Association Executive Committee, Armour Thyroid(USP) and combinedthyroxine/tri-iodothyronine as thyroid hormone replacement ( PDF ), su british-thyroid-association.org , British Thyroid Association, novembre 2007. URL consultato il 25 dicembre 2013 (archiviato dall' url originale il 3 dicembre 2008) .
- ^ Ebling PR, ESA Position Statement on Desiccated Thyroid or Thyroid Extract ( PDF ), su endocrinesociety.org.au , Endocrine Society of Australia, 2011. URL consultato il 13 dicembre 2013 (archiviato dall' url originale il 26 gennaio 2014) .
- ^ Ochs, N; Auer, R; Bauer, DC et al. , Meta-analysis: subclinical thyroid dysfunction and the risk for coronary heart disease and mortality (Meta-analysis), in Annals of Internal Medicine , vol. 148, n. 11, giugno 2008, pp. 832-45, DOI : 10.7326/0003-4819-148-11-200806030-00225 , PMID 18490668 .
- ^ Villar HC, Saconato H, Valente O, Atallah AN, Thyroid hormone replacement for subclinical hypothyroidism (Review, meta-analysis), in Heloisa Cerqueira Cesar Esteves Villar (a cura di), Cochrane Database of Systematic Reviews , n. 3, 2007, pp. CD003419, DOI : 10.1002/14651858.CD003419.pub2 , PMID 17636722 .
- ^ The Royal College of Physicians, The Association for Clinical Biochemistry The Society for Endocrinology, The British Thyroid Association et al , The Diagnosis and Management of Primary Hypothyroidism ( PDF ), su british-thyroid-association.org , 19 novembre 2008. URL consultato il 16 giugno 2013 (archiviato dall' url originale il 7 dicembre 2013) .
- ^ SM Reid, Middleton, P; Cossich, MC; Crowther, CA; Bain, E, Interventions for clinical and subclinical hypothyroidism pre-pregnancy and during pregnancy , in Sally M Reid (a cura di), Cochrane Database of Systematic Reviews , vol. 5, n. 5, 2013, pp. CD007752, DOI : 10.1002/14651858.CD007752.pub3 , PMID 23728666 .
- ^ a b c d e Hypothyroidism , su Merck Veterinary Manual, 10th edition (online version) , 2012. URL consultato il 25 dicembre 2013 .
- ^ a b c d CT Mooney, Canine hypothyroidism: A review of aetiology and diagnosis , in New Zealand Veterinary Journal , vol. 59, n. 3, maggio 2011, pp. 105-114, DOI : 10.1080/00480169.2011.563729 , PMID 21541883 .
Bibliografia
- Elaine N. Marieb, Il corpo umano, anatomia fisiologia salute , Zanichelli, 2004, ISBN 978-88-08-11257-6 .
- Fabrizio Monaco, Malattie della tiroide , SEU, 2007, ISBN 978-88-89548-57-8 .
- E. Puxeddu, F. Santeusanio, Malattie delle ghiandole endocrine, del metabolismo e della nutrizione , in Paolo Brunetti e Fausto Santeusanio (a cura di), Trattato di Medicina Interna, fondato da Paolo Larizza , Volume III, Piccin Nuova Libraria, 2011, ISBN 978-88-299-2111-9 .
- ( EN ) Cooper, DS; Braverman LE (a cura di), Werner & Ingbar's the thyroid: a fundamental and clinical text , 10th, Philadelphia, Wolters Kluwer/Lippincott Williams & Wilkins Health, ISBN 1-4511-2063-X .
- ( EN ) DL Longo, Fauci, AS; Kasper, DL; Hauser, SL; Jameson, JL; Loscalzo, J, 341: disorders of the thyroid gland , in Harrison's principles of internal medicine , 18th, New York, McGraw-Hill, 2011, ISBN 0-07-174889-X .
- ( EN ) World Health Organization, UNICEF, ICCIDD, Assessment of iodine deficiency disorders and monitoring their elimination ( PDF ), 3rd, Geneva, World Health Organization, 2008, ISBN 978-92-4-159582-7 .
Voci correlate
Altri progetti
-
 Wikizionario contiene il lemma di dizionario « ipotiroidismo »
Wikizionario contiene il lemma di dizionario « ipotiroidismo » -
 Wikimedia Commons contiene immagini o altri file su ipotiroidismo
Wikimedia Commons contiene immagini o altri file su ipotiroidismo
Collegamenti esterni
- ( EN ) Ipotiroidismo , su Enciclopedia Britannica , Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 24494 · LCCN ( EN ) sh85063828 · GND ( DE ) 4161154-8 · BNF ( FR ) cb12317444k (data) |
|---|