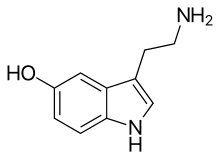
Serotonina
| Serotonina | |
|---|---|
| Numele IUPAC | |
| 3- (2-aminoetil) -1 H -indol-5-ol | |
| Denumiri alternative | |
| 5-HT 5-hidroxitriptamina | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 10 H 12 N 2 O |
| Masa moleculară ( u ) | 176,22 |
| numar CAS | |
| Numărul EINECS | 200-058-9 |
| PubChem | 5202 |
| DrugBank | DB08839 |
| ZÂMBETE | C1=CC2=C(C=C1O)C(=CN2)CCN |
| Proprietăți fizico-chimice | |
| Constanta de disociere a acidului (pKa) la 298 K. | 9,8; 11.1 |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
 | |
| Atenţie | |
| Fraze H | 302 - 312 - 315 - 319 - 332 - 335 |
| Sfaturi P | 261 - 280 - 305 + 351 + 338 [1] |
Serotonina sau 5-hidroxitriptamina ( 5-HT ) [N 1] este o triptamină , sintetizată din aminoacidul triptofan ( 5-HTP ), care la animale este produs în principal de neuronii serotoninergici din sistemul nervos central și de celulele enterocromafine din sistemul gastrointestinal tractului , unde participă la numeroase funcții biologice. Se găsește, însă, nu numai la animale, ci și la ciuperci, plante și otravă a unor insecte (precum și la nivelul spinilor unor plante) pentru capacitatea sa de a provoca durere la locul injectării. De asemenea, este produs de unele microorganisme, cum ar fi amibele. [2]
Substanța a fost izolată în Pavia de Vittorio Erspamer în 1935 , clasificată inițial ca polifenol ; doi ani mai târziu, în urma studiilor efectuate asupra glandelor cutanate ale discoglossului și ale glandelor salivare ale caracatițelor , a fost apoi redenumită enteramină, numită apoi serotonină în 1948 .
Excesul de serotonină poate duce în cazuri foarte rare la un episod de criză cunoscut sub numele de sindromul serotoninei . Sale formula chimică este C 10 H 12 N 2 O, greutatea moleculară este 176,22, numărul CAS 50-67-9.
Distribuție, biosinteză și degradare
Cele mai mari concentrații de 5-HT se găsesc în trei locuri diferite ale corpului:
- Peretele intestinal . Celulele enterocromafine conțin aproximativ 90% din cantitatea totală de 5-HT prezentă în organism: aceste celule, derivate din creasta neuronală și similare cu cele ale medularei suprarenale, sunt amestecate cu celule mucoase și se găsesc în principal în stomac și în intestinul subțire. Contribuie la reglarea motilității și secrețiilor gastrointestinale. [3] [4]
- În sânge . O parte din 5-HT secretată de celulele enterocromafine intră în fluxul sanguin unde este colectată, printr-un sistem de transport activ (captare) de către trombocite , care o acumulează din plasmă. Acționează asupra dilatației vaselor și ajută la reglarea homeostaziei și a proceselor de vindecare. [5]
- În sistemul nervos central . 5-HT este produs de un grup relativ mic de celule, conținute în principal în structuri numite nuclei de rafe , un set de nouă nuclee ale creierului, ale căror conexiuni se extind în întregul sistem nervos central, până la măduva spinării. Sistemul serotoninergic este implicat în funcții importante, de exemplu, joacă un rol în reglarea dispoziției, emoțiilor și sexualității, funcțiilor cognitive, reglarea somnului și a apetitului. [6] [7]
Metabolism
Biosinteza 5-HT endogenă urmează o cale similară cu cea a noradrenalinei , cu diferența că aminoacidul precursor este triptofan , în loc de tirozină . Triptofanul este transformat în 5-hidroxitriptofan datorită acțiunii triptofan-hidroxilazei . 5-hidroxitriptofanul (5-HTP) astfel produs este decarboxilat la 5-HT, de către enzima decarboxilază. Trombocitele acumulează 5-HT în timpul trecerii lor prin circulația intestinală, unde concentrația locală este relativ mare. 5-HT este adesea stocat în neuroni și celule enterocromafine ca un co-transmițător împreună cu diverși hormoni peptidici, cum ar fi somatostatina , substanța P și polipeptida vasoactivă intestinală.
Degradarea 5-HT are loc printr-o deminație oxidativă , catalizată de monoaminooxidază , urmată de oxidare la acid 5-hidroxiindolacetic (5-HIAA) și de enzima sulfotransferază care duce la formarea triptaminei-O-sulfat. Aminoacizii cu lanț ramificat reduc absorbția triptofanului (și, prin urmare, producția de serotonină) la nivelul barierei hematoencefalice (barieră care separă sistemul vascular de sistemul nervos central).
Funcţie
La nivelul diferitelor țesuturi, serotonina are diferite efecte fiziologice
- Tractul gastro-intestinal . 5-HT determină creșterea motilității intestinale, parțial datorită unui efect direct asupra celulelor musculare netede și parțial datorită unui efect excitator indirect asupra neuronilor enterici. 5-HT stimulează, de asemenea, secreția de lichide; de asemenea, provoacă greață și vărsături prin stimularea mușchilor netezi și a nervilor senzoriali din stomac. Reflexul peristaltic, evocat de creșterea presiunii într-un segment al intestinului, este mediat, cel puțin parțial, de secreția serotoninei de către celulele enterocromafine, ca răspuns la stimulul mecanic. Celulele cromafinei răspund, de asemenea, la stimularea vagală, provocând secreția de 5-HT.
- Vasele de sânge . De obicei are o acțiune contractilă asupra vaselor mari, atât ale arterelor, cât și ale venelor. Activarea receptorilor 5-HT 1D dă naștere la vasoconstricție a vaselor mari intracraniene, a căror dilatare contribuie la migrena.
- Trombocite . 5-HT provoacă agregarea trombocitelor prin intermediul receptorilor 5-HT 2A , iar trombocitele care se colectează în vase eliberează mai mult 5-HT. Dacă endoteliul este intact, eliberarea de 5-HT din trombocitele atașate determină vasodilatație, care permite fluxului sanguin să curgă; dacă este deteriorat, 5-HT provoacă constricție și obstrucționează în continuare fluxul sanguin.
- Terminațiile nervoase . 5-HT stimulează terminațiile nervoase senzoriale nociceptive, în principal prin intermediul receptorilor 5-HT 3 . Dacă este injectat în piele, provoacă durere.
- Sistemul nervos central . 5-HT joacă un rol fundamental în sistemul nervos central, în principal de tip reglator, unde excită unii neuroni și îi inhibă pe alții; sinteza și eliberarea sa sunt gestionate fin atât de stimulii nervoși, cât și de sistemele de reglare, cum ar fi sistemul presinaptic autoinhibitor care inhibă eliberarea neurotransmițătorilor de la terminațiile nervoase.
În plus, serotonina este implicată în metabolismul osos, [8] în dezvoltarea și repararea organelor precum ficatul [9] și inima, [10] reglarea temperaturii corpului, a inimii și a ritmului respirator. Serotonina este un antagonist necompetitiv al testosteronului și estradiolului, deoarece ridică cortizolul și crește nivelul prolactinei, rezultând inhibarea factorului de eliberare a gonadotropinei. Serotonina este frâna naturală a ejaculării reflexul și un nivel scăzut al acestui neurotransmitator este principala cauză constituțională a prematură ejaculare.
Sistem nervos central
În sistemul nervos central, serotonina îndeplinește numeroase funcții, de la reglarea dispoziției , somnului , temperaturii corpului, sexualității , empatiei, funcțiilor cognitive, creativității și apetitului . Se consideră că modificări patologice ale funcției circuitelor serotoninergice sunt implicate în numeroase tulburări neuropsihiatrice , cum ar fi migrenă , tulburare obsesiv-compulsivă , depresie și schizofrenie, tulburări de anxietate și dispoziție în general, tulburări alimentare (foame nervoase și bulimie ), ejaculare prematură masculină și fibromialgia pentru a numi câteva, deși nu este clar modul exact în care aceste schimbări sunt implicate în aceste condiții. Prin urmare, manipularea circuitelor cerebrale ale serotoninei se află în centrul mecanismului de acțiune al numeroaselor medicamente psihotrope, în special antidepresive (cum ar fi antidepresivele SSRI precum Dropaxin , Prozac și Zoloft , antidepresive triciclice și inhibitori de monoaminooxidază ) și antipsihotice, dar și unele droguri (cum ar fi cocaina, psihedelicele, MDA și MDMA ).
Serotonina și depresia
De-a lungul anilor, cultura populară, cu acoperire mediatică, [11] a descris lipsa serotoninei ca fiind cauza depresiei și mai general a stărilor negative, contribuind la generarea mitului „hormonului fericirii” [12] și, în consecință, a pastilelor fericite. , deoarece unele antidepresive sunt adesea definite, în special în SUA. [13] [14] Cu toate acestea, această teorie, născută din studii uneori negate efectuate încă din anii 1960, se dovedește a fi o simplificare excesivă a rolului real al acestui neurotransmițător în geneza tulburărilor psihiatrice, atât de mult încât astăzi lipsa de serotonină nu este considerată o cauză a depresiei și acest concept este reiterat și în manualul Asociației Americane de Psihiatrie. [15]
Legătura dintre deficiența de serotonină și depresie apare din observațiile experimentale efectuate începând cu anii 1960, în special de către cărturarul Joseph Schildkraut care în 1965 a publicat un studiu în care a susținut această teorie. [16] În anii următori, alte studii au părut să confirme această ipoteză, detectând niveluri scăzute de metaboliți (produși de descompunere) ai serotoninei în creierul cobaiilor deprimați și în lichidul cefalorahidian al pacienților cu gânduri suicidare. Acest lucru a condus la dovezi care confirmă „Ipoteza monoaminergică” a depresiei, ceea ce a condus, prin urmare, cercetarea farmacologică către studiul compușilor capabili să reechilibreze din ce în ce mai selectiv aceste presupuse „dezechilibre chimice”. [14] Cu toate acestea, până în prezent numeroase studii au pus sub semnul întrebării legătura dintre deficitul de serotonină și depresie, subliniind faptul că cercetarea care părea să confirme această teorie a fost adesea efectuată cu erori metodologice și pe eșantioane prea mici de subiecți și că eficacitatea tratamentului medicamentos se crede că crește concentrațiile de serotonină, cum ar fi ISRS, nu dovedește o astfel de legătură. [12] [14]
Într-adevăr, încercările de a induce sau reduce depresia prin manipularea directă a nivelurilor de serotonină au produs rezultate mixte și nesemnificative. Într-un studiu, de exemplu, unui grup de pacienți cu depresie li s-au administrat doze mari de triptofan, precursorul esențial al aminoacizilor serotoninei, dar acest lucru nu a avut niciun efect asupra depresiei. [17] Experimentul opus, care reduce nivelurile de triptofan din dietă, este incapabil să inducă depresia. [18] Reducerea drastică a nivelurilor de serotonină prin utilizarea unui inhibitor al triptofan hidroxilazei (enzima care produce serotonină), p-cloro fenilalanina , a indus o recidivă depresivă la doar 30% dintre pacienții deja deprimați și în tratamentul cu un antidepresiv serotoninergic , inducând niciun efect special asupra dispoziției la pacienții sănătoși. [19] [20] În prezent, cercetările nu au identificat leziuni în nuclee care produc serotonină și nici o deficiență reală a acestui neurotransmițător în creierul pacienților cu depresie, [12] studiile în creștere evidențiază complexitatea și mecanismele actuale de înțelegere slabă. a creierului sugerează că o teorie a depresiei „neurotransmițător unic” este nerealistă. [21]
Cel mult, scăderea posibilă a nivelurilor de serotonină ar putea fi un efect secundar al altor modificări biochimice care pot apărea în timpul unei tulburări depresive. [22] [23] De exemplu, studiile au arătat că antidepresivele, secundare modificării nivelurilor de serotonină pe care le induc, activează mecanisme biologice (cum ar fi eliberarea factorilor neurotrofici, activarea metabolismelor antiinflamatorii, desensibilizarea receptorilor de monoamină, alterarea a expresiei genice cu inducerea sau reprimarea anumitor gene) despre care se crede că sunt responsabile pentru efectele terapeutice. [24]
Încercările de manipulare a serotoninei în sistemul nervos central prin nutriție nu produc rezultate semnificative asupra nivelurilor percepute de bunăstare și dispoziție.
Comportamentul sexual
Serotonina afectează direct și indirect comportamentul sexual. Face acest lucru atât deoarece circuitele de serotonină sunt direct implicate în percepția sentimentelor de empatie și legătura emoțională (despre care se crede că sunt induse de o creștere a cantității acestui neurotransmițător în special neuroni și care duce, printre altele, la eliberarea de oxitocină) și deoarece circuitele serotoninei sunt capabile să regleze indirect activitatea altor neurotransmițători implicați în percepția dorinței sexuale, de exemplu dopamina (în acest caz o creștere a nivelului serotoninei determină o scădere a celor ale dopaminei, precum și a altor efecte asupra sistemului nervos central, care duc în general la scăderea libidoului). Acesta este motivul pentru care multe medicamente antidepresive, care acționează direct asupra circuitelor serotoninei, sunt capabile să influențeze puternic comportamentul sexual, provocând în unele cazuri chiar disfuncții sexuale pe termen lung [25] .
În ceea ce privește influența serotoninei asupra sferei sexuale, un studiu publicat în revista Nature în 2011 a arătat că șoarecii masculi lipsiți genetic de celulele creierului utilizate pentru sinteza serotoninei dezvoltă un interes sexual egal față de șoarecii masculi și femele, încercând în 50% cazuri de împerechere mai întâi cu masculi și apoi cu femele. Dacă un precursor al serotoninei este injectat la acești șoareci masculi, după o jumătate de oră se întorc să se împerecheze cu șoareci femele ca prioritate. [26] Teza controversată [27] este că, cel puțin la animale, deficitul de serotonină este principalul factor al preferinței homosexuale. În schimb, chiar și la șoareci s-a văzut că excesul de serotonină nu duce la alegerea sexului opus, ci la o situație de indiferență față de orice activitate sexuală. Acest fenomen al scăderii libidoului și al oricărei dorințe și aspirații în general este cunoscut și la om, de exemplu, printre efectele secundare cunoscute ale medicamentelor antidepresive.
Efecte farmacologice
Serotonina își realizează efectele farmacologice prin 2 moduri diferite:
- Prin legarea la receptori speciali (comutatoare chimice) dispuse pe suprafața celulei, a căror activare dă naștere eliberării de mesageri chimici secundari care sunt responsabili de acțiunea biologică a serotoninei. La oameni au fost identificați 14 receptori de serotonină diferiți, cuplați atât la canalele ionice, cât și la proteinele G. [28]
- Prin serotonilare, adică alterarea conformației proteinelor indusă de legarea serotoninei de acestea și care activează diferite răspunsuri biologice. Secreția de insulină indusă de serotonină [29] sau contracția musculară [30] este un exemplu de răspunsuri biologice datorate serotonilării.
Odată ce acțiunea sa biologică s-a încheiat, serotonina poate fi fie transportată de fluxul sanguin, fie poate fi reabsorbită de celulele care o eliberează printr-un sistem de transport activ (recaptarea serotoninei) pentru a fi apoi stocată în interiorul celulelor sau degradată de enzime speciale. În sistemul nervos central, 90% din serotonină este recuperată prin acest sistem, în timp ce doar 10% se pierde. Doi transportatori ai serotoninei au fost descoperite până în prezent: SERT (Serotonină Transporter) , care a fost mult timp considerat a fi proteinei transportor numai cu membrana pentru serotonină și care este ținta farmacologică a mai multor medicamente ( SSRI antidepresive, antidepresivele triciclice ) sau substanțe de abuz (. Cocaina , MDMA) și singurul transportor recent descoperit pentru monoamine cu afinitate scăzută (PMAT). [31]
Receptorii serotoninei
Receptorii serotoninei se găsesc în sistemul nervos central și periferic , pe membrana celulară a celulelor nervoase și în alte tipuri de celule . Receptorii serotoninei influențează diverse procese biologice și neurologice, cum ar fi agresivitatea , anxietatea , pofta de mâncare , cunoașterea , învățarea , memoria , dispoziția , greața , somnul și termoreglarea . Receptorii serotoninei sunt ținta unei varietăți de medicamente și substanțe narcotice, inclusiv multe antidepresive (inhibitori ai transportorului serotoninei și diferiți agoniști / antagoniști ai receptorilor ), antipsihotice (antagoniști ai receptorilor 5HT 2A-C ), anorectici și halucinogeni (agoniști 5HT 2A ).
| Receptor | K i (nM) | Funcția și efectul agoniștilor / antagoniștilor |
|---|---|---|
| Familia 5-HT1 cuplată la G i / o și inducând inhibarea adenilat ciclazei. | ||
| 5-HT 1A | 3.17 | Memorie (agonist ↓); învățare (agonist ↓); anxietate (agonist ↓); depresie (agonist ↓); simptome ale schizofreniei (agonist parțial ↓); analgezie (agonist ↑); agresivitate (agonist ↓); eliberarea de dopamină în cortexul frontal (agonist ↑); sinteza și eliberarea serotoninei (agonist ↓); eliberarea de oxitocină și alți hormoni (agonist ↑) |
| 5-HT 1B | 4.32 | Vasoconstricție (agonist ↑); agresivitate (agonist ↓); masa osoasă (↓). sinteza și eliberarea serotoninei |
| 5-HT 1D | 5.03 | Vasoconstricție (agonist ↑) |
| 5-HT 1E | 7.53 | |
| 5-HT 1F | 10 | |
| Familia 5-HT2 cuplată la G q și activarea fosfolipazei C. | ||
| 5-HT 2A | 11.55 | Efect psihedelic (agonist ↑); depresie (agonist ↑ & antagonist ↓); anxietate (antagonist ↓); simptome ale schizofreniei (antagonist ↓); eliberarea norepinefrinei din locus coeruleus (antagonist ↓); eliberarea glutamatului din cortexul prefrontal (agonist ↑); ureză (agonist ↑) |
| 5-HT 2B | 8,71 | Funcția cardiovasculară (agoniștii cresc riscul de hipertensiune pulmonară și valvulopatie), empatie (prin fus și neuroni Von Economo) |
| 5-HT 2C | 5.02 | Eliberarea dopaminei în căile mezocorticolimbice (agoniști ↓); eliberarea acetilcolinei în cortexul prefrontal (agoniști ↑); apetit (agoniști ↓); efecte antipsihotice (agoniști ↑); efecte antidepresive (agoniști și antagoniști ↑) |
| Alți receptori | ||
| 5-HT 3 | 593 | Emesis (agoniști ↑); anxioliză (antagoniști ↑). |
| 5-HT 4 | 125,89 | Peristaltismul intestinal (agoniști ↑); Memorie și învățare (agoniști ↑); efecte antidepresive (agoniști ↑). Semnalizare prin G αs cu activarea adenilat ciclazei. |
| 5-HT 5A | 251.2 | Consolidarea memoriei. Semnalizarea prin G i / o cu inhibarea adenilat ciclazei. |
| 5-HT 6 | 98,41 | Cunoaștere (antagoniști ↑); efecte antidepresive (agoniști și antagoniști ↑); efect anxiolitic (antagoniști ↑). Semnalizarea prin G s cu activarea adenilat ciclazei. |
| 5-HT 7 | 8.11 | Cunoaștere (antagoniști ↑); efecte antidepresive (antagoniști ↑). Semnalizarea prin G s cu activarea adenilat ciclazei. |
Medicamente care acționează asupra receptorilor serotoninergici
- Agoniști ai receptorilor 5-HT 1D (sumatriptan). Sunt folosite pentru tratamentul migrenei.
- 5-HT3 receptori antagoniști (ondasetron). Acestea sunt utilizate ca medicamente anti-emetice, în special pentru a controla greața și vărsăturile severe cauzate de multe tipuri de chimioterapie anticancerigenă.
- 5-HT cu antagoniști ai receptorilor 2 (metisergidă). De asemenea, blochează alți receptori 5-HT, precum și receptori -adrenergic și histaminergic. Sunt folosite pentru profilaxia migrenei.
- 5-HT 4 agoniști ai receptorilor (metoclopramid). Stimulează activitatea peristaltică coordonată.
- 5-HT7 receptorilor antagoniști (amisulpridă): antidepresiv.
Alcaloizi ergotici
Alcaloizii „ ergotului ” sunt produși de o ciupercă ( Claviceps purpurea ) care infestează recolta de cereale. Simptomele otrăvirii constau în principal din tulburări psihice și o vasoconstricție periferică intensă și dureroasă care duce la gangrenă . Alcaloizii de ergot sunt molecule complexe a căror structură bazică este acidul lisergic (un alcaloid tetraciclic natural).
Acțiuni
Efectele alcaloizilor de ergot par a fi mediate în principal de receptorii 5-HT, glutammaergici, adrenergici sau dopaminici. Toți alcaloizii de ergot provoacă stimulare musculară netedă. Principalele efecte farmacologice sunt următoarele.
- Efecte vasculare . Ergotamina determină o creștere accentuată a tensiunii arteriale, datorită activării receptorilor α-adrenergici cu vasoconstricția consecventă. În același timp, ergotamina antagonizează efectul de presiune al adrenalinei.
Utilizare clinică
Singura utilizare clinică a ergotaminei este în tratamentul atacurilor de migrenă care nu răspund la analgezice simple.
Notă
Adnotări
Bibliografic
- ^ Sigma Aldrich; rev. din 26.04.2012 referitoare la clorhidrat
- ^ (EN) Kiyoon Kang, Sangkyu Park Young Soon Kim, Biosinteza și producția biotehnologică a derivaților serotoninei în Microbiologie aplicată și biotehnologie, Vol. 83, nr. 1, 1 mai 2009, pp. 27–34, DOI : 10.1007 / s00253-009-1956-1 . Adus la 13 august 2017 .
- ^ (EN) Jessica M. Yano, Yu și Kristie Gregory P. Donaldson, Bacteriile indigene din microbiota intestinală reglează biosinteza serotoninei gazdă în celulă, vol. 161, n. 2, 9 aprilie 2015, pp. 264-276, DOI : 10.1016 / j.cell.2015.02.047 . Adus la 13 august 2017 .
- ^ Miles Berger, John A. Gray și Bryan L. Roth, The Expanded Biology of Serotonin , în Revista anuală a medicinii , vol. 60, n. 1, 1 februarie 2009, pp. 355–366, DOI : 10.1146 / annurev.med.60.042307.110802 . Adus la 13 august 2017 .
- ^ Derek A. Mann și Fiona Oakley, semnalizarea serotoninei paracrine în fibroza tisulară , în Biochimica et Biophysica Acta , vol. 1832, nr. 7, 2013-7, pp. 905–910, DOI : 10.1016 / j.bbadis.2012.09.009 . Adus la 13 august 2017 .
- ^ Paul W. Andrews, Aadil Bharwani și Kyuwon R. Lee, Serotonina este superioară sau inferioară? Evoluția sistemului serotoninergic și rolul său în depresie și răspunsul antidepresiv , în Neuroscience & Biobehavioral Reviews , vol. 51, pp. 164–188, DOI :10.1016 / j.neubiorev.2015.01.018 . Adus la 13 august 2017 .
- ^ Elizabeth A. Daubert și Barry G. Condron, Serotonina: un regulator al morfologiei și circuitelor neuronale , în Tendințe în neuroștiințe , vol. 33, nr. 9, 2010-9, pp. 424-434, DOI : 10.1016 / j.tins.2010.05.005 . Adus la 13 august 2017 .
- ^ Clifford J Rosen, Breaking into bone biology: serotonin's secrets , în Nature Medicine , vol. 15, nr. 2, pp. 145–146, DOI : 10.1038 / nm0209-145 .
- ^ (EN) Ramadhan B. Matondo, Carine Punt și Judith Homberg, Ștergerea transportorului de serotonină la șobolani perturbă homeostazia serotoninei fără a afecta regenerarea ficatului , în American Journal of Physiology - Gastrointestinal and Liver Physiology, vol. 296, nr. 4, 1 aprilie 2009, pp. G963 - G968, DOI : 10.1152 / ajpgi.90709.2008 . Adus la 13 august 2017 (arhivat din original la 13 august 2017) .
- ^ Marieb, Elaine Nicpon, 1936-, Essentials of human anatomy & physiology , ediția a IX-a, Pearson / Benjamin Cummings, 2009, ISBN 0-321-51342-8 ,OCLC 174094368 .
- ^ Nathan P. Greenslit și Ted J. Kaptchuk, Antidepresive și publicitate: psihofarmaceutice în criză , în The Yale Journal of Biology and Medicine , vol. 85, nr. 1, 29 martie 2012, pp. 153–158. Adus la 13 august 2017 .
- ^ a b c Jeffrey R. Lacasse și Jonathan Leo, Serotonina și depresia: o deconectare între reclame și literatura științifică , în PLOS Medicine , vol. 2, nr. 12, 8 noiembrie 2005, pp. e392, DOI : 10.1371 / journal.pmed.0020392 . Adus la 1 noiembrie 2017 .
- ^ Herzberg, David L. (David Lowell), Happy pills in America: from Miltown to Prozac , Johns Hopkins University Press, 2009, ISBN 978-0-8018-9814-3 ,OCLC 212399905 .
- ^ A b c (EN) David Healy, Serotonina și depresia , în BMJ, vol. 350, 21 aprilie 2015, pp. h1771, DOI : 10.1136 / bmj.h1771 . Adus la 1 noiembrie 2017 .
- ^ Jeffrey R Lacasse și Jonathan Leo, Serotonina și depresia: o deconectare între reclame și literatura științifică , în PLoS Medicine , vol. 2, nr. 12, 2005-12, DOI : 10.1371 / journal.pmed.0020392 . Adus la 13 august 2017 .
„Cu toate acestea, pe lângă ceea ce spun acești autori despre serotonină, este de asemenea important să ne uităm la ceea ce nu se spune în literatura științifică. Din câte știm, nu există un singur articol revizuit de colegi care să poată fi citat cu precizie pentru a susține în mod direct afirmațiile privind deficitul de serotonină în orice tulburare mintală, în timp ce există multe articole care prezintă contrareviziune. Mai mult, Manualul de diagnostic și statistic al tulburărilor mentale (DSM), care este publicat de Asociația Americană de Psihiatrie și conține definițiile tuturor diagnosticelor psihiatrice, nu enumeră serotonina ca cauză a oricărei tulburări mentale. Manualul de psihiatrie clinică American Psychiatric Press abordează deficitul de serotonină ca o ipoteză neconfirmată, afirmând: „Experiența suplimentară nu a confirmat ipoteza de epuizare a monoaminei” » . - ^ A. Coppen, Biochimia tulburărilor afective , în The British Journal of Psychiatry: The Journal of Mental Science , vol. 113, nr. 504, noiembrie 1967, pp. 1237-1264. Adus la 1 noiembrie 2017 .
- ^ J. Mendels, JL Stinnett și D. Burns, precursori de amină și depresie , în Archives of General Psychiatry , vol. 32, nr. 1, ianuarie 1975, pp. 22-30. Adus la 1 noiembrie 2017 .
- ^ KA Smith, CG Fairburn și PJ Cowen, Recidiva depresiei după epuizarea rapidă a triptofanului , în Lancet (Londra, Anglia) , vol. 349, n. 9056, 29 martie 1997, pp. 915–919. Adus la 1 noiembrie 2017 .
- ^ HG Ruhé, NS Mason e AH Schene, Mood is indirectly related to serotonin, norepinephrine and dopamine levels in humans: a meta-analysis of monoamine depletion studies , in Molecular Psychiatry , vol. 12, n. 4, April 2007, pp. 331–359, DOI : 10.1038/sj.mp.4001949 . URL consultato il 1º novembre 2017 .
- ^ Philip J Cowen e Michael Browning, What has serotonin to do with depression? , in World Psychiatry , vol. 14, n. 2, 2015-6, pp. 158–160, DOI : 10.1002/wps.20229 . URL consultato il 1º novembre 2017 .
«The best evidence that serotonin plays a role in the pathophysiology of depression comes from studies of “tryptophan depletion”, where an acute dietary manipulation is employed to produce a transient lowering in brain serotonin activity through diminishing availability of its precursor amino acid, tryptophan. In healthy participants with no risk factors for depression, tryptophan depletion does not produce clinically significant changes in mood; however, recovered depressed patients free of medication can show brief, clinically relevant, depressive symptomatology (4). Interestingly, the same is true of recovered depressed patients undergoing catecholamine depletion with alpha-methyl-para-tyrosine (5). Overall, this evidence suggests that impairing serotonin function can cause clinical depression in some circumstances, but is neither necessary nor sufficient. In addition, the depressogenic effects of tryptophan depletion are much more apparent in people who have experienced prior episodes of depression than in those simply at high risk of illness, for example by virtue of a strong family history (6). This suggests that low serotonin function may compromise mechanisms involved in maintaining recovery from depression rather than having a primary effect to lower mood in all vulnerable people. These findings also hint at a role for diminished tryptophan availability in triggering depression, particularly in people with a previous history of illness. Interestingly, lower plasma levels of tryptophan are one of the few reasonably robust findings in patients with more severe forms of depression (7) and, more recently, have been linked to peripheral inflammation and consequent induction of the tryptophan metabolizing enzyme indoleamine 2,3-dioxygenase (8). Inflammation could therefore produce depression in vulnerable individuals by lowering plasma tryptophan and diminishing brain serotonin activity. Conceivably, such an effect could explain the diminished efficacy of SSRIs in depressed patients with high levels of inflammatory biomarkers.» . - ^ Philip J Cowen e Michael Browning, What has serotonin to do with depression? , in World Psychiatry , vol. 14, n. 2, 2015-6, pp. 158–160, DOI : 10.1002/wps.20229 . URL consultato il 1º novembre 2017 .
«In biological psychiatry, pathophysiological hypotheses are not easily refuted. More often they simply seem to become irrelevant as new models of causation take their place. In an era of neural networks and systems level neuroscience, “single” neurotransmitter theories of depression look increasingly implausible. Is serotonin still worth thinking about in relation to depression?» . - ^ ( EN ) HG Ruhé, NS Mason e AH Schene, Mood is indirectly related to serotonin, norepinephrine and dopamine levels in humans: a meta-analysis of monoamine depletion studies , in Molecular Psychiatry , vol. 12, n. 4, 16 gennaio 2007, pp. 331–359, DOI : 10.1038/sj.mp.4001949 . URL consultato il 13 agosto 2017 .
- ^ ( EN ) Jeanene Swanson, Unraveling the Mystery of How Antidepression Drugs Work , in Scientific American . URL consultato il 13 agosto 2017 .
«In fact, SSRIs fail to work for mild cases of depression, suggesting that regulating serotonin might be an indirect treatment only. “There's really no evidence that depression is a serotonin-deficiency syndrome,” says Alan Gelenberg, a depression and psychiatric researcher at The Pennsylvania State University. “It's like saying that a headache is an aspirin-deficiency syndrome.” SSRIs work insofar as they reduce the symptoms of depression, but “they're pretty nonspecific,” he adds. Now, research headed up by neuroscientists David Gurwitz and Noam Shomron of Tel Aviv University in Israel supports recent thinking that rather than a shortage of serotonin, a lack of synaptogenesis (the growth of new synapses, or nerve contacts) and neurogenesis (the generation and migration of new neurons) could cause depression. In this model lower serotonin levels would merely result when cells stopped making new connections among neurons or the brain stopped making new neurons. So, directly treating the cause of this diminished neuronal activity could prove to be a more effective therapy for depression than simply relying on drugs to increase serotonin levels.» . - ^ Chirisse Taylor, Ashwana D. Fricker e Lakshmi A. Devi, Mechanisms of action of antidepressants: from neurotransmitter systems to signaling pathways , in Cellular signalling , vol. 17, n. 5, 2005-5, pp. 549–557, DOI : 10.1016/j.cellsig.2004.12.007 . URL consultato il 1º novembre 2017 .
- ^ Rachele Mazzaracca, Disfunzione sessuale post-SSRI: quando gli antidepressivi lasciano il segno , su Osservatorio Malattie Rare . URL consultato il 13 agosto 2020 .
- ^ Natura & Matematica: Serotonina: dal buonumore ai gusti sessuali?
- ^ One neurotransmitter to rule sexual preference? , su neurorexia.com . URL consultato il 14 febbraio 2014 (archiviato dall'url originale il 23 febbraio 2014) .
- ^ David E. Nichols e Charles D. Nichols, Serotonin Receptors , in Chemical Reviews , vol. 108, n. 5, 1º maggio 2008, pp. 1614–1641, DOI : 10.1021/cr078224o . URL consultato il 13 agosto 2017 .
- ^ Nils Paulmann, Maik Grohmann e Jörg-Peter Voigt, Intracellular Serotonin Modulates Insulin Secretion from Pancreatic β-Cells by Protein Serotonylation , in PLoS Biology , vol. 7, n. 10, 27 ottobre 2009, DOI : 10.1371/journal.pbio.1000229 . URL consultato il 1º novembre 2017 .
- ^ Stephanie W. Watts, Jessica RC Priestley e Janice M. Thompson, Serotonylation of Vascular Proteins Important to Contraction , in PLoS ONE , vol. 4, n. 5, 25 maggio 2009, DOI : 10.1371/journal.pone.0005682 . URL consultato il 1º novembre 2017 .
- ^ Mingyan Zhou, Karen Engel e Joanne Wang, Evidence for Significant Contribution of a Newly Identified Monoamine Transporter (PMAT) to Serotonin Uptake in the Human Brain , in Biochemical pharmacology , vol. 73, n. 1, 1º gennaio 2007, pp. 147–154, DOI : 10.1016/j.bcp.2006.09.008 . URL consultato il 1º novembre 2017 .
Altri progetti
-
 Wikiquote contiene citazioni di o su serotonina
Wikiquote contiene citazioni di o su serotonina -
 Wikizionario contiene il lemma di dizionario « serotonina »
Wikizionario contiene il lemma di dizionario « serotonina » -
 Wikimedia Commons contiene immagini o altri file su serotonina
Wikimedia Commons contiene immagini o altri file su serotonina
Collegamenti esterni
- Serotonina , in Enciclopedia Italiana , Istituto dell'Enciclopedia Italiana .
- ( EN ) Serotonina , su Enciclopedia Britannica , Encyclopædia Britannica, Inc.
- Serotonina - mypersonaltrainer.it
- Serotonin: 9 Questions and Answers - in webmd.com
- Serotonina, dal buonumore ai gusti
| Controllo di autorità | Thesaurus BNCF 22001 · LCCN ( EN ) sh85120301 · GND ( DE ) 4054614-7 · BNF ( FR ) cb11973615q (data) · NDL ( EN , JA ) 00570824 |
|---|