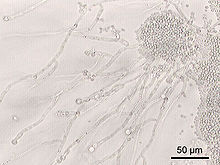
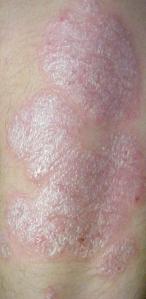
Psoriazis
| Psoriazis | |
|---|---|
| Băiat cu psoriazis | |
| Specialitate | dermatologie |
| Etiologie | Inflamaţie |
| Cartierul general afectat | Piele |
| Clasificare și resurse externe (EN) | |
| OMIM | 177900 |
| Plasă | D011565 |
| MedlinePlus | 000434 |
| eMedicină | 1943419 , 1108072 , 1107850 , 1107949 , 1108220 , 331037 și 394752 |
Psoriazisul (din grecescul ψωρίασις - psōríasis , „ mâncărime ”) este o boală inflamatorie a pielii , de obicei de natură cronică și recidivantă . Factorii autoimuni, genetici și de mediu intervin în patogeneza sa. Psoriazisul este o patologie comună, fără o corelație specială cu sexul sau vârsta; cu toate acestea, se pare că este legat de un risc crescut de boli cardiovasculare , [1] [2] incluzând accident vascular cerebral și infarct miocardic , [3] [4], iar tratarea hiperlipidemiei pacienților ( niveluri ridicate de lipide din sânge ) poate duce la îmbunătățire. [5] Sunt recunoscute mai multe forme de psoriazis: psoriazis pustular și forme nepustulare, inclusiv psoriazisul în plăci (aproximativ 80% din formele de psoriazis), gutat, invers și eritrodermic.
În psoriazisul în plăci, pielea se acumulează rapid și se îngroașă în zonele afectate de leziuni, dând un aspect solz alb-argintiu. Deși tulburarea poate apărea în orice zonă a corpului, ea apare în general la coate , genunchi , scalp și partea lombară a spatelui, precum și la nivelul palmelor mâinilor , tălpilor picioarelor și în regiunea genitală. . Boala apare cel mai frecvent, dar nu exclusiv, pe suprafețele extensoare ale membrelor . Boala cronică și recurentă este variabilă în ceea ce privește gradul de afectare a pielii. Acestea variază de la subiecți cu un număr foarte limitat de patch-uri mici la subiecți cu corpul acoperit aproape complet de leziuni.
Unghiile și unghiile de la picioare sunt frecvent afectate de tulburare, numită distrofie psoriazică a unghiilor. Aproximativ 50% dintre persoanele cu psoriazis dezvoltă afectarea unghiilor. [6] Acesta este uneori singurul loc afectat de boală. Psoriazisul poate provoca, de asemenea, inflamații articulare, ducând la afecțiunea cunoscută sub numele de artrită psoriazică . Aproximativ 30% dintre persoanele cu psoriazis (variind de la 6% la 48%) vor dezvolta ulterior artrită psoriazică. [7]
Cauzele care stau la baza psoriazisului nu sunt încă pe deplin înțelese, dar se crede că componenta genetică și imunologică joacă un rol fundamental. Mai mulți factori de mediu sunt capabili să declanșeze sau să agraveze psoriazisul. Dintre acestea, un rol important îl joacă traumele cutanate, procesele infecțioase și unele medicamente .
fundal
Potrivit unor cercetători, primele descrieri referitoare la psoriazis ar apărea deja în Codurile asiriene babiloniene (aproximativ 2000 î.Hr. ) care ne vorbesc despre bolile pielii solzoase, în unele papirusuri egiptene și în mai multe cărți ale Vechiului Testament .
Se spune că psoriazisul este una dintre bolile de piele menționate în Biblie în capitolele 13 și 14 din Levitic și care sunt menționate în Biblia ebraică sub numele de Tzaraat . "Dacă un bărbat are o pustulă sau o pată albă în pielea corpului său ... durerea din Tzaraat ... acel om va fi condus de preot care va examina durerea de pe pielea corpului" Pentru o astfel de piele boli, sunt furnizate și unele prescripții comportamentale. O confirmare indirectă ar putea veni din faptul că în ebraică cuvântul utilizat în prezent pentru a defini psoriazisul este sapachat și este de origine biblică, dar cu un sens necunoscut. [8]
Hipocrate din secolul al V-lea î.Hr. oferă o descriere destul de detaliată a unor leziuni descuamative, probabil psoriazice și se referă la acestea cu numele de „ psora ”. Celsus în secolul I d.Hr. oferă o descriere exactă a dermatozei și sugerează tratarea acestuia cu preparate de sulf . Medicul grec Claudio Galen a folosit termenul „psoriazis” referindu-se la unele leziuni cutanate solzoase și mâncărime, sfătuind pacienții să folosească băi frecvente și unguente uleioase. [9]
De peste o mie de ani, cunoștințele și terapia dermatozei nu au făcut progrese și medicii îi sfătuiesc pe pacienți să folosească băi cu ape sulfuroase, noroi, unguente sau uleiuri care transportă gudron și preparate sulfuroase. Boala este adesea confundată alternativ cu lepra sau scabia , ceea ce duce frecvent la izolarea socială a pacienților. [10] [11]

Boala la sfârșitul secolului al XVIII-lea devine cunoscută sub numele de „iepurele lui Willan” atunci când dermatologii englezi Robert Willan (1757-1812) și Thomas Bateman o diferențiază de alte boli ale pielii și clarifică manifestările și complicațiile acesteia. În opinia lor, lepra se caracterizează prin leziuni regulate și circulare, în timp ce psoriazisul este întotdeauna neregulat ca aspect și formă. Robert Willan a identificat două categorii diferite de leziuni, psoriazisul discoid pe care l-a numit leprosa Graecorum (echivalent cu Lepra Vulgaris sau Lepra willani) și psora leprosa . [12]
Cei mai renumiți dermatologi ai secolului al XIX-lea s-au dedicat aprofundării studiului bolii, care în opinia lor era sistemică (de fapt vorbeau despre „boala psoriazică”), considerând-o legată de modificări nespecificate ale organelor interne și ale sistemului nervos. . Abia în 1841 de către dermatologul austriac Ferdinand von Hebra , fondatorul noii școli vieneze de dermatologie, condiția a primit în cele din urmă numele definitiv de psoriazis, derivat din cuvântul grecesc psora care înseamnă mâncărime. [13] [14] Descrierea poate fi găsită în Atlas der Hautkrankheiten (Atlasul bolilor cutanate) al lui von Hebra.
Istoria tratamentelor
Istoria psoriazisului este plină de tratamente de eficacitate dubioasă și toxicitate ridicată. Aceste tratamente s-au bucurat de popularitate scurtă și largă în anumite perioade de timp sau în anumite zone geografice. Vechii egipteni obișnuiau să încerce tratamente topice bazate pe substanțe gudroase și excremente de câini, pisici și alte animale. Remediile fanteziste pe bază de ape sulfuroase, urină , săruri marine care trebuie aplicate local sunt asociate cu terapii orale care necesită sorbirea bulionului de vipere .
La mijlocul anilor 1700, în special în Regatul Unit , se recomandă o vindecare a psoriazisului cu preparate pe bază de mercur : terapia include atât aplicații locale, cât și tratament general. Toxicitatea mercurului a făcut în curând această încercare terapeutică mai puțin populară. Cu toate acestea, mercurul rămâne utilizat mult timp în paste și unguente pentru tratamentul bolilor de piele și psoriazisului. [15] [16] [17]
Trebuie remarcat faptul că, chiar și în ultimii ani, s-a încercat tratamentul acestei patologii cu complexe de cupru și preparate care conțin salicilat de cupru, cu rezultate slabe și efecte toxice. [18] În secolele al XVIII-lea și al XIX-lea, psoriazisul, printre alte remedii, a fost tratat folosind așa-numita soluție Fowler , adică o soluție care conține 1% arseniat de potasiu . Din nou, compusul s-a dovedit a fi extrem de toxic și cancerigen . [17] [19]
Cu toate acestea, arsenicul a continuat să fie utilizat pe scară largă în dermatologie, atât în Statele Unite ale Americii, cât și în Europa , sub formă de soluție Fowler și pilule asiatice care conțin, de asemenea, opiu sau piper. [20] Arsenicul face încă parte din medicina tradițională chineză. [21] În secolul XX , razele Grenz (numite și razele Bucky), o formă de radiație X moale, au fost utilizate pe scară largă în tratamentul psoriazisului și a altor tulburări ale pielii. Mecanismul precis de acțiune al acestor raze nu a fost niciodată pe deplin înțeles, dar tratamentul pare să aibă un efect foarte bun asupra psoriazisului, în special a scalpului. [22] [23] Această terapie din ultimii ani a fost înlocuită cu terapia cu radiații ultraviolete .
Epidemiologie
Psoriazisul la caucazieni afectează la fel de des bărbații și femeile.
La orientali și în special la japonezi , sexul masculin este predominant față de femeie, cu un raport de 2 la 1. [24] Poate apărea la orice vârstă, dar este mai frecvent de la 10 la 40 de ani, și în în special în momentul pubertății și menopauzei . Deoarece pacienții cu psoriazis au o speranță de viață similară cu persoanele care nu sunt bolnavi, prevalența bolii crește odată cu vârsta. [25] [26]
Psoriazisul se găsește la 2-3% din populația generală, cu o prevalență de 0,1% în Japonia , [24] [27] de 1,5% în populația Marii Britanii , [28] de 2,6% din populația SUA și mai mică procente în țările din Africa de Vest . În Italia, conform datelor din studiul PraKtis, un studiu realizat de Centrul de Studii GISED în colaborare cu DOXA și Laboratorul General de Epidemiologie al Institutului de Cercetări Farmacologice „Mario Negri” , prevalența psoriazisului ajunge la 3,1%, arătând că una dintre cele mai frecvente boli dermatologice. [29]
Incidența și prevalența psoriazisului este de fapt foarte neclară. Conform unei revizuiri din 2012 care a luat în considerare 53 de studii efectuate în întreaga lume, prevalența la copii variază de la aproximativ 0% în Taiwan la 2,1% în Italia. La adulți, aceeași cifră variază de la 0,91% înregistrată în Statele Unite la 8,5% din valoarea găsită în Norvegia . Din nou la adulți, boala variază de la 78,9 / 100 000 subiecți în fiecare an ( Statele Unite ) până la 230/100 000 subiecți ani înregistrați în Italia.
Aceste date variate par să sugereze că boala diferă nu numai în funcție de grupa de vârstă luată în considerare, ci și în funcție de regiunea geografică studiată, cu o tendință spre o frecvență mai mare în țări mai îndepărtate de ecuator . [30]
Etiologie
Etiologia psoriazisului este încă necunoscută, deși unele date disponibile par să indice o origine multifactorială. Factorii genetici , factorii imuni și factorii de mediu sunt cu siguranță implicați în sensibilitatea la psoriazis și artrita psoriazică. [31]
În prezent există două ipoteze principale inerente procesului care are loc în dezvoltarea bolii.
Prima ipoteză consideră psoriazisul ca o tulburare a creșterii excesive și a reproducerii celulelor pielii. Problema este pur și simplu privită ca o tulburare a epidermei și a keratinocitelor .
A doua ipoteză vede boala ca pe o tulburare mediată de imunitate, în care reproducerea excesivă a celulelor pielii este secundară factorilor produși de sistemul imunitar .
Limfocitele T , care joacă un rol central în imunitatea mediată de celule , sunt activate și migrează către dermă, declanșând eliberarea de citokine (în special factorul de necroză tumorală-alfa TNF-α ) care la rândul său provoacă inflamație și reproducere rapidă a celulelor pielii. Încă nu este clar ce factori declanșează activarea celulelor T.
Ipoteza mediată de imunitate a fost susținută de observația că medicamentele imunosupresoare pot reduce sau rezolva plăcile psoriazice. Cu toate acestea, rolul sistemului imunitar nu este pe deplin înțeles. De fapt, s-a raportat recent că leziunile de tip psoriazic pot fi declanșate la șoareci lipsiți de limfocite T. Cu toate acestea, modelele animale pot fi suprapuse psoriazisului uman numai în anumite privințe. [32] Funcția de barieră cutanată afectată pare să joace un rol în susceptibilitatea la dezvoltarea psoriazisului. [33]
În unele privințe, psoriazisul pare a fi o boală idiosincrazică . Majoritatea persoanelor cu psoriazis se confruntă cu faptul că boala se poate agrava sau îmbunătăți fără niciun motiv aparent. Studiile asupra factorilor asociați cu psoriazisul tind să fie limitați de faptul că se bazează pe probe mici și, în general, pe indivizi spitalizați. Prin urmare, aceste studii nu pot fi întotdeauna definite ca reprezentative pentru populația care suferă de psoriazis și, de fapt, rezultatele contradictorii sunt raportate în literatura medicală.
Evenimentul declanșator al primului focar de psoriazis este uneori stresul fizic sau mental, traumatisme sau leziuni ale pielii sau infecții, adesea streptococice.
Alte afecțiuni despre care s-a raportat că sunt asociate cu agravarea bolii sunt enumerate mai jos.
Factori declanșatori și / sau exacerbatori
Deoarece psoriazisul este o boală cronică caracterizată prin perioade de remisie care alternează cu faze de exacerbare, recunoașterea factorilor declanșatori este de asemenea importantă pentru a evita obiceiurile și comportamentele care pot agrava sau induce o reapariție a bolii.
Leziuni
- Traumatisme locale ( fenomen Koebner ; psoriazisul în plăci)
- Iritarea (varianta fenomenului lui Koebner ; [34] [35] psoriazisul în plăci)
- Arsuri solare sau UV [36] (placă sau psoriazis pustular)
Infecții
- Candida albicans [37] [38]
- Viremie (psoriazis gutat )
- Specii de streptococi (psoriazis gutat) [39] [40] [41]
- Staphylococcus aureus [42]
- Infecții ale căilor respiratorii superioare [43] (psoriazis gutat la copii)
- Malassezia ovalis (psoriazis al scalpului) [44]
- Infecția cu virusul imunodeficienței umane ( HIV ) [45]
În ceea ce privește infecția cu HIV, trebuie amintit că apariția psoriazisului poate reprezenta manifestarea inițială a unei infecții avansate, adesea trecute cu vederea de pacientul însuși. [46] [47] [48] Acest fapt este aparent un paradox. [49] De fapt, multe tratamente imunosupresoare tradiționale utilizate pentru tratarea psoriazisului au ca rezultat o reducere a limfocitelor T (care apare în mod natural în timpul infecției cu HIV) și sunt asociate cu o îmbunătățire a stării. Dimpotrivă, starea imunosupresiei cauzate de HIV duce la o exacerbare a psoriazisului. [50] Deci, în mod paradoxal, ne confruntăm cu o afecțiune, psoriazisul, mediat de celulele T care apare atunci când celulele T în sine scad. În plus, psoriazisul este de obicei mediat de citokinele de tip 1, în timp ce în HIV, citokinele de tip 2 tind să predomine. [49] [51] Se presupune că reducerea celulelor T de tip CD4 poate provoca o supraactivare a celulelor CD8, care sunt responsabile de exacerbarea psoriazisului la pacienții cu HIV pozitiv. Este probabil ca atât în prezența, cât și în absența infecției cu HIV, psoriazisul să fie mediat în mare parte de celulele T cu memorie CD8, probabil cu un rol cheie în interferonul gamma secretat de aceste celule. [49]
Medicamente

- Clorochina [52] (un medicament utilizat în terapia antipaludică )
- Săruri de litiu [53] [54]
- Interferon [55] [56]
- Beta-blocante [53] [54]
- Inhibitori ai ECA [57]
- Indometacină [58]
- Săruri de aur [56]
- AINS și salicilați [59]
- Tetracicline [59]
- Nu mai luați corticosteroizi [58]
- Alergice reacții la medicamente
Alții

- Stresuri emoționale (divorțuri, schimbări de locuri de muncă și altele) [60] [61] și fizice [62]
- Xeroză (psoriazis în plăci)
- Consumul de alcool [63] și tutun [64] [65] [66]
- Obezitatea [67]
- Factori psihosomatici [68]
- Sezon sau schimbări climatice
- Hipocalcemie [69] [70] [71] (rar)
Potrivit mai multor autori, unele dintre comorbiditățile menționate mai sus sunt mai degrabă efectele decât cauzele bolii.
Patogenie
Există dovezi puternice că psoriazisul este o boală polifactorială caracterizată printr-o eterogenitate genetică, clinică și histologică considerabilă, chiar și la nivelul acelorași leziuni.
Se pare că disregularea compartimentului de imunitate mediat celular ( limfocitele T ) și a răspunsului epidermic la anumiți stimuli joacă un rol fundamental în geneza și menținerea acestei tulburări. În special, se pare că există diferiți factori care declanșează dereglarea limfocitelor T [72]
Factori genetici
Se știe că incidența psoriazisului este crescută la persoanele cu HLA-B13, HLA-B17, HLA-DR7, HLA-Bw57, chiar dacă penetrarea genelor pare să fie destul de scăzută și expresia lor neregulată. Cu toate acestea, cea mai puternică asociere cu antigenele de histocompatibilitate de clasa I este cu HLA-Cw06. [31]
În primele studii privind ereditatea psoriazisului s-a emis ipoteza că boala era transmisibilă ca trăsătură autosomală dominantă cu o penetranță de 60%. [73] Această ipoteză a fost incorectă și în 1972 Watson a propus un model multifactorial de moștenire. Conform acestui model, pentru apariția debutului psoriazisului a fost necesar să se integreze atât mai mulți factori genetici, cât și evenimente declanșatoare. Acestea din urmă sunt în general de tip antigenic și / sau de mediu.
În studiul lui Watson s-a arătat că incidența psoriazisului la copiii părinților sănătoși, adică fără modificări psoriazice, a fost de 7,8%. Acest procent a crescut la 16,4% atunci când un singur părinte a avut psoriazis pentru a ajunge la un procent de 50% dacă ambii părinți au fost afectați. [74] Pacienții cu familiaritate tind să-și prezinte leziunile la o vârstă statistic semnificativă mai mică decât a pacienților necunoscuți.
Într-un studiu din 2009 cu scopul de a determina riscul de reapariție a artritei psoriazice și a psoriazisului necomplicat la rudele de gradul întâi ale pacienților cu artrită psoriazică a arătat că acest risc, o estimare bună a eredității bolii, este de 30-55% la rudele de gradul I ale subiecților cu artrită psoriazică, în timp ce scade la 8-10% la rudele de gradul I ale subiecților cu psoriazis. [75]
Valoarea principală a studiilor genetice asupra psoriazisului este cu siguranță în încercarea de a descoperi mecanismele moleculare în joc și căile enzimatice pentru a identifica potențialele ținte ale noilor medicamente. [76] [77]

Analiza legăturii la nivelul genomului a identificat nouă loci (localizări), pe diferiți cromozomi, asociați cu psoriazisul. Acești loci sunt denumiți loci de sensibilitate la psoriazis (PSORS) și au fost numerotați de la 1 la 9. [78] [79] Primul dintre acești locus (PSORS1) este situat în regiunea HLA (6p21.3). O asociere puternică a alelei HLA-Cw6 cu acest locus a fost raportată pentru prima dată în literatura medicală într-un studiu al populației finlandeze. În loci deja menționați găsim o serie de gene. Multe dintre aceste gene se află pe căile metabolice implicate în procesul inflamator. Unele mutații ale acestor gene sunt extrem de frecvente în psoriazis. [80]
Factorul cheie este probabil PSORS1, reprezentând 35-50% din moștenirea psoriazisului. PSORS1 controlează genele care codifică proteinele care afectează sistemul imunitar sau care se găsesc în piele în cantități mai mari la persoanele cu psoriazis. PSORS1 se găsește pe cromozomul 6 în complexul major de histocompatibilitate (MHC). [81]
Trei gene ale locusului PSORS1 au o asociere puternică cu psoriazisul vulgar: varianta HLA- C HLA-Cw6, care codifică o proteină MHC de clasa I; Varianta CCHCR1 WWC, care codifică o proteină spirală care este supraexprimată în epiderma subiecților care suferă de psoriazis; CDSM , varianta alelei 5, care codifică corneodesmosina , o proteină de aderență a pielii, foarte importantă în faza terminală de diferențiere a epidermei, supraexprimată în psoriazis. [80]
Studiile genomice au arătat că, pe lângă cele deja menționate, alte gene sunt implicate și în unele variante ale caracteristicilor psoriazisului. Unele dintre aceste gene codifică proteinele care acționează ca mediatori ai inflamației și care vizează anumite celule ale sistemului imunitar. Unele dintre aceste gene sunt implicate și în alte boli autoimune. [82]
Dintre aceste gene, merită o mențiune specială: IL12B , plasat pe cromozomul 5q, care exprimă interleukina-12B; IL23R , localizat pe cromozomul 1p, care exprimă receptorul interleukinei-23 și este implicat în procesul de diferențiere a celulelor T. [83] [84] [85]
Aceste gene se află pe calea metabolică care pune capăt reglării în sus a factorului de necroză tumorală-α și a factorului nuclear kB, implicate în procesul inflamator.
În 2012, a fost identificată prima genă legată direct de psoriazis. Unele studii științifice au sugerat că o mutație rară în gena care codifică proteina CARD14 plus un factor de declanșare a mediului este suficientă pentru a provoca psoriazisul în plăci, cea mai comună formă de psoriazis. [86] [87]
Factori postinfecțioși
Se știe că psoriazisul (în special sub formă gutată ) este adesea precedat de infecții cauzate de streptococ α-hemolitic, stafilococ auriu și alte bacterii, sau de infecții virale (de exemplu cu virusul varicelo-zoster ), candida. La nivel cutanat, există în esență trei tipuri de celule ( macrofage tisulare , celule Langerhans și celule dendritice ) cu funcția de a ataca proteinele și de a introduce unele fragmente ( epitopi ) în complexele MHC I și II pentru a „prezenta” antigenii la nivelul receptorii celulari T. Trebuie amintit că la subiecții care suferă de psoriazis la nivel cutanat găsim în principal limfocite T CD8 + în timp ce la nivel dermic limfocite T CD4 + .
Când o proteină de membrană periferică de tip B7 (prezentă pe suprafața celulelor care prezintă antigenul activat) se leagă de receptorul CD28 sau CD152 ( CTLA-4 ) al limfocitului T, se produce un semnal de activare / costimulare după care celula T astfel activat începe să producă citokine și, în special, interleukina 2 (IL-2) care la rândul său activează alte limfocite T și interferonul gamma , care îmbunătățește expresia suprafeței celulare a antigenelor MHC. [88]
Unele substanțe definite ca superantigene , în general toxine bacteriene care stimulează regiunea variabilă a lanțului beta (V β ) al receptorului de celule T (TCR), sunt prezentate imediat și, prin urmare, nu necesită medierea complexului MHC. Aceste superantigene se pot atașa de fapt direct la regiunea V beta-2 a celulelor T CD4 + . [89]
Stimularea cauzată de superantigeni activează un număr mare de limfocite T CD4 + și implică eliberarea unui număr mare de citokine, inclusiv interleukina 22 (IL-22), interferonul gamma și diferiți factori de creștere , care atrag limfocitele T CD8 + și epidermele Limfocite T. Rezultatul este o hiperstimulare a keratinocitelor suprabazale, care are ca rezultat o hiperproliferare a acestora asociată cu o rezistență crescută la apoptoză (moarte celulară programată) și crește expresia keratinei , inclusiv a keratinei 14.
Datorită unei omologii puternice între keratina 14 și proteina M-6 a grupului A streptococ beta hemolitic, este probabil ca multe limfocite T activate deja de superantigene bacteriene și, în mod specific, de antigenul streptococic M-6, să reacționeze apoi cu keratinocite și proteina keratină 14. Aceasta ar activa cascada evenimentelor care pot sta la baza leziunilor psoriazisului gutat. [90]
Factori imunologici
În psoriazis, celulele imune se deplasează de la derm spre epidermă, unde stimulează celulele pielii (keratinocite) să prolifereze. Psoriazisul nu pare a fi o adevărată boală autoimună. De fapt, într-o boală autoimună, sistemul imunitar confundă o proteină din organism cu un antigen extern și o atacă. Cu toate acestea, un antigen extern care acționează ca într-o boală autoimună clasică nu a fost încă identificat cu certitudine. Oricare ar fi factorul declanșator, cercetătorii au identificat deja multe dintre celulele imune implicate în psoriazis, precum și multe substanțe active și semnale chimice (ad z γ-interferon , limfokine ) pe care celulele le trimit reciproc pentru a coordona procesul inflamator. La sfârșitul acestui proces, celulele imune, cum ar fi celulele dendritice și limfocitele T, trec de la dermă la epidermă, continuând să secrete semnale chimice pro-inflamatorii, cum ar fi factorul de necroză tumorală-α , interleukina-1β și interleukina- 6. , interleukina-22 , care provoacă în schimb proliferarea keratinocitelor. [91] [92] Trebuie amintit că epiderma psoriazică este într-un fel deja predispusă la un răspuns anormal: nivelurile diferitelor substanțe și reactivitatea țesuturilor la substanțele prezente în mod normal sunt de fapt anormale. De fapt, pielea psoriazică are niveluri ridicate de factor de creștere a nervilor (NGF), care stimulează, de asemenea, proliferarea keratinocitelor, a β- endorfinei și a factorilor angiogenici și prezintă un răspuns aberant la γ-interferon, cu reducere mai degrabă decât creștere, a apoptozei celulare. . Rezultatul final al interacțiunii dintre substanțele active și substratul activ este deci proliferarea keratinocitelor, maturarea incompletă a acestora, neovascularizarea și inflamația. La rândul lor, keratinocitele eliberează chemokine care stimulează în continuare limfocitele T, creând astfel un cerc vicios de inflamație auto-indusă.
Sistemul imunitar constă dintr-un sistem imun înnăscut și un sistem imunitar adaptativ. În sistemul înnăscut, celulele imune au capacitatea de a răspunde imediat la un număr mare de proteine și antigene găsite în mod obișnuit pe agenți patogeni (recunoașterea unui număr limitat de profiluri non-auto moleculare extrem de răspândite în natură). În schimb, sistemul imunitar adaptiv și celulele sale răspund la proteine și la alți antigeni care sunt prezentați de alte celule. În psoriazis, ADN-ul acționează ca un stimul inflamator și prin activarea celulelor dendritice plasmacitoide îi împinge să producă interferon-α. Ca răspuns la celulele dendritice și limfocitele T, keratinocitele produc peptide antimicrobiene și o serie de citokine, cum ar fi interleukina-1, interleukina-6 și factorul de necroză tumorală-α, care duce la recrutarea altor celule inflamatorii, producând inflamații suplimentare. [91]
Celulele dendritice acoperă decalajul dintre sistemele imune înnăscute și adaptive. Sunt în număr crescut în leziunile psoriazice și induc proliferarea limfocitelor și a celulelor T de tip 1. Unele celule dendritice sunt capabile să producă factor de necroză tumorală-α, care invocă celule imune suplimentare și menține și stimulează inflamația. L'immunoterapia mirata, la terapia con psoraleni e la terapia a raggi ultravioletti A (PUVA), riduce il numero di cellule dendritiche. [76]
I linfociti T come si è visto migrano dal derma nell'epidermide. Sono attratti a livello epidermico dal rilascio di alfa-1 beta-1 integrina, una molecola di segnalazione sul collagene nell'epidermide. I linfociti T dei soggetti affetti da psoriasi secernono interferone-γ ed interleuchina-17. L'interleuchina-17 è anche associata all'interleuchina-22. L'interleuchina-22 induce i cheratociti a proliferare. [76]
Un'ipotesi è che la psoriasi comporti un difetto nelle cellule T regolatorie e nella regolazione mediata dalla citochina interleuchina-10. [93]
Fattori autoimmuni
Non è del tutto chiaro in che modo i fattori autoimmuni possano porsi nella patogenesi della psoriasi. Certamente una buona percentuale di pazienti psoriasici produce anticorpi ( IgA e IgG ) per la gliadina , con conseguente attivazione della risposta linfocitaria . [94] Questi stessi pazienti mostrano una eccellente riduzione dei sintomi con diete senza glutine . [95] [96] [97]
Anatomia patologica
Le lesioni psoriasiche si presentano a livello istologico come zone di iperproliferazione, con un turnover epidermico accelerato di circa 10 volte rispetto alla pelle normale, con una incompleta maturazione dei cheratociti e mantenimento dei nuclei nello strato corneo (paracheratosi), con neovascolarizzazione tortuosa, aumento del flusso ematico , essudato proteico e vasi linfatici immaturi; da notare l'infiltrazione di neutrofili polimorfi nell'epidermide. Anche la pelle non lesionata dei pazienti psoriasici presenta delle anormalità: la psoriasi viene indotta più facilmente, in particolare dopo un trauma ( Fenomeno di Koebner ), e vari medicinali possono causare delle acutizzazioni. Vi sono più cellule disponibili per sintesi del DNA ei livelli di glicogeno (più elevati nelle lesioni) sono ridotti rispetto alla pelle di individui non psoriasici. [98]
Clinica
Classificazione
I sintomi della psoriasi possono manifestarsi in una varietà di forme. Le varianti includono la psoriasi a placche, la psoriasi pustolosa, la psoriasi guttata e la psoriasi flessurale. La psoriasi è un disturbo cronico e recidivante della pelle. Esistono diversi tipi di classificazioni.
In base alla gravità (estensione sulla superficie corporea) la psoriasi può essere divisa in:
- leggera: presenza di un numero limitato di placche, in genere meno del 3% della superficie cutanea è interessata.
- moderata: dal 3 al 10% della superficie cutanea è occupato da placche
- grave: oltre il 10% della superficie cutanea corporea
Dal punto di vista clinico la psoriasi può essere distinta in:
| Tipo di psoriasi | Frequenza | Aspetto |
|---|---|---|
| Psoriasi pustolosa | 3% | Aree di pustole sensibili, a contenuto purulento, sterili, limitate alle mani o piedi oppure estese. Le lesioni sono talvolta dolorose e invalidanti. Frequente il coinvolgimento di unghie ed articolazioni. |
| Psoriasi eritrodermica | 3% | Macchie grandi, infiammate, eritematose su gran parte della superficie corporea. Talvolta associata a prurito intenso, dolore e sensazione di bruciore. Spesso si sviluppa in pazienti con psoriasi a placche che interrompono bruscamente un trattamento sistemicico. Decisamente grave, l'infiammazione e la desquamazione estrema interrompono la funzione di barriera cutanea e ne alterano le capacità di termoregolazione. |
| Psoriasi inversa | 4% | Sono tipiche le aree lisce ed asciutte di cute infiammata ed arrossata. Manca la desquamazione. Localizzata spesso su superfici flessorie: ascelle, regioni sottomammarie, inguine, natiche e regione genitale. |
| Psoriasi guttata | 10% | Formata da tipiche papule singole, piccole, rosse e desquamanti. Localizzata più spesso sul tronco (parte superiore), arti e talvolta cuoio capelluto. Rispetto alla psoriasi a placche le lesioni appaiono meno ispessite e squamose. Insorgenza durante l'infanzia e l'adolescenza. Spesso associata ad infezioni quali tonsillite e faringite da streptococchi . |
| Psoriasi a placche | 80% | Si caratterizza per le placche rosse, circoscritte, ricoperte da squame bianco-argentee. Localizzata spesso su ginocchia, gomiti, cuoio capelluto. È il tipo più frequente di psoriasi. Assume spesso una denominazione particolare a seconda della sede, estensione e gravità. |
Altre forme particolari di psoriasi:
- Psoriasi nummulare (a moneta)
- Psoriasi pustolosa palmare e plantare (psoriasi pustolosa tipo Barber) [99]
- Psoriasi pustolosa anulare
- Psoriasi seborroica
- Psoriasi oculare
- Psoriasi del cuoio capelluto
- Psoriasi delle mucose
- Onicopsoriasi
- Psoriasi pustolosa localizzata
- Psoriasi pustolosa generalizzata (psoriasi pustolosa di von Zumbusch) [100]
- Psoriasi nevoide
- Acrodermatite continua suppurativa di Hallopeau (caratterizzata da pustole ricorrenti alla piega e al letto ungueale delle falangi distali di mani e piedi)
- Artrite Psoriasica
Segni e sintomi
Le manifestazioni più comuni sono papule e placche eritematose ben delimitate ricoperte di scaglie argentee o opalescenti. Le lesioni sono di varie dimensioni e la severità può variare da pochi punti di desquamazione di tipo forforoso a dermatosi generali con artrite (artrite psoriasica), esfoliazioni ed eruzioni debilitanti. Nonostante il nome significhi "condizione pruriginosa" il prurito non è sempre presente; in alcuni casi tale sintomo è presente nelle vulviti psoriasiche dove le lesioni da grattamento possono essere simili a quelle da lichen simplex [101]
I siti più comuni per le lesioni sono lo scalpo (inclusa la zona retroauricolare), le zone di estensione di gomito e ginocchio e la zona lombo-sacrale, ma in alcune sue forme si trova nelle zone di flessione, sui genitali e sulla pianta dei piedi e il palmo delle mani . Le lesioni guariscono senza lasciare cicatrici e senza disturbare la crescita dei peli .
Il 30-50% dei soggetti presenta degenerazioni delle unghie , con ipercheratosi, ispessimento, detrito subunguale, onicolisi , distorsione. Nella fase eruttiva un trauma può causare la comparsa di lesioni lineari ( Fenomeno di Koebner ).
Qualità di vita
La psoriasi ha un forte impatto negativo sulla vita di chi ne è colpito. I casi gravi di psoriasi incidono sulla salute e sulla qualità di vita del paziente in misura simile ad altre malattie croniche, quali ad esempio la depressione , l' ipertensione arteriosa , l' insufficienza cardiaca congestizia , il diabete mellito ed altre ancora. [102] A seconda della gravità e della localizzazione delle lesioni i soggetti affetti da psoriasi possono provare un marcato disagio fisico e qualche disabilità. Il prurito e il dolore possono interferire con molte normali attività quotidiane, come ad esempio la cura di sé o il sonno. La presenza delle chiazze sulle mani o sui piedi possono impedire al paziente di svolgere determinate professioni, alcune attività sportive (ad esempio il nuoto), e talvolta anche il semplice relazionarsi con gli altri. Le chiazze localizzate sul cuoio capelluto possono essere particolarmente imbarazzanti, e le placche desquamanti nei capelli vengono spesso scambiate per forfora .
Alcuni pazienti cambiano in modo radicale le proprie abitudini sociali a causa della malattia. Il sentirsi limitati nell'andare al mare in spiaggia o non poter andare in piscina, temere di indossare abiti corti o senza maniche in determinate occasioni per il timore che si vedano le chiazze, sentire il bisogno di coprirsi prima di incontrare una persona per la prima volta, nel timore di non conoscere quali reazioni potrebbe provare a causa della psoriasi, tutto ciò è decisamente frustrante e limitante.
Il senso di disagio e l'impatto sociale è certamente più grave e pesante per i pazienti più giovani o adolescenti. Un teen-ager tende a vivere con frustrazione, vergogna e rabbia il non poter partecipare a tutte le attività del gruppo dei pari. Non tutti riescono a sviluppare adeguate strategie di convivenza con la malattia. Il disagio psicologico può portare a una depressione significativa e al ritiro e isolamento sociale. I giovani, così come gli adulti, sviluppano una cattiva immagine di sé che nasce dai timori legati alla paura del rifiuto pubblico e alle preoccupazioni inerenti alla sfera emotiva e sessuale. Una ricerca condotta dalla European Federation of Psoriasis Patient Associations (EUROPSO) ha evidenziato che più della metà dei pazienti affetti da psoriasi severa considera la propria condizione un significativo problema nello svolgimento della vita di tutti i giorni. [103]
Esistono molti strumenti per misurare la qualità della vita dei pazienti affetti da psoriasi e altri disturbi dermatalogici. Alcuni studi scientifici hanno confermato che i pazienti avvertono spesso una diminuzione della qualità della vita. [104] Tra i sintomi sembra essere soprattutto il prurito che contribuisce maggiormente a far scadere la qualità della vita. [105] Uno studio del 2010 ha verificato l'efficacia di una semplice scala di autovalutazione del prurito, suddivisa in 6 punti (0 = nessun prurito; 5 = prurito molto severo) o (prurito), e basata sulle risposte dei pazienti. Le conclusioni dello studio sono favorevoli all'utilizzo di questo strumento di autovalutazione, ritenendolo una misura valida dell'intensità del prurito nei pazienti con psoriasi a placche da moderata a grave. La scala sarebbe anche in grado di discriminare tra i soggetti che necessitano di uno specifico trattamento e quelli che non ne necessitano. [106]
Gravità
Come già ricordato la psoriasi, sulla base della estensione, è generalmente classificata come lieve (interessante meno del 3% del corpo), moderata (colpisce tra il 3 ed il 10% del corpo) o grave (oltre il 10% del corpo coinvolto). Tuttavia la gravità della malattia può basarsi anche su altri fattori: ad esempio il grado di attività della malattia (grado di arrossamento della placca, spessore), la risposta a precedenti terapie, e l'impatto emotivo e sociale della malattia sulla persona.
Il " Psoriasis Area Severity Index " (PASI) è lo strumento di misura più utilizzato per la psoriasi. L'indice PASI combina la valutazione della gravità delle lesioni e l'area interessata in un unico punteggio compreso tra 0 (assenza di malattia) a 72 (massima malattia). L'indice venne introdotto nel 1978 da due medici svedesi, Fredriksson e Pettersson, nel corso di uno studio che valutava l'efficacia di un derivato dell'acido retinoico in pazienti sofferenti di una forma cronica e severa di psoriasi generalizzata, al fine di valutare l'evoluzione nel tempo e l'efficacia del trattamento somministrato. [107]
Il punteggio PASI, molto utilizzato negli studi scientifici, ha trovato una scarsa possibilità di applicazione in ambito ambulatoriale e ciò ha portato allo sviluppo di versioni semplificate: tra queste il "Simplified Psoriasis Area Severity Index" (SPASI) [108] e versioni autosomministrabili quali il "Self-Administered Psoriasis Area and Severity Index" (SAPASI). [109]
Diagnosi
La diagnosi di psoriasi si basa sulla anamnesi , (eventuale storia familiare di psoriasi, andamento attuale della malattia, presenza di prurito, fattori scatenanti, trattamenti precedenti), e sull'esame fisico che prende in considerazione l'aspetto del rash cutaneo , con particolare attenzione al colore delle lesioni, le dimensioni, la morfologia, la distribuzione nelle diverse regioni corporee interessate.
Nel corso della valutazione fisica deve essere dedicata una particolare attenzione al cuoio capelluto , alla regione ombelicale, alle unghie ed ai glutei.
Non è necessario ricorrere a speciali procedure diagnostiche. Tuttavia può essere opportuno ricercare il cosiddetto segno di Auspitz , cioè la presenza di numerose emorragie puntiformi dopo asportazione di una placca psoriasica. [110] Si deve però tenere presente che il segno non è né sensibile né specifico. [111]
Gli esami di laboratorio non sono dirimenti. In genere si può riscontrare negatività del fattore reumatoide , aumento della proteina C-reattiva e della velocità di eritrosedimentazione . Ulteriori studi possono essere effettuati per chiarire la causa di eventuali sovrainfezioni delle lesioni, in particolare colture di microorganismi e funghi.
Raramente potrebbe essere necessario ricorrere ad una biopsia cutanea per una corretta diagnosi differenziale. [112]
Diagnosi differenziale
- Dermatite seborroica [113] (particolarmente nel caso di alcune lesioni sul cuoio capelluto)
- Eczema cronico
- Eczema nummulare
- Dermatite atopica (nell'infanzia) [114]
- Lichen simplex cronico
- Pitiriasi rosea (particolarmente per lesioni del tronco) [115]
- Pitiriasi rubra pilaris (lesioni del tronco)
- Tinea corporis (lesioni del tronco) [116]
Trattamento
Il trattamento della psoriasi si basa su una serie di misure generali che comprendono un'adeguata idratazione topica (uso di sostanze emollienti), un'adeguata esposizione alla radiazione solare e l'utilizzo di sostanze catramose e oli minerali. In generale la forma lieve tende a rispondere alle misure topiche, mentre la forma moderata richiede trattamenti fototerapici. Più complesso il trattamento della forma grave, che spesso necessita di misure e agenti di tipo sistemico. [117]
Terapia locale
La terapia della psoriasi dev'essere personalizzata. La psoriasi a placche è comunemente trattata con il calcipotriolo e con farmaci steroidei come il betametasone. I farmaci di prima scelta, nelle forme a estensione limitata, includono preparazioni topiche emollienti come la vaselina , creme idratanti, bagni con sali di magnesio, unguenti contenenti olii essenziali vegetali con scopo lenitivo e di riduzione della secchezza che accompagna l'accumulo di pelle sulle placche psoriasiche. Tra gli agenti cheratolitici l' acido salicilico è probabilmente il più efficace e quello maggiormente in uso. In genere negli unguenti base la concentrazione si aggira intorno al 5%, ma si possono raggiungere titoli di acido salicilico del 10-15%. Anche l' urea a concentrazioni del 10-20% può essere utilizzata con il medesimo significato. Tra gli agenti antiflogistici le sostanze cortisoniche (ad esempio flurandrenolide ) si dimostrano spesso efficaci e ad azione rapida ma non prive di effetti indesiderati. Tra gli agenti riduttori si può ricorrere al catrame (vegetale, bituminoso - ittiolo e tumenolo - o coaltar), il quale però può rivelarsi irritante, quindi deve necessariamente applicarsi su cute poco sensibile e per brevi periodi. Un posto di rilievo nel trattamento locale è occupato dalla crisarobina [118] (un prodotto vegetale estratto dall'Andira araroba) e dai suoi analoghi sintetici antralina [119] o ditranolo. [120] Queste sostanze interferiscono con la sintesi del DNA, con conseguente effetto citotossico. [121]
Tra le terapie locali può essere annoverata l' ittioterapia .
Foto-chemioterapia
La prima forma di fototerapia nella psoriasi è stata certamente l'esposizione della pelle alla luce del sole. La ricerca ha permesso di stabilire che lunghezze d'onda di 311-313 nm sono le più efficaci. Speciali lampade a UVB ( radiazione ultravioletta B) a banda stretta sono state sviluppate a questo scopo. [122] Il tempo e l'intensità dell'esposizione deve essere controllata e limitata per evitare un'eccessiva esposizione ed ustioni della pelle. Per questo motivo le moderne attrezzature sono totalmente programmabili nel funzionamento e dotate di spegnimento automatico, una volta trascorso il tempo programmato.
In alternativa si può ricorrere alla PUVA terapia, cioè all'uso in associazione di psoraleni assunti per via orale e delle radiazioni ultraviolette A (UVA). Il meccanismo di azione della terapia PUVA è sconosciuta, ma probabilmente determina l'attivazione degli psoraleni, i quali inibiscono la rapida ed anormalmente riproduzione delle cellule della cute psoriasica. [123] La PUVA-terapia può essere associata a nausea , cefalea , stanchezza , bruciore e prurito . Il trattamento con PUVA e psolareni è anche associato ad un aumentato rischio di cancro cutaneo, [124] in particolare melanoma maligno e carcinoma squamocellulare. [125] Per questo motivo la PUVA-terapia, utilizzabile secondo diversi schemi di trattamento, non può essere impiegata a lungo termine.
Terapia sistemica

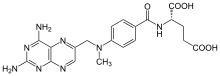
Il trattamento per via sistemica viene riservato ai soggetti con forme gravi o particolarmente estese, oppure a quei pazienti nei quali i trattamenti topici o fototerapici si sono dimostrati inefficaci. La decisione di iniziare una terapia per via sistemica in un soggetto affetto da psoriasi deve essere considerata con grande attenzione e, in ogni caso, deve essere preceduta dalla esecuzione dei normali esami ematochimici e dal controllo dei test di funzionalità epatica a causa della potenziale tossicità di molti farmaci.
I principali agenti attivi nella psoriasi per via sistemica sono il metotrexate , la ciclosporina A ed i retinoidi ( acitretina e etretinato).
La ciclosporina A (CsA) è un farmaco immunosoppressore comunemente utilizzato per controllare il rigetto dei trapianti d'organo. Il suo possibile utilizzo nel trattamento della psoriasi fu accidentalmente scoperto alla fine degli anni '70. [126] Quando è utilizzato al dosaggio di 3–5 mg/kg/die risulta molto attivo ed efficace. Ottenuta la remissione clinica (in genere entro 2 mesi di terapia) è possibile passare a un dosaggio di mantenimento oppure sospendere il trattamento. I cicli di trattamento non dovrebbero superare la durata di 6 mesi, eventualmente ripetibili in caso di recidiva.
Il methotrexate (MTX) è un altro farmaco immunosoppressore che viene utilizzato per via orale, intramuscolare o endovenosa. La maggior parte dei pazienti risponde a dosi comprese tra 7,5 e 15 mg/settimana. Il farmaco risulta mielotossico ed epatotossico, soprattutto a dosaggi elevati. [127]
L' etretinato (E) è indicato in alcuni tipi di psoriasi. Il farmaco viene assunto per via orale ed il dosaggio che permette di ottenere una buona risposta terapeutica in genere è compreso tra 0,75 e 1 mg/kg/die. Il farmaco può comportare un innalzamento dei valori di trigliceridi e colesterolo, nonché danni osteoarticolari, talvolta clinicamente non evidenti ma documentabili con l'esecuzione di radiografiche vertebrali. Altri effetti avversi che compaiono con una certa frequenza con l'utilizzo dei retinoidi, sono di carattere muco-cutaneo e la loro intensità è spesso dose-correlata.
L'acitretina in molti Paesi ha sostituito l'etretinato. Si tratta di un retinoide con effetti molto simili a quest'ultimo, somministrabile per via orale e caratterizzato da un metabolismo più rapido. [128] [129]
Farmaci biologici
I farmaci biologici rappresentano uno dei maggiori progressi ottenuti dalla medicina negli ultimi anni in campo terapeutico.
Il successo di queste nuove terapie risiede nella loro grande selettività d'azione che consente di ottenere, nella maggior parte dei casi, una notevole efficacia terapeutica con assenza di tossicità per gli organi nel trattamento a lungo termine ed una buona tollerabilità. I farmaci biologici si caratterizzano per la capacità di interferire in modo selettivo, a vari livelli e con modalità di azione differenti, nei processi immunologici che scatenano e sostengono la psoriasi. Come è noto da anni ed è già stato trattato nella sezione patogenesi, nello sviluppo della psoriasi sono infatti coinvolte sia cellule proprie della cute, quali i cheratociti , sia cellule del sangue destinate alla regolazione delle risposte immunitarie, come i linfociti T . È proprio l'alterazione del fisiologico "dialogo" fra questi due tipi di cellule che dà luogo a uno squilibrio nella sintesi dei prodotti dei linfociti T, con abnorme produzione di una serie di molecole di interazione cellulare che porta, in ultima analisi, alla flogosi, all'eritema e alla formazione di squame.
I farmaci biologici finora prodotti, ottenuti attraverso le tecniche del DNA ricombinante, agiscono su specifiche molecole attivate nella psoriasi, quali il TNF-alfa o l'interleuchina 12/23, andando a colpire selettivamente uno dei «centri vitali» della malattia. Questi farmaci sono anticorpi monoclonali privi di tossicità d'organo nel lungo termine. Questo significa che una volta iniziati, non è prevista una loro sospensione, a meno di eventi avversi, intolleranza o inefficacia. La somministrazione, che in genere avviene tramite iniezioni sottocutanee o infusione endovenosa, può essere adeguatamente diluita nel tempo con intervalli tra i trattamenti che vanno da una settimana a dodici settimane in relazione all'emivita della singola molecola. L'intervallo tra le somministrazioni determina un conseguente miglioramento della qualità della vita del paziente, che può aderire in modo più agevole al progetto terapeutico. La storia clinica di neoplasia controindica il ricorso ai farmaci biologici. L'efficacia di questi ultimi inoltre, in particolare degli anti-TNF-alfa, è notevolmente ridotta nei soggetti obesi. [130]
I farmaci biologici registrati dall'EMA ( European Medicines Agency ) sono stati monitorati in un registro italiano nell'ambito del progetto "PsoCare", da alcuni centri di riferimento, per verificarne la tollerabilità, l'efficienza e l'efficacia a lungo termine.
Etanercept
L' etanercept è una proteina di fusione ottenuta tramite tecniche di DNA ricombinante del recettore umano p75 del fattore TNF-alfa con la frazione Fc dell' immunoglobulina umana IgG1. La proteina funziona da recettore solubile per il TNF-alfa e possiede un'affinità di legame per il TNF-alfa più alta di quella degli altri recettori solubili. Il farmaco viene somministrato con punture sottocutanee somministrate settimanalmente. L'etanercept, registrato all'EMEA ( Agenzia europea per i medicinali ), è un farmaco indicato per la psoriasi, l' artrite psoriasica , l' artrite reumatoide e la spondilite anchilosante .
Efalizumab
L' efalizumab è un anticorpo monoclonale umanizzato ricombinante che lega specificatamente un'importante molecola di adesione dei linfociti T, fondamentale in tre processi chiave nella genesi della psoriasi, quali il legame dei linfociti ad altre cellule, la migrazione dal sangue al derma e l'attivazione delle cellule T, che conduce al rilascio delle citochine infiammatorie e alla proliferazione dei cheratinociti. Questo farmaco è stato registrato all'EMEA, indicato per la psoriasi e somministrato con punture sottocutanee. L'efalizumab è stato sospeso dall'EMA (precedentemente chiamata EMEA) nel febbraio 2009 per elevata tossicità (rischio di morte per leucoencefalopatia multifocale progressiva) e scarsa efficacia [131] [132] .
Infliximab
L' infliximab è un anticorpo monoclonale chimerico che si lega con alta specificità e affinità sia alla forma solubile sia a quella trans-membrana del Tumor Necrosis Factor (TNF-alfa), inibendone l'attività. Il TNF-alfa è una citochina pro-infiammatoria presente ad alti livelli nelle lesioni psoriasiche e nella sinovia articolare di pazienti con artrite psoriasica. Numerose evidenze dimostrano che esiste una correlazione fra la gravità della patologia cutanea e l'aumentata concentrazione di TNF-alfa nel siero. L'infliximab pertanto agisce riducendo l'infiammazione e l'iperproliferazione rispettivamente dell'eritema e della formazione della squama. Attualmente in Italia è stato approvato nella terapia dell' artrite reumatoide , della malattia di Crohn , della spondilite anchilosante , per l'artrite psoriasica e per la psoriasi. La somministrazione del farmaco avviene per via endovenosa.
Adalimumab
L' adalimumab è un anticorpo monoclonale che ha come target il TNF-alfa. L'anticorpo viene somministrato per via sottocutanea in preparazione liquida alla dose di 40 mg ogni due settimane. Come tutti gli anti TNF-alfa possiede una grande selettività d'azione, cioè è in grado di agire solo sull'attività della molecola, senza interferire con altri sistemi dell'organismo. Nel 2008 il farmaco è stato approvato per l'utilizzo nella psoriasi e nella artrite psorisiaca. Nel 2018 è il risultato il farmaco che ha generato il maggior fatturato nel mondo, con 19.936 milioni di dollari. Attualmente, a seguito della scadenza del brevetto, sono disponibili numerosi biosimilari di adalimumab.
Alefacept
L' alefacept è una proteina di fusione umana LFA-3/IgG1 che agisce bloccando l'interazione tra le cellule che presentano l'antigene ei linfociti T. Il farmaco è stato approvato dalla Food and Drug Administration (FDA) ma non ha mai ricevuto l'approvazione dall'autorità europea European Medicines Agency (EMA). Nel 2011 la società farmaceutica che lo produceva comunicava di aver cessato la promozione, la produzione, le distribuzione e la vendita del farmaco per problemi di approvvigionamento. [133]
Ustekinumab
L' ustekinumab è un anticorpo monoclonale IgGk1 interamente umano, che lega interleuchina 12 e 23 , approvato per la psoriasi a placche e per artrite psoriasica sia da FDA che da EMA [134] . L'anticorpo si è dimostrato efficace anche nella malattia di Crohn [135] . Viene somministrato per via sottocutanea in dosaggio da 45 mg per individui con peso inferiore o uguale a 100 kg e 90 mg per individui con peso superiore a 100 kg ogni 12 settimane.
Prognosi
La maggior parte delle persone con psoriasi presentano solo lievi lesioni cutanee che possono essere trattate efficacemente con terapie topiche. [136]
Tuttavia, è noto che la psoriasi possa avere un impatto negativo sulla qualità della vita, sia del paziente che dei suoi familiari. [137] A seconda della gravità e della localizzazione dei focolai, gli individui possono sperimentare un rilevante disagio fisico e alcune difficoltà motorie. Prurito e dolore possono interferire con le attività di base, come la cura di sé e il sonno . [138] La partecipazione alle attività sportive, lo svolgimento di alcune professioni e la cura per i propri familiari, possono diventare attività difficili per coloro con lesioni sulle mani e sui piedi. [138] Placche presenti sul cuoio capelluto possono essere particolarmente imbarazzanti e possono essere scambiate per forfora . [139]
Gli individui con psoriasi possono accusare una scarsa immagine di sé che nasce dalla paura di incorrere nel pubblico rifiuto e dalle preoccupazioni psicosessuali. La psoriasi è stata associata a una bassa autostima e il disturbo depressivo è più comune tra coloro che soffrono di questa condizione. [140] Le persone con psoriasi spesso sono vittime di pregiudizi a causa dell'erronea credenza diffusa che essa sia contagiosa. [138] Il disagio psicologico può portare a depressione significativa e isolamento sociale ; un alto tasso di ideazione suicidiaria è stato associato con la malattia. [141] Esistono molti strumenti per misurare la qualità della vita dei pazienti affetti da psoriasi e altri disturbi dermatologici. La ricerca clinica ha indicato che i pazienti vanno incontro spesso ad una diminuzione della qualità della vita. [142] I bambini con psoriasi possono essere vittime di episodi di " bullismo ". [143]
Diverse condizioni sono associate con la psoriasi. Queste si verificano più frequentemente nelle persone anziane. Quasi la metà degli individui con psoriasi di età superiore ai 65 anni accusano almeno tre comorbilità mentre i due terzi ne hanno almeno due. [144]
Malattia cardiovascolare
La psoriasi è stata associata con l' obesità [140] e con numerosi altri disturbi cardiovascolari e metabolici. L'incidenza del diabete è più alto del 27% nelle persone affette dalla condizione rispetto a coloro che non ne soffrono.. [145] La psoriasi grave può essere ancora più fortemente associata con lo sviluppo di diabete rispetto alla psoriasi lieve. [145] I pazienti più giovani vedono anche un aumentato del rischio di sviluppare il diabete. [144] [146] Le persone con psoriasi o artrite psoriasica hanno un rischio leggermente più elevato di incorrere in malattie cardiache e infarti miocardici rispetto alla popolazione generale. Il rischio di malattia cardiovascolare sembra essere correlata con la gravità della psoriasi e con la sua durata. Non vi sono, tuttavia, consistenti prove che suggeriscono che la psoriasi possa essere associata ad un aumentato del rischio di morte per eventi cardiovascolari. L'assunzione di methotrexate può fornire un livello di protezione per il cuore . [144] [147]
Le probabilità di soffrire di ipertensione è 1,58 maggiore nelle persone con psoriasi rispetto a coloro che sono privi di questa condizione; tale dato risulta essere più elevato nei gravi casi di psoriasi. Una simile correlazione è stata osservata nelle persone che soffrono di artrite psoriasica, le cui probabilità di sviluppare ipertensione sono risultate 2,07 volte maggiori rispetto alla popolazione generale. La correlazione tra la psoriasi e l'ipertensione, al 2015, non è ancora stata compresa. Sono stati ipotizzati diversi meccanismi che potrebbero essere coinvolti, come la disregolazione delsistema renina-angiotensina , elevati livelli di endotelina 1 nel sangue e un aumento dello stress ossidativo. [146] [148] L'incidenza delle alterazioni del ritmo cardiaco come la fibrillazione atriale è di 1,31 volte maggiore nelle persone con psoriasi lieve e 1,63 volte maggiore nelle persone con psoriasi grave.[86] Si può riscontrare anche un leggero aumento del rischio di ictus soprattutto nei casi più gravi di psoriasi. [147] [149] Il trattamento degli alti livelli di colesterolo mediante l'assunzione di statine , è stata associata alla ridotta gravità della psoriasi, come misurato dal punteggio PASI , ed è stato anche correlata ad un miglioramento di altri fattori di rischio della malattia cardiovascolare, come i marker di infiammazione. [150] Tali effetti cardioprotettivi sono attribuiti alla capacità delle statine di migliorare il profilo lipidico del sangue e per via dei loro effetti anti-infiammatori. Si ritiene, pertanto, che l'uso di statine nei pazienti con psoriasi e iperlipidemia , comporti una diminuzione dei livelli di alta sensibilità alla proteina C-reattiva e TNF e ad una ridotta attività della proteina immunitaria LFA-1 . [150] Rispetto ai soggetti senza psoriasi, le persone con tale condizione hanno una probabilità maggiore di soddisfare i criteri per la sindrome metabolica . [151] [152]
Note
- ^ WH. Boehncke, S. Boehncke, Research in practice: the systemic aspects of psoriasis. , in J Dtsch Dermatol Ges , vol. 6, n. 8, agosto 2008, pp. 622-5, DOI : 10.1111/j.1610-0387.2008.06785.x , PMID 18564207 .
- ^ WH. Boehncke, S. Boehncke, Cardiovascular mortality in psoriasis and psoriatic arthritis: epidemiology, pathomechanisms, therapeutic implications, and perspectives. , in Curr Rheumatol Rep , vol. 14, n. 4, agosto 2012, pp. 343-8, DOI : 10.1007/s11926-012-0260-8 , PMID 22562431 .
- ^ T. Xu, Y. Zhang, Association Of Psoriasis With Stroke And Myocardial Infarction: Meta Analysis Of Cohort Studies. , in Br J Dermatol , agosto 2012, DOI : 10.1111/bjd.12002 , PMID 22897416 .
- ^ AB. Kimball, A. Guerin; D. Latremouille-Viau; AP. Yu; S. Gupta; Y. Bao; P. Mulani, Coronary heart disease and stroke risk in patients with psoriasis: retrospective analysis. , in Am J Med , vol. 123, n. 4, aprile 2010, pp. 350-7, DOI : 10.1016/j.amjmed.2009.08.022 , PMID 20362755 .
- ^ R. Ghazizadeh, M. Tosa; M. Ghazizadeh, Clinical improvement in psoriasis with treatment of associated hyperlipidemia. , in Am J Med Sci , vol. 341, n. 5, maggio 2011, pp. 394-8, DOI : 10.1097/MAJ.0b013e3181ff8eeb , PMID 21233693 .
- ^ C. Kahl, B. Hansen; K. Reich, [Nail psoriasis--an ignored disorder. Pathogenesis, diagnosis and therapy]. , in Hautarzt , vol. 63, n. 3, marzo 2012, pp. 184-91, DOI : 10.1007/s00105-011-2228-4 , PMID 22382303 .
- ^ MS. Day, D. Nam; S. Goodman; EP. Su; M. Figgie, Psoriatic arthritis. , in J Am Acad Orthop Surg , vol. 20, n. 1, gennaio 2012, pp. 28-37, DOI : 10.5435/JAAOS-20-01-028 , PMID 22207516 .
- ^ A. Shai, D. Vardy; A. Zvulunov, [Psoriasis, biblical afflictions and patients' dignity]. , in Harefuah , vol. 141, n. 5, maggio 2002, pp. 479-82, 496, PMID 12073533 .
- ^ L. Nardelli, [Psoriasis in the history of medicine]. , in G Ital Dermatol , vol. 100, Lug-Ago 1959, pp. 363-88, PMID 14426024 .
- ^ LK. Eckes, [Psoriasis and leprosy in the light of common history. A contribution on epidemiology and differential diagnosis]. , in Hautarzt , vol. 29, n. 6, giugno 1978, pp. 331-6, PMID 350808 .
- ^ A. Lyell, Leprosy and psoriasis. , in J Am Acad Dermatol , vol. 16, 3 Pt 1, marzo 1987, pp. 620-2, PMID 3546422 .
- ^ FO. Meenan, A note on the history of psoriasis. , in Ir J Med Sci , n. 351, marzo 1955, pp. 141-2, PMID 14353580 .
- ^ FS. Glickman, Lepra, psora, psoriasis. , in J Am Acad Dermatol , vol. 14, 5 Pt 1, maggio 1986, pp. 863-6, PMID 3519699 .
- ^ K. Holubar, Psoriasis--100 years ago. , in Dermatologica , vol. 180, n. 1, 1990, pp. 1-4, PMID 1968402 .
- ^ B. Gordon, PM. Inman; P. Trinder, Mercury absorption and psoriasis. , in Br Med J , vol. 2, n. 5003, novembre 1956, pp. 1202-6, PMID 13364416 .
- ^ F. Kern, N. Roberts; L. Ostlere; J. Langtry; RC. Staughton, Ammoniated mercury ointment as a cause of peripheral neuropathy. , in Dermatologica , vol. 183, n. 4, 1991, pp. 280-2, PMID 1667099 .
- ^ a b EM. Farber, History of the treatment of psoriasis. , in J Am Acad Dermatol , vol. 27, n. 4, ottobre 1992, pp. 640-5, PMID 1401327 .
- ^ JR. Sorenson, W. Hangarter, Treatment of rheumatoid and degenerative diseases with copper complexes: a review with emphasis on copper-salicylate. , in Inflammation , vol. 2, n. 3, settembre 1977, pp. 217-38, PMID 367963 .
- ^ Henry G. Piffard, "A Treatise On The Materia Medica And Therapeutics Of The Skin" , Sampson Low, Marston, Searle & Rivington, 1881.
- ^ Smith ML. Environmental and sports-related skin diseases. In: Bolognia, JL, et al., eds. Dermatology. 2nd ed. London: Mosby, 2008: 1364
- ^ RA. Schwartz, Arsenic and the skin. , in Int J Dermatol , vol. 36, n. 4, aprile 1997, pp. 241-50, PMID 9169318 .
- ^ B. Lindelöf, Grenz ray therapy in dermatology. An experimental, clinical and epidemiological study. , in Acta Derm Venereol Suppl (Stockh) , vol. 132, 1987, pp. 1-67, PMID 3481149 .
- ^ B. Lindelöf, [Grenz ray therapy]. , in Hautarzt , vol. 40, n. 1, gennaio 1989, pp. 4-7, PMID 2646248 .
- ^ a b H. Takahashi, K. Nakamura; F. Kaneko; H. Nakagawa; H. Iizuka, Analysis of psoriasis patients registered with the Japanese Society for Psoriasis Research from 2002-2008. , in J Dermatol , vol. 38, n. 12, dicembre 2011, pp. 1125-9, DOI : 10.1111/j.1346-8138.2010.01145.x , PMID 21951304 .
- ^ C. Bonifati, M. Carducci; A. Mussi; L. D'Auria; F. Ameglio, Recognition and treatment of psoriasis. Special considerations in elderly patients. , in Drugs Aging , vol. 12, n. 3, marzo 1998, pp. 177-90, PMID 9534019 .
- ^ MA. de Rie, AY. Goedkoop; JD. Bos, Overview of psoriasis. , in Dermatol Ther , vol. 17, n. 5, 2004, pp. 341-9, DOI : 10.1111/j.1396-0296.2004.04037.x , PMID 15379769 .
- ^ A. Kawada, T. Tezuka; Y. Nakamizo; H. Kimura; H. Nakagawa; M. Ohkido; A. Ozawa; A. Ohkawara; H. Kobayashi; S. Harada; A. Igarashi, A survey of psoriasis patients in Japan from 1982 to 2001. , in J Dermatol Sci , vol. 31, n. 1, febbraio 2003, pp. 59-64, PMID 12615365 .
- ^ JM. Gelfand, R. Weinstein; SB. Porter; AL. Neimann; JA. Berlin; DJ. Margolis, Prevalence and treatment of psoriasis in the United Kingdom: a population-based study. , in Arch Dermatol , vol. 141, n. 12, dicembre 2005, pp. 1537-41, DOI : 10.1001/archderm.141.12.1537 , PMID 16365254 .
- ^ L. Naldi, P. Colombo; EB. Placchesi; R. Piccitto; L. Chatenoud; C. La Vecchia, Study design and preliminary results from the pilot phase of the PraKtis study: self-reported diagnoses of selected skin diseases in a representative sample of the Italian population. , in Dermatology , vol. 208, n. 1, 2004, pp. 38-42, DOI : 10.1159/000075044 , PMID 14730235 .
- ^ R. Parisi, DP. Symmons; CE. Griffiths; DM. Ashcroft, Global Epidemiology of Psoriasis: A Systematic Review of Incidence and Prevalence. , in J Invest Dermatol , settembre 2012, DOI : 10.1038/jid.2012.339 , PMID 23014338 .
- ^ a b V. Chandran, SP. Raychaudhuri, Geoepidemiology and environmental factors of psoriasis and psoriatic arthritis. , in J Autoimmun , vol. 34, n. 3, maggio 2010, pp. J314-21, DOI : 10.1016/j.jaut.2009.12.001 , PMID 20034760 .
- ^ R. Zenz, R. Eferl; L. Kenner; L. Florin; L. Hummerich; D. Mehic; H. Scheuch; P. Angel; E. Tschachler; EF. Wagner, Psoriasis-like skin disease and arthritis caused by inducible epidermal deletion of Jun proteins. , in Nature , vol. 437, n. 7057, settembre 2005, pp. 369-75, DOI : 10.1038/nature03963 , PMID 16163348 .
- ^ R. de Cid, E. Riveira-Munoz; PL. Zeeuwen; J. Robarge; W. Liao; EN. Dannhauser; E. Giardina; PE. Stuart; R. Nair; C. Helms; G. Escaramís, Deletion of the late cornified envelope LCE3B and LCE3C genes as a susceptibility factor for psoriasis. , in Nat Genet , vol. 41, n. 2, febbraio 2009, pp. 211-5, DOI : 10.1038/ng.313 , PMID 19169253 .
- ^ NJ. Fiumara, Psoriasis of the penis: Koebner reaction. Following oral genital exposure. , in J Am Vener Dis Assoc , vol. 3, 2 Pt 1, dicembre 1976, pp. 59-60, PMID 1010767 .
- ^ EW. Rosenberg, PW. Noah, The Koebner phenomenon and the microbial basis of psoriasis. , in J Am Acad Dermatol , vol. 18, 1 Pt 1, gennaio 1988, pp. 151-8, PMID 3279081 .
- ^ RM. Rosen, Annular pustular psoriasis induced by UV radiation from tanning salon use. , in J Am Acad Dermatol , vol. 25, 2 Pt 1, agosto 1991, pp. 336-7, PMID 1918477 .
- ^ A. Rebora, Candida and psoriasis. , in Acta Derm Venereol , vol. 84, n. 2, 2004, pp. 175; author reply 175, PMID 15206710 .
- ^ A. Waldman, A. Gilhar; L. Duek; I. Berdicevsky, Incidence of Candida in psoriasis--a study on the fungal flora of psoriatic patients. , in Mycoses , vol. 44, n. 3-4, maggio 2001, pp. 77-81, PMID 11413927 .
- ^ L. Naldi, L. Peli; F. Parazzini; CF. Carrel, Family history of psoriasis, stressful life events, and recent infectious disease are risk factors for a first episode of acute guttate psoriasis: results of a case-control study. , in J Am Acad Dermatol , vol. 44, n. 3, marzo 2001, pp. 433-8, DOI : 10.1067/mjd.2001.110876 , PMID 11209111 .
- ^ CM. Owen, RJ. Chalmers; T. O'Sullivan; CE. Griffiths, A systematic review of antistreptococcal interventions for guttate and chronic plaque psoriasis. , in Br J Dermatol , vol. 145, n. 6, dicembre 2001, pp. 886-90, PMID 11899140 .
- ^ CM. Owen, RJ. Chalmers; T. O'Sullivan; CE. Griffiths, Antistreptococcal interventions for guttate and chronic plaque psoriasis. , in Cochrane Database Syst Rev , n. 2, 2000, pp. CD001976, DOI : 10.1002/14651858.CD001976 , PMID 10796842 .
- ^ BS. Baker, AV. Owles; L. Fry, A possible role for vaccination in the treatment of psoriasis? , in G Ital Dermatol Venereol , vol. 143, n. 2, aprile 2008, pp. 105-17, PMID 18833037 .
- ^ EW. Rosenberg, PW. Noah; RB. Skinner, Microorganisms and psoriasis. , in J Natl Med Assoc , vol. 86, n. 4, aprile 1994, pp. 305-10, PMID 8040907 .
- ^ EW. Rosenberg, PW. Noah; RB. Skinner; R. Vander Zwaag; SK. West; JF. Browder, Microbial associations of 167 patients with psoriasis. , in Acta Derm Venereol Suppl (Stockh) , vol. 146, 1989, pp. 72-4; discussion 75, PMID 2609890 .
- ^ FC. Arnett, JD. Reveille; M. Duvic, Psoriasis and psoriatic arthritis associated with human immunodeficiency virus infection. , in Rheum Dis Clin North Am , vol. 17, n. 1, febbraio 1991, pp. 59-78, PMID 2041889 .
- ^ MA. Muñoz-Pérez, A. Rodriguez-Pichardo; F. Camacho; MA. Colmenero, Dermatological findings correlated with CD4 lymphocyte counts in a prospective 3 year study of 1161 patients with human immunodeficiency virus disease predominantly acquired through intravenous drug abuse. , in Br J Dermatol , vol. 139, n. 1, luglio 1998, pp. 33-9, PMID 9764146 .
- ^ J. Badger, TG. Berger; C. Gambla; JY. Koo, HIV and psoriasis. , in Clin Rev Allergy Immunol , vol. 14, n. 4, pp. 417-31, DOI : 10.1007/BF02771755 , PMID 9040969 .
- ^ TA. Maurer, Dermatologic manifestations of HIV infection. , in Top HIV Med , vol. 13, n. 5, pp. 149-54, PMID 16377853 .
- ^ a b c DJ. Fife, JM. Waller; EW. Jeffes; JY. Koo, Unraveling the paradoxes of HIV-associated psoriasis: a review of T-cell subsets and cytokine profiles. , in Dermatol Online J , vol. 13, n. 2, 2007, p. 4, PMID 17498423 .
- ^ E. Mallon, CB. Bunker, HIV-associated psoriasis. , in AIDS Patient Care STDS , vol. 14, n. 5, maggio 2000, pp. 239-46, DOI : 10.1089/108729100317696 , PMID 10833810 .
- ^ LM. Austin, M. Ozawa; T. Kikuchi; IB. Walters; JG. Krueger, The majority of epidermal T cells in Psoriasis vulgaris lesions can produce type 1 cytokines, interferon-gamma, interleukin-2, and tumor necrosis factor-alpha, defining TC1 (cytotoxic T lymphocyte) and TH1 effector populations: a type 1 differentiation bias is also measured in circulating blood T cells in psoriatic patients. , in J Invest Dermatol , vol. 113, n. 5, novembre 1999, pp. 752-9, DOI : 10.1046/j.1523-1747.1999.00749.x , PMID 10571730 .
- ^ R. Wolf, V. Ruocco, Triggered psoriasis. , in Adv Exp Med Biol , vol. 455, 1999, pp. 221-5, PMID 10599347 .
- ^ a b E. Dika, F. Bardazzi; R. Balestri; HI. Maibach, Environmental factors and psoriasis. , in Curr Probl Dermatol , vol. 35, 2007, pp. 118-35, DOI : 10.1159/0000106419 , PMID 17641494 .
- ^ a b M. O'Brien, J. Koo, The mechanism of lithium and beta-blocking agents in inducing and exacerbating psoriasis. , in J Drugs Dermatol , vol. 5, n. 5, maggio 2006, pp. 426-32, PMID 16703778 .
- ^ M. Afshar, AD. Martinez; RL. Gallo; TR. Hata, Induction and exacerbation of psoriasis with Interferon-alpha therapy for hepatitis C: A review and analysis of 36 cases. , in J Eur Acad Dermatol Venereol , giugno 2012, DOI : 10.1111/j.1468-3083.2012.04582.x , PMID 22671985 .
- ^ a b V. Milavec-Puretić, M. Mance; R. Ceović; J. Lipozenčić, Drug induced psoriasis. , in Acta Dermatovenerol Croat , vol. 19, n. 1, 2011, pp. 39-42, PMID 21489366 .
- ^ L. Fry, BS. Baker,Triggering psoriasis: the role of infections and medications. , in Clin Dermatol , vol. 25, n. 6, pp. 606-15, DOI : 10.1016/j.clindermatol.2007.08.015 , PMID 18021899 .
- ^ a b EA. Abel, LM. DiCicco; EK. Orenberg; JE. Fraki; EM. Farber, Drugs in exacerbation of psoriasis. , in J Am Acad Dermatol , vol. 15, 5 Pt 1, novembre 1986, pp. 1007-22, PMID 2878015 .
- ^ a b KH. Basavaraj, NM. Ashok; R. Rashmi; TK. Praveen, The role of drugs in the induction and/or exacerbation of psoriasis. , in Int J Dermatol , vol. 49, n. 12, dicembre 2010, pp. 1351-61, DOI : 10.1111/j.1365-4632.2010.04570.x , PMID 21091671 .
- ^ SP. Raychaudhuri, J. Gross, Psoriasis risk factors: role of lifestyle practices. , in Cutis , vol. 66, n. 5, novembre 2000, pp. 348-52, PMID 11107520 .
- ^ S. Jankovic, M. Raznatovic; J. Marinkovic; J. Jankovic; N. Maksimovic, Risk factors for psoriasis: A case-control study. , in J Dermatol , vol. 36, n. 6, giugno 2009, pp. 328-34, DOI : 10.1111/j.1346-8138.2009.00648.x , PMID 19500181 .
- ^ L. Manolache, D. Petrescu-Seceleanu; V. Benea, Life events involvement in psoriasis onset/recurrence. , in Int J Dermatol , vol. 49, n. 6, giugno 2010, pp. 636-41, DOI : 10.1111/j.1365-4632.2009.04367.x , PMID 20618467 .
- ^ SM. Behnam, SE. Behnam; JY. Koo, Alcohol as a risk factor for plaque-type psoriasis. , in Cutis , vol. 76, n. 3, settembre 2005, pp. 181-5, PMID 16268261 .
- ^ Naldi L., Rebora A., Dermatologia basata sulle prove di efficacia, 2006, Masson
- ^ RP. Dellavalle, KR. Johnson, Do smoking, obesity, and stress cause psoriasis? , in J Invest Dermatol , vol. 125, n. 1, luglio 2005, pp. vi-vii, DOI : 10.1111/j.0022-202X.2005.23792.x , PMID 15982291 .
- ^ Le sigarette bruciano anche la pelle - Corriere.it
- ^ L. Naldi, L. Chatenoud; D. Linder; A. Belloni Fortina; A. Peserico; AR. Virgili; PL. Bruni; V. Ingordo; G. Lo Scocco; C. Solaroli; D. Schena, Cigarette smoking, body mass index, and stressful life events as risk factors for psoriasis: results from an Italian case-control study. , in J Invest Dermatol , vol. 125, n. 1, luglio 2005, pp. 61-7, DOI : 10.1111/j.0022-202X.2005.23681.x , PMID 15982303 .
- ^ MA. Gupta, AK. Gupta; CN. Ellis; JJ. Voorhees, Some psychosomatic aspects of psoriasis. , in Adv Dermatol , vol. 5, 1990, pp. 21-30; discussion 31, PMID 2204373 .
- ^ Y. Lee, YH. Nam; JH. Lee; JK. Park; YJ. Seo, Hypocalcaemia-induced pustular psoriasis-like skin eruption. , in Br J Dermatol , vol. 152, n. 3, marzo 2005, pp. 591-3, DOI : 10.1111/j.1365-2133.2005.06460.x , PMID 15787848 .
- ^ S. Aksoylar, Y. Aydinok; E. Serdaroğlu; M. Coker; F. Ozdemir; F. Ozkinay, HDR (hypoparathyroidism, sensorineural deafness, renal dysplasia) syndrome presenting with hypocalcemia-induced generalized psoriasis. , in J Pediatr Endocrinol Metab , vol. 17, n. 7, luglio 2004, pp. 1031-4, PMID 15301053 .
- ^ T. Maeda, H. Hasegawa; A. Matsuda; M. Kinoshita; O. Matsumura; T. Mitarai, [Severe hypocalcemia compatible with idiopathic hypoparathyroidism associated with psoriasis vulgaris]. , in Nihon Naika Gakkai Zasshi , vol. 92, n. 12, dicembre 2003, pp. 2412-4, PMID 14743761 .
- ^ Diani M, Altomare G, Reali E, T cell responses in psoriasis and psoriatic arthritis , in Autoimmun Rev , vol. 14, n. 4, 2015, pp. 286-92, DOI : 10.1016/j.autrev.2014.11.012 , PMID 25445403 .
- ^ DC. ABELE, RL. DOBSON; JB. GRAHAM, HEREDITY AND PSORIASIS. STUDY OF A LARGE FAMILY. , in Arch Dermatol , vol. 88, luglio 1963, pp. 38-47, PMID 14042660 .
- ^ W. Watson, HM. Cann; EM. Farber; ML. Nall, The genetics of psoriasis. , in Arch Dermatol , vol. 105, n. 2, febbraio 1972, pp. 197-207, PMID 5060862 .
- ^ V. Chandran, CT. Schentag; JE. Brockbank; FJ. Pellett; S. Shanmugarajah; SM. Toloza; P. Rahman; DD. Gladman, Familial aggregation of psoriatic arthritis. , in Ann Rheum Dis , vol. 68, n. 5, maggio 2009, pp. 664-7, DOI : 10.1136/ard.2008.089367 , PMID 18524791 .
- ^ a b c FO. Nestle, DH. Kaplan; J. Barker, Psoriasis. , in N Engl J Med , vol. 361, n. 5, luglio 2009, pp. 496-509, DOI : 10.1056/NEJMra0804595 , PMID 19641206 .
- ^ AM. Bowcock, JN. Barker, Genetics of psoriasis: the potential impact on new therapies. , in J Am Acad Dermatol , vol. 49, 2 Suppl, agosto 2003, pp. S51-6, PMID 12894126 .
- ^ A. Pasić, J. Lipozencić; R. Ceović; K. Kostović, The genetics of psoriasis--selected novelties in 2008. , in Acta Dermatovenerol Croat , vol. 17, n. 3, 2009, pp. 176-81, PMID 19818216 .
- ^ LD. Sun, W. Li; S. Yang; X. Fan; KL. Yan; YH. Liang; M. Gao; Y. Cui; FL. Xiao; WH. Du; KY. Zhang, Evidence for a novel psoriasis susceptibility locus at 9q33-9q34 in Chinese Hans. , in J Invest Dermatol , vol. 127, n. 5, maggio 2007, pp. 1140-4, DOI : 10.1038/sj.jid.5700671 , PMID 17205061 .
- ^ a b Gudjónsson JE, Kárason A, Antonsdóttir AA, Rúnarsdóttir EH, Gulcher JR, Stefánsson K, Valdimarsson H, HLA-Cw6-positive and HLA-Cw6-negative patients with Psoriasis vulgaris have distinct clinical features , in J. Invest. Dermatol. , vol. 118, n. 2, 2002, pp. 362-5, DOI : 10.1046/j.0022-202x.2001.01656.x , PMID 11841557 .
- ^ RO. Leder, JN. Mansbridge; J. Hallmayer; SE. Hodge, Familial psoriasis and HLA-B: unambiguous support for linkage in 97 published families. , in Hum Hered , vol. 48, n. 4, pp. 198-211, PMID 9694251 .
- ^ Yim SH, Jung SH, Chung B, Chung YJ,Clinical implications of copy number variations in autoimmune disorders , in Korean J. Intern. Med. , vol. 30, n. 3, 2015, pp. 294-304, DOI : 10.3904/kjim.2015.30.3.294 , PMC 4438283 , PMID 25995659 .
- ^ M. Cargill, SJ. Schrodi; M. Chang; VE. Garcia; R. Brandon; KP. Callis; N. Matsunami; KG. Ardlie; D. Civello; JJ. Catanese; DU. Leong, A large-scale genetic association study confirms IL12B and leads to the identification of IL23R as psoriasis-risk genes. , in Am J Hum Genet , vol. 80, n. 2, febbraio 2007, pp. 273-90, DOI : 10.1086/511051 , PMID 17236132 .
- ^ RP. Nair, A. Ruether; PE. Stuart; S. Jenisch; T. Tejasvi; R. Hiremagalore; S. Schreiber; D. Kabelitz; HW. Lim; JJ. Voorhees; E. Christophers, Polymorphisms of the IL12B and IL23R genes are associated with psoriasis. , in J Invest Dermatol , vol. 128, n. 7, luglio 2008, pp. 1653-61, DOI : 10.1038/sj.jid.5701255 , PMID 18219280 .
- ^ JE. Gudjonsson, Genetic variation and psoriasis. , in G Ital Dermatol Venereol , vol. 143, n. 5, ottobre 2008, pp. 299-305, PMID 18833071 .
- ^ CT. Jordan, L. Cao; ED. Roberson; S. Duan; CA. Helms; RP. Nair; KC. Duffin; PE. Stuart; D. Goldgar; G. Hayashi; EH. Olfson, Rare and common variants in CARD14, encoding an epidermal regulator of NF-kappaB, in psoriasis. , in Am J Hum Genet , vol. 90, n. 5, maggio 2012, pp. 796-808, DOI : 10.1016/j.ajhg.2012.03.013 , PMID 22521419 .
- ^ CT. Jordan, L. Cao; ED. Roberson; KC. Pierson; CF. Yang; CE. Joyce; C. Ryan; S. Duan; CA. Helms; Y. Liu; Y. Chen, PSORS2 is due to mutations in CARD14. , in Am J Hum Genet , vol. 90, n. 5, maggio 2012, pp. 784-95, DOI : 10.1016/j.ajhg.2012.03.012 , PMID 22521418 .
- ^ BJ. Nickoloff, The immunologic and genetic basis of psoriasis. , in Arch Dermatol , vol. 135, n. 9, settembre 1999, pp. 1104-10, PMID 10490116 .
- ^ DY. Leung, JB. Travers; R. Giorno; DA. Norris; R. Skinner; J. Aelion; LV. Kazemi; MH. Kim; AE. Trumble; M. Kotb, Evidence for a streptococcal superantigen-driven process in acute guttate psoriasis. , in J Clin Invest , vol. 96, n. 5, novembre 1995, pp. 2106-12, DOI : 10.1172/JCI118263 , PMID 7593594 .
- ^ JE. Rasmussen, The relationship between infection with group A beta hemolytic streptococci and the development of psoriasis. , in Pediatr Infect Dis J , vol. 19, n. 2, febbraio 2000, pp. 153-4, PMID 10694004 .
- ^ a b Boehncke WH, Schön MP, Psoriasis , in Lancet , 2015, DOI : 10.1016/S0140-6736(14)61909-7 , PMID 26025581 .
- ^ Abbott R, Whear R, Nikolaou V, Bethel A, Coon JT, Stein K, Dickens C, Tumour necrosis factor-α inhibitor therapy in chronic physical illness: A systematic review and meta-analysis of the effect on depression and anxiety , in J Psychosom Res , 2015, DOI : 10.1016/j.jpsychores.2015.04.008 , PMID 25935351 .
- ^ Trifunović J, Miller L, Debeljak Ž, Horvat V, Pathologic patterns of interleukin 10 expression--a review , in Biochem Med (Zagreb) , vol. 25, n. 1, 2015, pp. 36-48, DOI : 10.11613/BM.2015.004 , PMC 4401305 , PMID 25672465 .
- ^ RJ. Chalmers, B. Kirby, Gluten and psoriasis. , in Br J Dermatol , vol. 142, n. 1, gennaio 2000, pp. 5-7, PMID 10651687 .
- ^ G. Michaëlsson, B. Gerdén; E. Hagforsen; B. Nilsson; I. Pihl-Lundin; W. Kraaz; G. Hjelmquist; L. Lööf, Psoriasis patients with antibodies to gliadin can be improved by a gluten-free diet. , in Br J Dermatol , vol. 142, n. 1, gennaio 2000, pp. 44-51, PMID 10651693 .
- ^ G. Michaëlsson, S. Ahs; I. Hammarström; IP. Lundin; E. Hagforsen, Gluten-free diet in psoriasis patients with antibodies to gliadin results in decreased expression of tissue transglutaminase and fewer Ki67+ cells in the dermis. , in Acta Derm Venereol , vol. 83, n. 6, 2003, pp. 425-9, DOI : 10.1080/00015550310015022 , PMID 14690336 .
- ^ G. Addolorato, A. Parente; G. de Lorenzi; ME. D'angelo Di Paola; L. Abenavoli; L. Leggio; E. Capristo; C. De Simone; M. Rotoli; GL. Rapaccini; G. Gasbarrini, Rapid regression of psoriasis in a coeliac patient after gluten-free diet. A case report and review of the literature. , in Digestion , vol. 68, n. 1, 2003, pp. 9-12, DOI : 10.73220 , PMID 12949434 .
- ^ A. Civatte, Psoriasis and Seborrhœic Eczema: Pathological Anatomy and Diagnostic Histology of the Two Dermatoses. , in Proc R Soc Med , vol. 18, Dermatol Sect, 1925, pp. 1-11, PMID 20908652 .
- ^ HW. Barber, Pustular Psoriasis of the Extremities. , in Proc R Soc Med , vol. 26, n. 4, febbraio 1933, pp. 329-33, PMID 19989109 .
- ^ TJ. Jaime, BA. Rodrigues; TJ. Jaime; ML. Barbo; DR. Simis, [Psoriasis of von Zumbusch. , in An Bras Dermatol , vol. 84, n. 3, luglio 2009, pp. 299-301, PMID 19668933 .
- ^ Malattie a carattere desquamativo , su msd-italia.it . URL consultato il 22 novembre 2011 (archiviato dall' url originale il 29 gennaio 2013) .
- ^ F. Sampogna, MM. Chren; CF. Melchi; P. Pasquini; S. Tabolli; D. Abeni, Age, gender, quality of life and psychological distress in patients hospitalized with psoriasis. , in Br J Dermatol , vol. 154, n. 2, febbraio 2006, pp. 325-31, DOI : 10.1111/j.1365-2133.2005.06909.x , PMID 16433804 .
- ^ L. Dubertret, U. Mrowietz; A. Ranki; PC. van de Kerkhof; S. Chimenti; T. Lotti; G. Schäfer, European patient perspectives on the impact of psoriasis: the EUROPSO patient membership survey. , in Br J Dermatol , vol. 155, n. 4, ottobre 2006, pp. 729-36, DOI : 10.1111/j.1365-2133.2006.07405.x , PMID 16965422 .
- ^ MJ. Bhosle, A. Kulkarni; SR. Feldman; R. Balkrishnan, Quality of life in patients with psoriasis. , in Health Qual Life Outcomes , vol. 4, 2006, p. 35, DOI : 10.1186/1477-7525-4-35 , PMID 16756666 .
- ^ D. Globe, MS. Bayliss; DJ. Harrison, The impact of itch symptoms in psoriasis: results from physician interviews and patient focus groups. , in Health Qual Life Outcomes , vol. 7, 2009, p. 62, DOI : 10.1186/1477-7525-7-62 , PMID 19580674 .
- ^ A. Gottlieb, J. Feng; DJ. Harrison; D. Globe, Validation and response to treatment of a pruritus self-assessment tool in patients with moderate to severe psoriasis. , in J Am Acad Dermatol , vol. 63, n. 4, ottobre 2010, pp. 580-6, DOI : 10.1016/j.jaad.2009.09.049 , PMID 20599294 .
- ^ T. Fredriksson, U. Pettersson, Severe psoriasis--oral therapy with a new retinoid. , in Dermatologica , vol. 157, n. 4, 1978, pp. 238-44, PMID 357213 .
- ^ BA. Louden, DJ. Pearce; W. Lang; SR. Feldman, A Simplified Psoriasis Area Severity Index (SPASI) for rating psoriasis severity in clinic patients. , in Dermatol Online J , vol. 10, n. 2, 2004, p. 7, PMID 15530297 .
- ^ SR. Feldman, AB. Fleischer; DM. Reboussin; SR. Rapp; ML. Exum; AR. Clark; L. Nurre, The self-administered psoriasis area and severity index is valid and reliable. , in J Invest Dermatol , vol. 106, n. 1, gennaio 1996, pp. 183-6, PMID 8592072 .
- ^ K. Holubar, H. Auspitz, The man behind the eponym. Remembering Heinrich Auspitz. , in Am J Dermatopathol , vol. 8, n. 1, febbraio 1986, pp. 83-5, PMID 3518525 .
- ^ JD. Bernhard, Auspitz sign is not sensitive or specific for psoriasis. , in J Am Acad Dermatol , vol. 22, 6 Pt 1, giugno 1990, pp. 1079-81, PMID 2370333 .
- ^ MT. Rahman, NS. Monami; S. Ferdousi; T. Tahmin, Skin biopsy and psoriasis. , in Mymensingh Med J , vol. 19, n. 3, luglio 2010, pp. 353-9, PMID 20639826 .
- ^ K. Nayek, MK. Dasgupta, Infantile pustular psoriasis--may mimic seborrhic dermatitis. , in Indian Pediatr , vol. 38, n. 9, settembre 2001, p. 1059, PMID 11568388 .
- ^ A. Krol, B. Krafchik, The differential diagnosis of atopic dermatitis in childhood. , in Dermatol Ther , vol. 19, n. 2, Ago 2009, pp. 73-82, DOI : 10.1111/j.1529-8019.2006.00058.x , PMID 16669989 .
- ^ GD. Eslick, Atypical pityriasis rosea or psoriasis guttata? Early examination is the key to a correct diagnosis. , in Int J Dermatol , vol. 41, n. 11, novembre 2002, pp. 788-91, PMID 12453007 .
- ^ N. Balato, L. Di Costanzo; A. Balato, Differential diagnosis of psoriasis. , in J Rheumatol Suppl , vol. 83, agosto 2009, pp. 24-5, DOI : 10.3899/jrheum.090216 , PMID 19661533 .
- ^ A. Menter, CE. Griffiths, Current and future management of psoriasis. , in Lancet , vol. 370, n. 9583, luglio 2007, pp. 272-84, DOI : 10.1016/S0140-6736(07)61129-5 , PMID 17658398 .
- ^ A. Krebs, H. Schaltegger, [Investigations on the mechanism of action of chrysarobin and dithranol (=Cignolin) in psoriasis. Indications for a cytostatic action of these drugs]. , in Experientia , vol. 21, n. 3, marzo 1965, pp. 128-9, PMID 5890422 .
- ^ AC. Miller, Anthralin cream as short contact therapy for psoriasis. , in Cutis , vol. 35, n. 6, giugno 1985, pp. 578-82, PMID 4017653 .
- ^ N. Haas, A. Wulff-Woesten; W. Sterry; H. Meffert, [Dithranol in the treatment of scalp psoriasis]. , in J Dtsch Dermatol Ges , vol. 1, n. 9, settembre 2003, pp. 688-93, PMID 16285275 .
- ^ J. Fuchs, G. Zimmer; RH. Wölbling; R. Milbradt, On the interaction between anthralin and mitochondria: a revision. , in Arch Dermatol Res , vol. 279, n. 1, 1986, pp. 59-65, PMID 2880567 .
- ^ JC. Beani, M. Jeanmougin, [Narrow-band UVB therapy in psoriasis vulgaris: good practice guideline and recommendations of the French Society of Photodermatology]. , in Ann Dermatol Venereol , vol. 137, n. 1, gennaio 2010, pp. 21-31, DOI : 10.1016/j.annder.2009.12.004 , PMID 20110064 .
- ^ E. Archier, S. Devaux; E. Castela; A. Gallini; F. Aubin; M. Le Maître; S. Aractingi; H. Bachelez; B. Cribier; P. Joly; D. Jullien, Efficacy of psoralen UV-A therapy vs. narrowband UV-B therapy in chronic plaque psoriasis: a systematic literature review. , in J Eur Acad Dermatol Venereol , 26 Suppl 3, maggio 2012, pp. 11-21, DOI : 10.1111/j.1468-3083.2012.04519.x , PMID 22512676 .
- ^ E. Archier, S. Devaux; E. Castela; A. Gallini; F. Aubin; M. Le Maître; S. Aractingi; H. Bachelez; B. Cribier; P. Joly; D. Jullien, Carcinogenic risks of psoralen UV-A therapy and narrowband UV-B therapy in chronic plaque psoriasis: a systematic literature review. , in J Eur Acad Dermatol Venereol , 26 Suppl 3, maggio 2012, pp. 22-31, DOI : 10.1111/j.1468-3083.2012.04520.x , PMID 22512677 .
- ^ RV. Patel, LN. Clark; M. Lebwohl; JM. Weinberg, Treatments for psoriasis and the risk of malignancy. , in J Am Acad Dermatol , vol. 60, n. 6, giugno 2009, pp. 1001-17, DOI : 10.1016/j.jaad.2008.12.031 , PMID 19344980 .
- ^ RK. Landow, New drugs for dermatologic diseases. , in Dermatol Clin , vol. 6, n. 4, ottobre 1988, pp. 575-84, PMID 3067917 .
- ^ A. Kuhn, V. Ruland; N. Patsinakidis; TA. Luger, Use of methotrexate in patients with psoriasis. , in Clin Exp Rheumatol , vol. 28, 5 Suppl 61, set-ott 2010, pp. S138-44, PMID 21044448 .
- ^ PS. Yamauchi, D. Rizk; NJ. Lowe, Retinoid therapy for psoriasis. , in Dermatol Clin , vol. 22, n. 4, ottobre 2004, pp. 467-76, x, DOI : 10.1016/S0733-8635(03)00126-8 , PMID 15450342 .
- ^ P. Berbis, [Acitretine]. , in Ann Dermatol Venereol , vol. 128, n. 6-7, Giu-Lug 2001, pp. 737-45, PMID 11460037 .
- ^ Lernia V, Tasin L, Pellicano R, Zumiani G, Albertini G, Impact of body mass index on retention rates of anti-TNF-alfa drugs in daily practice for psoriasis [ collegamento interrotto ] , in J Dermatolog Treat , vol. 23, n. 6, 2012, pp. 404-9, DOI : 10.3109/09546634.2011.593489 , PMID 21781016 .
- ^ Raccomandazione EMEA su base della NOTA INFORMATIVA dell'AIFA
- ^ PHARMASTAR - L'Emea raccomanda la sospensione dell'antipsoriasi Efalizumab
- ^ Voluntary US Market Discontinuation of Amevive® (alefacept) ( PDF ), su amevive.com . URL consultato il 1º dicembre 2012 .
- ^ Approvazione di Ustekinumab nel trattamento della psoriasi a placche da moderata a grave , su news.idsk.com .
- ^ Benson JM, Peritt D, Scallon BJ, et al. , Discovery and mechanism of ustekinumab: a human monoclonal antibody targeting interleukin-12 and interleukin-23 for treatment of immune-mediated disorders , in MAbs , vol. 3, n. 6, 2011, pp. 535-45, DOI : 10.4161/mabs.3.6.17815 , PMID 22123062 .
- ^ Samarasekera EJ, Sawyer L, Wonderling D, Tucker R, Smith CH, Topical therapies for the treatment of plaque psoriasis: systematic review and network meta-analyses , in Br J Dermatol , vol. 168, n. 5, 2013, pp. 954-67, DOI : 10.1111/bjd.12276/full , PMID 23413913 .
- ^ Prieto-Pérez R, Cabaleiro T, Daudén E, Ochoa D, Roman M, Abad-Santos F.,Genetics of Psoriasis and Pharmacogenetics of Biological Drugs , in Autoimmune Dis. , vol. 2013, n. 613086, agosto 2013, p. 613086, DOI : 10.1155/2013/613086 , PMC 3771250 , PMID 24069534 .
- ^ a b c Parrish L., Psoriasis: symptoms, treatments and its impact on quality of life , in Br J Community Nurs , vol. 17, n. 11, 2012, pp. 524, 526, 528, DOI : 10.12968/bjcn.2012.17.11.524 , PMID 23124421 .
- ^ Dessinioti C, Katsambas A,Seborrheic dermatitis: etiology, risk factors, and treatments: facts and controversies , in Clin Dermatol , vol. 31, n. 4, 2013, pp. 343-51, DOI : 10.1016/j.clindermatol.2013.01.001 , PMID 23806151 .
- ^ a b Menter, A.,Gottlieb, A., Feldman, SR, Van Voorhees, AS, Leonardi, CL, Gordon, KB, Lebwohl, M., Koo, JY., Elmets, CA, Korman, NJ, Beutner, KR, Bhushan, R., Guidelines of care for the management of psoriasis and psoriatic arthritis: Section 1. Overview of psoriasis and guidelines of care for the treatment of psoriasis with biologics , in J Am Acad Dermatol , vol. 58, n. 5, maggio 2008, pp. 826-50, DOI : 10.1016/j.jaad.2008.02.039 , PMID 18423260 .
- ^ Gelmetti C, Therapeutic moisturizers as adjuvant therapy for psoriasis patients , in Am J Clin Dermatol , vol. 10, Suppl 1, gennaio 2009, pp. 7-12, DOI :10.2165/0128071-200910001-00002 , PMID 19209948 .
- ^ Bhosle MJ, Kulkarni A, Feldman SR, Balkrishnan R,Quality of life in patients with psoriasis , in Health Qual Life Outcomes , vol. 4, 2006, p. 35, DOI : 10.1186/1477-7525-4-35 , PMC 1501000 , PMID 16756666 .
- ^ P Magin,Appearance-related bullying and skin disorders. , in Clinics in dermatology , vol. 31, n. 1, Jan–Feb 2013, pp. 66-71, DOI : 10.1016/j.clindermatol.2011.11.009 , PMID 23245976 .
- ^ a b c Thomas P. Habif, 8 , in Clinical dermatology a color guide to diagnosis and therapy , 5th, Edinburgh, Mosby Elsevier, 2010, ISBN 978-0-323-08037-8 .
- ^ a b Shlyankevich J, Mehta NN, Krueger JG, Strober B, Gudjonsson JE, Qureshi AA, Tebbey PW, Kimball AB, Accumulating Evidence for the Association and Shared Pathogenic Mechanisms Between Psoriasis and Cardiovascular-related Comorbidities , in Am J Med , vol. 127, n. 12, dicembre 2014, pp. 1148-53, DOI : 10.1016/j.amjmed.2014.08.008 , PMID 25149424 .
- ^ a b Armstrong AW, Harskamp CT, Armstrong EJ, Psoriasis and the risk of diabetes mellitus: a systematic review and meta-analysis , in JAMA Dermatol , vol. 149, n. 1, gennaio 2013, pp. 84-91, DOI : 10.1001/2013.jamadermatol.406 , PMID 23407990 .
- ^ a b Richard MA, Barnetche T, Horreau C, Brenaut E, Pouplard C, Aractingi S, Aubin F, Cribier B, Joly P, Jullien D, Le Maître M, Misery L, Ortonne JP, Paul C., Psoriasis, cardiovascular events, cancer risk and alcohol use: evidence-based recommendations based on systematic review and expert opinion , in J Eur Acad Dermatol Venereol , vol. 27, Supplement 3, agosto 2013, pp. 2-11, DOI : 10.1111/jdv.12162 , PMID 23845148 .
- ^ Armstrong AW, Harskamp CT, Armstrong EJ, The association between psoriasis and hypertension: a systematic review and meta-analysis of observational studies , in J Hypertens , vol. 31, n. 3, 2013, pp. 433-42, DOI : 10.1097/HJH.0b013e32835bcce1 , PMID 23249828 .
- ^ Psoriasis Linked to Stroke Risk , BBC, agosto 2011.
- ^ a b Ghazizadeh R, Tosa M, Ghazizadeh M, Clinical Improvement in Psoriasis with Treatment of Associated Hyperlipidemia , in Am J Med Sci , vol. 341, n. 5, 2011, pp. 394-8, DOI : 10.1097/MAJ.0b013e3181ff8eeb , PMID 21233693 .
- ^ Raychaudhuri SK, Maverakis E, Raychaudhuri SP, Diagnosis and classification of psoriasis , in Autoimmun Rev , S1568-9972, n. 14, gennaio 2014, pp. 00020-2, DOI : 10.1016/j.autrev.2014.01.008 , PMID 24434359 .
- ^ Tablazon IL, Al-Dabagh A, Davis SA, Feldman SR, Risk of cardiovascular disorders in psoriasis patients: current and future , in Am J Clin Dermatol , vol. 14, n. 1, febbraio 2013, pp. 1-7, DOI : 10.1007/s40257-012-0005-5 , PMID 23329076 .
Voci correlate
Altri progetti
-
 Wikizionario contiene il lemma di dizionario « psoriasi »
Wikizionario contiene il lemma di dizionario « psoriasi » -
 Wikimedia Commons contiene immagini o altri file sulla psoriasi
Wikimedia Commons contiene immagini o altri file sulla psoriasi
Collegamenti esterni
- ( EN ) Psoriasi , su Enciclopedia Britannica , Encyclopædia Britannica, Inc.
- Psoriasis International , su psoriasis-international.org . URL consultato il 7 luglio 2010 (archiviato dall' url originale il 20 giugno 2012) .
- Registro PSOCARE presso AIFA , su psocare.agenziafarmaco.it . URL consultato il 7 luglio 2010 (archiviato dall' url originale l'8 marzo 2010) .
- What is psoriasis? American Academy of Family Physicians, luglio 1995, revisionata/aggiornata ottobre 2008 , su familydoctor.org .
- Associazione Nazionale per la tutela del malato di Psoriasi e Vitiligine , su asnpv.it .
- Associazione per la Difesa degli Psoriasici , su adipso.org .
- Federazione Italiana della Psoriasi , su fedipso.it .
| Controllo di autorità | Thesaurus BNCF 13044 · LCCN ( EN ) sh85108334 · GND ( DE ) 4077221-4 · BNF ( FR ) cb119654848 (data) · NDL ( EN , JA ) 00954062 |
|---|