Nitrili
Nitrilii sunt compuși organici caracterizați prin grupa funcțională −C≡N. [1] În literatura industrială prefixul ciano- este preferat termenului nitril. Nitrilii sunt constituenți ai materialelor utilizate în mod obișnuit, cum ar fi cleiurile cianoacrilate și cauciucul nitrilic utilizat în mănușile de laborator și etanșanții auto.
Pe de altă parte, compușii anorganici care conțin grupa −C≡N se numesc cianuri . Atât nitrilii, cât și cianurile pot fi considerați derivați ai cianurilor saline, cum ar fi NaCN și KCN , dar, în general, nitrilii sunt mai puțin toxici.
Grupul funcțional −C≡N nu trebuie confundat cu grupul −N≡C, caracteristic izocianurilor .
Structura și proprietățile de bază
La nitrilii, grupul R - C≡N are geometrie liniară, deoarece carbonul triplu legat este hibridizat. Distanța C - N este scurtă ( 116 pm ), [2] în acord cu prezența unei triple obligațiuni. Nitrilii sunt compuși polari , după cum se indică prin valori ale momentului dipolar ridicat. În faza lichidă au o permitivitate electrică ridicată.
fundal
Cianura de hidrogen , nitrilul acidului formic , a fost primul nitril care a fost sintetizat de Carl Scheele în 1782. [3] [4] În 1811 Joseph Louis Gay-Lussac a reușit să prepare cianură de hidrogen pură, un compus foarte toxic și volatil. [5] În 1832 Friedrich Wöhler și Justus von Liebig au preparat cianură de benzoil și benzonitril , dar, având în vedere randamentul foarte scăzut, nu au putut determina proprietățile sale chimice și fizice și nici nu și-au putut propune structura. [6] În 1834 Théophile-Jules Pelouze a sintetizat propionitril . [7] În 1844 Hermann von Fehling a sintetizat benzonitrilul, reușind pentru prima dată să izoleze o cantitate suficientă pentru a-i determina structura. El a inventat termenul nitril care a fost folosit de atunci pentru a desemna acest grup de substanțe. [8] Ulterior, cercetările în acest domeniu au rămas rareori timp de aproape un secol, probabil din cauza toxicității acestor compuși. Începând cu anii 1940, diferite cianuri anorganice au fost ușor disponibile, iar nitrilii organici au devenit substanțe chimice excelente tonaj [ neclar ] . [3]
Sinteza industrială
Industrial, principalele metode pentru sinteza nitrilului sunt oxidarea și hidrocianarea amoniului .
Oxidarea amoniului
Amonoxidarea este oxidarea parțială a unei hidrocarburi în prezența amoniacului și a catalizatorilor adecvați, de obicei pe bază de vanadiu și molibden. Acest proces este utilizat pe scară largă pentru sinteza acrilonitrilului din propenă :
- CH 2 = CH - CH 3 + 3 ⁄ 2 O 2 + NH 3 → CH 2 = CH - CN + 3H 2 O
În acest proces, acetonitrilul se formează și ca produs secundar. Amonoxidarea este utilizată la scară industrială pentru a produce și alți nitril, inclusiv derivați de benzonitril, ftalonitril și izobutironitrie . [9]
Hidrocianare
Această metodă formează nitrilii prin adăugarea de cianuri de hidrogen sau ioni de cianură în alchene. Un exemplu tipic este hidrocianarea 1,3- butadienei pentru a forma adiponitril , precursorul nailonului 6,6: [9]
- CH 2 = CH - CH = CH 2 + 2HCN → NC (CH 2 ) 4 CN
Sinteza de laborator
La scară de laborator, sunt posibile diverse sinteze. [3] [9] Unele sunt:
Sinteza Kolbe
Sinteza Kolbe se bazează pe substituirea nucleofilă a unei halogenuri de alchil cu cianură de sodiu sau alte metale alcaline. Reacția se numește ciano-dehalogenare .
- R - CH 2 −X + NaCN → R - CH 2 −CN + NaX
Deshidratarea amidelor și oximelor
Deshidratarea unei amide primare (R-CO-NH 2 ) cu îndepărtarea unei molecule de apă duce la nitril. De exemplu, benzamida este convertită în benzonitril în prezența diclorofosfatului de etil și a DBU . Tautomerul A și aductul său de fosfat B se formează ca intermediari ai reacției. [10]
Deshidratarea ald oximelor (RCH = NOH) duce, de asemenea, la nitrili. Reactivi tipici pentru această reacție sunt trietilamina / dioxidul de sulf , zeoliții sau clorura de sulfuril . Această abordare este exploatată în sinteza cu un singur vas a nitrililor pornind de la aldehide și hidroxilamine: [11]
Reacția Sandmeyer
Reacția Sandmeyer poate fi exploatată pentru a obține nitrilii aromatici pornind de la anilină . Reacția se desfășoară prin săruri de diazoniu și necesită cianuri ale metalelor de tranziție. [12]
- ArN 2 + + CuCN → ArCN + N 2 + Cu +
Reacția Rosenmund-von Braun
Reacția Rosenmund-von Braun conduce, de asemenea , la nitrilii aromatici, prin tratarea halogenurilor de arii cu cianură de cupru (I) . [13]
Alte metode
- Transformarea N, N'-dialchil hidrazonelor în nitrili este o reacție foarte ușoară și eficientă. Se obține prin tratarea N, N-dialchilhidrazonei cu peroxid de hidrogen la 30%, într-un solvent mixt acetonitril-acid acetic-piridină într-un raport de 94,5-5-0,5 și în prezența a 1% metiltrixoreniu ca catalizator. Transformarea rapidă a hidrazonei în nitril este de 90%. Reacția este generală, deoarece apare cu hidrazone ale aldehidelor alifatice, aromatice și nesaturate și heterociclice. [14]
- NN = RHC (CH3) 2 + H 2 O 2 RCN
- Nitrilii pot fi obținuți și prin oxidarea aminelor primare. Oxidarea poate fi efectuată cu peroxidisulfate de potasiu , [15] acid tricloroizocianuric , [16] sau prin anodică electro- sinteză. [17]
- Nitrilii aromatici pot fi obținuți din chinone folosind trimetilsililcianură. Intermediarul cianohidrin sililat se face aromat cu tribromură de fosfor. [18]
Reacții
La nitrilii grupul –CN are proprietăți electrofile. La nitrilii alifatici, carbonul adiacent grupării –CN poate da reacții de substituție catalizate de baze.
Grupul nitril al unui compus organic poate da naștere la diverse reacții în funcție de condițiile și reactanții prezenți.
Hidroliză
Nitrilii pot fi hidrolizați în acizii carboxilici corespunzători. Un acid astfel obținut va fi caracterizat prin faptul că are încă un carbon decât halogenura de alchil din care a fost sintetizat nitrilul. Trecerea prin nitril permite, prin urmare, lanțul de atomi de carbon al unui substrat să fie prelungit cu o unitate.
- R-CH 2 -CN + 2 H 2 O + OH - → R-CH 2- COO - + NH 4 OH
Reducere
Reducerea nitrililor cu hidrogen duce la formarea de amine . În funcție de condiții, pot fi obținute și amine secundare și terțiare: [19]
- RC≡N + 2H 2 → R-CH 2 NH 2
- 2R-4H + 2 = N → (R-CH2) 2 - NH + NH3
- 3R-C = N + 6H 2 → (R-CH2) 3 - N + 2NH 3
Pot fi folosiți alți agenți reducători, cum ar fi tetrahidroaluminatul de litiu, borohidrura de litiu , [20] diboranul [21] sau sodiul elementar. [22]
Alchilarea
Nitrilii alchilici sunt suficient de acizi pentru a forma carbanioni de nitril, adică specii care au pierdut un proton din carbonul α în grupul nitril și care pot alchila o mare varietate de electrofili. [23] Nucleofilicitatea excepțională a acestor specii se datorează cerințelor sterice reduse ale unității CN și stabilizării sale inductive. Din aceste motive, nitrilii sunt ideali în sinteza chimiei farmaceutice pentru a forma noi legături carbon-carbon în prezența unor cerințe sterice stricte. Evoluțiile recente au arătat că natura contraionului metalic poate provoca o coordonare diferită a azotului nitrilului sau a carbonului nucleofil adiacent, cu consecințe profunde asupra reactivității și stereochimiei. [24]
Adaos nucleofil
Carbonul nitrilic este electrofil și, prin urmare, este susceptibil la adăugarea nucleofilă . Exemple sunt:
- Reacția lui Blaise cu reactivi organo-zincici
- Reacția Pinner cu alcooli
- Reacția Houben-Hoesch cu compuși aromatici pentru a forma arilchetone.
- În reacția Thorpe, nitrilii alifatici se autocondensează pentru a forma enamine . [25]
- Cu amine, cum ar fi sinteza creatinei din sarcozină și cianamidă [26]
Alte reacții
- Nitrilii pot reacționa, de asemenea, cu reactivii lui Grignard pentru a forma cetone prin formarea unei imine intermediare care suferă hidroliză:
- R-CN + R'-MgX → RC (NH) -R '→ R-CO-R'
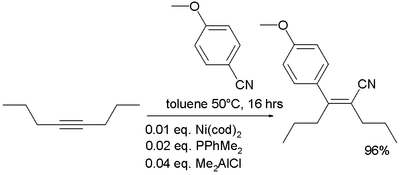
- Nitrilii se pot adăuga la alchine în prezența catalizatorilor. [27]
- Nitrilii sunt precursori ai complexelor nitrilice ale metalelor de tranziție utilizate ca reactanți și catalizatori. Câteva exemple sunt [Cu (MeCN) 4] + și PdCI2 (PhCN) 2 . [28]
Nitrilii utilizați în mod obișnuit
Un nitril utilizat pe scară largă în laborator este acetonitrilul (CH 3 -CN), utilizat ca solvent biologic amestecat cu o soluție tampon , pentru extragerea metaboliților din țesuturi și măsurarea concentrației acestora prin cromatografie .
Acrilonitrilul este utilizat în principal ca monomer pentru producerea de polimeri sintetici, în special poliacrilonitril pentru fibre acrilice. Este, de asemenea, o componentă a cauciucului sintetic.
Prezență în natură
Nitrilii apar în mod natural la o varietate de plante și animale. Peste 120 de nitrili au fost izolați din surse terestre și marine. Nitrilii se găsesc în mod obișnuit în endocarpul unor fructe, în special migdalele , și se dezvoltă în timpul gătirii culturilor de Brassica (cum ar fi varza, varza de Bruxelles și conopida) care eliberează nitrilii prin hidroliză. Mandelonitrilul este cianohidrina care eliberează cianură după ingerarea migdalelor sau a altor semințe de fructe. [29]
Aplicații în farmacologie
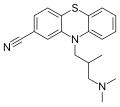
Peste 30 de produse farmaceutice care conțin nitril cu diverse indicații medicamentoase sunt comercializate în prezent, iar în cercetarea clinică există mai mult de 20 de alți derivați care conțin nitril. Grupul nitril este destul de robust și, în majoritatea cazurilor, nu este ușor metabolizat și trece prin corp neschimbat. [30] Unele produse farmaceutice care conțin nitril sunt vildagliptin , un medicament antidiabetic și anastrozol , utilizat în tratamentul cancerului de sân. Alte medicamente care conțin grupul nitril sunt prezentate în galerie.
Structura periciazinei , un antipsihotic studiat în tratamentul dependențelor de opiacee .
Structura citalopramului , un antidepresiv de tip ISRS .
Structura ciamemazinei , un antipsihotic .
Structura fadrozolului , un inhibitor al aromatazei utilizat în tratamentul cancerului de sân
Structura letrozolului , un inhibitor al aromatazei utilizat în tratamentul cancerului de sân.
Notă
- ^ McNaught și Wilkinson 1997
- ^ Ken-ichi și colab. 1974
- ^ a b c Mowry 1948
- ^ Scheele 1789
- ^ Gay-Lussac 1811
- ^ Wöhler și Liebig 1832
- ^ Pelouze 1834
- ^ Fehling 1844
- ^ a b c Pollak și Romeder 2002
- ^ Kuo și colab. 2007
- ^ Dewan și colab. 2006
- ^ Clarke și Read 2003
- ^ Koelsch și Whitney 1941
- ^ S. Stanković și Espenson 1998
- ^ Yamazaki și Yamazaki 1990
- ^ Chen și colab. 2003
- ^ Feldhues și Schäfer
- ^ Glöcklhofer și colab. 2015
- ^ Barrault și Pouilloux 1997
- ^ Soai și Ookawa 1986
- ^ Hutchins și Maryanoff 1973
- ^ Suter și Moffett 1934
- ^ Adams 1957
- ^ Fleming și Zhang
- ^ Schaefer și Bloomfield 2011
- ^ Smith și Tan 2006
- ^ Nakao și colab. 2007
- ^ Rach și Kühn 2009
- ^ Fleming 1999
- ^ Fleming și colab. 2010
Bibliografie
- ( EN ) R. Adams (eds), Organic Reactions, Volumul 9 , New York, John Wiley & Sons, 1957, ISBN 978-0471007265 .
- ( EN ) J. Barrault și Y. Pouilloux, Reacții catalitice de aminare: Sinteza aminelor grase. Controlul selectivității în prezența catalizatorilor multifuncționali , în Catalysis Today , vol. 37, n. 2, 1997, pp. 137-153, DOI : 10.1016 / S0920-5861 (97) 00006-0 .
- ( RO ) F.-E. Chen, Y.-Y. Kuang, H.-F. Dai, L. Lu și M. Huo, O oxidare selectivă și ușoară a aminelor primare în nitriți cu acid tricloroizocianuric , în Sinteză , vol. 17, 2003, pp. 2629-2631, DOI : 10.1055 / s-2003-42431 .
- ( EN ) HT Clarke și RR Read, o-Tolunitril și p-Tolunitril , în Org. Sintetizator. , 2003, p. 69, DOI : 10.1002 / 0471264180.os004.25 .
- ( EN ) SK Dewan, R. Singh și A. Kumar, One pot sinteza nitrililor din aldehide și clorhidrat de hidroxilamină folosind sulfat de sodiu (anhid) și bicarbonat de sodiu în mediu uscat sub iradiere cu microunde , în Arkivoc (ii) , 2006, pp. 41-44.
- ( DE ) H. Fehling, Ueber die Zersetzung des benzoësauren Ammoniaks durch die Wärme , în Justus Liebigs Ann. Chem. , vol. 49, 1844, pp. 91-97, DOI : 10.1002 / jlac.18440490106 .
"De la Laurent den von ihm entdeckten Körper schon Nitrobenzoyl genannt hat, auch schon ein Azobenzoyl existirt, so könnte man den aus benzoësaurem Ammoniak entstehenden Körper vielleicht Benzonitril nennen" . - ( EN ) U. Feldhues și HJ Schäfer, Oxidarea aminelor alifatice primare în nitriți la electrodul de hidroxid de nichel , în Sinteză , vol. 2, 1982, pp. 145-146, DOI : 10.1055 / s-1982-29721 .
- ( EN ) FF Fleming, produse naturale care conțin nitril , în Nat. Rep. Prod. , Vol. 16, 1999, pp. 597-606, DOI : 10.1039 / A804370A .
- ( EN ) F. Fleming și Z. Zhang, Nitrilii ciclici: avantaje tactice în sinteză , în Tetrahedron , vol. 61, nr. 4, 2005, pp. 747-789, DOI : 10.1016 / j.tet.2004.11.012 .
- ( EN ) FF Fleming, L. Yao, PC Ravikumar, L. Funk și BC Shook, Produse farmaceutice care conțin nitril: roluri eficace ale farmacoforului nitrilic , în J. Med. Chem. , vol. 53, nr. 22, 2010, pp. 7902-7917, DOI : 10.1021 / jm100762r .
- ( FR ) Gay-Lussac, Note sur acid prussique , în Annales de chimie , vol. 77, 1811, pp. 128-133.
- ( EN ) F. Glöcklhofer, M. Lunzer și J. Frölich, Easy Synthesis of Cyanoarenes from Quinones by Reductive Aromatization of Cyanohydrin Intermediates , în Synlett. , vol. 26, n. 7, 2015, pp. 950-952, DOI : 10.1055 / s-0034-1380150 .
- ( RO ) RO Hutchins și BE Maryanoff, 2-terț-butil-1,3-diaminoproan , în Org. Sintetizator. , vol. 53, 1973, p. 21, DOI : 10.15227 / orgsyn.053.0021 .
- ( EN ) K. Ken-ichi, F. Tsutomu și K. Kozo, Structuri moleculare ale cianurii de hidrogen și ale acetonitrilului, studiate prin difracție cu electroni în gaz , în Bull. Chem. Soc. Jpn. , vol. 47, nr. 2, 1974, pp. 299-304, DOI : 10.1246 / bcsj.47.299 .
- ( EN ) CF Koelsch și AG Whitney, The Rosenmund - von Braun nitrile synthesis , în J. Org. Chem. , vol. 6, nr. 6, 1941, pp. 795–803, DOI : 10.1021 / jo01206a002 . Adus pe 28 ianuarie 2014 .
- ( EN ) C.-W. Kuo, J.-L. Zhu, J.-D. Wu, C.-M. Chu și colab., O nouă procedură convenabilă pentru conversia amidelor primare în nitrili , în Chem. Comun. , Nu. 3, 2007, pp. 301-303, DOI : 10.1039 / b614061k .
- (EN) AD McNaught și A. Wilkinson, Nitriles , în IUPAC. Compendiu de terminologie chimică („Cartea de aur”) , ediția a II-a, Oxford, Blackwell Scientific Publications, 1997, ISBN 0-9678550-9-8 .
- ( EN ) DT Mowry, Prepararea nitrililor , în chim. Rev. , vol. 42, n. 2, 1948, pp. 189-283, DOI : 10.1021 / cr60132a001 .
- ( EN ) Y. Nakao, A. Yada, S. Ebata și T. Hiyama, A Dramatic Effect of Lewis-Acid Catalysts on Nickel-Catalyzed Carbocyanation of Alkynes , în J. Am. Chem. Soc. , Vol. 129, nr. 9, 2007, pp. 2428-2429, DOI : 10.1021 / ja067364x .
- ( DE ) J. Pelouze, Notiz über einen neuen Cyanäther , în Ann. Pharm. , vol. 10, 1834, p. 249, DOI : 10.1002 / jlac.18340100302 .
- ( EN ) SF Rach și FE Kühn, Complexe metalice de tranziție ligate cu nitril cu contranioni slab coordonatori și aplicațiile lor catalitice , în Chem. Rev. , vol. 109, nr. 5, 2009, pp. 2061-2080, DOI : 10.1021 / cr800270h .
- (RO) P. Pollak și G. Romeder, nitrili, în Enciclopedia Ullmann de Chimie Industrială , Wiley-VCH, 2002, DOI : 10.1002 / 14356007.a17_363 .
- ( EN ) JP Schaefer și JJ Bloomfield, The Dieckmann Condensation (Inclusiv condensarea Thorpe-Ziegler) , în Organic Reactions , vol. 15, nr. 1, 2011, pp. 1-203, DOI : 10.1002 / 0471264180.or015.01 .
- ( LA ) CW Scheele, De materia tingente caerulei berolinensis , în Opuscula Chemica și Physica , II, Leipzig, JG Müller, 1789.
- ( EN ) AL Smith și P. Tan, Sinteza creatinei: un experiment de laborator de licență în chimie organică , în J. Chem. Educ. , vol. 83, nr. 11, 2006, p. 1654, DOI : 10.1021 / ed083p1654 .
- ( EN ) K. Soai și A. Ookawa, Solvenți mixți care conțin metanol ca mediu de reacție util pentru reduceri chemoselective unice în borohidrura de litiu , în J. Org. Chem. , vol. 51, nr. 21, 1986, pp. 4000-4005, DOI : 10.1021 / jo00371a017 .
- ( EN ) S. Stanković și JH Espenson, Conversia oxidativă catalizată de MTO a N, N-dimetilhidrazonelor în nitrili , în Chem. Comun. , 1998, pp. 1579-1580, DOI : 10.1039 / A802723D .
- ( EN ) CM Suter și EW Moffett, Reducerea cianurilor alifatice și oxime cu alcool de sodiu și n-butilic , în J. Am. Chem. Soc. , Vol. 56, nr. 2, 1934, p. 487, DOI : 10.1021 / ja01317a502 .
- ( DE ) F. Wöhler și J. Liebig, Untersuchungen über das Radical der Benzoesäure , în Ann. der Pharmacie , vol. 3, nr. 3, 1832, pp. 249-282.
- ( EN ) S. Yamazaki și Y. Yamazaki, deshidrogenarea catalizată de nichel a aminelor în nitrili , în Bull. Chem. Soc. Jpn. , vol. 63, nr. 1, 1990, pp. 301-303, DOI : 10.1246 / bcsj.63.301 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe nitrile
Wikimedia Commons conține imagini sau alte fișiere pe nitrile
linkuri externe
- ( EN ) Nitriles , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.



![{\ displaystyle {\ ce {-> [{\ text {methyltrioxorenium cat.}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/85c618ae4450d0bab930da30a6d2740bc9242b21)