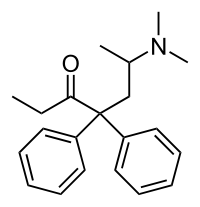
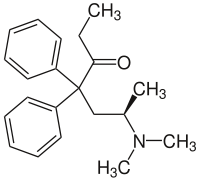
Metadonă
| Metadonă | |
|---|---|
| Numele IUPAC | |
| ( RS 6 dimetilamino-4,4 difenil-3 heptanonă ) | |
| Denumiri alternative | |
| (+/-) - Metadonă; (+/-) - clorhidrat de metadonă; dl-metadonă; Clorhidrat de DL-metadonă; Methadon; Metadonă HCL; Clorhidrat de metadonă; Clorhidrat de fenadonă | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 21 H 27 NR |
| Masa moleculară ( u ) | 309.445 g / mol |
| numar CAS | |
| Numărul EINECS | 200-996-9 |
| Codul ATC | N02 |
| PubChem | 4095 |
| DrugBank | DB00333 |
| ZÂMBETE | CCC(=O)C(CC(C)N(C)C)(C1=CC=CC=C1)C1=CC=CC=C1 |
| Proprietăți fizico-chimice | |
| Constanta de disociere a acidului (pKa) la 25 ° CK | 8,94 |
| Solubilitate în apă | în apă 48,5 mg / L (25 ° C) |
| Coeficientul de partiție 1-octanol / apă | 3,93 |
| Temperatură de topire | 235,0 ° C |
| Date farmacologice | |
| Grupa farmacoterapeutică | Narcotic; Analgezic; Agonist opioid; Antitusiv; |
| Mod de administrare | oral (NB: În Italia), intravenos, insuflație, sublingual, rectal. |
| Date farmacocinetice | |
| Biodisponibilitate | 40-90% (oral) |
| Legarea proteinelor | 85-90% la glicoproteina α1-acidă |
| Metabolism | hepatic |
| Jumătate de viață | 24 - 36 de ore |
| Excreţie | urinare și fecale |
| Informații de siguranță | |
Metadonă (cunoscută sub diferite nume, inclusiv: Polamidon, Eptadonă, Dolofină etc.) Este un opioid sintetic, utilizat în medicină ca analgezic în îngrijirea paliativă și utilizat pentru a reduce obișnuința în terapia de substituție a dependenței de droguri .
A fost sintetizat pentru prima dată în Germania în 1937; deși chimic diferit de morfină sau heroină , ca acestea acționează în primul rând asupra receptorului μ- opioid ( agonist pur) cu efecte clinice similare.
Metadonă este utilizată în mod util în controlul durerii cronice datorită duratei sale lungi de acțiune și a costului redus. De asemenea, a fost folosit de mulți ani în tratamentul dependenței de opiacee, deși este cunoscut riscul său potențial de dependență de droguri și toleranță . Sindromul de sevraj cu metadonă, deși similar calitativ cu cel al morfinei, are un debut mai lent, dar mai prelungit și cu simptome similare.
În 2005, Organizația Mondială a Sănătății (OMS) a inclus-o pe lista medicamentelor esențiale ; [1] aceasta, de asemenea, pentru eficacitatea bine documentată în terapia dependenței de droguri. [2]
fundal
În 1932 a fost descoperită petidina (numită petidină , Dolantin, Demerol, Dolosal. Etc.), [3] de O. Eisleb și O. Schaumann, [4] după decenii de cercetări privind compușii de origine vegetală asemănători petidinei , datorită, de asemenea, o doză de noroc și înțelepciune farmacologică. Noutatea descoperirii constă în faptul că pethidina a fost prima moleculă analgezică fără legătură chimică cu structura morfinei. [5]
Ulterior, Max Bockmühl și Gustav Ehrhart [6] [7] au lucrat la compuși cu o structură similară cu pethidina (Dolantin) în speranța de a găsi o substanță care să fie solubilă în apă și utilizabilă ca hipnotică și care să fie capabilă, de asemenea, să încetinească gastro-intestinalul. tranzit pentru a facilita intervenția chirurgicală. [8] [9] Cei doi angajați ai IG Farbenindustrie din Höchst -Am-Main, Germania, dezvoltă astfel metadonă, care a fost apoi brevetată la 11 septembrie 1941. [10]
Substanța a fost folosită și preferată petidinei, ca înlocuitor al morfinei, numai în timpul celui de-al doilea război mondial, când a devenit dificil să se găsească pethidină în Germania . Din cauza lipsei corelației chimice cu morfina și a diferitelor efecte secundare, aceasta nu a fost recunoscută ca analgezic; trebuia așteptată cercetarea post-al doilea război mondial pentru a înțelege potențialul terapeutic al acestei substanțe. [11] [12]
Numele se crede din greșeală că derivă din „adolfina” în cinstea lui Adolf Hitler , dar aceasta este doar o legendă urbană. Numele Dolophine, de fapt, derivă din unirea cuvintelor franceze Dolo r și fin , a fost întotdeauna o marcă înregistrată a Eli Lilly ; [13] este folosit și astăzi cu același nume.
După război, brevetul drogului a fost expropriat ca despăgubire pentru daune de război și documentele au fost exportate în Statele Unite . În 1947 , compania farmaceutică americană Eli Lilly, cu numele de Dolophine, a introdus-o pe piața SUA și mai târziu în alte țări din întreaga lume. În Germania, drogul a fost reintrodus în 1949 sub numele de Polamidon, de către Hoechst AG , moștenitorul IG Farben, acum fuzionat în Sanofi Aventis . [11]
Din 1960, metadona a fost utilizată în SUA ca substanță utilă în înțărcarea farmacologică definitivă a dependenței de opioide ( heroină ), pornind de la presupunerea științifică că dependența de opioide ar trebui tratată ca o boală metabolică obișnuită. [14] Aceste programe au fost ulterior reluate în diferite moduri din întreaga lume.
În Italia, din august 1980, a fost utilizat ca înlocuitor al heroinei împotriva simptomelor somatice datorate abstinenței în timpul înțărcării de heroină și opioide. [15] În mod semnificativ, în plus, de câteva decenii, în Italia, substanța farmacologică a găsit o utilizare utilă în terapia durerii oncologice sau cronice incoercibile [16] [17] ca alternativă la morfină , oxicodonă , [18] hidromorfonă și fentanil . [19] [20]
Caracteristici structurale și fizice
Sinteza compusului

Metadonă este produsă complet sintetic, spre deosebire de heroină, care se obține din substanțe semi-naturale produse sintetic din alcaloizii opiului, cum ar fi morfina. Din punct de vedere chimic și structural, acesta diferă semnificativ de morfină și heroină. Procesul de sinteză chimică a metadonei racemice este destul de simplu, se obține pornind de la nitril cu sinteza Kolbe și cu difenilacetonitrilul care este ușor disponibil. [21] Formarea unei L - (+) racem poate fi obținut cu acid tartric . [22]
Legate chimic de metadonă există următoarele molecule: [23] [24] [25] [26] [27] [28]
- Metadonă (4,4-difenil-6-dimetilaminoheptanonă-3,6-dimetilamino-4,4-difenil-3-heptanonă);
- Izometadonă (4,4-difenil-5-metil-dimetilaminohexa-niciun-3, 6-dimetilamino-5-metil-4,4-difenil-3-hexanonă);
- Alfa-metadol (a-4,4-difenil-6-dimetilaminoheptanol-3, a-6-dimetilamino-4,4-difenil-3-heptanol);
- Beta-metadol (β-4,4-difenil-6-dimetilamino-3-heptanol, β-6-dimetilamino-4,4-difenil-3-heptanol);
- Alfa-acetilmetadol (α-4,4-difenil-6-dimetilamino-3-acetoxiheptan, α-6-dimetilamino-4,4-difenil-3-acetoxiheptan);
- Beta-acetilmetadol (β-4,4-difenil-4-dimetilamino-3-acetoxiheptan, β 6-dimetilamino-4,4-difenil-3-acetoxiheptan);
- Fenadoxona (4,4-difenil-6-morfolinoheptanona-3, 6-morfolino-4,4-difenil-3-heptanona);
- 4,4-difenil-6-dimetilamino-3-exanonă;
- 4-Morfolino-2,2-difenil. butirat de etil (etil-2,2-difenil-4-morfolinobutirat);
- 4-dimetilamino-1,2-difenil-3-metil-2-propionoxibutan;
- 4,4-Difenil-6-piperidino-3-heptanonă (6-piperidino-4,4-difenileptan-3-onă).
Reactivitate și caracteristici chimice
Se prezintă sub formă de cristale incolore și inodor sau sub formă de pulbere cristalină albă. Solubil în apă, ușor solubil în alcool și în cloroform , practic insolubil în eter și în glicerol . PH-ul unei soluții de 1% în apă este între 4,5 și 6,5. Ar trebui depozitat în recipiente închise ermetic la o temperatură de 25 ° C, excursiile permise variind de la 15 grade la 30 ° C. Trebuie protejat de lumină. [29]
Metadonă este o substanță chirală , prin urmare, apare ca un amestec racemic de două molecule oglindă ( enantiomeri ) într-un raport reciproc de 1: 1, respectiv forma stângaci de metadonă (L) -metadonă și dextrorotară (D) - forma metadonă. (în sensul acelor de ceasornic). Forma dextrorotatoare posedă puternice proprietăți anti- tuse , dar este aproape în totalitate lipsită de proprietăți analgezice; rezultă că L-Polamidon (levometadonă) este de aproximativ două ori mai eficient decât un analgezic, la aceeași doză, decât forma racemică de metadonă. [30]
Enantiomerul pur are un punct de fierbere la 100 ° C; amestecul racemic ( eutectic ) se topește mai întâi cu un punct de topire de 77 ° C. Enantiomerii puri precum clorhidratul de metadonă au un punct de fierbere de 248 ° C; în timp ce în cazul amestecului de enantiomeri 1: 1, punctul de topire este de 237 ° C. [31]
Incompatibilitate chimică
S-a raportat că injecția cu clorhidrat de metadonă este incompatibilă fizic și / sau chimic cu soluții care conțin: aminofilină , clorură de amoniu , amobarbital de sodiu , clorotiazidă de sodiu , fenitoină de sodiu , heparină sodică , meticilină sodică , nitrofurantoină de sodiu , pentobarbital de sodiu , fenobarbital de sodiu , bicarbonat de sodiu și sodiu tiopental . [32]
Farmacocinetica
Clorhidratul de metadonă este ușor absorbit din tractul gastro-intestinal sau după o ' injecție subcutanată sau intramusculară. Este larg distribuit în țesuturi, se răspândește prin placentă și se distribuie în laptele matern . [33] [34] Rata de legare a proteinelor plasmatice este ridicată. Este metabolizat în ficat, în principal prin N-demetilare și ciclizare, iar metaboliții sunt excretați în bilă și urină. Metabolismul este catalizată în principal de către CYP3A4 , cu toate că alte citocromul P450 izoenzime poate juca , de asemenea , un rol. Are un timp de înjumătățire lung și este predispus la acumulare.
Farmacocinetica metadonei este deosebită prin faptul că are o lungă perioadă de înjumătățire prin eliminare, cu acumulare consecventă după dozele repetate, cu variații interindividuale largi, care pot fi în ordinea mărimii unui factor de 100 (de la 4 la 130 de ore). [35] [36] Acest lucru se datorează variabilității genetice diferite între indivizi în ceea ce privește producerea izoenzimelor CYP3A4 , CYP2B6 și CYP2D6 ; în plus, multe substanțe interferează cu acestea, modificând timpul de înjumătățire al medicamentului. [37]
În plus față de variațiile considerabile interindividuale, metadonă are diferențe în farmacocinetică, chiar și după doze unice, mai degrabă decât multiple. De fapt, timpul de înjumătățire plasmatică prin eliminare variază considerabil de la 15 la 60 de ore și poate fi mult mai lung decât cele 18 ore revendicate după o singură doză. Este necesară o ajustare fină a dozei pentru fiecare pacient în parte, cu administrări repetate.
Majoritatea studiilor farmacocinetice au fost făcute pe dependenți de droguri. Enantiomerul stângaci (L-metadonă) prezintă o afinitate de zece ori mai mare pentru receptorul μ , [38] cu o potență analgezică estimată de 8 până la 50 de ori mai mare decât D-metadonă. [30]
Cu toate acestea, ambii enantiomeri se leagă de receptorii NMDA . De asemenea, efectul terapeutic dorit al medicamentului: analgezia și supresia sindromului de sevraj , se găsesc aproape în totalitate cu izomerul R. [39]
Absorbţie
Calea principală de administrare a metadonei este orală, de fapt, se absoarbe rapid după administrarea orală și are o biodisponibilitate orală ridicată. După 30 de minute se găsește în plasmă; vârful de sânge este atins după aproximativ 4 ore cu o singură doză sub formă de tablete. Metadonă poate fi absorbită din mucoasa bucală. Concentrația maximă în SNC este obținută după 1-2 ore după administrarea intramusculară sau subcutanată; cu aceste administrări există o relație liniară între eficacitate și doza administrată. [40]
Distribuție
Metadonă suferă o distribuție considerabilă în țesuturi, iar legarea de proteine este de 60 - 90%, în special în cazul glicoproteinei α1-acide . [40]
Metabolism
Metadonă are doi metaboliți principali: [40] [41]
- 2-etilidin-1,5-dimetil-3,3-difenilpirolidină (EDDP),
- 2-etil-3,3-difenil-5-metilpirolidine,
ambii sunt inactivați în ficat.
Au fost descriși alți metaboliți, inclusiv metadol și normetadol. Este metabolizat de enzimele CYP3A4 , CYP2B6 și CYP2D6 , cu o mare variabilitate interindividuală. [42] N-desmetilat de CYP 3A4 este un metabolit inactiv al metadonei. [43]
Ficatul poate fi, de asemenea, un loc important de depozitare pentru metadonă, care nemodificat poate fi adesea reciclat în plasmă cu recirculare enterohepatică. Acest lucru face dificilă gestionarea dozei de medicament, deoarece acest rezervor natural poate modifica cinetica plasmatică a medicamentului administrat în mod repetat. [44]
Eliminare
Metaboliții sunt excretați în fecale și urină împreună cu metadonă nemetabolizată. Excreția urinară de metadonă este dependentă de pH, cu cât pH-ul este mai mic, cu atât eliminarea este mai mare. [40]
Farmacodinamica

1. Membrana celulară
2. Canal blocat de Mg2 + cu blocarea site-ului (3)
3. Site blocat de Mg2 +
4. Sit de legare pentru halucinogeni
5. Site de legare pentru Zn2 +
6. Loc de legare pentru agoniști (glutamat) și / sau antagoniști ai ligandului (APV)
7. Situl de glicozilare
8. Situl de legare a protonilor
9. Situl de legare a glicinei
10. Situl de legare a poliaminei
11 Spațiul extracelular
12. Spațiul intracelular
13. Subunitatea complexului
Metadonă acționează asupra complexului receptorului ionofor pentru NMDA , asupra căruia acționează glutamatul ; întrucât acesta este un mediator chimic cu acțiune de excitare, blocul competitiv al acestui receptor, operat de metadonă, determină acțiuni anti-excitare [45] (transmisia electrică este redusă).
Metadona are aproximativ o putere echianalgezică egală cu de 3-4 ori cea a morfinei , dar provoacă mai puțină euforie și are o acțiune farmacologică mai durabilă; este mult mai bine absorbit decât morfina și modul în care provoacă constipație și crește presiunea biliară. De asemenea, induce dependență fizică, cum ar fi morfina. [46]
Principala utilizare în algologia cu metadonă este la pacienții cu durere de cancer și / sau care nu răspund la morfină sau alte opiacee puternice. De asemenea, atunci când există efecte adverse pentru alte opioide, acesta este frecvent utilizat în rotație cu opioide. [47] Are mai multe avantaje farmacodinamice și farmacocinetice față de alte opioide, cum ar fi: biodisponibilitate orală și rectală ridicată, activitate analgezică multimodală cu analgezie de lungă durată, lipsă de metaboliți activi, excreție predominant fecală, cost scăzut și numai efect imunosupresor slab. Dimpotrivă, dezavantajele sunt legarea ridicată cu proteinele plasmatice și timpul de înjumătățire plasmatică lungă și variabilă, un metabolism extins cu citocromul P450 și numeroasele interacțiuni medicamentoase consecvente, dificultatea de a găsi doza echianalgezică cu ceilalți opioizi și în cele din urmă când administrat subcutanat apariția reacțiilor locale. [48] Posibila apariție a unei prelungiri a intervalului QT , un efect secundar care poate duce la aritmii potențial fatale, este atribuibilă numai enantiomerului dextrorotator al metadonei, în timp ce nu are loc numai cu utilizarea L-metadonă. [38]
Metadonă [49] este un opioid sintetic unic datorită caracteristicilor sale farmacologice. Cele mai importante diferențe cu alte opioide sunt, în primul rând, biodisponibilitatea orală foarte remarcabilă, care ajunge până la 90%, în plus, poate fi detectată în plasmă după 30 de minute de administrare orală, cu nivelurile plasmatice maxime după 4-6 ore. Acest lucru este în contrast cu medicamentele opioide care au o absorbție slabă și neregulată. În al doilea rând, este durata variabilă și prelungită de acțiune care poate fluctua între 12 și 150 de ore după o singură doză. Starea de echilibru poate fi atinsă după o zi sau o săptămână și acest lucru poate fi explicat prin modificări ale activității de legare a citocromului P450 3A (CYP3A) și a α1-lipoproteinelor. [50] Din aceste motive, metadona nu este adecvată ca tratament de primă linie în durerea acută. Mai mult, toxicitatea sa întârziată poate persista chiar și după suspendare, datorită acumulării sale în compartimentele extra vasculare.
Cu toate acestea, profilul său farmacocinetic particular permite administrarea o dată pe zi la subiecții abstinenți la opioide. [51]
Totuși, este foarte util în programele de rotație a opioidelor, deoarece pare să existe doar toleranță parțială cu ceilalți agoniști opioizi. [52] Aceasta permite salvarea subiectului care nu mai răspunde la un alt opioid. [53]
În plus față de receptorul μ , acționează și asupra receptorilor NMDA ( receptori ionotropi de glutamat ). [54] Această acțiune este bine documentată și s-a dovedit a fi de mare folos în durerea neuropatică, unde metadonă poate fi utilizată cu succes. [55] [56] De fapt, medicamentul este utilizat și în acest tip de durere, dar este utilizat în principal în durerea cronică a cancerului. [57] [58]
De asemenea, este utilizat recent în durerea acută în ciuda cineticii sale nefavorabile, exploatând în acest caz formulările injectabile, mai ales atunci când există o componentă a durerii neuropatice [59] sau există o toleranță față de alte opioide precum morfina [60] sau fentanilul. [61] Acest lucru în special în fața cazurilor dificile de durere intratabilă; folosind calea intravenoasă sau pompa elastomerică (PCA). [60] [61] [62] Cu toate acestea, aceasta este o abordare riscantă din cauza riscului ridicat de acumulare a medicamentelor în compartimentele extracelulare.
De asemenea, a fost utilizat epidural în durerea postoperatorie acută cu rezultate bune, cu perfuzii continue sau intermitente la intervale de „doar 8 ore”. [63] [64]
Pe scurt, metadonă este un puternic agonist opioid cu profil farmacocinetic care permite administrarea orală o dată sau de două ori pe zi. De asemenea, are activitate antagonică asupra receptorului NMDA, util pentru activitatea sa analgezică, în special în stările de durere neuropatică. Datorită toleranței încrucișate limitate cu alte opioide, poate fi foarte utilă în gestionarea stărilor de durere nociceptivă la pacienții care au devenit toleranți la alte opioide utilizate mai frecvent, cum ar fi morfina sau fentanilul (rotația opioidelor). [58]
Indicații
Indicații aprobate
Indicațiile aprobate (pe etichetă ) conform prospectului, din 01/04/2006, sunt: [65]
Sindroame dureroase severe la pacienții care nu mai răspund la tratamentul secvențial cu analgezice, antiinflamatoare nesteroidiene, opioide slabe.
Tratamentul de încetare a stupefiantelor. Tratamentul de detoxifiere și tratamentul de întreținere trebuie urmate sub supraveghere medicală. Dacă metadona este administrată pentru tratamentul dependenței de heroină timp de mai mult de trei săptămâni, procedura trece de la tratamentul sindromului de sevraj acut la terapia de întreținere.
Deși metadonă creează dependență, este utilizată ca terapie pentru sindroamele de sevraj cu heroină și ca terapie de întreținere din următoarele motive:
- Concentrația pe parcursul zilei este aproape constantă, doar o singură administrare pe zi.
- Administrarea orală nu are efectele euforice ale administrării intravenoase.
Utilizarea acestuia ca analgezic în sindroamele dureroase de natură oncologică și non-oncologică este susținută de o literatură considerabilă și, printre aceste lucrări, există și studii despre sindroamele severe de durere de spate sau Durerea lombară (LBP). [66]
Indicații neaprobate
Metadonă este utilizată în două indicații care nu sunt aprobate ( off-label ) de către autoritățile de reglementare; primul ca antituse și al doilea, încă experimental, ca anti- leucemic .
Antitusiv
Metadonă sub formă de sirop la o concentrație egală cu aproximativ o treime din concentrația de metadonă lichidă utilizată pentru dependența de opiacee, este utilizată în țările în care este disponibilă, ca sirop pentru tuse violentă se potrivește pacienților cu cancer. [67] Studiile au arătat că antitusivele narcotice sunt utile în tusea neproductivă; [68] conform altor studii, acest lucru este discutabil sau nu prezintă niciun beneficiu. [69]
Alte opiacee antitusive
Alte opiacee naturale și semisintetice cu efecte antitusive sunt:
- codeina ,
- etilmorfină ,
- dihidrocodeina ,
- benzilmorfină ,
- laudanum ,
- dihidroizocodeină ,
- nicocodeină ,
- nicodicodeină ,
- hidrocodonă ,
- hidromorfonă ,
- acetildihidrocodeina ,
- tebacon ,
- diamorfină ( heroină ),
- acetilmorfon ,
- noscapină ,
- folcodina e
- alții.
Printre antitussigens sintetice sunt: dimemothorphan și dextrometorfanul și nelmorfinani grupului, tipepidine derivată din thiambutene și alte medicamente derivate de metadonă, cum ar fi levometadonă , normetadonă și noscapină.napsilat de levopropoxifen .
Tratamentul leucemiei
Cercetătorii germani au descoperit că metadonă este, de asemenea, în mod surprinzător, un antileucemic pentru formele rezistente de leucemie . De fapt, un studiu, publicat la 1 august 2008 într-un număr al Cancer Research , un jurnal al Asociației Americane de Cercetare a Cancerului , sugerează că metadonă este o nouă terapie promițătoare pentru leucemie, în special la pacienții care nu răspund la chimioterapie și radioterapie . [70] Alte două studii ulterioare sugerează activitate citotoxică cu metadonă potențial utilă în această și alte indicații. [71] [72]
Toxicologie
Edemul pulmonar întârziat poate apărea în urma administrării de metadonă într-o venă, acționează prin mecanisme centrale care modifică permeabilitatea capilară pulmonară. [73]
Există mai mulți agenți toxici care pot induce indirect o activare metabolică care implică celulele tecului și granuloasei ovariene, inclusiv heroină și metadonă, care au un efect activator asupra axei hipotalamus-hipofiză . [74] Mai mult, metadonă este suspectată de inducerea toxicității timpurii a dezvoltării prin transmiterea părinților prin placentă . [75]
Sindromul de abstinență neonatală apare între 30 și 90% dintre sugarii expuși in utero la heroină sau metadonă. Simptomele sevrajului neonatal sunt mai frecvente dacă doza zilnică de metadonă a mamei depășește 20 mg. Majoritatea nou-născuților vor avea simptome brute de sevraj și devin simptomatice la 48 de ore după naștere, dar simptomele de sevraj sunt raportate și la nou-născuții care încep la 7-14 zile după naștere . În aceste cazuri, alăptarea este protectoare împotriva sindromului de sevraj al sugarului. [76]
Multe studii sugerează că femeile care urmează tratament de întreținere cu metadonă în timpul sarcinii vor avea creștere în greutate fetală și gestație mai lungă. În timp ce prezintă nou-născuților o greutate la naștere și o circumferință inferioară a capului. Deși nu există o creștere a defectelor congenitale la descendenții femeilor care consumă metadonă în timpul sarcinii. [76]
Contraindicații
Metadonă este împovărată cu numeroase și importante contraindicații care sfătuiesc utilizarea acesteia la mai multe tipuri diferite de pacienți. [65]
- Atac astmatic acut.
- Boală pulmonară obstructivă cronică .
- Boală cardiacă organică.
- Inima pulmonară .
- Diabet necompensat .
- Ficatul și nefropatia .
- Insuficiență respiratorie.
- Hipersensibilitate la compus și la excipienții acestuia.
- Hipertensiune intracraniană.
- Hipotensiune .
- Hipovolemie .
- Porfiria .
- Constipație severă.
- Traumatism cranioencefalic.
Metadona nu este recomandată la copii, din cauza documentației rare existente. [65]
Efecte secundare
Cele mai grave efecte secundare [77] sunt: depresie respiratorie și într-o măsură mai mică depresie circulatorie, stop respirator, șoc și stop cardiac. Rareori cazuri de prelungire a intervalului QT și cazuri de torsada vârfurilor .
Cele mai frecvente efecte secundare sunt: un sentiment de vid în cap, amețeli , sedare , greață , vărsături , transpirație și hipotensiune ortostatică .
Alte reacții adverse sunt:
- Pe sistemul nervos central: euforie , disforie , slăbiciune, cefalee , insomnie , agitație, dezorientare și tulburări vizuale.
- Pe sistemul gastro-intestinal: gură uscată, anorexie , constipație și spasm al tractului biliar. Sistemul cardiovascular: înroșirea feței, bradicardie , palpitații , leșin și sincopă .
- Pe sistemul genito-urinar: retenție urinară sau dificultate la urinare , efect antidiuretic și libidou redus și / sau impotență sexuală.
- Manifestări alergice: mâncărime , urticarie , alte reacții cutanate, edem și rareori urticarie vasculitică.
Glicerolul prezent în compoziție poate provoca: cefalee, tulburări de stomac și diaree . Benzoatul de sodiu poate provoca: iritarea membranelor mucoase. De asemenea, poate crește riscul de icter la nou-născut. [65]
Doze terapeutice
Analgezie

Doza de clorhidrat de metadonă utilizată în tratamentul durerii oncologice sau cronice implacabile variază de la 2,5 la 10 mg administrată cu intervale de 3-8 ore în funcție de intensitatea durerii. În mod obișnuit și inițial, doza este de 5 până la 10 mg la fiecare 6 până la 8 ore, cu doza de medicament ajustată în funcție de răspuns. [65]
Pentru a evita riscul de acumulare și supradozaj, se recomandă ca în cazul utilizării prelungite a metadonului să nu se administreze mai mult de două ori pe zi. Poate fi administrat oral sau prin injecție subcutanată sau intramusculară. Când este necesară calea parenterală, calea intramusculară este preferată căii subcutanate la pacienții cu disfagie . [65]
Rotația opioidelor
La pacienții cu durere cronică prezentă mult timp este uneori necesară efectuarea așa-numitei rotații opioide . [78]
Si intende con essa il passaggio da un oppioide ad un altro, di solito, ad intervalli di circa un paio di settimane e, più comunemente, diversi mesi. La rotazione degli oppioidi è utile, perché il passaggio ad un altro oppioide permette di mantenere basse le dosi, e con ciò meno effetti collaterali, per ottenere l'effetto desiderato. [79]
Quando con il nuovo oppioide, usato in sostituzione del primo, sono necessarie dosi più elevate può crescere la tolleranza e la tossicità in relazione all'aumentare gli effetti analgesici . Allora è il momento ruotare di nuovo verso un altro oppioide. Tale rotazione degli oppioidi è una pratica standard per la gestione di pazienti con problemi di sviluppo di tolleranza. Di solito, quando si fa la rotazione degli oppioidi, non si può scendere ad una dose corrispondente a quella iniziale, perché c'è una tolleranza crociata, che occorre superare con dosi più alte del nuovo oppioide.
Tuttavia, il metadone ha una più bassa tolleranza crociata, quando si passa ad esso da altri oppioidi, rispetto agli altri oppiacei. [80] Questo permette che il metadone può essere iniziato con una dose bassa, e il tempo per il passaggio ad un successivo oppioide è più lungo. [79] [81]
Inoltre, secondo quanto riportato da molti pazienti con dolore, il metadone offre meno sedazione a dosaggio equivalente con altri oppioidi, rendendolo per questo motivo preferibile ad essi. L'uso del metadone è vantaggioso per questo motivo essendo la sedazione una seria complicanza della terapia con oppioidi nel dolore da cancro e nel dolore cronico incoercibile. [82]
Rotazione morfina vs metadone
Per il calcolo delle dosi equivalenti si fa riferimento a tabelle simili a quella riportata. La rotazione di ogni oppioide che va sostituito con il metadone va effettuata in due tappe, prima l'oppioide da sostituire deve essere equiparato al dosaggio equivalente di morfina OS; quindi il dosaggio equivalente di morfina ottenuto va equiparato al rispettivo dosaggio equivalente di metadone secondo le opportune tavole di conversione (vedi dopo). [53][83] [84]
Per esempio: Fentanil TDS → Morfina OS → Metadone OS
Equivalenza per la conversione immediata di morfina in rotazione con il metadone[85]
| Dose di morfina | Ratio di conversione a metadone |
|---|---|
| <100 mg/24 h | 1: 3 1 mg metadone ogni 3 mg di morfina |
| 101– 300 mg/24 h | 1: 5 |
| 301– 600 mg/24 h | 1: 10 |
| 601– 800 mg/24 h | 1: 12 |
| 801 - 1-1,000 mg/24 h | 1: 15 |
| > 1.000 mg/24 h | 1: 20 |
Dipendenza da oppioidi
Il metadone cloridrato è usato come parte del trattamento della dipendenza da oppiacei, anche se con l'uso prolungato di metadone si può determinare dipendenza. Nel trattamento dell'astinenza da oppioidi, o nella detossificazione da questi, il metadone è somministrato inizialmente in dosi sufficienti a sopprimere i sintomi di astinenza. Scopo di queste terapie è quello di garantire un'accettabile vita sociale e lavorativa dei tossicodipendenti evitando anche così fenomeni criminali legati alla ricerca della dose quotidiana di stupefacente. [86]
Una miscela contenente 1 mg/ml di metadone cloridrato viene comunemente utilizzata per le persone dipendenti da oppiacei. Una dose giornaliera da 10 a 20 mg di metadone cloridrato per via orale può essere somministrata inizialmente e, se necessario, aumentata da 10 a 20 mg al giorno fino a quando non si manifestano segni di crisi di astinenza o di intossicazione. Dopo la stabilizzazione, che spesso è raggiunta con una dose giornaliera di 40 a 60 mg, la dose di metadone va gradualmente diminuita fino al raggiungimento della sospensione totale. [87]
Dosi simili possono anche essere somministrato per iniezione sottocutanea o intramuscolare. Alcuni schemi di trattamento per la dipendenza da oppiacei possono anche prevedere una terapia di mantenimento con metadone molto prolungata nel tempo, questa viene regolata sulle esigenze personali dell'individuo con una dose giornaliera. Sono stati riportati casi di soggetti trattati con 120 mg o più al giorno. [87]
In Italia una serie di regolamenti di polizia sanitaria e norme giuridiche regolamentano la distribuzione ed assunzione della terapia sostitutiva nelle tossicodipendenze con il metadone; la somministrazione del metadone avviene in strutture chiamate SERT .[88]
Sovradosaggio
Gli effetti tossici del sovradosaggio da metadone possono essere trattati con naloxone . [89] Nonostante la maggior durata d'azione nel tempo del metadone, il naloxone è preferito, con la necessità di dosi ripetute di naloxone nella terapia del trattamento dell' overdose . Il naltrexone ha una emivita più lunga ma è più difficile da titolare. Se una dose eccessiva di antagonista degli oppioidi viene somministrata ad un paziente dipendente, il risultato sarà una crisi d'astinenza anche grave. Quando, invece, si usa il naloxone, esso viene prontamente eliminato e la eventuale crisi d'astinenza dura poco; al contrario le dosi di naltrexone richiedono più tempo per essere eliminato dal paziente. [89]
Il problema dell'overdose da metadone consiste nell'azione fugace del naloxone che una volta terminata costringe a pronte somministrazioni di ulteriori dosi per evitare gli effetti di sovradosaggio subentranti, che sono in funzione dei dosaggi di metadone ingerito. [90] [91]
Gravidanza e allattamento
L'uso in gravidanza nelle donne che intendono sospendere l'assunzione di eroina, è possibile, purché ciò sia fatto sotto stretto controllo medico. Il farmaco può essere usato fino alla fine della gravidanza con dosaggi stabili. L'eventuale sospensione del trattamento va effettuato sotto stretto controllo di medici specialisti e non andrebbe mai fatto prima della XIV settimana di gestazione e non dopo la XXXII, per evitare il rischio di aborto e di parto pretermine , rispettivamente. [65] Il farmaco non può essere usato durante il travaglio di parto. [40]
Avvertenze
Il medicinale contiene saccarosio : 1 ml di sciroppo contiene 0.4 g di zucchero. Questo va tenuto presente nei soggetti diabetici compensati. La massima dose giornaliera comporta l'assunzione di 48 g di zucchero; è quindi sconsigliato per i pazienti che soffrono di intolleranza ereditaria al fruttosio , di disturbi nell'assorbimento degli zuccheri: glucosio e galattosio , o di mancanza degli enzimi : sucrasi e isomaltasi , necessari alla digestione degli zuccheri. [65]
Interazioni
I farmaci che acidificano le urine o le alcalinizzano possono avere un effetto importante sulla farmacocinetica del metadone in quanto l'eliminazione corporea ( clearance ) a pH acido è maggiore; mentre questa diminuisce a pH urinario alcalino. [92]
Molti farmaci andrebbero assunti sotto stretta sorveglianza se si consuma succo di pompelmo, tra questi vi è anche il metadone. [93]
Antibatterici
I sintomi da astinenza sono stati segnalati in pazienti sottoposti a metadone, quando hanno usato la rifampicina che è un potente induttore enzimatico . [94] [95] [96] Invece, con l'uso contemporaneo di ciprofloxacina , che inibisce i citocromi: CYP1A2 e CYP3A4 , si hanno segni di tossicità da metadone; [97] con casi di torsione di punta. [98]
Antidepressivi
Gli SSRI come fluoxetina [99] [100] e fluvoxamina [99] [100] e non solo, [101] possono potenziare gli effetti di alcuni analgesici oppioidi; tali interazioni possono determinare la tossicità da metadone quando usati in contemporanea. [102] [103] [104]
Antiepilettici
Sono stati riportati casi di sindrome da astinenza conseguenti all'uso contemporaneo di metadone e antiepilettici [105] quali la carbamazepina , il fenobarbital [106] e la fenitoina . [107] [108]
Antimicotici
L'uso del metadone con il fluconazolo è causa dell'aumento delle concentrazioni sieriche di metadone, anche se non sembra necessario fare un aggiustamento della posologia. [109]
Antivirali
Il metadone aumenta forse le concentrazioni plasmatiche di zidovudina . [110] Vi è una limitata evidence che nelfinavir o ritonavir può ridurre le concentrazioni plasmatiche di metadone. [111] Indinavir [112] e saquinavir [113] non hanno avuto alcun effetto sulle concentrazioni plasmatiche di metadone. Lopinavir - ritonavir insieme possono ridurre le concentrazioni di metadone e determinare torsione di punta . [114]
Nevirapina è stata segnalata come capace di ridurre le concentrazioni plasmatiche di metadone con sintomi di astinenza manifesti quando viene somministrata a pazienti insieme al metadone. [115] Un'interazione simile può esserci quando l' efavirenz è viene assunto insieme al metadone. [116]
Altre interazioni
Altre interazioni degne di nota sono documentate tra il metadone ei seguenti farmaci:
Atracurio , [117] Baclofen , [118] Buprenorfina , [119] [117] Desflurano , [120] Duloxetina , [121] Etomidate , [120] [122] Isoflurano , [120] [123] Ketamina , [124] [125] Linezolid , [126] Mepiramina , [127] Metoclopramide , [128] Procainamide , [129] Propofol , [124] Rocuronio , [130] Trifluoperazina , [131] Amiodarone , [132] [133] Astemizolo , [134] Desipramina , [135] Droperidolo , [136] Gatifloxacina [137] e Rifabutina . [137] [138]
Note
- ^ Methadone WHO Model Lists of Essential Medicines Archiviato il 27 febbraio 2011 in Internet Archive .
- ^ RP Mattick, C Breen, J Kimber, Marina Davoli: "Methadone maintenance therapy versus no opioid replacement therapy for opioid dependence" Cochrane Drugs and Alcohol Group, 2009
- ^ ( EN ) UNODC - Bulletin on Narcotics - 1956 Issue 1 - 002 , su unodc.org .
- ^ O. Eisleb and O . Schaumann , Dtsch. Med. Wschr. 65, 867 (1939).
- ^ ( EN ) UNODC - Bulletin on Narcotics - 1951 Issue 2 - 005 , su unodc.org .
- ^ Max Bockmühl e Ehrhart, Eichler A. O e Farah (1957) Experimentellen Handbuch Der Pharmakologie. Springer-Verlag, Berlin.
- ^ ( EN ) disinformation | m is for methadone , su old.disinfo.com (archiviato dall' url originale l'11 gennaio 2012) .
- ^ Bäumler E (1968) A Century of Chemistry. Econ Verlag, Düsseldorf.
- ^ Erhahart G e Ruschig H. (1972) Arzneimittel Entwicklung Darstellung Wirkung, Band 1, Therapeutica mit Wirkung auf das Nervensystem Z
- ^ ( DE ) Methadone patent application , su drugtext.org (archiviato dall' url originale il 9 gennaio 2012) .
- ^ a b ( EN ) web.archive.org , su exchangesupplies.org (archiviato dall' url originale il 20 novembre 2003) .
- ^ Glen R. Hanson, Peter J. Venturelli e Annette E. Fleckenstein, Drugs and society , Jones & Bartlett Learning, pp. 269–, ISBN 978-0-7637-3732-0 .
- ^ Methadone Briefing , su exchangesupplies.org . URL consultato il 9 luglio 2007 (archiviato dall' url originale il 20 novembre 2003) .
- ^ Nicholas Seivewright, assisted by Mark Parry: "Community Treatment of Drug Misuse: More Than Methadone"; Cambridge University Press, 2009
- ^ Nicola Garzotto, Psichiatria pratica , PICCIN, 1985, pp. 197–, ISBN 978-88-299-0184-5 .
- ^ S. Mercadante, Opioid rotation for cancer pain: rationale and clinical aspects. , in Cancer , vol. 86, n. 9, novembre 1999, pp. 1856-66, PMID 10547561 .
- ^ Mercadante S, Ferrera P, Villari P, Adile C, Casuccio A., Switching from oxycodone to methadone in advanced cancer patients , in Supportive Care in Cancer , vol. 20, n. 1, luglio 2011, pp. 191-194, PMID 21901297 .
- ^ MA. Benítez-Rosario, A. Salinas-Martín; A. Aguirre-Jaime; L. Pérez-Méndez; M. Feria, Morphine-methadone opioid rotation in cancer patients: analysis of dose ratio predicting factors. , in J Pain Symptom Manage , vol. 37, n. 6, giugno 2009, pp. 1061-8, DOI : 10.1016/j.jpainsymman.2008.05.016 , PMID 19171458 .
- ^ Gensini GF., New disposition for pain therapy in Italy, center for headache should be integrated in the network , in Neurological Sciences , vol. 32, maggio 2011, p. 67-70, PMID 21533716 .
- ^ PW. Walker, S. Palla; BL. Pei; G. Kaur; K. Zhang; J. Hanohano; M. Munsell; E. Bruera, Switching from methadone to a different opioid: what is the equianalgesic dose ratio? , in J Palliat Med , vol. 11, n. 8, ottobre 2008, pp. 1103-8, DOI : 10.1089/jpm.2007.0285 , PMID 18980450 .
- ^ E. Breitmaier: Alkaloide , Teubner-Verlag, 1997, S. 158.
- ^ Merck & Co., US 2 644 010, 1953.
- ^ World Health Organization (1949), Official Records of the World Health Organization, No. 19, p. 32.
- ^ World Health Organization, Techn. Rep. Ser. 1950, No. 21.
- ^ World Health Organization, Techn. Rep. Ser. 1952, No. 57.
- ^ World Health Organization, Techn. Rep. Ser. 1954, No. 76.
- ^ World Health Organization, Techn. Rep. Ser. 1955, No. 95.
- ^ World Health Organization, Techn. Rep. Ser. 1956, No. 102.
- ^ Q. Alan Xu e Timothy L. Madden, Analytical Methods for Therapeutic Drug Monitoring and Toxicology , John Wiley and Sons, 15 febbraio 2011, pp. 309–, ISBN 978-0-470-45561-6 .
- ^ a b Ebadi, Manuchair S., Desk Reference of Clinical Pharmacology, Second Edition , Boca Raton, CRC, 2007, p. 420, ISBN 1-4200-4743-4 .
- ^ Kuhnert-Brandstätter, M.; Friedl, L.: Beitrag zur thermischen Analyse und zur Polymorphie optischer Antipoden: Pantolacton, Methadon und Usninsäure, Mikrochim. Acta 1979 II, S. 97–110.
- ^ ( EN ) pubchem.ncbi.nlm.nih.gov .
- ^ de Castro A, Jones HE, Johnson RE, Gray TR, Shakleya DM, Huestis MA, Maternal methadone dose, placental methadone concentrations, and neonatal outcomes , in Clinical Chemistry 2011 , vol. 57, gennaio 2011, pp. 449-458, PMID 21245372 .
- ^ Glatstein MM, Garcia-Bournissen F, Finkelstein Y, Koren G, Methadone exposure during lactation , in College of Family Physicians of Canada , dicembre 2008, PMID 19074706 .
- ^ Kell MJ, Utilization of plasma and urine methadone concentrations to optimize treatment in maintenance clinics: I. Measurement techniques for a clinical setting , in Journal of addictive diseases: the official journal of the ASAM, American Society of Addiction Medicine , vol. 13, n. 1, 1994, pp. 5–26, PMID 8018740 .
- ^ Eap CB, Buclin T, Baumann P, Interindividual variability of the clinical pharmacokinetics of methadone: implications for the treatment of opioid dependence , in Clinical pharmacokinetics , vol. 41, n. 14, 2002, pp. 1153–93, PMID 12405865 .
- ^ John Manfredonia,Prescribing Methadone for Pain Management in End-of-Life Care , su jaoa.org , JAOA The Journal of the American Osteopathic Association, 18 marzo 2005.
- ^ a b Alessandro Zotto, Guido Mannaioni, Farmacologia e tossicologia del L-metadone , in Italian Journal of the Addictions , vol. 7, n. 26, giugno 2017, pp. 7-9.
- ^ Lynn RK, Olsen GD, Leger RM, Gordon WP, Smith RG, Gerber N, The secretion of methadone and its major metabolite in the gastric juice of humans: comparison with blood and salivary concentrations , in Drug Metab. Dispos. , vol. 4, n. 5, 1976, pp. 504–9, PPMID 10151.
- ^ a b c d e Laurence L. Brunton, Louis Sanford Goodman, Donald Blumenthal, Iain Buxton, Goodman and Gilman's manual of pharmacology and therapeutics , McGraw-Hill Professional, 28 settembre 2007, pp. 361–, ISBN 978-0-07-144343-2 .
- ^ Larson ME, Richards TM,Quantification of a methadone metabolite (EDDP) in urine: assessment of compliance , in Clin Med Res , vol. 7, n. 4, dicembre 2009, pp. 134–41, DOI : 10.3121/cmr.2009.859 , PMC 2801695 , PMID 19920164 .
- ^ Shiran MR, Lennard MS, Iqbal MZ, et al. ,Contribution of the activities of CYP3A, CYP2D6, CYP1A2 and other potential covariates to the disposition of methadone in patients undergoing methadone maintenance treatment , in Br J Clin Pharmacol , vol. 67, n. 1, gennaio 2009, pp. 29–37, DOI : 10.1111/j.1365-2125.2008.03312.x , PMC 2668081 , PMID 19133059 .
- ^ Armstrong SC, Cozza KL, Med-psych drug-drug interactions update , in Psychosomatics , vol. 43, n. 2, 2002, pp. 169–70, PMID 11998586 .
- ^ ( LT ) Reingardiene D, Jodziūniene L, Lazauskas R, [Methadone treatment and its dangers] , in Medicina (Kaunas) , vol. 45, n. 5, 2009, pp. 419–25, PMID 19535889 .
- ^ Matsui A, Williams JT, Activation of μ-opioid receptors and block of KIR 3 potassium channels and NMDA receptor conductance by l- and d-methadone in rat locus coeruleus , in Br. J. Pharmacol. , vol. 161, n. 6, novembre 2010, pp. 1403–13, DOI : 10.1111/j.1476-5381.2010.00967.x , PMID 20659105 .
- ^ Richard Finkel, Michelle Alexia Clark, Pamela C. Champe, Luigi X. Cubeddu, Pharmacology , Lippincott Williams & Wilkins, 1º luglio 2008, pp. 165–, ISBN 978-0-7817-7155-9 .
- ^ Pollock AB, Tegeler ML, Morgan V, Baumrucker SJ, Morphine to Methadone Conversion: An Interpretation of Published Data , in Am J Hosp Palliat Care , giugno 2010, DOI : 10.1177/1049909110373508 , PMID 20555039 .
- ^ Leppert W, The role of methadone in cancer pain treatment--a review , in Int. J. Clin. Pract. , vol. 63, n. 7, luglio 2009, pp. 1095–109, DOI : 10.1111/j.1742-1241.2008.01990.x , PMID 19570126 .
- ^ ( EN ) Schmidt, Robert F., Encyclopedia of Pain , Berlin, Springer, 2006, ISBN 3-540-33447-5 .
- ^ Romach MK, Piafsky KM, Abel JG, Khouw V, Sellers EM, Methadone binding to orosomucoid (alpha 1-acid glycoprotein): determinant of free fraction in plasma , in Clin. Pharmacol. Ther. , vol. 29, n. 2, febbraio 1981, pp. 211–7, PMID 7193106 .
- ^ Vetulani J, Drug addiction. Part III. Pharmacotherapy of addiction , in Pol J Pharmacol , vol. 53, n. 5, 2001, pp. 415–34, PMID 11990060 .
- ^ Davis AM, Inturrisi CE, d-Methadone blocks morphine tolerance and N-methyl-D-aspartate-induced hyperalgesia , in J. Pharmacol. Exp. Ther. , vol. 289, n. 2, maggio 1999, pp. 1048–53, PMID 10215686 .
- ^ a b Benítez-Rosario MA, Feria M, Salinas-Martín A, Martínez-Castillo LP, Martín-Ortega JJ, Opioid switching from transdermal fentanyl to oral methadone in patients with cancer pain , in Cancer , vol. 101, n. 12, dicembre 2004, pp. 2866–73, DOI : 10.1002/cncr.20712 , PMID 15529307 .
- ^ Inturrisi CE, Pharmacology of methadone and its isomers , in Minerva Anestesiol , vol. 71, n. 7-8, 2005, pp. 435–7, PMID 16012416 .
- ^ Shah S, Diwan S, Methadone: does stigma play a role as a barrier to treatment of chronic pain? , in Pain Physician , vol. 13, n. 3, 2010, pp. 289–93, PMID 20495594 .
- ^ Yennurajalingam S, Peuckmann V, Bruera E, Recent developments in cancer pain assessment and management , in Support Cancer Ther , vol. 1, n. 2, gennaio 2004, pp. 97–110, DOI : 10.3816/SCT.2004.n.003 , PMID 18628186 .
- ^ Shaiova L, The role of methadone in the treatment of moderate to severe cancer pain , in Support Cancer Ther , vol. 2, n. 3, aprile 2005, pp. 176–80, DOI : 10.3816/SCT.2005.n.010 , PMID 18628169 .
- ^ a b Moulin DE, Clark AJ, Gilron I, et al. ,Pharmacological management of chronic neuropathic pain - consensus statement and guidelines from the Canadian Pain Society , in Pain Res Manag , vol. 12, n. 1, 2007, pp. 13–21, PMC 2670721 , PMID 17372630 .
- ^ Watson CP, Methadone for neuropathic pain: a new use for an old drug? , in Can J Neurol Sci , vol. 32, n. 3, agosto 2005, pp. 271–2, PMID 16225164 .
- ^ a b Fitzgibbon DR, Ready LB, Intravenous high-dose methadone administered by patient controlled analgesia and continuous infusion for the treatment of cancer pain refractory to high-dose morphine , in Pain , vol. 73, n. 2, novembre 1997, pp. 259–61, PMID 9415514 .
- ^ a b Santiago-Palma J, Khojainova N, Kornick C, et al. , Intravenous methadone in the management of chronic cancer pain: safe and effective starting doses when substituting methadone for fentanyl , in Cancer , vol. 92, n. 7, ottobre 2001, pp. 1919–25, PMID 11745266 .
- ^ Sabatowski R, Kasper SM, Radbruch L, Patient-controlled analgesia with intravenous L-methadone in a child with cancer pain refractory to high-dose morphine , in J Pain Symptom Manage , vol. 23, n. 1, gennaio 2002, pp. 3–5, PMID 11779660 .
- ^ Prieto-Alvarez P, Tello-Galindo I, Cuenca-Peña J, Rull-Bartomeu M, Gomar-Sancho C, Continuous epidural infusion of racemic methadone results in effective postoperative analgesia and low plasma concentrations , in Can J Anaesth , vol. 49, n. 1, gennaio 2002, pp. 25–31, DOI : 10.1007/BF03020415 , PMID 11782325 .
- ^ ( ES ) Prieto-Alvarez MP, Fuentes-Bellido JG, López-Cebollada J, Lorenzo-Foz JP, [Comparative study of postoperative analgesia with methadone and fentanyl in continuous peridural perfusion] , in Rev Esp Anestesiol Reanim , vol. 44, n. 8, ottobre 1997, pp. 305–9, PMID 9424683 .
- ^ a b c d e f g h Metadone Cl Molteni 1Mg , su torrinomedica.it (archiviato dall' url originale il 23 luglio 2011) .
- ^ Reid MC, Engles-Horton LL, Weber MB, Kerns RD, Rogers EL, O'Connor PG,Use of opioid medications for chronic noncancer pain syndromes in primary care , in J Gen Intern Med , vol. 17, n. 3, marzo 2002, pp. 173–9, PMC 1495018 , PMID 11929502 .
- ^ Molassiotis A, Smith JA, Bennett MI, et al. ,Clinical expert guidelines for the management of cough in lung cancer: report of a UK task group on cough , in Cough , vol. 6, 2010, p. 9, DOI : 10.1186/1745-9974-6-9 , PMC 2978117 , PMID 20925935 .
- ^ Bolser DC,Pharmacologic management of cough , in Otolaryngol. Clin. North Am. , vol. 43, n. 1, febbraio 2010, pp. 147–55, xi, DOI : 10.1016/j.otc.2009.11.008 , PMC 2827356 , PMID 20172264 .
- ^ Dicpinigaitis PV, Currently available antitussives , in Pulm Pharmacol Ther , vol. 22, n. 2, aprile 2009, pp. 148–51, DOI : 10.1016/j.pupt.2008.08.002 , PMID 18771744 .
- ^ Claudia Friesen, Mareike Roscher, Andreas Alt and Erich Miltner, Methadone, Commonly Used as Maintenance Medication for Outpatient Treatment of Opioid Dependence, Kills Leukemia Cells and Overcomes Chemoresistance , in Cancer Research , vol. 68, n. 15, 2008, pp. 6059–6064, DOI : 10.1158/0008-5472.CAN-08-1227 , PMID 18676827 .
- ^ Perez-Alvarez S, Cuenca-Lopez MD, de Mera RM, et al. , Methadone induces necrotic-like cell death in SH-SY5Y cells by an impairment of mitochondrial ATP synthesis , in Biochim. Biophys. Acta , vol. 1802, n. 11, novembre 2010, pp. 1036–47, DOI : 10.1016/j.bbadis.2010.07.024 , PMID 20691259 .
- ^ Perez-Alvarez S, Iglesias-Guimarais V, Solesio ME, et al. , Methadone induces CAD degradation and AIF-mediated necrotic-like cell death in neuroblastoma cells , in Pharmacol. Res. , vol. 63, n. 4, aprile 2011, pp. 352–60, DOI : 10.1016/j.phrs.2010.12.001 , PMID 21145398 .
- ^ Rousseaux, Colin George; Haschek, Wanda M.; Wallig, Matthew A., Fundamentals of toxicologic pathology , Amsterdam, Elsevier/Academic Press, 2010, pp. 121, 357,, ISBN 0-12-370469-3 .
- ^ Rousseaux, Colin George; Haschek, Wanda M.; Wallig, Matthew A., Fundamentals of toxicologic pathology , Amsterdam, Elsevier/Academic Press, 2010, p. 609, ISBN 0-12-370469-3 .
- ^ Rousseaux, Colin George; Haschek, Wanda M.; Wallig, Matthew A., Fundamentals of toxicologic pathology , Amsterdam, Elsevier/Academic Press, 2010, p. 642, ISBN 0-12-370469-3 .
- ^ a b Peter Staats; Wallace, Mark, Pain medicine and management: just the facts , New York, McGraw-Hill, Medical Pub. Division, 2005, p. 228, ISBN 0-07-141182-8 .
- ^ Methadone , su nlm.nih.gov , MedlinePlus (archiviato dall' url originale il 27 febbraio 2008) .
- ^ Opioid rotation for toxicity reduction in terminal cancer patients , su Journal of Pain and Symptom Management , Volume 10, Issue 5, July 1995, Pages 378-384.
- ^ a b S. Mercadante, La gestione del dolore postoperatorio. Linee guida di trattamento. Con CD-ROM , Elsevier srl, 2007, pp. 67–, ISBN 978-88-214-2992-7 .
- ^ Individualized use of methadone and opioid rotation in the comprehensive management of cancer pain associated with poor prognostic indicators , su pain , Elsevier, Amsterdam, PAYS-BAS, 1996, vol. 67, no1, pp. 115-119 (30 ref.). URL consultato il 25 febbraio 2011 (archiviato dall' url originale il 30 dicembre 2011) .
- ^ Aldo Zangara, Terapia medica ragionata , PICCIN, 2002, pp. 92–, ISBN 978-88-299-1649-8 . URL consultato il 24 febbraio 2011 .
- ^ N. Moryl, J. Santiago-Palma; C. Kornick; S. Derby; D. Fischberg; R. Payne; PL. Manfredi, Pitfalls of opioid rotation: substituting another opioid for methadone in patients with cancer pain. , in Pain , vol. 96, n. 3, aprile 2002, pp. 325-8, PMID 11973005 .
- ^ Connie Henke Yarbro, Margaret Hansen Frogge e Michelle Goodman, Cancer nursing: principles and practice , Jones & Bartlett Learning, 2005, pp. 676–, ISBN 978-0-7637-4720-6 .
- ^ V. Tim Malhotra e Natalie Moryl, Dx/Rx: palliative cancer care , Jones & Bartlett Learning, 27 gennaio 2006, pp. 30–, ISBN 978-0-7637-2639-3 .
- ^ Bruce Chabner, Thomas J. Lynch e Dan L. Longo, Harrison's Manual of Oncology , McGraw Hill Professional, pp. 183–, ISBN 978-0-07-141189-9 .
- ^ M. Connock, A. Juarez-Garcia; S. Jowett; E. Frew; Z. Liu; RJ. Taylor; A. Fry-Smith; E. Day; N. Lintzeris; T. Roberts; A. Burls, Methadone and buprenorphine for the management of opioid dependence: a systematic review and economic evaluation. , in Health Technol Assess , vol. 11, n. 9, marzo 2007, pp. 1-171, iii-iv, PMID 17313907 .
- ^ a b H. Joseph, S. Stancliff; J. Langrod, Methadone maintenance treatment (MMT): a review of historical and clinical issues. , in Mt Sinai J Med , vol. 67, n. 5-6, pp. 347-64, PMID 11064485 .
- ^ Carlo Barbera, Giuseppe De Carlo e Luca De Carlo, Testo unico di pubblica sicurezza , Maggioli Editore, 2008, pp. 786–, ISBN 978-88-387-4029-9 .
- ^ a b L. Nicholls, L. Bragaw; C. Ruetsch, Opioid dependence treatment and guidelines. , in J Manag Care Pharm , vol. 16, 1 Suppl B, febbraio 2010, pp. S14-21, PMID 20146550 .
- ^ Nicholls L, Bragaw L, Ruetsch C, Opioid dependence treatment and guidelines , in J Manag Care Pharm , vol. 16, 1 Suppl B, febbraio 2010, pp. S14–21, PMID 20146550 .
- ^ Mannelli P, Patkar AA, Peindl K, Gorelick DA, Wu LT, Gottheil E,Very low dose naltrexone addition in opioid detoxification: a randomized, controlled trial , in Addict Biol , vol. 14, n. 2, aprile 2009, pp. 204–13, DOI : 10.1111/j.1369-1600.2008.00119.x , PMC 2657183 , PMID 18715283 .
- ^ Nilsson MI, Grönbladh L, Widerlöv E, Anggård E, Pharmacokinetics of methadone in methadone maintenance treatment: characterization of therapeutic failures , in Eur. J. Clin. Pharmacol. , vol. 25, n. 4, 1983, pp. 497–501, PMID 6653644 .
- ^ Ebadi, Manuchair S., Desk Reference of Clinical Pharmacology, Second Edition , Boca Raton, CRC, 2007, p. 34, ISBN 1-4200-4743-4 .
- ^ Deiss RG, Rodwell TC, Garfein RS, Tuberculosis and illicit drug use: review and update , in Clin. Infect. Dis. , vol. 48, n. 1, gennaio 2009, pp. 72–82, DOI : 10.1086/594126 , PMID 19046064 .
- ^ Totah RA, Allen KE, Sheffels P, Whittington D, Kharasch ED, Enantiomeric metabolic interactions and stereoselective human methadone metabolism , in J. Pharmacol. Exp. Ther. , vol. 321, n. 1, aprile 2007, pp. 389–99, DOI : 10.1124/jpet.106.117580 , PMID 17259447 .
- ^ Raistrick D, Hay A, Wolff K,Methadone maintenance and tuberculosis treatment , in BMJ , vol. 313, n. 7062, ottobre 1996, pp. 925–6, PMC 2352264 , PMID 8876100 .
- ^ Herrlin K, Segerdahl M, Gustafsson LL, Kalso E, Methadone, ciprofloxacin, and adverse drug reactions , in Lancet , vol. 356, n. 9247, dicembre 2000, pp. 2069–70, DOI : 10.1016/S0140-6736(00)03409-7 , PMID 11145498 .
- ^ Nair MK, Patel K, Starer PJ, Ciprofloxacin-induced torsades de pointes in a methadone-dependent patient , in Addiction , vol. 103, n. 12, dicembre 2008, pp. 2062–4, DOI : 10.1111/j.1360-0443.2008.02390.x , PMID 19469750 .
- ^ a b Eap CB, Bertschy G, Powell K, Baumann P, Fluvoxamine and fluoxetine do not interact in the same way with the metabolism of the enantiomers of methadone , in J Clin Psychopharmacol , vol. 17, n. 2, aprile 1997, pp. 113–7, PMID 10950475 .
- ^ a b Iribarne C, Picart D, Dréano Y, Berthou F, In vitro interactions between fluoxetine or fluvoxamine and methadone or buprenorphine , in Fundam Clin Pharmacol , vol. 12, n. 2, 1998, pp. 194–9, PMID 9565774 .
- ^ Bush E, Miller C, Friedman I, A case of serotonin syndrome and mutism associated with methadone , in J Palliat Med , vol. 9, n. 6, dicembre 2006, pp. 1257–9, DOI : 10.1089/jpm.2006.9.1257 , PMID 17187532 .
- ^ Baumann P, Pharmacokinetic-pharmacodynamic relationship of the selective serotonin reuptake inhibitors , in Clin Pharmacokinet , vol. 31, n. 6, dicembre 1996, pp. 444–69, PMID 8968657 .
- ^ ( ES ) Moreno Brea MR, Rojas Corrales O, Gibert-Rahola J, Micó JA, [Drug interactions of methadone with CNS-active agents] , in Actas Esp Psiquiatr , vol. 27, n. 2, 1999, pp. 103–10, PMID 10380152 .
- ^ Greenwald MK,Behavioral economic analysis of drug preference using multiple choice procedure data , in Drug Alcohol Depend , vol. 93, n. 1-2, gennaio 2008, pp. 103–10, DOI : 10.1016/j.drugalcdep.2007.09.002 , PMC 2248460 , PMID 17949924 .
- ^ Alleyne S, Alao A, Batki SL, Lamotrigine-associated rash and blood dyscrasias in a methadone-treatment patient with hepatitis C , in Psychosomatics , vol. 47, n. 3, 2006, pp. 257–8, DOI : 10.1176/appi.psy.47.3.257 , PMID 16684944 .
- ^ Jackson L, Ting A, McKay S, Galea P, Skeoch C,A randomised controlled trial of morphine versus phenobarbitone for neonatal abstinence syndrome , in Arch. Dis. Child. Fetal Neonatal Ed. , vol. 89, n. 4, luglio 2004, pp. F300–4, DOI : 10.1136/adc.2003.033555 , PMC 1721707 , PMID 15210660 .
- ^ McBay AJ, Toxicological findings in fatal poisonings , in Clin. Chem. , vol. 19, n. 4, aprile 1973, pp. 361–5, PMID 4574410 .
- ^ Tong TG, Pond SM, Kreek MJ, Jaffery NF, Benowitz NL, Phenytoin-induced methadone withdrawal , in Ann. Intern. Med. , vol. 94, n. 3, marzo 1981, pp. 349–51, PMID 7224382 .
- ^ Cobb MN, Desai J, Brown LS, Zannikos PN, Rainey PM, The effect of fluconazole on the clinical pharmacokinetics of methadone , in Clin. Pharmacol. Ther. , vol. 63, n. 6, giugno 1998, pp. 655–62, DOI : 10.1016/S0009-9236(98)90089-3 , PMID 9663180 .
- ^ Trapnell CB, Klecker RW, Jamis-Dow C, Collins JM, Glucuronidation of 3'-azido-3'-deoxythymidine (zidovudine) by human liver microsomes: relevance to clinical pharmacokinetic interactions with atovaquone, fluconazole, methadone, and valproic acid , in Antimicrob. Agents Chemother. , vol. 42, n. 7, luglio 1998, pp. 1592–6, PMC 105651 , PMID 9660989 .
- ^ Moody DE, Fang WB, Lin SN, Weyant DM, Strom SC, Omiecinski CJ,Effect of rifampin and nelfinavir on the metabolism of methadone and buprenorphine in primary cultures of human hepatocytes , in Drug Metab. Dispos. , vol. 37, n. 12, dicembre 2009, pp. 2323–9, DOI : 10.1124/dmd.109.028605 , PMC 2784702 , PMID 19773542 .
- ^ Kharasch ED, Hoffer C, Whittington D, Walker A, Bedynek PS, Methadone pharmacokinetics are independent of cytochrome P4503A (CYP3A) activity and gastrointestinal drug transport: insights from methadone interactions with ritonavir/indinavir , in Anesthesiology , vol. 110, n. 3, marzo 2009, pp. 660–72, DOI : 10.1097/ALN.0b013e3181986a9a , PMID 19225389 .
- ^ Coles LD, Lee IJ, Hassan HE, Eddington ND, Distribution of saquinavir, methadone, and buprenorphine in maternal brain, placenta, and fetus during two different gestational stages of pregnancy in mice , in J Pharm Sci , vol. 98, n. 8, agosto 2009, pp. 2832–46, DOI : 10.1002/jps.21644 , PMID 19116954 .
- ^ Lüthi B, Huttner A, Speck RF, Mueller NJ, Methadone-induced Torsade de pointes after stopping lopinavir-ritonavir , in Eur. J. Clin. Microbiol. Infect. Dis. , vol. 26, n. 5, maggio 2007, pp. 367–9, DOI : 10.1007/s10096-007-0293-5 , PMID 17440756 .
- ^ Esteban J, Pellín Mde L, Gimeno C, et al. , Increase of R-/S-methadone enantiomer concentration ratio in serum of patients treated with either nevirapine or efavirenz , in Drug Metab Lett , vol. 2, n. 4, dicembre 2008, pp. 269–79, PMID 19356104 .
- ^ Manfredi R, Calza L, Chiodo F, Efavirenz versus nevirapine in current clinical practice: a prospective, open-label observational study , in J. Acquir. Immune Defic. Syndr. , vol. 35, n. 5, aprile 2004, pp. 492–502, PMID 15021314 .
- ^ a b Keller GA, Ponte ML, Di Girolamo G, Other drugs acting on nervous system associated with QT-interval prolongation , in Curr Drug Saf , vol. 5, n. 1, gennaio 2010, pp. 105–11, PMID 20210727 .
- ^ Haney M, Hart CL, Foltin RW, Effects of baclofen on cocaine self-administration: opioid- and nonopioid-dependent volunteers , in Neuropsychopharmacology , vol. 31, n. 8, agosto 2006, pp. 1814–21, DOI : 10.1038/sj.npp.1300999 , PMID 16407903 .
- ^ Nicholls L, Bragaw L, Ruetsch C, Opioid dependence treatment and guidelines , in J Manag Care Pharm , vol. 16, 1 Suppl B, febbraio 2010, pp. S14–21, PMID 20146550 .
- ^ a b c Mellon RD, Simone AF, Rappaport BA, Use of anesthetic agents in neonates and young children , in Anesth. Analg. , vol. 104, n. 3, marzo 2007, pp. 509–20, DOI : 10.1213/01.ane.0000255729.96438.b0 , PMID 17312200 .
- ^ Vorspan F, Ksouda K, Bloch V, et al. , A case report of transient but clinically relevant interaction between methadone and duloxetine: a reply to McCance-Katz et al , in Am J Addict , vol. 19, n. 5, settembre 2010, pp. 458–9, DOI : 10.1111/j.1521-0391.2010.00062.x , PMID 20716309 .
- ^ ( FR ) Gaudreau J, [Aurore, child martyr. Essay on violence done to children] , in Sante Ment Que , vol. 17, n. 1, 1992, pp. 55–72, PMID 1515533 .
- ^ Bosmans T, Schauvliege S, Gasthuys F, et al. , Cardiovascular effects of epidural administration of methadone, ropivacaine 0.75% and their combination in isoflurane anaesthetized dogs , in Vet Anaesth Analg , vol. 38, n. 2, marzo 2011, pp. 146–57, DOI : 10.1111/j.1467-2995.2011.00595.x , PMID 21303446 .
- ^ a b Meyer MR, Maurer HH, Absorption, distribution, metabolism and excretion pharmacogenomics of drugs of abuse , in Pharmacogenomics , vol. 12, n. 2, febbraio 2011, pp. 215–33, DOI : 10.2217/pgs.10.171 , PMID 21332315 .
- ^ Mercadante S, Villari P, Ferrera P, Arcuri E, David F, Opioid switching and burst ketamine to improve the opioid response in patients with movement-related pain due to bone metastases , in Clin J Pain , vol. 25, n. 7, settembre 2009, pp. 648–9, DOI : 10.1097/AJP.0b013e3181a68a85 , PMID 19692808 .
- ^ Steinberg M, Morin AK, Mild serotonin syndrome associated with concurrent linezolid and fluoxetine , in Am J Health Syst Pharm , vol. 64, n. 1, gennaio 2007, pp. 59–62, DOI : 10.2146/ajhp060227 , PMID 17189581 .
- ^ Katchman AN, Koerner J, Tosaka T, Woosley RL, Ebert SN, Comparative evaluation of HERG currents and QT intervals following challenge with suspected torsadogenic and nontorsadogenic drugs , in J. Pharmacol. Exp. Ther. , vol. 316, n. 3, marzo 2006, pp. 1098–106, DOI : 10.1124/jpet.105.093393 , PMID 16278312 .
- ^ Chen PP, Chui PT, Gin T, Comparison of ondansetron and metoclopramide for the prevention of post-operative nausea and vomiting after major gynaecological surgery , in Eur J Anaesthesiol , vol. 13, n. 5, settembre 1996, pp. 485–91, PMID 8889424 .
- ^ Junttila MJ, Gonzalez M, Lizotte E, et al. , Induced Brugada-type electrocardiogram, a sign for imminent malignant arrhythmias , in Circulation , vol. 117, n. 14, aprile 2008, pp. 1890–3, DOI : 10.1161/CIRCULATIONAHA.107.746495 , PMID 18391123 .
- ^ Auer U, Mosing M, Moens YP, The effect of low dose rocuronium on globe position, muscle relaxation and ventilation in dogs: a clinical study , in Vet Ophthalmol , vol. 10, n. 5, 2007, pp. 295–8, DOI : 10.1111/j.1463-5224.2007.00553.x , PMID 17760708 .
- ^ Hofling CK, Winslow WW, Kellner R, Drug therapy , in Prog Neurol Psychiatry , vol. 27, 1972, pp. 339–54, PMID 4575598 .
- ^ Prosser JM, Mills A, Rhim ES, Perrone J,Torsade de pointes caused by polypharmacy and substance abuse in a patient with human immunodeficiency virus , in Int J Emerg Med , vol. 1, n. 3, settembre 2008, pp. 217–20, DOI : 10.1007/s12245-008-0052-0 , PMC 2657284 , PMID 19384521 .
- ^ Poluzzi E, Raschi E, Moretti U, De Ponti F, Drug-induced torsades de pointes: data mining of the public version of the FDA Adverse Event Reporting System (AERS) , in Pharmacoepidemiol Drug Saf , vol. 18, n. 6, giugno 2009, pp. 512–8, DOI : 10.1002/pds.1746 , PMID 19358226 .
- ^ ( FR ) Furlan V, Taburet AM, [Drug interactions with antiretroviral agents] , in Therapie , vol. 56, n. 3, 2001, pp. 267–71, PMID 11475806 .
- ^ Silva de Lima M, Farrell M, Lima Reisser AA, Soares B, WITHDRAWN: Antidepressants for cocaine dependence , in Cochrane Database Syst Rev , n. 2, 2010, pp. CD002950, DOI : 10.1002/14651858.CD002950.pub2 , PMID 20166064 .
- ^ Gongadze N, Kezeli T, Antelava N, Prolong QT interval and "torsades de pointes" associated with different group of drugs , in Georgian Med News , n. 153, dicembre 2007, pp. 45–9, PMID 18250496 .
- ^ a b Brahm NC, Yeager LL, Fox MD, Farmer KC, Palmer TA, Commonly prescribed medications and potential false-positive urine drug screens , in Am J Health Syst Pharm , vol. 67, n. 16, agosto 2010, pp. 1344–50, DOI : 10.2146/ajhp090477 , PMID 20689123 .
- ^ Gerber JG, Rhodes RJ, Gal J, Stereoselective metabolism of methadone N-demethylation by cytochrome P4502B6 and 2C19 , in Chirality , vol. 16, n. 1, gennaio 2004, pp. 36–44, DOI : 10.1002/chir.10303 , PMID 14628297 .
Bibliografia
Linee guida
Le Linee guida pubblicate nel mondo che riguardano il metadone sono n. 10, secondo una ricerca effettuata su Pubmed ed aggiornata al 25 febbraio 2011; così suddivise per argomento:
Linee guida nel dolore oncologico
- Hanks GW, Conno F, Cherny N, et al. , Morphine and alternative opioids in cancer pain: the EAPC recommendations , in Br. J. Cancer , vol. 84, n. 5, marzo 2001, pp. 587–93, DOI : 10.1054/bjoc.2001.1680 , PMC 2363790 , PMID 11237376 .
Linee guida nel dolore non oncologico
- Chou R, Fanciullo GJ, Fine PG, et al. , Clinical guidelines for the use of chronic opioid therapy in chronic noncancer pain , in J Pain , vol. 10, n. 2, febbraio 2009, pp. 113–30, DOI : 10.1016/j.jpain.2008.10.008 , PMID 19187889 .
- Trescot AM, Helm S, Hansen H, et al. , Opioids in the management of chronic non-cancer pain: an update of American Society of the Interventional Pain Physicians' (ASIPP) Guidelines [ collegamento interrotto ] , in Pain Physician , vol. 11, 2 Suppl, marzo 2008, pp. S5–S62, PMID 18443640 .
- Moulin DE, Clark AJ, Gilron I, et al. , Pharmacological management of chronic neuropathic pain - consensus statement and guidelines from the Canadian Pain Society , in Pain Res Manag , vol. 12, n. 1, 2007, pp. 13–21, PMC 2670721 , PMID 17372630 . URL consultato il 5 gennaio 2012 (archiviato dall' url originale il 10 novembre 2012) .
- Moulin DE, Clark AJ, Gilron I, et al. , Pharmacological management of chronic neuropathic pain - consensus statement and guidelines from the Canadian Pain Society , in Pain Res Manag , vol. 12, n. 1, 2007, pp. 13–21, PMC 2670721 , PMID 17372630 . URL consultato il 5 gennaio 2012 (archiviato dall' url originale il 10 novembre 2012) .
Linee guida nelle tossicodipendenze
- ( NL ) Westra M, de Haan HA, Arends MT, van Everdingen JJ, Klazinga NS, [Guideline 'Medicinal care for drug addicts in penal institutions'] , in Ned Tijdschr Geneeskd , vol. 153, 2009, pp. A726, PMID 20051159 .
- ( ES ) Miró JM, Torre-Cisnero J, Moreno A, et al. , [GESIDA/GESITRA-SEIMC, PNS and ONT consensus document on solid organ transplant (SOT) in HIV-infected patients in Spain (March, 2005)] , in Enferm. Infecc. Microbiol. Clin. , vol. 23, n. 6, 2005, pp. 353–62, PMID 15970168 .
- ( FR ) Michel L, Maguet O, [Guidelines for substitution treatments in prison populations] , in Encephale , vol. 31, 1 Pt 1, 2005, pp. 92–7, PMID 15971645 .
- Barry J, Bourke M, Buckley M, et al. , Hepatitis C among drug users: consensus guidelines on management in general practice , in Ir J Med Sci , vol. 173, n. 3, 2004, pp. 145–50, PMID 15693384 .
- Fiellin DA, Barthwell AG, Guideline development for office-based pharmacotherapies for opioid dependence , in J Addict Dis , vol. 22, n. 4, 2003, pp. 109–20, PMID 14723481 .
- Yoast R, Williams MA, Deitchman SD, Champion HC, Report of the Council on Scientific Affairs: methadone maintenance and needle-exchange programs to reduce the medical and public health consequences of drug abuse , in J Addict Dis , vol. 20, n. 2, 2001, pp. 15–40, DOI : 10.1300/J069v20n02_03 , PMID 11318395 .
Testi
Farmacologia e clinica
- Gian Paolo Novelli, Roberta Casali e Rocco D. Mediati, Terapia del dolore , SEE Editrice Firenze, 1999, pp. 80–, ISBN 978-88-8465-021-4 .
- Sebastiano Mercadante, Il dolore nel paziente neoplastico , Elsevier srl, 2009, pp. 142–, ISBN 978-88-214-3067-1 .
- ( EN ) Laurence L. Brunton, Louis Sanford Goodman, Donald Blumenthal, Iain Buxton, Goodman and Gilman's manual of pharmacology and therapeutics , McGraw-Hill Professional, 28 settembre 2007, pp. 361–, ISBN 978-0-07-144343-2 .
- ( EN ) Anthony J. Trevor, Bertram G. Katzung e Susan B. Masters, Katzung and Trevor's pharmacology , McGraw-Hill Professional, 11 dicembre 2007, pp. 264–, ISBN 978-0-07-148869-3 .
- ( EN ) Jane C Ballantyne, Scott M Fishman e James P. Rathmell, Bonica's Management of Pain , Lippincott Williams & Wilkins, 1º ottobre 2009, pp. 1186–, ISBN 978-0-7817-6827-6 .
- ( EN ) Bruce Chabner, Thomas J. Lynch e Dan L. Longo, Harrison's Manual of Oncology , McGraw Hill Professional, 11 novembre 2007, pp. 183–, ISBN 978-0-07-141189-9 .
- ( EN ) accessdate Eduardo Bruera e Russell K. Portenoy, Cancer pain: assessment and management , Cambridge University Press, 2003, pp. 122–, ISBN 978-0-521-77332-4 .
- ( EN ) Connie Henke Yarbro, Debra Wujcik e Barbara Holmes Gobel, Cancer Nursing: Principles and Practice , Jones & Bartlett Learning, 21 aprile 2010, pp. 710–, ISBN 978-0-7637-6357-2 .
- ( EN ) Derek Doyle, Geoffrey Hanks e Nathan I. Cherny, Oxford textbook of palliative medicine , Oxford University Press, 11 gennaio 2005, pp. 324–, ISBN 978-0-19-856698-4 .
- ( EN ) DA Warrell, Timothy M. Cox e John D. Firth, Oxford textbook of medicine , Oxford University Press, 2003, pp. 1015–, ISBN 978-0-19-857014-1 .
- ( EN ) Alan F. Schatzberg, Jonathan O. Cole e Charles DeBattista, Manual of Clinical Psychopharmacology , American Psychiatric Pub, 8 aprile 2010, pp. 573–, ISBN 978-1-58562-377-8 .
- ( EN ) John P. Cloherty, Eric C. Eichenwald e Ann R. Stark, Manual of neonatal care , Lippincott Williams & Wilkins, 2008, pp. 217–, ISBN 978-0-7817-6984-6 .
Consultabili:
- ( EN ) Nalini Vadivelu, Essentials of Pain Management , Springer, 3 marzo 2011, pp. 686–, ISBN 978-0-387-87578-1 . URL consultato il 5 gennaio 2012 .
- ( EN ) Gerald Briggs, Roger K. Freeman e Sumner J. Yaffe, Drugs in Pregnancy and Lactation: A Reference Guide to Fetal and Neonatal Risk , Lippincott Williams & Wilkins, 29 marzo 2011, pp. 916–, ISBN 978-1-60831-708-0 . URL consultato il 5 gennaio 2012 .
- ( EN ) Michael D. Stubblefield, Cancer rehabilitation principles and practice , Demos Medical Publishing, 22 aprile 2009, pp. 488–, ISBN 978-1-933864-33-4 . URL consultato il 5 gennaio 2012 .
Tossico-dipendenze
- Carlo Barbera, Giuseppe De Carlo e Luca De Carlo, Testo unico di pubblica sicurezza , Maggioli Editore, 2008, pp. 786–, ISBN 978-88-387-4029-9 .
- Umberto Nizzoli, Trattato completo degli abusi e delle dipendenze , PICCIN, 2002, pp. 753–, ISBN 978-88-299-1648-1 .
- Marcello Cesa-Bianchi , Aspetti psicologici della tossicodipendenza in una metropoli: ricerche su l'adolescente, la famiglia, il medico , Editoriale Jaca Book, 1987, pp. 200–, ISBN 978-88-16-95031-3 .
- Celeste Franco Giannotti, Dipendenze: la qualità della cura nei servizi , FrancoAngeli, 2003, pp. 171–, ISBN 978-88-464-5102-6 .
- G. Strepparola, Curare gli eroinomani: l'uso del metadone nel panorama italiano ed europeo , FrancoAngeli, 2005, pp. 23–, ISBN 978-88-464-6505-4 .
- Luca Fazzi e Antonio Scaglia, Tossicodipendenza e politiche sociali in Italia , FrancoAngeli, 2001, pp. 115–, ISBN 978-88-464-2945-2 .
- Paolo Rigliano, Piaceri drogati. Psicologia del consumo di droghe , Feltrinelli Editore, 2004, pp. 166–, ISBN 978-88-07-81790-8 .
- Mauro Cibin e GP Guelfi, Il trattamento con metadone , FrancoAngeli, 2004, pp. 239–, ISBN 978-88-464-5604-5 .
- Giorgio Pietrostefani, Il sistema droga. Per capire le cause e punire di meno , Editoriale Jaca Book, 1998, pp. 164–, ISBN 978-88-16-28050-2 .
- ( EN ) Joyce H. Lowinson, Pedro Ruiz e Robert B. Millman, Substance abuse: a comprehensive textbook , Lippincott Williams & Wilkins, 2005, pp. 1246–, ISBN 978-0-7817-3474-5 .
- ( EN ) Cath Harrison e Alan Gibson, Practical Neonatology for MRCPCH and Beyond , Churchill-Livingston, 25 settembre 2009, pp. 28–, ISBN 978-0-443-07070-9 .
- ( EN ) Harold E. Doweiko, Concepts of Chemical Dependency , Cengage Learning, 2009, pp. 389–, ISBN 978-0-495-50580-8 .
- ( EN ) Kathleen M. King, Methadone-Associated Overdose Deaths: Factors Contributing to Increased Deaths and Efforts to Prevent Them , DIANE Publishing, June 2010, ISBN 978-1-4379-1471-9 .
Voci correlate
Altri progetti
-
 Wikiquote contiene citazioni di o su metadone
Wikiquote contiene citazioni di o su metadone -
 Wikizionario contiene il lemma di dizionario « metadone »
Wikizionario contiene il lemma di dizionario « metadone » -
 Wikimedia Commons contiene immagini o altri file su metadone
Wikimedia Commons contiene immagini o altri file su metadone
Collegamenti esterni
- www.sims.it/metadone , su sims.it .
- www.salus.it , su salus.it . URL consultato il 25 febbraio 2011 (archiviato dall' url originale il 26 giugno 2015) .
- ( EN )www.ncbi.nlm.nih.gov , su ncbi.nlm.nih.gov .
- ( EN ) www.drugs.com/methadone.html , su drugs.com .
- ( EN ) www.rxlist.com/dolophine-drug.htm , su rxlist.com .
- ( EN ) withdrawal-symptoms-methadone/ , su withdrawalsymptomsmethadone.com . URL consultato il 25 febbraio 2011 (archiviato dall' url originale il 27 febbraio 2011) .
| Controllo di autorità | LCCN ( EN ) sh85084373 · GND ( DE ) 4038959-5 · NDL ( EN , JA ) 00567621 |
|---|